Er:YAG激光与传统机械去龋效果的体外可行性比较
2021-07-01葛米雪周红艳杨颜菁
邵 钰,尚 琼,郭 蓉,葛米雪,周红艳,杨颜菁,3
龋病治疗目前主要依靠涡轮高低速手机去除腐质,但会产生震动、噪声等问题。随着微创治疗中减轻患者的疼痛并取得更好的治疗效果观念的普及,微创治疗的这种原则也逐渐应用于口腔临床中。在众多微创治疗方法中,Er:YAG激光作为治疗龋病的一种新技术得到了广泛的关注。Er:YAG激光可以精准到小于1 mm的口腔区域,这使得在使用Er:YAG激光去除受感染的牙本质的同时,能够最大限度地保留周围健康的组织。一些研究表明,Er:YAG还可以减少去龋过程中产生过高温度,高温对牙髓活力可能产生不利的影响[1-2]。Er:YAG激光已经在儿童口腔科中得到了广泛的应用[3]。尽管Er:YAG激光在口腔科领域显示出了很大的潜力,但目前尚缺乏科学证据来阐明其在洞形制备和粘接修复中的具体作用机制。此外,一些研究发现Er:YAG激光和传统机械方法在粘接强度、微渗漏和去龋操作时间等许多方面没有差异。
本实验旨在为Er:YAG激光去除龋坏和粘接修复提供更多的实验依据。通过实验比较Er:YAG激光和常规机械方法制备窝洞的微拉伸强度和微渗漏深度,并通过扫描电子显微镜(SEM)观察两种方法制备的牙面,从组织学的角度评价这两种牙本质去除方法的治疗效果并测定各自的去龋时间。
1 材料与方法
1.1 离体牙收集
经南京医科大学附属口腔医院伦理委员会批准(批准号:PJ-2017-033-001)并经患者同意,本研究收集因牙周病变或阻生而新鲜拔除的人恒磨牙36颗,其牙合面有达牙本质深层的龋坏,为Ⅴ类洞。同时经放射学检查,排除静止龋、继发龋和已露髓的牙齿。去除牙齿周围的软组织并清除牙菌斑和根面牙石[4]。所有离体牙在4 ℃的生理盐水中保存,并在1周内使用。36颗离体牙随机编号为1~36。
1.2 样品制备和分组
用低速切割机(Isomet,美国)将离体牙的每个龋损切成大小大致相等的两半(图1),分成A、B两个样本,A样本纳入对照组,B样本纳入实验组[2]。实验组按照 Er:YAG激光治疗仪(Fotona M002-3A/4,德国)的临床操作规程进行去龋,并采取以下措施:①操作者和助手佩戴护目镜;②实验参数设置为切割牙釉质,300 mJ,30 Hz;切割牙本质,200 mJ,20 Hz;③进行光纤头距龋坏部位1 mm的非接触扫描照射;④评估和再次照射,直至所有龋坏被清除。对照组采用高速手机去除无基釉以及釉牙本质交界处的腐质,然后用低速手机彻底去除腐质,达到去除软化着色牙本质的标准。

离体牙根据龋洞被均匀地切成两半
1.3 微拉伸粘接强度测试
编号为1~13的牙齿,用于测试微拉伸粘接强度(mTBS)。用Er:YAG激光去除龋坏组织或用手机去腐,直到肉眼和探诊检查都认为去尽腐质。所有的工作由同一个研究人员完成。冲洗和干燥后,用自酸蚀粘接剂(3M Adper Easy One,美国)处理窝洞,并用通用纳米树脂(FiltekTMZ350XT,美国)修复。充填后置于37 ℃生理盐水中24 h。将牙冠分离后,用低速切割机(Isomet,美国)将牙本质-树脂粘接面(窝洞侧壁)制成1 mm×1 mm的哑铃形试件(图2)。每个样本可制备2~4个实验试件。用502胶粘剂(氰基丙烯酸酯粘合剂)将试件固定到微拉伸测力仪上(BISCO,美国),并施加拉应力,直到断裂。然后测量拉伸断口的载荷数值(N),并用游标卡尺测量断面的边长。mTBS(MPa)=试样拉断时的载荷(N)/断面处截面积(mm2)。测试重复3次,计算平均值。

图2 将试件固定在测试夹具上进行微拉伸粘接强度测试Fig.2 Test pieces fixed on the test fixture for the microtensile bond strength test
1.4 微渗漏测试
编号为14~26的牙齿用于测试微渗漏深度。从去龋到修复的操作程序与微拉伸粘接强度试验中的操作程序相同。样品保存在37 ℃的生理盐水中。随后,样品置于5 ℃和55 ℃的冷热循环仪(Will,中国)中进行实验,每次浸泡30 s,交替5 000次。在距离粘接边缘1 mm处涂3层无色指甲油,以防止正常牙齿染色。标本在1%碱性品红中浸泡24 h后,切成1 mm厚的切片,体视显微镜(Nikon,日本)20倍下观察,并测量染料渗透深度(最深处至界面的垂直距离)。
1.5 组织学评价
编号为27~32的牙齿用于组织学观察。实验组和对照组各6个样本,去龋方法与前述方法相同。截去牙根,在4%多聚甲醛溶液中固定48 h,10%硝酸脱钙、脱水后石蜡包埋,全自动半薄轮转切片机切片,厚度4 μm样本各制20张切片。从所有标本中随机抽取8张切片,HE染色。HE染色步骤:样品依次用二甲苯Ⅰ和Ⅱ以及100%、95%、80%和75%乙醇脱蜡,然后用苏木精和伊红染色,并以乙醇的升序(75%、80%、95%和100%)脱水。最后,每张切片用中性树胶封住,在正置荧光显微镜(LEICA,德国)200倍视野下进行形态学检查。在窝洞底部中央连续观察6个视野。牙本质小管被染成蓝紫色的部分,是残留的细菌以及碎屑,记为“感染”的牙本质小管,统计6个视野内感染牙本质小管的数量,评分如下,0:无感染牙本质小管;1:1~10个感染牙本质小管;2:10~20个感染牙本质小管;3:20个以上感染牙本质小管。
1.6 扫描电子显微镜评价
取编号为33~36的牙齿,用扫描电子显微镜观察牙本质表面形态。用Er:YAG激光(n=4)和传统器械(n=4)进行去龋。将标本制成大小相同(4.0 mm×4.0 mm×2.5 mm)的牙体组织块,并对其底部进行抛光处理。然后将其浸泡在2.5%戊二醛溶液中固定。经50%、70%、80%、90%和100%乙醇梯度脱水后,用HELIOS NanoLab 600i电子显微镜进行表面形貌观察。使用扫描电子显微镜在两个放大倍数下进行分析:2 000倍和3 500倍。
1.7 去龋时间
记录前4部分实验中实验组和对照组的去龋时间,以开始去腐为始,以明确达到临床腐质去尽标准为终,计算平均去龋时间并进行分析。
1.8 统计学方法
使用SPSS 22.0进行统计分析。用配对样本t检验对实验组和对照组的mTBS、微渗漏深度、组织学实验和去龋时间等数据进行统计学分析。在所有的检验中,P<0.05被认为有统计学意义。
2 结 果
2.1 微拉伸粘接强度
两个实验组的平均mTBS值和标准差如表1所示,实验组比对照组有更好的微拉伸粘接强度。

表1 对照组和实验组的微拉伸粘接强度
2.2 微渗漏深度
用体视显微镜在放大20倍的视野下观察切片中染料的渗透深度如图3所示。两组的平均微渗漏深度如表2所示,虽然实验组的平均微渗漏深度低于对照组,但差异无统计学意义(P=0.059)。

A:对照组的部分;B:实验组的部分
P>0.05
2.3 组织学分析
牙本质小管染色视野如图4所示。传统机械治疗的洞底光滑、平整、连续,而Er:YAG激光去龋的洞底粗糙、熔化、凹凸不平。感染牙本质染色分析结果如表3所示。两组间感染牙本质评分差异有统计学意义(P=0.007)。

A:对照组组织切片( ×200)显示牙本质小管大量破坏和细菌阻塞,腔底光滑连续;B:实验组组织切片( ×200)显示牙本质小管少量破坏,细菌残留较少,腔底不规则粗糙
2.4 扫描电镜结果
扫描电镜观察结果如图5所示。对照组牙本质表面形成一层厚厚的玷污层,牙本质小管结构不清、数量少、管腔栓塞。相反,实验组的牙本质表面无玷污层且高低起伏呈鱼鳞状,牙本质小管开口清晰,管内未见栓塞。
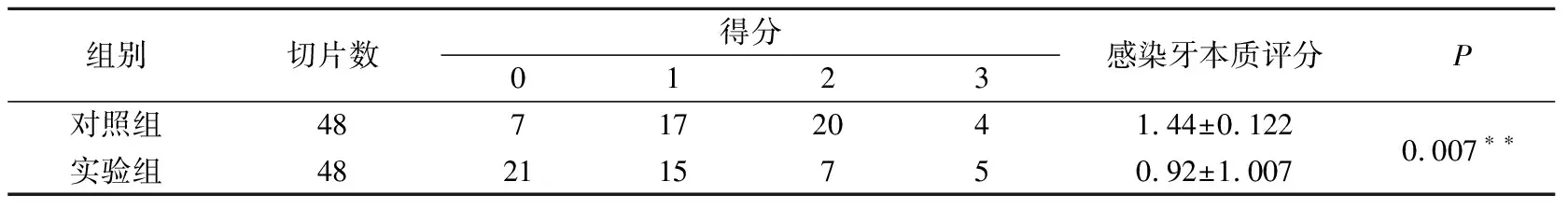
表3 对照组和实验组感染牙本质评分

A1和A2:对照组牙本质表面形态(A1: ×2 000;A2: ×3 500),洞形表面不规则,有玷污层,少数牙本质小管开放;B1和B2:实验组牙本质表面形态(B1: ×2 000;B2: ×3 500)呈层次化鳞片状,有大量开放的牙本质小管
2.5 去龋所需时间
表4显示了Er:YAG激光和传统机械法的平均去龋时间。实验组去龋所需的时间明显长于对照组(P<0.05)。

表4 对照组和实验组的去龋时间Tab.4 Duration of caries removal of the control and study groups
3 讨 论
龋病是世界上最常见的口腔疾病,在成人和儿童中有很高的患病率[5-6]。传统的去除龋坏的方法依赖于涡轮手机[6]。这种广泛使用的方法快速方便,但会产生震动和声音,从而引起许多患者(特别是儿童)的焦虑和不适。此外,这种依赖于触觉和光学标准去除龋坏的机械方法存在过度去除健康牙齿或遗留龋坏组织的可能,这两种结果都会导致牙髓损伤或感染[7]。近年来,微创的概念在口腔科,特别是儿童口腔科得到了发展,它侧重于减轻患者的疼痛并取得更好的效果。遵循微创牙科的原则,相继提出了多种可选择的非侵入性方法,包括激光去龋法、非创伤性修复治疗(ART)、新型聚合物切割器械(塑料和陶瓷切割器械)、气磨法、声波法和化学机械法等[8-9]。
传统的机械方法在除龋过程中会产生噪声和震动,给患者尤其是儿童带来不适和恐惧,解决这些不足迫切需要新技术的出现[10]。在龋病治疗中引入和应用Er:YAG激光可作为传统手机的一种新的替代措施。1964年,Goldman首次将激光应用于治疗龋齿[11]。1997年,在获得美国食品和药物管理局(FDA)的批准后,口腔科引入了Er:YAG激光,用于去除龋坏和制备洞形[10]。Er:YAG激光去除龋坏的基本作用机制是它对龋坏牙釉质和牙本质中水分子的热效应。水和羟基磷灰石的吸收峰与Er:YAG激光的2 940 nm波长重合,将吸收大量的激光能量而产生热,温度迅速升高,汽化,进而产生微爆炸使牙体硬组织结构破碎,达到切割硬组织的目的。由于龋齿组织比健康的牙体组织含有更多的水分,对Er:YAG激光的高吸收性,使Er:YAG激光成为了一种可选择的去龋方法,减少波及健康的牙齿结构[1]。与传统方法相比,Er:YAG激光具有许多不可否认的优点,如在洞形制备过程中震动和噪音小,减少了局部麻醉的使用,可以减少患者的恐惧和不适等。
充填物与牙体组织的粘接存在几个问题,如充填材料断裂和边缘微渗漏等[4,12-14]。这些都是充填体临床耐久性面临的主要挑战。微拉伸粘接强度和微渗漏深度是近年来研究中评价充填体粘接质量的主要指标。1995年,Pashley 等考虑到较小的粘接面积(<2 mm×2 mm)能更准确地反映实际粘接强度,提出了微拉伸粘接强度的概念。由于粘接面较小,压力更加均匀,试件的断裂部位主要发生在粘接面[15-16]。在本实验中,微拉伸试件被制成哑铃形,从而使粘接面积尽可能小,并控制在1 mm2内[17]。在目前的体外研究中,使用Er:YAG激光与传统的机械方法相比获得了更好的粘接强度。树脂和牙体组织之间的微渗漏会影响边缘封闭,并导致继发龋、牙齿过敏、病理性牙髓改变或充填体松动等后果[12]。除了树脂和粘接剂体系的粘接质量和聚合收缩外,微渗漏的发生还与窝洞制备过程中使用的工具有关[14,18]。在本研究中,我们认为与传统方法相比,Er:YAG激光去龋可以减少树脂修复技术的微渗漏,但在统计学上没有显著差异。我们的结果与Yaman 等的结果是一致的[19]。据报道,牙釉质和牙本质表面纹理的物理变化可能会影响微渗漏,这与Er:YAG激光的照射频率和时间有关。较高的照射频率和照射时间可导致牙本质熔化和重结晶[12],从而使牙本质组织的胶原纤维融合,减少树脂向纤维间隙和管间扩散。此外,牙本质熔化可能与Er:YAG激光束的类型、剂量或角度有关,这可能导致了微渗漏深度不同的结果。
现代理念认为去除牙本质龋是去除大部分受感染的软化龋坏组织,以防止微生物入侵,保护牙髓活力,并为修复准备合适的窝洞[2,20]。以往的研究表明,较高频率的Er:YAG激光(25~30 Hz)会导致受激光照射的牙本质产生裂纹、熔融等热损伤现象,而传统机械制备则会产生明显的玷污层[2,21]。在目前的体外研究中,我们根据牙本质小管中细菌沉积的数量来评估去龋的效果,显示Er:YAG激光对感染牙本质的清洁效果优于传统机械法,对照组的组织切片中断裂的牙本质小管融合成串珠状,而实验组的牙本质小管几乎没有阻塞和膨胀。另一个不同之处在于传统涡轮机处理的洞底比Er:YAG激光处理的洞底部更平整。
我们通过扫描电子显微镜观察到,经Er:YAG激光处理的牙本质表面微形态清晰,牙本质小管开放、清晰,与Sallam等[15]和Chiniforush等[22]的研究结果一致。关于牙本质龋的治疗,玷污层的存在会使树脂和粘接剂系统的粘接强度降低,而牙本质小管的开放则可以增强修复材料和牙体之间的粘接强度[22]。SEM结果也证实了Er:YAG激光照射组具有较高的结合强度。然而,由于本研究的局限性,在使用Er:YAG激光或传统机械进行窝洞预备后,没有对牙本质和树脂之间的相互作用模式进行SEM评估。
使用Er:YAG激光去除龋坏所花费的平均时间明显高于使用传统机械法去除龋坏所需的平均时间。与之前的一项研究[3]是一致的。可能是因为Er:YAG激光的使用时间包括手动切换参数的时间,导致了Er:YAG激光的工作时间较长。
体外实验结果可能不能准确反映体内的情况。因此,还需要对Er:YAG激光用于乳牙和恒牙的釉质龋和牙本质龋的窝洞制备进行进一步的研究。
4 结 论
本研究进一步证实了Er:YAG激光用于牙釉质龋和牙本质龋治疗的可行性。与传统的机械制备方法相比,Er:YAG激光的使用可提高树脂与牙本质组织的粘接强度,减少牙本质小管中的细菌残留,是一种高效的窝洞制备方法。此外,有效去除玷污层和随后暴露开放的牙本质小管也是实验组粘接强度增加的促进因素。然而,实验组和对照组的平均微渗漏深度没有显著差异。同时,实验组的去龋时间较对照组长。本研究结果为选择Er:YAG激光去龋提高临床治疗效果提供了依据。
