起搏器特殊起搏程序在心房颤动管理中的应用价值
2021-06-30蔡宝珍董颖雪
蔡宝珍 董颖雪
心房颤动(简称房颤)是临床上常见的心律失常之一,目前多达1/3的心动过缓患者合并有房颤,其与缺血性卒中、心力衰竭、栓塞等心脑血管疾病的发病率和死亡率密切相关[1-2]。因此,预防和(或)终止房颤的发生已成为临床上重要的治疗目标。
现代起搏器具备了更加综合的特殊起搏程序,如心房优先起搏(APP)、模式转换后的超速起搏(POMP)、抗心动过速起搏(a ATP)、管理心室起搏(MVP)等程序,成为配合抗心律失常药物和射频导管消融术治疗/管理房颤的另一种选择。本研究旨在评价与DDDR模式相比,DDDRP、MVP及DDDRP+MVP模式开启相应的特殊起搏程序或功能后是否能降低房颤负荷、延缓房颤病程进展,以及降低患者术后心血管病住院、死亡及卒中等风险。
1 资料与方法
1.1 临床资料 本院2016年7月至2017年12月因缓慢性心律失常合并阵发性房颤或心房扑动(简称房扑)符合2012年ACCF/AHA/HRS双腔心脏起搏器植入指南的患者;且至少有一次经ECG或Holter证实的房性快速心律失常病史(包括房扑、房颤)。排除标准:①完全性房室传导阻滞或心室起搏依赖(起搏比例≥40%);②房室结消融术后和房颤导管射频消融术后;③持续性房颤或永久性房颤;④希蒲系统起搏;⑤严重的心脏瓣膜疾病/心脏瓣膜置换术后。
1.2 研究方法 所有患者均接受双腔起搏器植入。起搏器型号包括:A3DR01、ADDRL1、PM2124、PM2112、Biotronik Estella DR-T、Boston Scientific J173。所有患者自植入双腔起搏器时均开启模式转换功能(模式转换频率为180 bpm)及房颤监测功能。将术后第1个月的起搏器程控数据作为基线资料,排除平均心室起搏比≥40%的患者,将其余符合条件的患者中无房颤管理程序者纳入DDDR组,具有房颤管理程序者随机分配到DDDR组、DDDRP组、MVP组或DDDRP+MVP组。DDDRP、MVP和DDDRP+MVP组自术后第1个月末开启相应的房颤管理程序,包括APP、POMP、a ATP、MVP四种程序。术前及术后13个月通过心脏超声测量右室内径(RVD)、左室内径(LVD)、左房内径(LAD)和左室射血分数(LVEF)。
1.3 观察指标 主要观察指标为房颤负荷,是指随访时间内平均每日房颤发作时间,即每日发生房颤的累积总时间/随访时间,以百分率(%)表示。次要观察指标:进展为持续性房颤、心血管病再住院、心房起搏比和心室起搏比、心脏结构重构和左心功能等。心血管病再住院是指在术后的随访期间因心力衰竭、恶性心律失常事件、心肌梗死、卒中或其他心血管事件而再住院或导致的死亡。
1.4 起搏器程序设定 DDDR组基线频率为60次/分,上限跟踪频率为120次/分,APP、POMP、aATP及MVP功能均关闭。在DDDR模式的基础上,DDDRP组开启APP、POMP、a ATP功能;MVP组只开启MVP功能;DDDRP+MVP组开启APP、POMP、a ATP及MVP功能。
1.5 随访 所有患者在术后第1、4及7个月,此后每6个月行起搏器功能程控检查。患者的心血管病住院情况和生存状态可通过电话与患者或患者家属联系。
1.6 统计学分析 用SPSS 22.0软件进行数据的统计分析。连续性数据表示为平均数(SDs)、中位数和四分位数范围(IQR);其中正态分布的测量数据用均值±标准差(±s)表示,使用T检验和(或)方差分析进行组间比较;不符合正态分布的测量数据用中位数和四分位数间距表示,组间对比采用秩和检验。计数资料以例数和百分比表示,各组间采用卡方检验(χ2检验)进行比较。
通过Kruskal-Wallis检验比较组间房颤负荷和心房、心室起搏百分比。应用配对样本的非参数检验分析各组心房、心室起搏比以及房颤负荷的组内差异。采用Kaplan-Meier检验分析各组首次持续性房颤的发生时间,并通过时序检验进行累计危害曲线的对比,采用Cox比例风险回归模型评价持续性房颤的危险性和术后心血管病住院的风险,并合成比例风险模型,计算出95%可信区间(CI)的危害比(HR)。以α=0.05为检验水平,P<0.05为差异有显著性。
2 结果
共纳入138名患者[年龄(74.0±9.2)岁;男n=54,39%],其中DDDR组65例(随机21例,无房颤管理程序的44例)、DDDRP组20例、MVP组22例、DDDRP+MVP组31例。本研究中位随访时间为15个月(13,15);其中DDDR组的中位随访时间为13个月(13,15);DDDRP组的中位随访时间为15个月(14,15);MVP组的中位随访时间为15个月(15,15);DDDRP+MVP组的中位随访时间为15个月(14,15)。所有患者的基线特征无统计学差异(表1)。
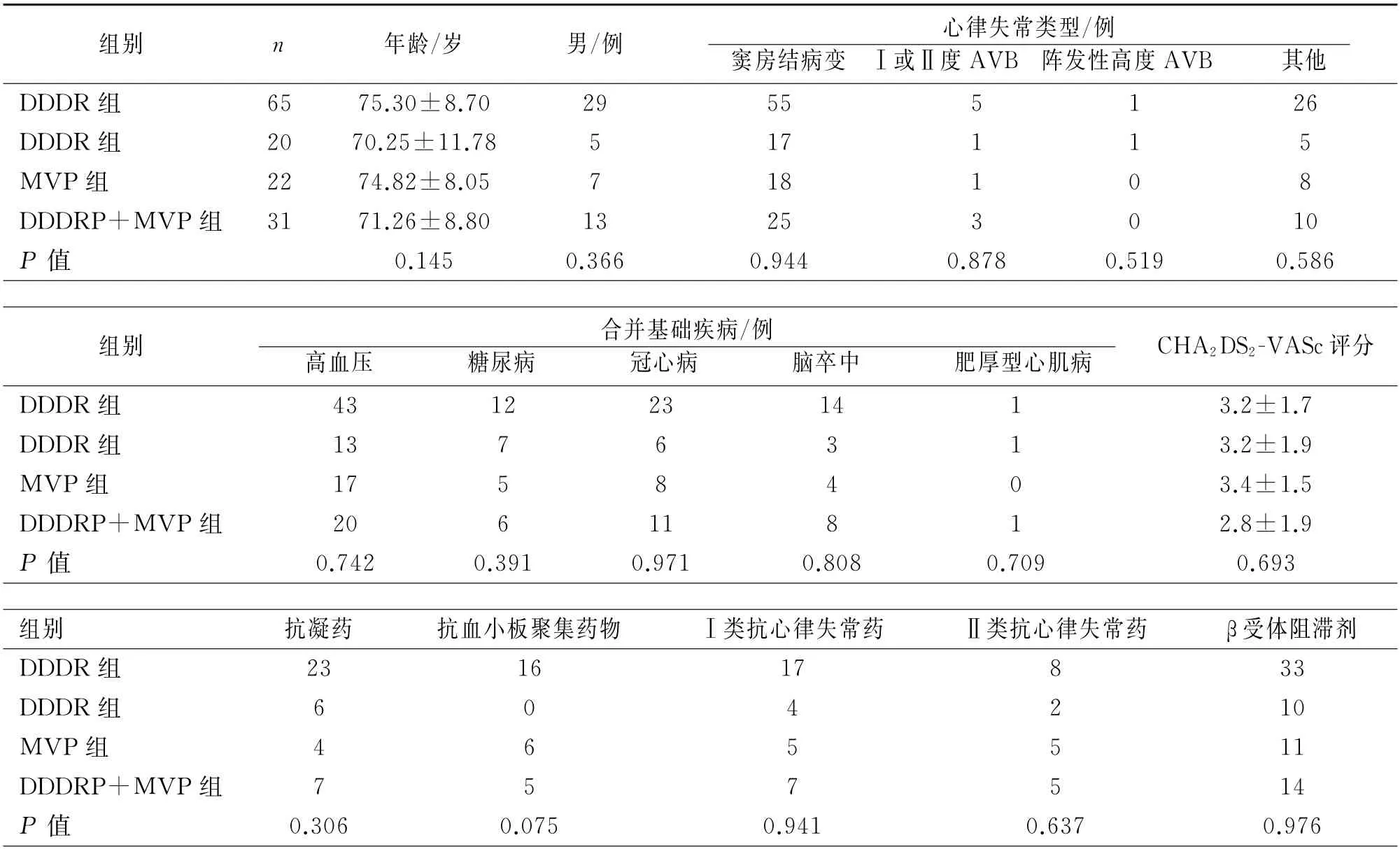
表1 四组患者基线资料
2.1 四组房颤负荷、心房与心室起搏比的比较 与术后1个月比较,术后13个月,DDDR组的心室起搏比及房颤负荷均升高(P均<0.005);DDDRP组的心房起搏比增加(P<0.005),MVP组的心室起搏比降低(P<0.005),但均未降低房颤负荷(P>0.005);DDDRP+MVP组的心房起搏比升高(P<0.005),心室起搏比和房颤负荷均降低(P均<0.005),见表2。
随访13个月,DDDRP组和DDDRP+MVP组的心房起搏比较DDDR组和MVP组均增加(P<0.001);MVP组和DDDRP+MVP组的心室起搏比较DDDR组和DDDRP组均降低(P<0.001);DDDRP+MVP组的房颤负荷低于DDDR组、DDDRP组和MVP组(P均<0.005);DDDRP组和MVP组的房颤负荷较DDDR组无明显变化(P均>0.005),见表2。

表2 四组房颤负荷、心房与心室起搏比的比较/%
2.2 四组进展为持续性房颤的比较 随访13个月,共9例发展为持续性房颤:DDDR组7例,MVP组2例。通过Kaplan-Meier检验分析示:各组间发生持续性房颤的风险无差异(P=0.267)。
2.3 四组心血管病再住院的比较 随访13个月,共52例因心血管病再入院:DDDR组39例,其中1例在术后第3个月死于急性脑梗塞;DDDRP组4例(HR=0.427,95%CI:0.15~1.216,P=0.111 vs DDDR组);MVP组7例(HR=0.757,95%CI:0.338~1.695,P=0.498 vs DDDR组);DDDRP+MVP组2例(HR=0.128,95%CI:0.031~0.532,P=0.005 vs DDDR组)。采用Cox回归分析(图1)示:校正性别和年龄后,DDDRP+MVP组的心血管病住院风险较DDDR组(HR=7.825,95%CI:1.878~32.593,P=0.005)和MVP组(HR=5.923,95%CI:1.226~28.619,P=0.027)均降低,DDDRP组、MVP组与DDDR组则无差异,见图1。
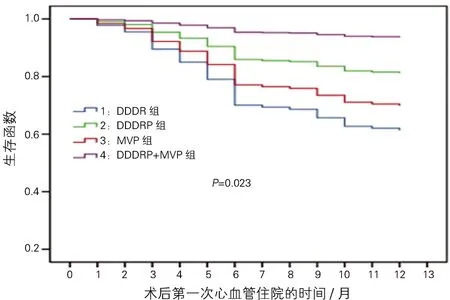
图1 心血管病住院的Cox比例风险模型
2.4 四组心房结构重构及左心功能的变化 各组患者在术前及术后13个月,无论是否打开相应的房颤管理功能,RVD、LVD、LAD、LVEF均无差异(P均>0.05),见表3。
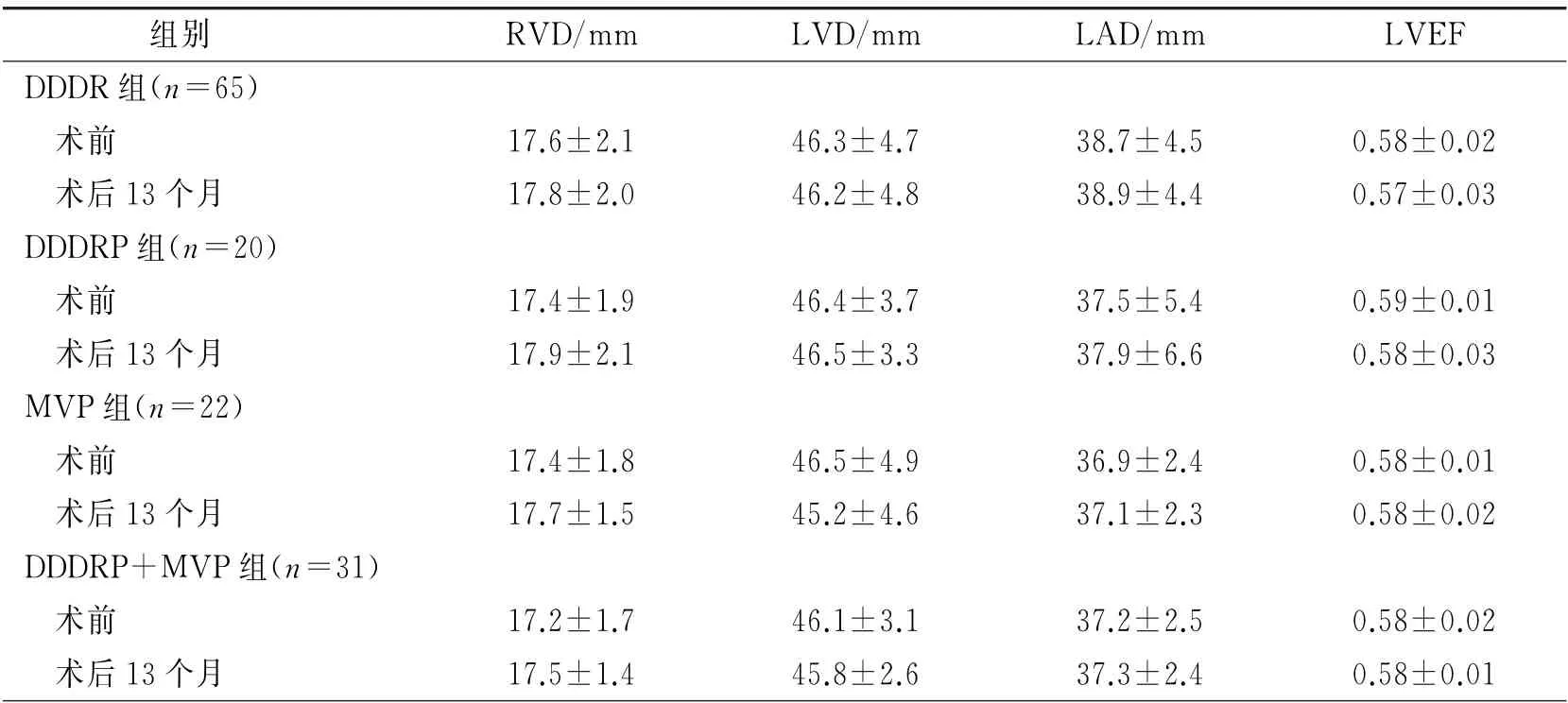
表3 四组心脏结构重构和左心功能的比较
3 讨论
房性早搏(premature atrial complexes,PACs)数量的增加会导致心房折返性房颤,APP程序主要是通过抑制PACs以减少房颤的发作。有关研究显示:APP程序可以明显提高心房起搏比,使PACs的数量减少,但未明显改变房颤负荷和房颤的发作频率[3]。房颤的早期复发(early recurrences of atrial fibrillation,ERAF)是房颤的重要触发机制[4]。ERAF的产生主要原因是在恢复窦性心律后,心房的有效不应期缩短,心房的电生理特性处于高度脆弱期[5-7]。心房有效不应期的缩短使心房内更易形成折返环;当心房肌细胞之间存在有效不应期的差异时,会使心房有效不应期的离散度增加,促进心房内折返环的形成或形成单向的阻滞,使房颤更易触发并得以维持。研究表明[5,7],在患有高比例ERAF的患者中启用POMP程序,可有效抑制ERAF,从而明显降低了房颤负荷。另一研究表明[6],以ERAF为靶点的POMP并没有减少房颤的发作次数或降低房颤负荷,主要原因考虑为120次/分的超速起搏抑制不足和房颤终止与PMOP干预之间的延迟。a ATP终止房性快速心律失常片段的成功率在19%~79%之间[8-9]。有研究表明[2],约64%患者的房性快速心律失常都经历了节律和速率的转变,当房性快速心律失常的节律变得更加规整或速率减慢时,aATP就有机会尝试终止它;折返性房性快速心律失常更易通过a ATP程序终止,其疗效范围在30%~60%。综上,a ATP可以成功终止部分房性快速心律失常,但并不一定能减轻房性快速心律失常的负荷,其原因为:首先,有些房性快速心律失常事件和“成功的”a ATP终止事件实际上是自发性终止的巧合[10]。第二,a ATP可能会缩短某些房性快速心律失常的持续时间,但总体的房颤负荷可能会因为发作持续较长的某些片段而产生偏差。以前关于通过心房起搏以预防/终止房颤的许多研究都只检验了单一的心房起搏程序,基本都得出了矛盾的结果,这可能与同一个患者的房颤发病模式的变异性以及不同患者的房颤发病机制的异质性相关。一项关于联合应用心房起搏程序(包括APP、AMS、POMP三种程序)预防阵发性房颤的研究结果表明[11],这种综合的心房起搏程序降低了房颤的发生次数,但房颤的总负荷亦无变化。本研究结果表明,对比DDDR模式,DDDRP模式(包括APP、POMP、a ATP)并未降低房颤负荷及持续性房颤的发生风险。其原因为:第一,心房起搏预防房性快速心律失常的概念是通过观察窦房结病变患者较高的心房起搏比与房性快速心律失常发生率降低的关系提出来的;阵发性房颤伴窦房结病变的患者,心房预防性起搏可明显降低房颤的复发率,但对阵发性房颤合并非窦房结病变导致的缓慢性心律失常者,提高心房起搏频率可能并不能降低房颤的发生率[8,11]。考虑到组间群体的差异,本研究还进行了DDDRP组组内自身对照,亦得出相同结果。第二,心房超速起搏不但增加了心房起搏,也无意中增加了心室起搏,不必要的心室起搏可能会掩盖或抵消心房起搏和aATP起搏的疗效,这在一定程度上解释了之前关于心房超速起搏和a ATP起搏的单独或混合研究的结果异质性[12-13]。第三,房颤的发病机制尚不完全明确,仅43%的房颤与PACs相关,22%的房颤与心动过缓有关,27%的房颤与ERAF有关[4,14]。通过对发病机制的理解,可以使特殊的心房起搏程序适用于个别患者,因此还需更进一步地研究来确定心房起搏的应答,为患者“量身定做”适应的算法。第四,心房基质的差异。心房基质是房颤的维持机制,房颤可能是心房基质进展的临床表现。电重构在一定时间内是可逆的,心房基质的慢性结构重构则是不可逆的[4,15]。
心室去同步化和不必要的心室起搏会增加房颤的发生风险[12-13,16]。MVP功能允许更多的室上性激动沿着自身的传导系统传递,最大限度的降低不必要的心室起搏。本研究表明,开启单一MVP功能一年后,右室起搏比明显低于DDDR组,但房颤负荷无明显变化;在MVP组进行开启MVP功能前后的组内自身对比,亦得出相同的结果。既往研究表明[1],通过控制心室起搏以减少心室刺激,与持续性房颤发生率的降低有一定关系,但单一的MVP功能并不能显著减少房颤或复合终点的发生。
本研究表明,联合应用心房起搏和管理心室起搏模式,即DDDRP+MVP起搏,心室起搏比和房颤负荷较DDDR起搏模式均减低,组内对照亦得出相同的结果;且就降低心血管住院风险而言,DDDRP+MVP起搏亦优于DDDR起搏和单一的MVP功能。该结果与既往研究结果是一致的[1-2,12-13]。说明DDDRP+MVP起搏模式成功实现了节律的控制,心房起搏和管理心室起搏的联合作用降低了房颤负荷。然而,本研究中,四组间发生持续性房颤的风险并没有显著差异,其原因考虑为:首先,该研究纳入的均为阵发性房颤,总体的房颤负荷较低。第二,单中心、小样本研究。第三,心房基质的差异。目前临床上可通过标测心房低电压区和瘢痕区的范围大小来比较不同类型的房颤的基质差异,并以此来判断房颤的预后。
