高蛋白营养棒储藏期硬化机理及抗硬化措施的研究进展
2021-06-16王明礼宋超男李奕莛姜瞻梅侯俊财
王明礼,赵 旭,姜 瑞,宋超男,李奕莛,陈 君,姜瞻梅,侯俊财
(东北农业大学,乳品科学教育部重点实验室,黑龙江哈尔滨 150030)
高蛋白营养棒是一类经过原料混合、冷法挤压和切块包装等步骤制作的营养均衡的方便食品,外形类似于牛轧糖,还伴随有一些巧克力涂层等。营养棒可以在短时间内有效的补充机体所需要的能量,因此被广泛的应用于运动食品和军事食品中[1]。目前,高蛋白营养棒的产业发展已逐具规模,并且可以根据消费者的饮食爱好定制性添加一些辅料,市场逐渐扩大,有取代传统零食的趋势[2-3]。高蛋白营养棒的水分活度一般在0.5~0.6之间,常温储藏至少有6~12个月的货架期[4]。食品的质地会影响消费者的感官体验而对消费者的接受程度产生重大的影响[5]。在储藏期间,营养棒的风味、质地、颜色等都会发生变化,其中以硬度变化尤为突出,极大地限制了其货架期[6-8]。
营养棒的硬化机理非常复杂,组分的不同以及外部因素等对其硬化都会产生影响。近年来,为了抑制储藏期内营养棒的硬化,国内外学者对营养棒的硬化机理进行了大量的研究,也提出了一些有效的延缓硬化方法。目前对于营养棒的研究大部分聚焦在通过控制体系组分内反应和采用不同原料等方面抑制硬度的变化。
因此,本文重点从高蛋白营养棒硬化机理、抑制硬化方法等方面进行综述,并提出今后研究方向,为生产中的实际应用提供有效的参考。
1 高蛋白营养棒
营养棒的组分通常包括蛋白质、脂类、碳水化合物以及一些保湿剂等。其中,高蛋白营养棒的蛋白质含量通常在15%~50%之间,商业用的营养棒包含动物以及植物来源的多种蛋白质,主要有乳清蛋白、酪蛋白和大豆蛋白等,它们通常采取分离蛋白(蛋白质含量高于90%)或浓缩蛋白(蛋白质含量低于90%)的形式添加到产品中,保持蛋白质在营养需求与成本之间有良好的平衡[9]。高蛋白营养棒中还含有约10%~50%的碳水化合物,主要以葡萄糖浆、果葡糖浆和麦芽糖糖浆等形式存在,这些糖浆可以提供面团形成时所需的水并且起到粘结的作用,还有一些碳水化合物以蔗糖、葡萄糖等结晶糖的形式添加[10-11]。甘油等小分子多羟基化合物(polyhydroxy compounds,PHCs)常作为保湿剂和增塑剂添加到营养棒体系中[12-14],山梨糖醇和麦芽糖醇等也作为甜味剂以及保湿剂。另外,一些花生油、大豆油或可可脂经常添加到配方中补充脂肪的含量,还可以根据消费者的口味选择性的添加坚果、维生素和膳食纤维等以提高营养价值和新颖的口感。高蛋白营养棒中仅添加少量的水分,因为大部分未经热处理的食品需要较低的水分活度抑制微生物的生长,这些水可以在体系中充当增塑剂保持系统的稳定性[15]。
市场上销售的营养棒大多采用挤压法加工生产,原料及辅料混合在一起形成面团,混合容器需要有夹层控制温度使面团保持柔软便于挤压,面团经过挤压机被挤压形成长条状,最后切割成型,有些营养棒在包装前还要进行干燥和涂层工序使其货架期可长达1年之久[11]。由于各组分混合在一起时会形成一个未达到动态平衡的体系,在生产完成和食用之间通常存在相当长的时间间隔,在此期间,多个化学、物理反应会依次或同时发生,组分之间的相互作用都有可能对体系的品质产生影响。
2 高蛋白营养棒硬化机理
大量的试验研究发现,导致高蛋白营养棒硬化的机制主要是糖结晶[16]、相分离[17]、水分迁移[9,17]、蛋白自聚集[17-18]、美拉德反应[17,19]等。营养棒的硬化过程一般分为前期和中后期两个阶段[20],前期阶段通常是营养棒制作完成后的几周或一个月内,不同组分之间的物理变化对硬度的增加起主要作用[21]。中后期阶段主要是储藏几个月之后,由于储藏条件的影响和美拉德反应引起的蛋白质聚集导致硬度的大幅度增加[22]。
2.1 糖结晶
高蛋白营养棒生产中常用的糖类主要有葡萄糖、蔗糖、葡萄糖浆、果葡糖浆和麦芽糖糖浆等,由于不同糖成分在水溶液中的溶解度不同,例如蔗糖与葡萄糖在水中的溶解度较低,因此如果在加工过程添加的蔗糖或葡萄糖过多就可能储藏过程中析出结晶。结晶体会在水分和PHCs体系之间占据一定的体积,结晶现象导致充当体系增塑剂的糖类的比例下降,结晶体在随后的储藏期中体积逐渐变大,使营养棒硬度增加[21]。
Loveday等[19]通过核磁共振发现水分、脂质和PHCs之间存在很强的相互作用,并指出在贮藏50 d内其分子迁移率不断变化,水分和PHC的迁移率大大降低,证实了葡萄糖的结晶是营养棒的硬化的一个原因。共焦显微图像也证明了糖结晶现象(图1)。现阶段高蛋白营养棒的生产工艺中可以使用溶解性能较好的糖浆来代替蔗糖和葡萄糖,例如果葡糖浆、麦芽糖浆等,从而有效避免糖结晶导致的营养棒储藏期硬度增加。

图1 乳清分离蛋白营养棒共焦显微照片[17]Fig.1 Whey protein isolate nutrition bar confocal micrograph[17]注:A为WPI营养棒制作后1 h;B为储藏1 d; C为储藏4 d;D为储藏18 d;d为葡萄糖晶体。
2.2 相分离
相分离通常是决定食品质地、机械稳定性以及外观形象的主要因素[23]。溶液中存在多种组分,由于性质的不同会分离成不同的相,降低了系统的自由能,导致系统的熵增加[24]。
在贮藏过程中,食品中水分与低分子量PHCs的羟基缔合会产生较高的渗透压,从而形成强大的驱动力,很可能导致水分从蛋白颗粒表面迁移,进而导致颗粒之间进一步缔合,最终形成两相或者三相基质[19]。最近研究中发现,在简单的糖蛋白系统中,相分离通常与糖的结晶或玻璃化转变有关[25-26]。但是在高蛋白营养棒中发现溶解的蛋白质与糖浆形成的连续相与蛋白质颗粒和脂肪球等小分子等极性物质形成的分散相之间的组分重排是相分离的主要原因。首先,由于蛋白质和碳水化合物均不溶于脂质,因此,在贮藏过程中,它们不会从脂肪球中排除,只有一些蛋白质分子可以分布在脂质和糖浆界面上。其次,随着蛋白质的逐渐水合,越来越多的水与蛋白质结合,连续相中的水被拉入分散相中[26]。若糖和蛋白质保留在单一相中,营养棒不会发生硬化。相分离现象会使得蛋白质在有效体积空间内发生浓缩效应,引发蛋白质自聚集,导致营养棒的硬度增加[21]。根据微观图像显示,相分离在营养棒制成的第一天内就开始发生[19],并且在相分离阶段中,部分水合的蛋白质颗粒对营养棒的硬化起关键作用。因此,食品储藏时间、蛋白质以及糖的种类都对营养棒硬度变化有影响[24]。
2.3 水分迁移
水分含量和水分活度都对食品的品质以及储藏稳定性有很大的影响[27]。在任何情况下,产品中“湿”和“干”这两种组分的水合作用都趋于平衡,不是在水分含量上而是在水分活度(AW)上达到平衡。例如葡萄干和奶油面团这两种成分在相同水分含量下界面处并不平衡,但在界面两侧水分活度相同时达到稳定的平衡状态,这充分证实水分的迁移不是浓度或体积的差异引起,而是水的化学势的差异造成的[28],这种解释在高蛋白营养棒体系中同样也适用。
高蛋白营养棒系统在初期阶段未达到动态平衡,各成分根据溶解以及水合的不同状况形成了不均匀的分散体,组分之间存在水分活度梯度。由于势能差的驱动,水分及其他小分子化合物会从高水分活度区迁移至低水分活度区(水分从蛋白质向糖类和甘油的迁移),使得蛋白质分子的水合作用改变,并引发一些不良反应,蛋白质颗粒在分子层面或者宏观层面上的后续变化都会导致营养棒整体的质地变化[19]。同时糖浆由于水分的转移导致产品的增塑能力降低,导致贮藏初期产品硬化[29]。普遍认为,营养棒中存在结合水和游离水两种状态的水,游离水是指与蛋白质表面的相互作用较弱,并且是紧邻蛋白质分子的溶液区域中的一部分[30],结合水指与蛋白质和糖分子之间具有很强的水离子相互作用,并且可能具有氢离子和水偶极相互作用的水分子,不同的水分状态之间的交换在蛋白质颗粒表面周围的水合层发生[31]。当AW值介于0.3~0.7之间时,蛋白质可以吸收多层水和一些毛细管水[32],Zhou等[18]观察到,蛋白质缓冲溶液(含水量40%)在34 ℃储存过程中变硬,产品中结合水含量由64%增加到68%,而游离水则由36%降低至30%。
大豆蛋白、乳清蛋白、乳清分离蛋白或酪蛋白酸钠制成的模型蛋白棒在储藏前期硬度增加被认为是由水与小分子(如甘油和山梨糖醇)迁移导致的[17,33]。含酪蛋白酸钠的高蛋白营养棒的硬化通常在制备后立即发生,而乳清蛋白体系最为稳定[34],这主要是由于乳清蛋白分子的亲水性最强,使体系中蛋白质颗粒大部分被水合,所以产品在贮藏前期能够保持较软的硬度。已经证明,水分迁移引起的乳清蛋白聚集形成的聚集体分为两类:可溶性聚集体和不溶性聚集体,并且在35 ℃条件下储藏下,不溶性聚集体在前3 d形成速度较快,随后变得增加缓慢[18,31]。大豆蛋白具有较强的疏水性,大部分蛋白质分子被水合,并且小分子的迁移率仍较高,颗粒之间以非共价相互作用松散的堆积在一起,导致系统的溶解度大大降低,硬化程度要高于乳清蛋白。对于酪蛋白酸钠体系,酪蛋白颗粒在部分水合时会溶胀,并且这些蛋白质颗粒通过非共价相互作用进一步融合并形成网状结构,因此会呈现出最高的硬度[35]。
2.4 二硫键引起的蛋白自聚集
水分等小分子迁移后发生的固态或半固态蛋白质的自聚集主要是通过形成分子间二硫键或者是分子间非共价作用导致的(图2)。分子间二硫键引发的蛋白聚集主要有两种作用机制:一种是通过分子间硫醇-二硫键的交换,另一种是赖氨酸与天冬酰胺或谷氨酰胺的羰基反应或与消除二硫键后形成的脱氢丙氨酸衍生物反应而实现的[36-38]。Zhou等[18]通过乳清分离蛋白和磷酸盐缓冲液配制的乳清蛋白/缓冲液模型系统也证实了这一点,通过对比分别加入十二烷基硫酸钠、盐酸胍、尿素后蛋白质聚集体的溶解度证实分子间氢键以及疏水相互作用等与蛋白质聚集没有很大关系;通过对比加入二硫苏糖醇(DL-Dithiothreitol,DTT)前后聚集体的溶解度证实分子间二硫键的形成与蛋白质的聚集现象有很大关联度。非共价相互作用可能首先形成非共价连接的聚集体,进一步引发了可溶性聚集体内部和之间的二硫键的形成,从而形成了较大的不溶性聚集体[39]。
不同蛋白质之间由于水分迁移导致的蛋白聚集的机制有所不同,如牛血清蛋白和乳球蛋白等蛋白质主要通过分子间硫醇二硫键的作用,非共价作用较弱[17-18],而在卵清蛋白、葡萄糖氧化酶等其他蛋白中可能主要以非共价作用形成蛋白聚集体[36]。
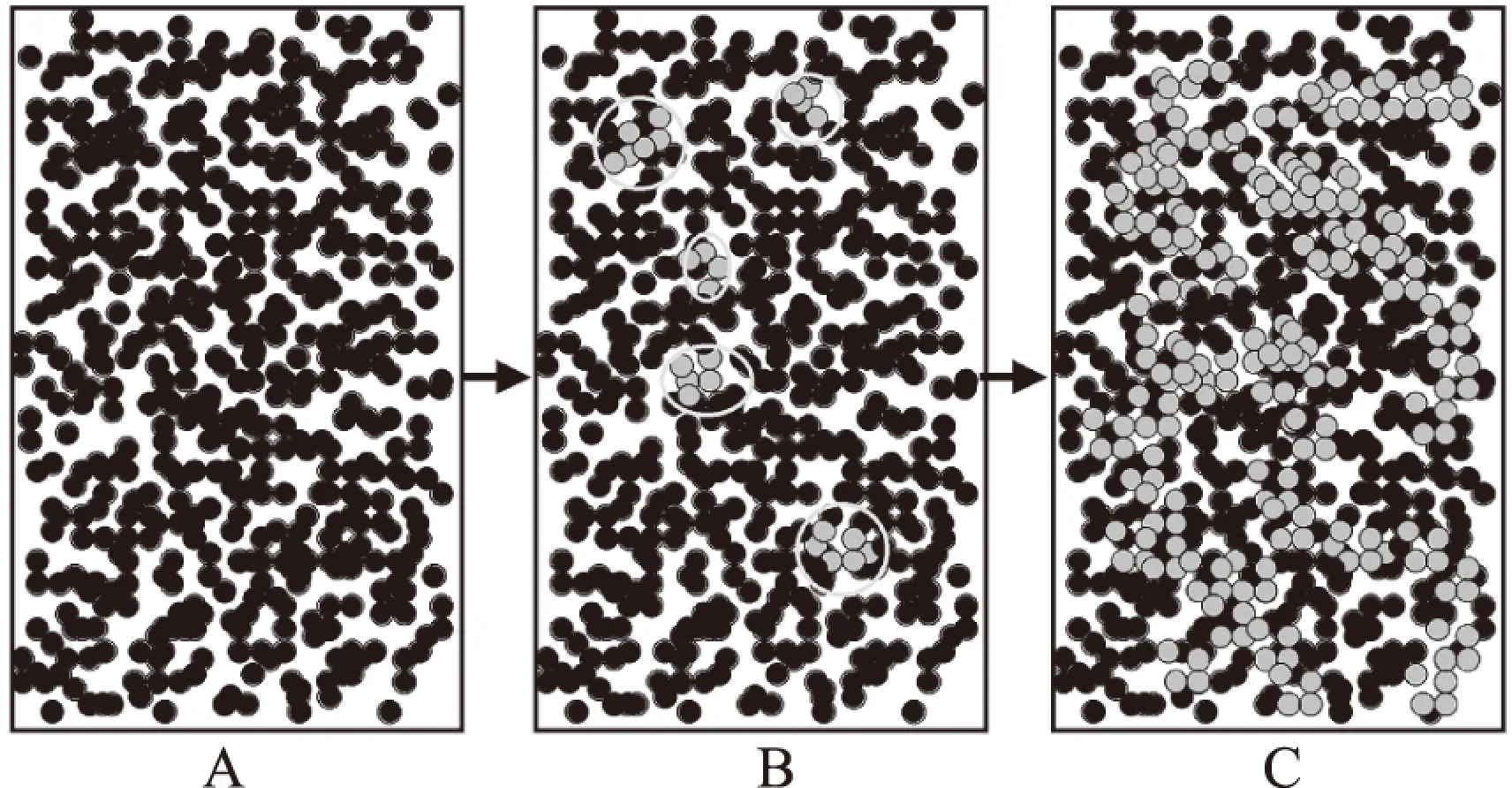
图2 模型系统中二硫键引起的蛋白质聚集[31]Fig.2 Protein aggregation caused by disulfide bonds in model systems[31]注:A:新编制的模型系统;B:形成单独的蛋白质聚集体; C:形成聚集体网络。图中的黑色球代表没有聚集的 蛋白质分子或颗粒,灰色球代表聚集的 蛋白质分子或颗粒(主要是分子间二硫键)。
2.5 美拉德反应引起蛋白聚集
美拉德反应是指氨基化合物和羰基化合物之间的一类化学反应[40]。高蛋白营养棒富含蛋白质,并且添加了糖类作为增塑剂,因此,产品在长期贮藏过程中,蛋白质与还原糖之间可能发生美拉德反应,使得蛋白质分子糖基化,产生不溶性聚集体,导致营养棒硬化[41]。由于高蛋白营养棒水分活度处在0.5~0.6之间,美拉德反应在水分活度为0.6~0.8区间内会快速进行[42],因此,营养棒在储藏期间容易发生美拉德反应。
美拉德反应会对营养棒的质地、外观、营养价值以及风味等都产生一定的影响,甚至会产生对人体有害的羧甲基赖氨酸[20]。美拉德反应引起的蛋白聚集在储藏前期影响不大,可能是由于参与反应的一些赖氨酸残基位于蛋白质的内部或者位于无法结合的位点上,因此,不能与葡萄糖或乳糖分子结合发生反应[19]。而随着储藏期的延长,水分在整个体系中的迁移与蛋白质水合,增加了蛋白质的柔韧性以及小分子还原糖迁移到蛋白质空间内部与氨基结合的可能性,因此,有研究认为储藏后期蛋白质分子共价交联产生的蛋白聚集体是使得营养棒硬度大幅增加的主要原因[43-44]。
3 抑制高蛋白营养棒储藏期内硬化的方法
3.1 添加蛋白质水解物
高蛋白营养棒在所有的营养棒中蛋白质含量是最高的,虽然能够补充更高的能量,但事实上蛋白质的浓度与体系的硬度有密切的关系。蛋白质颗粒具有不同的临界体积分数(φ),当体系添加的蛋白质高于该临界值,营养棒体系会保持颗粒状或粉末状;当低于该临界值体系具有太高的流动性,所以添加量应保证体系能有足够保持应力而不发生形变[9]。研究证实水解蛋白在不同的pH和温度下都具有更高的溶解度,多蛋白混合使用比单一蛋白体系能更好的控制硬度的变化[45],可能是由于水解乳清蛋白会产生氨基酸和多肽段[24]。当完整蛋白与部分水解的乳清分离蛋白配合使用时,水解蛋白由于具有较高的吸湿性以及较低的玻璃态转变温度,能够在液相中吸收更多的水分,保持蛋白质-水-PHCs系统的稳定,减缓了不同相之间的分离,保持了柔软的质地,延长了产品的货架期[26,46]。
Mcmahon等[24]分别使用不同水解程度的乳清蛋白分离物与乳清分离蛋白制成营养棒并进行储藏加速试验,研究发现当蛋白质水解物添加到配方中时,营养棒容易成型且变得更有柔韧性。在储藏期间,蛋白质水解物的添加量极显著影响营养棒的硬度(P<0.001)。Rao等[47]探究了牛酪蛋白及其水解物对营养棒储藏期硬度的影响,发现乳清分离蛋白营养棒储藏28 d硬度超过12 N(超过12 N时消费者难以接受),而含有牛酪蛋白或酪蛋白水解物的营养棒储藏35 d后未达到12 N。当用酪蛋白代替10%(w/w)的乳清分离蛋白储藏35 d 后营养棒的硬度比乳清分离蛋白模型的硬度降低了约54%,产生的原因可能是水解物可抑制二硫键诱导的蛋白质聚集,从而对存储过程中营养棒的硬度产生影响。同时有研究发现由更多亲水性蛋白质制成的营养棒硬度适中,在存储过程中更稳定[26]。因此,在营养棒制备过程中使用水解蛋白部分替代完整的蛋白质能有效的降低储藏期硬度的增大,但有一些水解产物由于自身的苦味会导致营养棒的口感下降,同样影响高蛋白营养棒的口感。
3.2 改变蛋白质的性质
使用含量为80% 的浓缩乳蛋白(milk protein concentrate powder with 80% protein,MPC80)配制成的高蛋白营养棒在储藏过程中会快速的变硬[48-49]。浓缩乳蛋白(milk protein concentrate,MPC)中酪蛋白含量在80%以上,且酪蛋白大多以酪蛋白胶束的形式存在,在储藏过程中相邻的酪蛋白胶束之间交联,提高了粉末表面的疏水性,表面疏水性的增加和酪蛋白胶束相互作用导致粉末的表面形成了一层由熔融酪蛋白胶束的薄层组成的皮层,水分较难渗透,使得酪蛋白复水性能较差,影响体系中的水分子等小分子迁移,导致制作形成的营养棒硬度较大,口感粗糙[45,50]。
蛋白质的粒径会影响颗粒比表面积,酪蛋白胶束中的一些慢溶解成分限制了复水性的速率,提高颗粒的亲水性会提升MPC的复水性[50-51]。在余韵[50]的实验中,通过喷雾干燥时雾化小液滴获得小的MPC颗粒粒径,结果发现,小粒径蛋白粉末的溶解度高于大粒径的溶解度,并且陈化后的小粒径蛋白粉末的溶解度下降值明显小于大粒径的溶解度下降值,在后期的储藏期间内粒径越小的体系形成均一稳定相的速率要快于大粒径的样品,陈化后也是如此;通过离子交换脱钙处理调控酪蛋白胶束的状态,发现脱钙率与胶束解离程度呈现正相关趋势,在脱钙率达到28.3%时,体系稳定且硬度适中;通过添加磷脂囊泡调节蛋白颗粒的亲水性,发现添加的磷脂量越多,体系中水分子等小分子的迁移速率越快,当添加量为10%时,营养棒体系的硬度得到极大改善。Banach等[51]将含量为85%蛋白质(milk protein concentrate powder with 85% protein,MPC85)的浓缩乳蛋白进行气流粉碎和冷冻干燥,通过研磨可以暴露出蛋白颗粒掩盖的疏水性残基而增加MPC85的表面疏水性,除去内部堵塞的空气,使营养棒体系中有更多的颗粒堆积,提升颗粒的再水化能力而改善了体系成分之间的内聚力。实验结果证实细磨的MPC85比未处理的MPC85配制的营养棒更有内聚力不易断裂,且储藏期间也不易发生质地硬度的变化。Banach等[52]通过挤压和烘烤对MPC80进行了改性,通过挤压和烘烤改变了MPC80中游离巯基含量,减少了内部聚集并降低了储存期间的蛋白质的溶解度,实验结果发现在42 d的存储期内,使用改性的MPC80配制的营养棒只观察到有限的微观结构变化,溶解度降低同时组分之间的相变轻微,因此可能是通过减缓组分之间的相分离减缓了营养棒的硬化。与未经处理的MPC80相比,在75或110 ℃烘烤4 h的MPC80产生的营养棒分别具有最小的纹理变化和增加的断裂力[7,53],经挤压得到的MPC80与喷雾干燥的MPC80相比,MPC80粉末具有较宽的粒径分布,质地更柔软,储藏期较稳定且粘结性能好[48]。通过挤压作用,MPC80中相邻蛋白质之间的二硫键以及蛋白质糖基化作用增强,显著降低了蛋白质的游离巯基(P<0.05)和游离胺(P<0.05)的浓度,使得反应性能降低,同时通过提升蛋白湿润性,挤压得到的MPC80更容易发生水合,但是在储藏期间由美拉德反应形成的聚集体更加普遍[54]。
转谷氨酰胺酶(Transglutaminase,TGase)通过将谷氨酰胺残基与蛋白内或蛋白间的赖氨酸残基交联来进行蛋白修饰,使其具有更高的持水能力。交联的蛋白质成分具有较少的胺基团可用于参与美拉德反应,很有可能限制储藏阶段硬度的增加[55]。Banach等[56]通过转谷氨酰胺酶制备出低交联和高交联的MPC营养棒,在储藏阶段发现Tgase交联蛋白降低了营养棒的硬度,并降低了易碎性,但随着时间的延长硬度的增加与未修饰的相比差距不大,长期储存中没有优势。
3.3 半胱氨酸抑制二硫键生成
Zhou等[18]通过加入DTT证实了二硫键与硬度变化的关系,如果可以防止蛋白质粉末中巯基-二硫键交换反应,则可以抑制营养棒的硬化,从而延长保质期,但是目前通过抑制或破坏二硫键来抑制储藏期营养棒硬化的研究并不多。
DTT是一种带有毒性的二硫键分离剂,不允许加入到食品中。一些游离的巯基封闭剂,如N-乙基马来酰亚胺(N-Ethylmaleimide,NEM)、2-碘乙酰胺或碘乙酸也同样因为毒性而不能作为添加剂发挥有效的抑制作用[26]。可以通过降低pH到6以下降低乳清分离蛋白溶液中的硫醇-二硫键交换反应,但是,由于营养棒体系的水分活度不高,若将pH降低至6以下时,可能导致pH接近乳清蛋白的等电点,使蛋白更容易析出产生聚集,因此这个方法也不一定有效。半胱氨酸(Cysteine,Cys)作为一种食品添加剂可以抑制美拉德反应,能够增加食品的亮度,还可以通过硫醇-二硫键交换反应裂解二硫键并增加蛋白质凝胶强度[57]。Wang等[58]发现半胱氨酸能够封闭二硫键,导致球形蛋白解折叠,从而降低了凝胶硬度。Zhu等[10]对半胱氨酸进行了试验,发现在储藏初期添加Cys和NEM后营养棒的硬度明显的降低,在35 d的储藏期后,添加Cys的营养棒硬度值变化比未添加Cys的变化幅度小,而添加过量的Cys却加速了营养棒硬度的增加,这说明适量添加Cys对硬度的变化有控制作用。因此,在高蛋白营养棒的配制时,可以适量添加半胱氨酸延长货架期。
3.4 抑制美拉德反应
研究证实晚期糖基化终末产物(advanced glycation end products,AGEs)的形成与营养棒储藏过程中褐变与硬化之间有直接的关系[19]。多酚类物质能够与蛋白质通过特异性相互作用发生可逆性与不可逆性的结合,进而改变蛋白质分子的表面性质和影响蛋白分子的抗氧化性与糖基化程度[59-60]。一些多酚类物质例如白藜芦醇,表儿茶素,迷迭香酸和槲皮素等被认为在面包与饼干等食品中模型中作为AGEs抑制剂[61-62]。Khalifa等[63]探究了微囊化的桑果多酚(microencapsulated mulberry polyphenol,MMP)对乳清蛋白营养棒体系储藏期硬度的变化,发现不同比例的MMP在储藏期抑制了蛋白模型中荧光AGEs的生成,储藏45 d后20%添加量的MMP降低了66.79%的AGEs形成,并有效减缓了营养棒硬度的增加。这是由于MMP能够通过氢键和π-π相互作用与乳清蛋白亚基片段发生作用阻止了乳清蛋白的糖基化反应,减缓了高蛋白营养棒储藏期的硬度变化。但谷满屯[64]探究发现,白藜芦醇在营养棒体系储藏后期对美拉德反应的抑制效果开始显现,但是对硬度变化的影响较小。
3.5 降低分子迁移
分子迁移在高蛋白模型中前期硬化的一个主要原因,因此,最小化分子迁移是控制高蛋白营养棒硬化的一个方法,但是对这方面进行的相关研究也较少。为了避免食品中因水分迁移而造成的物理反应和化学变化,解决方案之一在于限制成分之间存在的水分活度梯度,通常使用能够与水发生相互作从而降低最高相对湿度相的水分活度的溶质来实现,如糖、盐或多元醇等。湿润剂的使用通常受到溶解度,反应性,对质地和味道等影响的限制[28,65]。
水胶体是食品工业中广泛使用的水溶性多糖,可以改善食品的微观结构和物理特性[66]。Li等[35]探究不同水胶体对营养棒体系的硬度影响,发现黄原胶(xanthan gum,XG)能够有效降低由酪蛋白酸钠配制的营养棒的硬度变化,且效果与XG的浓度呈现正相关趋势。这可能是由于XG等水胶体的存在会与酪蛋白酸钠颗粒竞争水,并保留在蛋白质颗粒的间隙中,而较少的水会迁移到蛋白颗粒中,降低了酪蛋白颗粒的水合作用,进而保持硬度的稳定。Meng等[67]发现使用二氧化硅(SiO2)和磷酸钙(Ca3(PO4)2)等抗结块剂能够降低浓缩乳蛋白制备的营养棒的硬度,可能是因为抗结块剂会通过空间位阻在吸湿性颗粒表面形成了水分屏障或在蛋白颗粒之间形成了物理屏障[68],同时抗结块剂会与蛋白颗粒竞争水,减少了蛋白颗粒的水合作用,抑制了水分等小分子在组分之间的转移,控制了硬度的增加。
除此以外,现阶段还有一些新型的保存中间水分食品的方法,例如创新的渗透脱水技术,电渗透脱水,高压处理和气调包装等[69],但是高蛋白营养棒体系与常规的中间水分食品还是有一定的区别,这些储藏措施是否会对营养棒的硬度有所影响仍需进一步的试验探究。
4 展望
综上所述,高蛋白营养棒在储藏期硬度的变化是一个复杂的变化过程,涉及到前期的物理变化以及中后期的化学反应,通过抑制分子迁移、控制二硫键生成、改变蛋白质的性质以及抑制美拉德反应等措施控制储藏期硬化已初见成效,那么如何在保持营养棒的口感、营养和质地的前提下,开发新型、能量高、抗硬化的高蛋白营养棒可能是未来研究的方向。
