愈肝散结方联合华蟾素注射液治疗中晚期原发性肝癌的临床研究
2021-06-11刘伟侯爱画黄晓明马春燕谭松孙敏
刘伟, 侯爱画, 黄晓明, 马春燕, 谭松, 孙敏
烟台市中医医院,山东 烟台 264001
2020年原发性肝癌全球新增病例约90.6万,死亡病例约80万例,其死亡数位于所有癌症死亡第三位[1]。原发性肝癌在我国高发,是常见恶性肿瘤第四位和所有肿瘤第二位的致死病因。原发性肝癌的治疗手段有手术、介入、射频消融、化疗、靶向、免疫治疗、中医药治疗。目前手术及介入治疗是治疗肝癌的最有效方法,但大部分肝癌确诊时已经属于中晚期,丧失了外科手术及局部治疗的机会。以仑伐替尼、索拉非尼、瑞戈非尼等为代表的靶向药物,免疫检查点抑制剂阿替利珠单抗联合抗血管生成药物贝伐珠单抗、阿帕替尼联合卡瑞利珠单抗以及以奥沙利铂为主的化疗药物均为指南所推荐,但直至2021年3月仑伐替尼和免疫治疗药物卡瑞利珠单抗才进入医保,本研究开始时除索拉非尼外其余药物均未进入医保,且药物可及性较差,大部分小城市及农村地区的肝癌患者药物选择范围仍很窄,患者生活质量差。2010年CSCO年会上报告的研究表明,采用FOLFOX4方案治疗晚期肝癌,在无进展生存期和总生存期及疾病控制率等方面相对于阿霉素单药更优[2],因此被指南推荐应用。而中医药有价格低廉、使用方便等优点,在烟台市中医医院肿瘤科广泛应用,取得良好临床疗效。愈肝散结方为我科运用多年的治疗肝癌的经验方,为我院国家级名中医传承工作室专家、全国中医传承工作室指导老师孙敏教授经验方,此方有着疏肝健脾,养阴柔肝,化痰祛瘀,解毒散结的作用,前期研究显示临床疗效显著[3,4]。华蟾素注射液临床疗效确切,为治疗肝癌的常用中成药制剂。二者联合应用在我科应用多年,前期临床观察取得较好临床疗效,故自2017年开始进行此项研究,观察愈肝散结方联合华蟾素注射液与FOLFOX4方案化疗治疗中晚期原发性肝癌的疗效,现报告如下。
1 资料与方法
1.1 研究对象
此随机对照试验在山东省烟台市中医医院进行。选取2017年3月至2019年10月在我院就诊的130例中晚期肝细胞癌患者,采用随机数字表法进行分组,试验组65例,对照组65例。研究者知情同意研究方案并签署书面知情同意书。本试验通过烟台市中医医院伦理委员会批准(伦理审批号:2017-383)。
1.2 病例选择标准
纳入标准:(1)18~75岁,签署知情同意书,依从性好,可随访者;(2)病理组织学或细胞学检查证实为肝细胞肝癌,或影像学加甲胎蛋白(AFP)检查符合全国统一的临床诊断标准并诊断为Ⅲ期、Ⅳ期中晚期肝癌;(3)因病情不适合或者个人原因无法行介入、靶向药、免疫药物治疗;(4)其血液学和生化指标在以下范围内:中性粒细胞绝对计数≥1.5×109/L,血小板≥80×109/L,血清肌酐<110 μmol/L,总胆红素≤1.5UNL(正常上限),谷丙转氨酶、谷草转氨酶和碱性磷酸酶≤3UNL;(5)预计生存期≥3个月;(6)所有患者均至少有一个可测量的肿瘤病灶,复治患者与末次治疗时间至少已间隔4周以上;(7)卡氏评分(karnofsky performance status,KPS)在60分以上者。
排除标准:(1)合并有其它恶性肿瘤者;(2)急性心、脑血管病者,有严重外伤或接受手术者,严重感染者;(3)患精神障碍疾病不能配合研究者;(4)严重慢性胃肠道疾病者。
剔除标准:(1)由于主观或客观原因中途停止治疗或病情恶化死亡者;(2)临床或实验室资料不全无法判定疗效者;(3)治疗过程出现非肿瘤原因导致的死亡者;(4)依从性差,不能配合治疗者。
1.3 治疗方法
治疗组:给予愈肝散结方口服联合华蟾素注射液静滴治疗。愈肝散结方组成:鳖甲15 g、龟板15 g、八月札15 g、山慈菇15 g、茯苓20 g、白术15 g、大枣10 g组成,采用北京康仁堂药业有限公司的中药配方颗粒,不需煎煮,预混包装,即冲即服。用法:每天两次,早晚各一次,每次一包,温水冲服,持续应用至华蟾素注射液治疗疗程全部结束。华蟾素注射液:为安徽金蟾生化股份有限公司生产的,生产批号为Z34020274。用法:因华蟾素注射液对外周静脉刺激较重,所有患者给予经外周静脉置入中心静脉置管(Peripherally Inserted Central Catheter,PICC),华蟾素注射液30 ml+5%葡萄糖500 ml静脉滴注,1天1次,21天为1个疗程,休息1周后重复使用,每4周1个疗程,若病情未进展或未出现不可耐受毒性,则可应用4个疗程,至少完成2个疗程后评价,部分肿瘤标志物明显升高或症状明显加重患者可提前复查。
对照组:采用标准的FOLFOX4方案化疗。即奥沙利铂85 mg/m2iv,d1;亚叶酸钙200 mg/m2iv 2 h,d1、d2;5-FU,400 mg/m2静推,d1、d2;继以600 mg/m2持续静滴22h,d1、d2。14天为1周期,2周期为1疗程。系统化疗持续至患者出现病情进展或不可耐受的毒性反应,如病情未出现进展或不可耐受的毒性,则可应用4个疗程。化疗前常规给予5-羟色胺3受体拮抗剂预防性止吐。至少完成2个疗程后评价,部分AFP持续升高或症状明显加重患者可提前复查。
1.4 疗效判定
治疗前进行基线评价,包括年龄、性别、分期、肿瘤单发及多发、肝功能分级、KPS评分、中医证候积分等。疗效评价在治疗后每8周进行,采用实体肿瘤评价标准RECIST1.1进行评价:完全缓解(complete response,CR):所有目标病灶消失;部分缓解(partial response,PR):基线病灶长径总和缩小30%;疾病稳定(stable disease,SD):基线病灶长径总和有缩小但未达PR或有增加但未达PD;疾病进展(progressive disease,PD):基线病灶长径总和增加20%或出现新病灶。电话随访间隔为半个月,总随访时间为12个月。评价目标包括两组的客观缓解率(objective response rate,ORR)、疾病控制率(disease control rate,DCR)、中位生存期(Median overall survival,mOS)、中位无疾病进展生存期(Median progression free survival,mPFS)、KPS评分、中医症状的变化以及进行安全性评价。ORR=(CR+PR)/总例数×100%,DCR=(CR+PR+SD)/总例数×100%。中医证候疗效按照《中药新药临床研究指导原则》制订:把腹胀、乏力、纳呆、便溏、情志抑郁等按照轻中重分别记为1、2、3分,治疗前后按照积分值进行疗效评价:(1)显效:临床中医证候积分下降≥70%;(2)有效:30%≤临床中医证候积分下降<70%;(3)无效:临床中医证候积分下降<30%或上升。有效率=(显效+有效/总数)×100%。
1.5 统计学方法
采用SPSS19.0软件进行统计分析,计量资料将采用均数±标准差进行统计描述,计数资料采用绝对数(频数)与相对数(率、比)进行统计描述,组间比较:二分类变量采用卡方检验,单向有序多分类变量(等级资料)采用Ridit分析或秩和检验;生存分析采用Kaplan-Meier、Log Rank方法、寿命表法等。以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料
在治疗过程中因各种原因产生脱落病例22例,其中治疗组脱落10例(无法耐受愈肝散结方味道拒绝继续用药3例,因华蟾素注射液引起胃肠道反应拒绝继续用药2例,依从性差、不能每天服用愈肝散结方5例),对照组脱落12例(因家庭原因拒绝继续治疗3例,因手足麻木拒绝继续治疗3例,依从性差、不按时返院治疗4例,资料不全2例),最后可评价疗效108例,其中治疗组55例,对照组53例。两组研究对象的性别、年龄等一般资料比较,差异无统计学意义(P>0.05),具有可比性(见表1)。
表1 两组患者的基线特征(±s)Table 1 Baseline characteristics of two groups
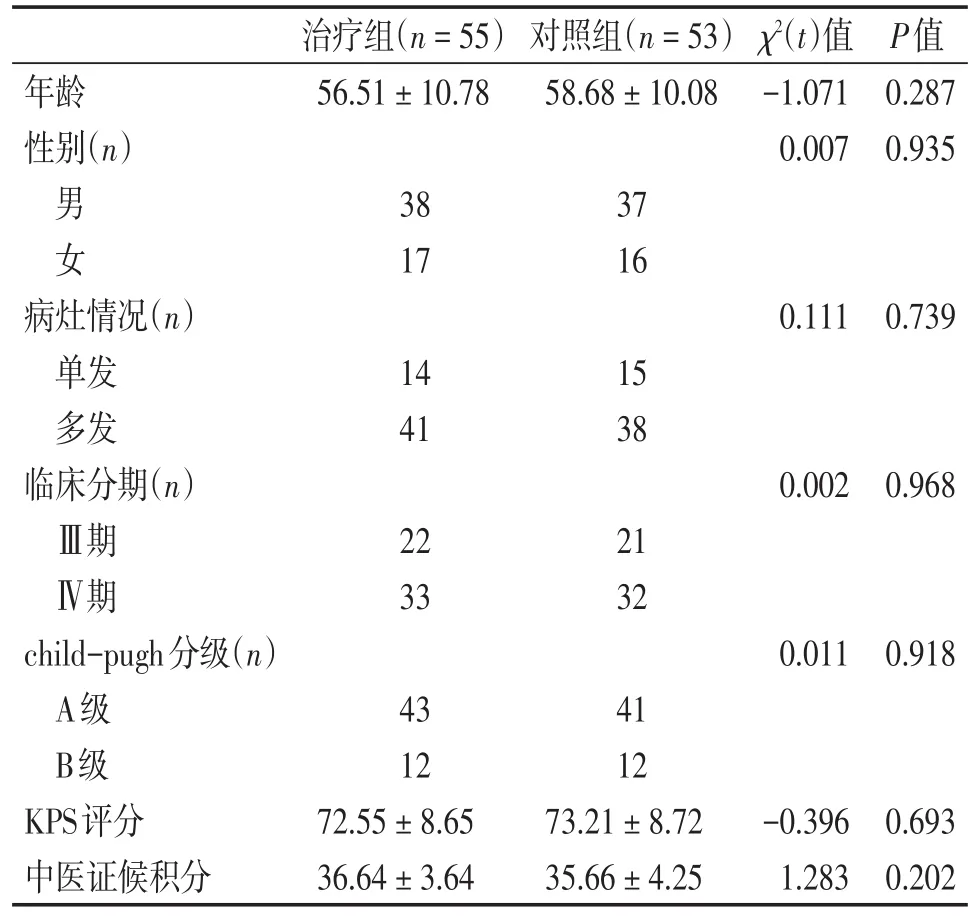
表1 两组患者的基线特征(±s)Table 1 Baseline characteristics of two groups
年龄性别(n)治疗组(n=55)56.51±10.78对照组(n=53)58.68±10.08 χ2(t)值-1.071 0.007 P值0.287 0.935男女38 17 37 16病灶情况(n)单发多发临床分期(n)Ⅲ期Ⅳ期child-pugh分级(n)A级B级KPS评分中医证候积分0.1110.739 14 41 15 38 0.0020.968 22 33 21 32 0.0110.918 43 12 72.55±8.65 36.64±3.64 41 12 73.21±8.72 35.66±4.25-0.396 1.283 0.693 0.202
2.2 两组疗效比较
两组患者经治疗后,瘤体的变化情况如下:治疗组CR 0例,PR 8例,SD 20例,PD 27例,ORR为14.5%,DCR为50.9%;对照组CR为0例,PR为8例,SD为16例,PD 29例,ORR为15.0%,DCR为45.3%,经统计学分析,两组差异无统计学意义(P>0.05)(见表2)。

表2 两组治疗后瘤体变化情况Table 2 Changes of tumor after treatment in two groups
2.3 两组患者的无进展生存期
治疗组的中位无进展生存时间为3.5个月,对照组的中位无进展生存时间为3.3个月,经统计学分析,两组差异无统计学意义(P>0.05)(见表3,图1)。
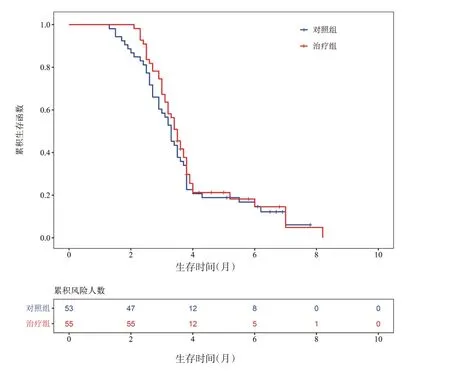
图1 两组患者的无进展生存期的比较Figure 1 Comparison of progression-free survival between two groups
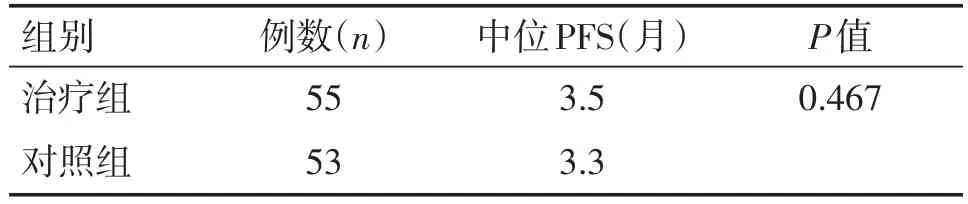
表3 两组患者的中位PFSTable 3 Median progression free survival of two groups
2.4 两组患者的中位生存时间
截止到随访时间结束,治疗组共有47人出现统计终点(肝癌死亡),对照组有44人出现统计终点(肝癌死亡),治疗组的中位OS为7.9个月,对照组的中位OS为7.5个月,经统计学分析,两组差异无统计学意义(P>0.05)(见表4,图2)。
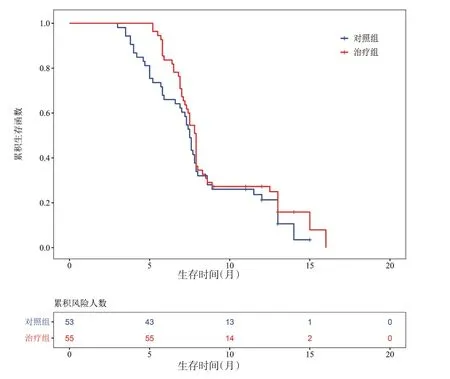
图2 两组患者的中位生存时间的比较Figure 2 Comparison of median overall survival between two groups

表4 两组患者的中位OSTable 4 Median overall survival of two groups
2.5 两组KPS比较
经治疗后,治疗组KPS评分较治疗前升高,治疗前后差异有统计学意义(P<0.01)。对照组KPS评分较治疗前降低,治疗前后差异有统计学意义(P<0.01)。比较两组治疗前后差值,差异有统计学意义(P<0.01)(见表5)。
表5 两组患者KPS评分(±s)Table 5 KPS score of two groups

表5 两组患者KPS评分(±s)Table 5 KPS score of two groups
组别治疗组对照组例数55 53治疗前72.20±8.87 73.33±8.83治疗后79.09±5.19 69.62±9.40 P值(治疗前后比较)<0.001 0.005
2.6 两组中医证候及中医症状改善情况比较
2.6.1 中医证候疗效比较
对治疗前后的中医证侯积分分析,治疗组显效为9例,有效为35例,无效为11例,有效率为80%。对照组显效的为8例,有效为22例,无效为23例,有效率为56.6%。经统计学分析,两组差异有统计学意义(P< 0.05)(见表6)。

表6 两组患者中医证候疗效比较[n(%)]Table 6 Comparison of TCM syndrome efficacy
2.6.2 中医证候积分比较
两组患者的中医证候积分在经过治疗后均有降低,但治疗组的中医证侯积分的下降更为明显,经统计学分析,两组治疗前后积分差值比较差异有统计学意义(P<0.05)(见表7)。
表7 中医证候积分比较(±s)Table 7 Comparison of TCM syndrome score

表7 中医证候积分比较(±s)Table 7 Comparison of TCM syndrome score
组别治疗组对照组例数55 53治疗前36.64±3.64 35.66±4.25治疗后25.13±7.24 28.25±8.34 P值(治疗前后比较)<0.001<0.001
2.6.3 中医症状改善情况比较
经统计分析,治疗组主要在腹胀、乏力、纳呆、便溏、情志抑郁等症状方面,具有明显改善。对照组在相关症状方面没有明显改善(表8)。
表8 两组中医主要症状改善情况(±s)Table 8 Improvement of main TCM symptoms in two groups
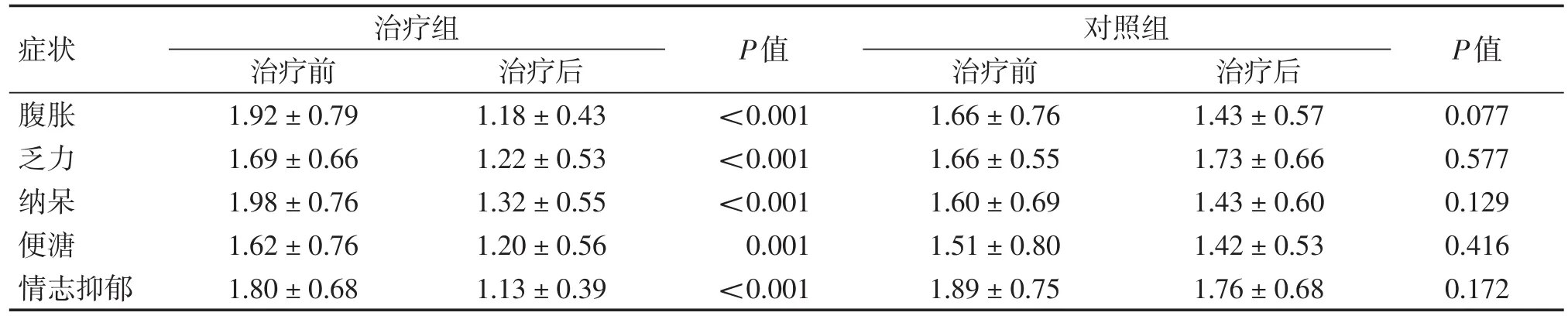
表8 两组中医主要症状改善情况(±s)Table 8 Improvement of main TCM symptoms in two groups
注:P值为各组治疗前后比较。
症状腹胀乏力纳呆便溏情志抑郁P值0.077 0.577 0.129 0.416 0.172对照组治疗组治疗前1.92±0.79 1.69±0.66 1.98±0.76 1.62±0.76 1.80±0.68治疗后1.18±0.43 1.22±0.53 1.32±0.55 1.20±0.56 1.13±0.39 P值<0.001<0.001<0.001 0.001<0.001治疗前1.66±0.76 1.66±0.55 1.60±0.69 1.51±0.80 1.89±0.75治疗后1.43±0.57 1.73±0.66 1.43±0.60 1.42±0.53 1.76±0.68
2.7 两组不良事件比较
治疗组与对照组相比,在白细胞减少、消化道反应、肝功能损害、心脏毒性、神经毒性方面,治疗组明显少于对照组(见表9)。
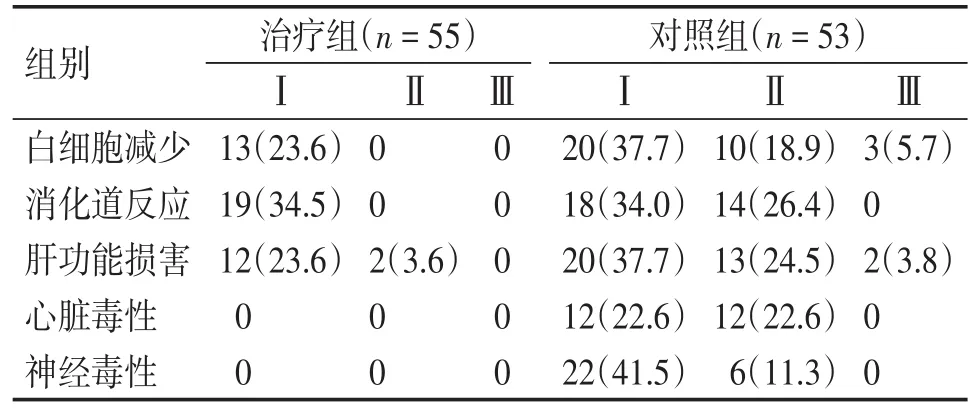
表9 两组不良事件发生情况比较[n(%)]Table 9 Comparison of adverse events between two groups
3 讨论
肝癌为全球范围内高发病率、高病死率的恶性肿瘤之一,在我国大部分肝癌患者诊断时即为中晚期,无手术及介入治疗机会[5],因此预后差。中华医学会推荐FOLFOX4方案为肝功能Childpuhg A级或较好的B级(小于等于7分)患者的一线治疗,但由于其一些不良反应发生率较高,限制了其应用。
愈肝散结方为我院肿瘤科应用十余年的经验方,临床观察疗效确切,且有多项研究证实了此方的有效性及安全性[3,4]。此方为我院孙敏教授经验方,孙教授认为肝癌的病因为情志不舒,肝气郁结,肝郁犯脾,脾失健运,痰湿瘀血阻滞,或者肝炎邪毒损伤,气机不畅,血行受阻,湿热瘀毒阻滞所致,提出肝癌总病机“肝郁脾虚、湿瘀痰毒”学说。肝主疏泄,肝体阴而用阳,故应注重疏肝理气与养阴柔肝并用,标本兼治,以恢复肝主疏泄之功能;“见肝之病,知肝传脾,当先实脾”,且脾未后天之本,气血生化之源,脾主运化,脾之运化功能正常,则气血运行流畅,湿瘀毒邪有出路,从而缓解病情。其提出治法为“疏肝健脾,养阴柔肝,化痰祛瘀,解毒散结”。在此理论基础上组方的愈肝散结汤,组成药物为鳖甲、龟板、山慈菇、八月札、茯苓、白术、大枣,具有疏肝健脾,养阴柔肝,化痰祛瘀,解毒散结的功效,体现了“肝脾同调”的治疗大法及“扶正祛邪”治疗原则。方中鳖甲滋养肝阴,软坚散结;龟板滋阴潜阳,益肾健骨,体现“滋水涵木”思想;山慈菇消肿散结、化痰清热解毒;八月札疏肝理气、软坚散结;白芍养阴柔肝,缓急止痛;茯苓、白术健脾化湿,培助“后天之本”,肝脾同治;大枣补中益气,养血安神。方中各药经现代药理研究证实均有一定调节免疫力和抗肿瘤作用,如鳖甲在提高机体的免疫力、抗肿瘤等方面具有较好的临床功效[6]。山慈菇具有抗肿瘤、抗新生血管形成的作用,临床上可以应用于多种肿瘤的治疗[7]。龟甲,别名龟板,为乌龟的背、腹甲,具有提高细胞免疫及体液免疫功能的作用[8]。八月札,别称预知子,有研究检测出八月札含有三萜及皂苷类物等物质,其具有抗肿瘤、抗炎等作用[9]。茯苓的有效成分可以抑制抗肿瘤药物的耐药[10]。大枣中含有大量的多糖等物质,能够提高巨噬细胞的吞噬作用,还具有诱导肿瘤细胞凋亡的作用[11]。白术能抑制肿瘤细胞增殖,促进机体的免疫功能,包括增强T淋巴细胞的增殖以及体液免疫等作用,从而增加对肿瘤的抑制作用及减少肿瘤细胞侵袭[12]。
华蟾素注射液为中华大蟾蜍的全皮经提取加工制成的水溶性成分,华蟾素的化学成分有蟾毒内酯类、吲哚生物碱类、多肽等。现代药理研究证实,华蟾素注射液可抑制肿瘤细胞增殖,促使其凋亡,还能抑制新生血管形成[13],增强免疫应答[14]。且多项研究证实华蟾素注射液联合中药能减毒增效[15,16]。另外我国大部分肝癌患者具有HBV感染的情况,华蟾素注射液能够起到抗乙肝病毒的作用[17]。而抗病毒治疗在肝癌的综合治疗过程中起到重要作用。我们研究中选用了愈肝散结方联合华蟾素注射液治疗中晚期肝癌,期待取得增效作用。
本研究结果显示,愈肝散结方联合华蟾素注射液在缩小瘤体、稳定瘤体方面,疗效与FOLFOX4方案疗效相当。生存分析治疗组较对照组的mPFS及mOS均有延长趋势,但差异无统计学意义,提示对于中晚期肝癌患者接受愈肝散结方联合华蟾素注射液可达到与化疗相当的生存期。而从生活质量来看,治疗组在改善临床症状(腹胀、乏力、纳呆、便溏、情志抑郁),提高KPS评分方面优于FOLFOX4组,且治疗组不良反应少,特别对于FOLFOX4方案常出现的神经毒性、心脏毒性,治疗组均未出现。提示愈肝散结方与华蟾素注射液的联合应用,能够扶助机体的正气,改善患者的体力状况,减轻患者不适症状,在生活质量更好的情况下得到与化疗相当的生存时间。虽然中医治疗组在缩小瘤体方面不明显,但能有更好的生活质量,起到“带瘤生存”的目的,这正是中医药治疗的优势所在。
