血清suPAR、PBEF、VE-Cad水平与脓毒症所致ARDS患者病情、部分炎性反应指标及预后的关系*
2021-05-26吴莎莎王宗强吴红栋
吴莎莎,杨 帅,沈 超,王宗强,吴红栋
珠海市人民医院/暨南大学附属珠海医院急诊医学部,广东珠海 519000
脓毒症是临床常见的急危重症,全球每年新增约3 150万例脓毒症患者,530万例患者面临死亡威胁[1]。随着老龄化、肿瘤发病率增加、侵入性操作增加,我国脓毒症发病率和病死率呈逐年增加趋势[2]。脓毒症可导致多器官受累,其中急性呼吸窘迫综合征(ARDS)是脓毒症常见并发症之一,可明显加重患者病情,增加患者病死率[3]。炎症瀑布反应、氧化应激诱导的肺泡-毛细血管内皮屏障通透性破坏是ARDS的主要病理基础。可溶性尿激酶型纤溶酶原激活物受体(suPAR)属于纤溶酶原激活物系统,被认为是一种稳定的炎症标志物,参与感染、慢性疾病、肿瘤等多种疾病发病过程[4]。前B细胞克隆增强因子(PBEF)是一种新型促炎因子,可激活下游炎性反应通路,促使炎症因子释放,破坏肺泡上皮和肺毛细血管内皮细胞结构和功能,导致急性肺损伤[5]。血管内皮钙黏蛋白(VE-Cad)是参与内皮细胞连接的最重要黏附分子,在维持血管内皮细胞结构和完整性方面具有重要作用[6]。本研究拟探讨suPAR、PBEF、VE-Cad水平与脓毒症所致ARDS患者病情、其他几项炎性反应指标和预后的关系,旨在为临床病情评估、预后预测提供参考。
1 资料与方法
1.1一般资料 选择2018年7月至2020年6月本院收治的80例脓毒症所致ARDS患者纳入ARDS组。纳入标准:(1)脓毒症诊断参考《中国脓毒症/脓毒性休克急诊治疗指南(2018)》[3];(2)ARDS诊断按照欧洲危重病医学会拟定的ARDS诊断标准进行[7];(3)入住重症监护病房(ICU)治疗,住院时间大于72 h。排除标准:(1)心力衰竭或液体过负荷引起的呼吸衰竭,肺挫伤、严重烧伤、重症胰腺炎等其他因素引起的ARDS;(2)合并肺癌、肺栓塞、肺结核、慢性阻塞性肺疾病等肺部疾病;(3)合并血液系统、免疫系统疾病。另选择同期本院收治的178例住院期间未发生ARDS的脓毒症患者纳入对照组,均排除肺部相关疾病,包括呼吸衰竭、肺癌、肺栓塞、肺结核、慢性阻塞性肺疾病等。两组研究对象一般资料比较,差异无统计学意义(P>0.05),具有可比性,见表1。本研究所有研究对象或其直系亲属均签署知情同意书,且本研究获得本院医学伦理委员会批准。
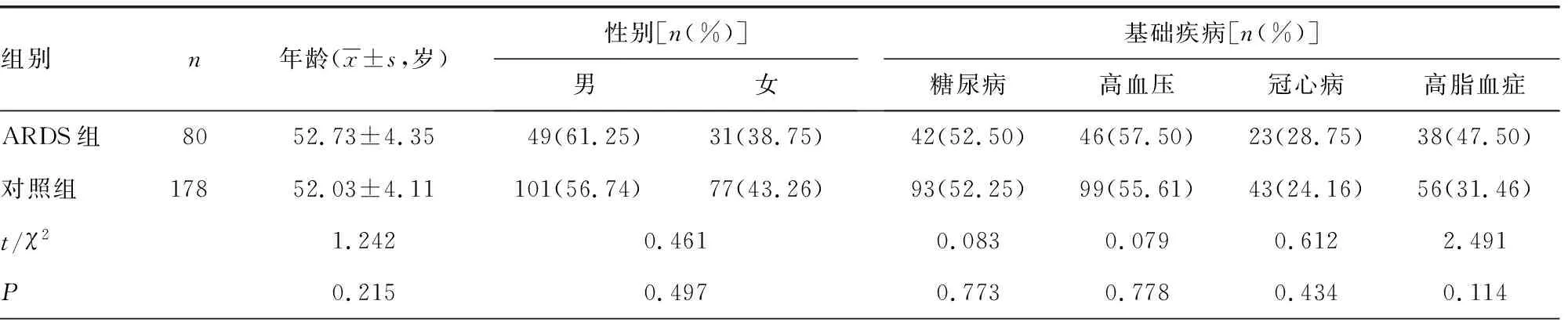
表1 ARDS组与对照组一般资料比较

组别n感染类型[n(%)]泌尿系统感染导管相关血流感染腹腔感染其他脓毒症分级[n(%)]一般脓毒症脓毒症休克ARDS组8046(57.50)53(66.25)28(35.00)12(15.00)40(50.00)40(50.00)对照组17898(55.06)102(57.30)50(28.09)36(20.22)95(53.37)83(46.63)t/χ20.3801.8421.2500.9950.163P0.5380.1750.2640.3190.686
1.2方法 所有研究对象于入院当天上午空腹状态下采集外周静脉血5 mL,注入真空采血管,经3 000 r/min离心10 min(离心半径10 cm),分离血清保存于—80 ℃超低温冰箱。快速解冻血清标本,采用ALISEI全自动酶标仪应用酶联免疫吸附试验法检测血清suPAR、PBEF、VE-Cad水平,试剂盒购自北京科美东雅生物技术有限公司。双抗体夹心酶联免疫吸附试验法检测血清C反应蛋白(CRP)、降钙素原(PCT)、白细胞介素-6(IL-6)水平,试剂盒购自上海蓝基生物科技有限公司,仪器为Model 550酶标仪,仪器购自美国伯乐生命医学产品有限公司。所有操作均按试剂盒说明书严格执行。
1.3观察指标 比较ARDS组与对照组入住ICU 24 h内序贯器官衰竭评估(SOFA)评分、急性生理与慢性健康状况Ⅱ(APACHE Ⅱ)评分,以及suPAR、PBEF、VE-Cad、CRP、PCT、IL-6水平。根据入院24 h氧合指数(PaO2/FiO2),对ARDS组患者进行ARDS分级,分为轻度(PaO2/FiO2:201~300 mm Hg)、中度(PaO2/FiO2:101~<201 mm Hg)、重度(PaO2/FiO2:<101 mm Hg)[7],比较不同ARDS分级患者的血清suPAR、PBEF、VE-Cad水平。 追踪脓毒症所致ARDS患者入院28 d内预后情况,分为生存组和死亡组,并对脓毒症所致ARDS患者预后进行单因素分析及多因素Logistic回归分析。
2 结 果
2.1ARDS组与对照组各项评分及指标比较 ARDS组APACHE Ⅱ评分、SOFA评分及血清suPAR、PBEF、VE-Cad、CRP、PCT、IL-6水平均高于对照组,差异有统计学意义(P<0.05)。见表2。
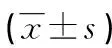
表2 ARDS组与对照组各项评分及指标比较
2.2不同ARDS分级患者血清suPAR、PBEF、VE-Cad水平比较 ARDS组不同ARDS分级患者的血清suPAR、PBEF、VE-Cad水平比较,差异有统计学意义(P<0.05)。血清suPAR、PBEF、VE-Cad水平在轻度、中度、重度患者间依次升高,两两比较,差异有统计学意义(P<0.05)。见表3。
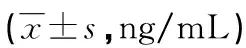
表3 不同ARDS分级患者血清suPAR、PBEF、VE-Cad水平比较
2.3血清suPAR、PBEF、VE-Cad水平与其他几项炎性反应指标及评分的相关性 ARDS组血清suPAR、PBEF、VE-Cad水平与APACHE Ⅱ评分、SOFA评分及CRP、PCT、IL-6水平均呈正相关(P<0.05)。见表4。
2.4影响脓毒症所致ARDS患者预后的单因素分析 80例脓毒症所致ARDS患者入院28 d内死亡31例(38.75%),存活49例(61.25%)。两组年龄、性别、体质量指数、基础疾病、感染部位比较,差异无统计学意义(P>0.05)。死亡组APACHE Ⅱ评分、SOFA评分、脓毒症休克比例及血清suPAR、PBEF、VE-Cad、CRP、PCT、IL-6水平高于存活组,机械通气时间、ICU住院时间长于存活组,脏器衰竭个数多于存活组,差异均有统计学意义(P<0.05)。死亡组ARDS分级以重度为主,存活组以轻度、中度为主,差异有统计学意义(P<0.05)。见表5。
2.5影响脓毒症所致ARDS患者预后的多因素Logistic回归分析 以脓毒症所致ARDS患者28 d存活情况为因变量(赋值:0=存活,1=死亡),以脓毒症分级(赋值:0=严重脓毒症,1=脓毒症休克)、机械通气时间、ICU住院时间、脏器衰竭个数、APACHE Ⅱ评分、SOFA评分、ARDS分级(赋值:1=轻度,2=中度,3=重度)、suPAR、PBEF、VE-Cad、CRP、PCT、IL-6为自变量,建立Logistic回归模型。结果显示ARDS分级(重度)、高APACHE Ⅱ评分及高水平CRP、PCT、suPAR、PBEF、VE-Cad是脓毒症所致ARDS患者不良预后的危险因素(P<0.05),见表6。
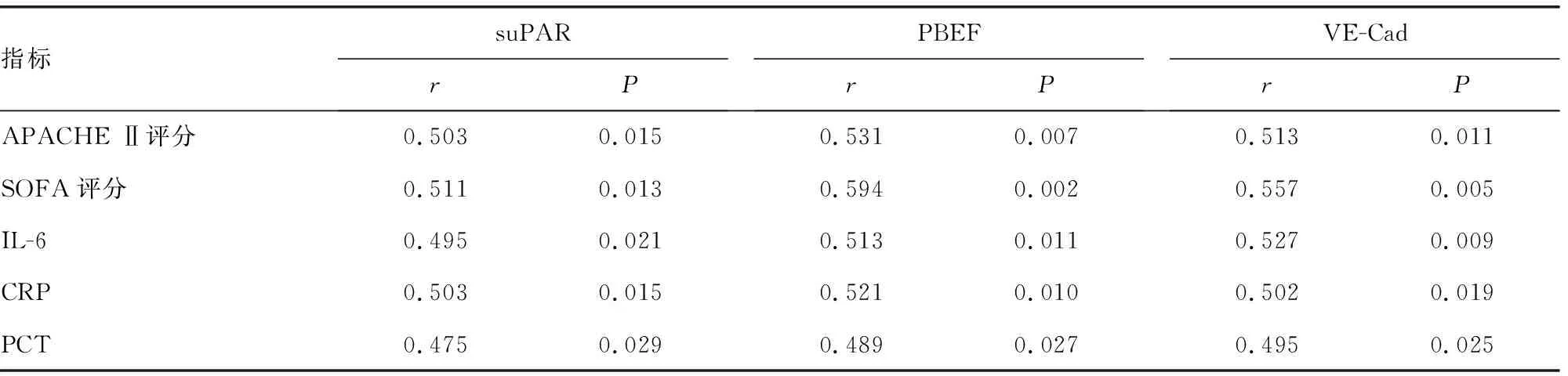
表4 血清suPAR、PBEF、VE-Cad与其他几项炎性反应指标及评分的相关性
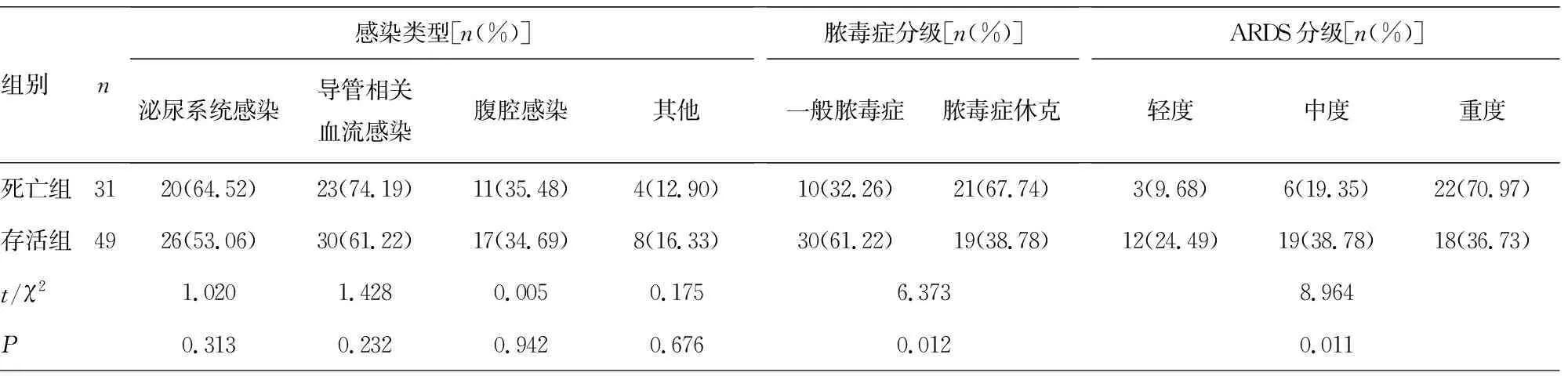
组别n感染类型[n(%)]泌尿系统感染导管相关血流感染腹腔感染其他脓毒症分级[n(%)]一般脓毒症脓毒症休克ARDS分级[n(%)]轻度中度重度死亡组3120(64.52)23(74.19)11(35.48)4(12.90)10(32.26)21(67.74)3(9.68)6(19.35)22(70.97)存活组4926(53.06)30(61.22)17(34.69)8(16.33)30(61.22)19(38.78)12(24.49)19(38.78)18(36.73)t/χ21.0201.4280.0050.1756.3738.964P0.3130.2320.9420.6760.0120.011
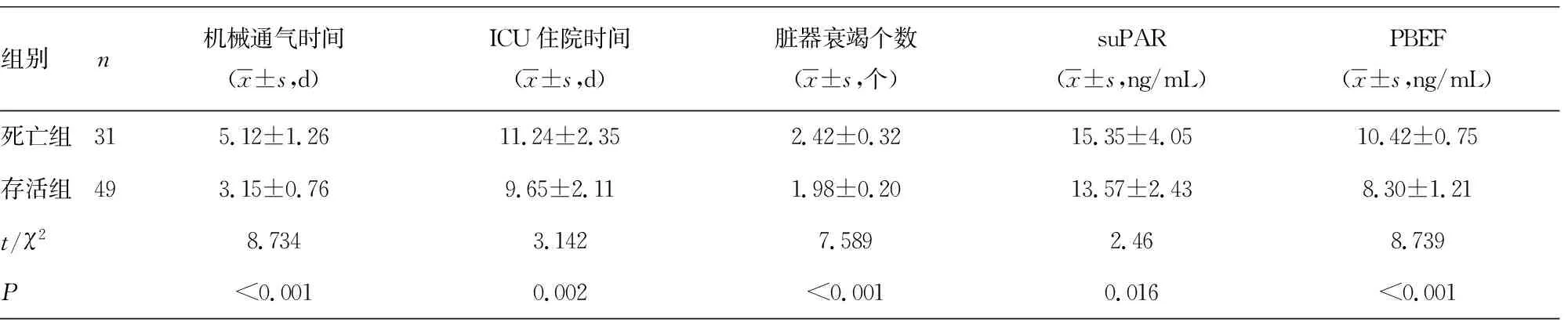
组别n机械通气时间(x±s,d)ICU住院时间(x±s,d)脏器衰竭个数(x±s,个)suPAR(x±s,ng/mL)PBEF(x±s,ng/mL)死亡组315.12±1.2611.24±2.352.42±0.3215.35±4.0510.42±0.75存活组493.15±0.769.65±2.111.98±0.2013.57±2.438.30±1.21t/χ28.7343.1427.5892.468.739P<0.0010.002<0.0010.016<0.001
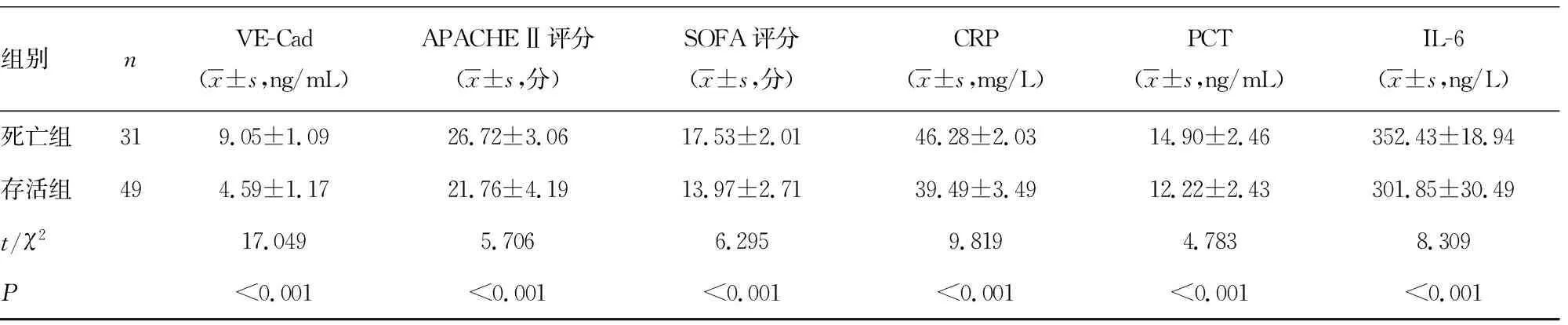
组别nVE-Cad(x±s,ng/mL)APACHE Ⅱ 评分(x±s,分)SOFA评分(x±s,分)CRP(x±s,mg/L)PCT(x±s,ng/mL)IL-6(x±s,ng/L)死亡组319.05±1.0926.72±3.0617.53±2.0146.28±2.0314.90±2.46352.43±18.94存活组494.59±1.1721.76±4.1913.97±2.7139.49±3.4912.22±2.43301.85±30.49t/χ217.0495.7066.2959.8194.7838.309P<0.001<0.001<0.001<0.001<0.001<0.001
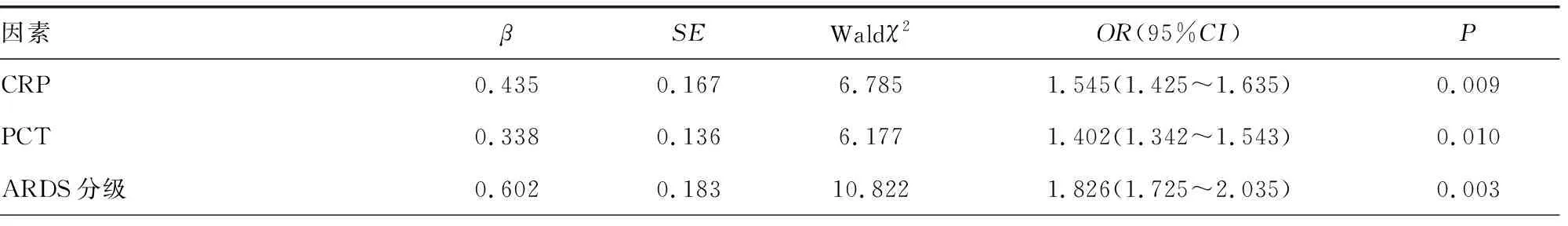
表6 影响脓毒症所致ARDS患者预后的多因素Logistic回归分析
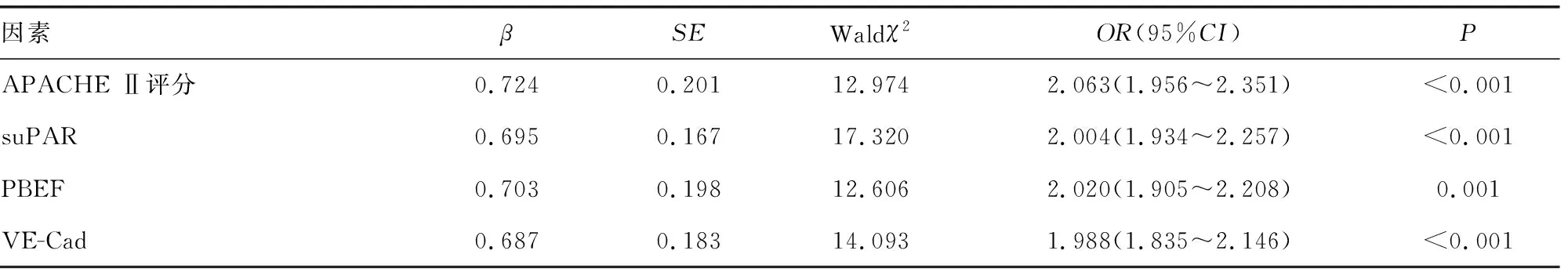
续表6 影响脓毒症所致ARDS患者预后的多因素Logistic回归分析
3 讨 论
脓毒症是一种常见的致命疾病,脓毒症所致ARDS会明显增加患者住院时间[8]。目前,缺乏有效的预防和救治措施,临床治疗以对症支持治疗为主,尽管近年来对ARDS相关分子机制研究不断深入,对ARDS患者的通气策略不断改进,但是其病死率仍居高不下[9]。目前,临床对脓毒症所致ARDS患者的病情和预后的评估通常参考APACHE Ⅱ评分、SOFA评分及临床症状等因素,但均存在一定主观性,依赖医生经验,因此评估难度较大。由于脓毒症介导的炎症瀑布反应、氧化应激反应,可诱导肺泡-毛细血管内皮屏障通透性改变并导致呼吸系统损伤,进而造成ARDS,因此,与炎性反应和内皮功能相关的指标可能具有评估脓毒症所致ARDS病情和预后的功能。
suPAR是尿激酶型纤维酶原激活物受体的可溶形式,通过与配体尿激酶型纤溶酶原激活物结合介导纤溶酶原活化、信号转导、黏附转移细胞等[10]。本研究发现,suPAR水平在脓毒症所致ARDS患者中明显升高,且随着ARDS分级的升高而升高,与APACHE Ⅱ评分、SOFA评分及CRP、PCT、IL-6水平呈正相关。CHEN等[11]研究指出suPAR与脓毒症所致ARDS患者APACHE Ⅱ评分、SOFA评分及CRP、TNF-α、IL-1β、IL-8水平呈正相关,suPAR是脓毒症所致ARDS的独立预测因子。结合本研究结果,说明suPAR参与脓毒症患者肺损伤过程,推测suPAR参与脓毒症所致ARDS可能的机制为在炎性反应刺激下,小气道上皮细胞中suPAR呈高表达,suPAR表达增加促使大量炎性反应细胞释放,并驱使单核细胞、T淋巴细胞、中性粒细胞等在肺部浸润,加重肺部炎性反应损伤。其次,血管外纤维蛋白沉积和纤溶异常是ARDS主要表现,suPAR可能通过促使肺纤维化参与ARDS病情进展。WANG等[12]报道显示,suPAR高表达还可能诱导气道上皮细胞发生间质转化形成成纤维细胞或肌成纤维细胞,促使慢性非阻塞性肺疾病患者肺纤维化进程。 GEBOERS等[13]也报道,suPAR通过复杂分子信号通路、基因表达模式参与小气道纤维化和肺气肿等发病机制。
PBEF是一种具有多种生物学作用的细胞因子,PBEF表达可激活下游炎症因子和趋化因子表达,扩大炎性反应,并能抑制中性粒细胞凋亡,延长炎性反应时间,进而破坏肺泡-毛细血管屏障,导致急性肺损伤[14]。目前,关于PBEF与ARDS的报道多为基础研究,缺乏临床研究。本研究发现PBEF在脓毒症所致ARDS患者中明显升高,说明PBEF同样参与了脓毒症患者急性肺损伤过程,相关分析表明,PBEF与CRP、PCT、IL-6呈正相关,说明PBEF水平过高可能诱导炎症因子释放,发挥协同作用机制。动物研究显示,PBEF可促使TNF-α、IL-1β等炎症因子释放,加剧ARDS大鼠肺组织损伤[15]。PBEF通过多种途径参与ARDS过程,PBEF可激活下游Toll样受体4、P38/促分裂素原活化蛋白激酶信号通路、转录激活因子3等,调控炎性反应,促使炎症介质合成,扩大炎性反应,进而诱导肺泡-毛细血管屏障通透性增加及肺泡上皮细胞凋亡,最终导致ARDS的发生[5]。抑制PBEF可减轻肺组织氧化应激和炎性反应[16]。
VE-Cad是血管内皮细胞黏附连接的特异性钙黏蛋白,特异性表达于内皮细胞,具有调控血管通透性、增生、新生血管形成等作用,在维持血管内皮细胞极性和完整性方面发挥重要作用[17]。本研究发现,VE-Cad在脓毒症所致ARDS患者中也明显升高,与APACHE Ⅱ评分、SOFA评分呈正相关,说明VE-Cad同时参与了脓毒症肺损伤发病和进展。相关分析显示,VE-Cad与炎性反应指标呈正相关,可能原因为脓毒症炎性反应过程中,炎性反应指标刺激VE-Cad胞内羟基末端和连环蛋白磷酸化,导致其与连环蛋白联合体解聚,破坏细胞连接,增加血管通透性,进而导致肺血管屏障受损[18]。而抑制VE-Cad表达可抑制炎性反应相关蛋白、趋化因子表达,改善微血管内皮细胞通透性[19]。以上结果提示在脓毒症炎性反应刺激下VE-Cad表达增加,进而诱导了ARDS的发生。本研究结果发现,在脓毒症所致ARDS患者中,死亡组suPAR、PBEF、VE-Cad水平高于存活组,影响脓毒症所致ARDS患者预后的多因素Logistic回归分析结果显示,高水平suPAR、PBEF、VE-Cad是脓毒症所致ARDS患者不良预后的危险因素,说明持续高水平suPAR、PBEF、VE-Cad可能预示着不良临床结局的发生。分析原因为suPAR、PBEF过度合成和释放,促使CRP、PCT、IL-6产生,进而介导炎症瀑布反应,在炎性反应刺激下VE-Cad大量合成,加剧肺血管内皮损伤,导致富含蛋白液体渗漏至肺组织间隙,引起肺水肿,影响肺通气和换气功能,PaO2/FiO2下降,进而加剧病情进展,导致不良结局发生。本研究中多因素Logistic回归分析显示,高APACHE Ⅱ评分是脓毒症所致ARDS患者不良预后的危险因素。APACHE Ⅱ评分是评估危重病患者预后的常用敏感指标,与重症患者病死率密切相关[20]。ARDS分级是对ARDS患者病情严重程度进行分级,分级越高,病情越重,预后越差,重度ARDS是ARDS患者不良预后的危险因素[21]。
综上所述,脓毒症所致ARDS患者血清suPAR、PBEF、VE-Cad水平均升高,高水平suPAR、PBEF、VE-Cad可能与患者病情加重和预后不良存在密切关系。suPAR、PBEF、VE-Cad有望成为诊断脓毒症所致ARDS潜在生物学指标和临床治疗新靶点。
