HPLC-PDA法测定兽用中药液体制剂中非法添加的四种解热镇痛类药物
2021-04-19张亦菲黄家莺张浩然华贤辉
徐 汀,张亦菲,黄家莺,张浩然,田 恺,华贤辉,曹 莹
(上海市兽药饲料检测所,上海 201103)
解热镇痛药是一类能使患病的发热动物的体温降至正常,并能缓解疼痛的药物。这类药物大多数对风湿病和痛风疼痛能减轻其症状,有一定抗炎作用,不易产生耐受性及成瘾性[1]。但运用不当则不利于对患病动物的诊断从而延误病情,同时在中兽药中非法添加解热镇痛类药物,导致养殖场在不知情的状况下使用也会导致很多不良反应的产生[2]。因此急需一种稳定,可靠的方法来监测中兽药液体制剂中非法添加解热镇痛类药物的现象。
中兽药作为我国传承千年的医药学组成之一,是我国防治畜禽疾病的有效药剂, 具有很好的研究应用价值[3]。而现代医药学研究发现,许多中草药有效成分中所含有的物质,能够制成的中兽药制剂并用于动物疫病的防控,均具有激活免疫细胞的活性,调节免疫作用,增强免疫功能;又有抗病毒、抗细菌、抗氧化、抗应激及促生长之作用等[4]。中药液体制剂是按形态分类的一大类制剂, 系指中药提取物分散在液体介质中形成的可供内服或外用的液态制剂[5-6]。随着禁抗时代的到来,市场上对能够替代抗生素类产品的需求越来越大,而此时对这类中兽药的监控也应该得到更大的关注[7]。因此,本文选择了中兽药中的液体制剂,在参考了相关文献后[8-9],结合了非法添加检测技术的特点,建立了中兽药液体制剂中非法添加对乙酰氨基酚、安乃近、安替比林、氨基比林的HPLC-PDA检测方法,为中兽药中非法添加解热镇痛类药物的监测提供了方法。
1 仪器与试药
1.1 仪器 分析天平:感量0.01 mg,AB265-S,梅特勒-托利多仪器(上海)有限公司;高效液相色谱仪:Waters e2695,配二极管阵列检测器(PDA),沃特世公司;纯水机:Molatom 1810A,中国重庆摩尔水处理设备有限公司;酸度计:PHS-3C 电位计,上海仪电科学仪器股份有限公司。
1.2 试药 对乙酰氨基酚对照品(Dr. Ehrenstorfer GmbH,批号为C15846000,含量99.9%)、安乃近对照品(中国食品药品检定研究院,批号为100002-201607,含量94.5%)、氨基比林对照品(中国药品生物制品检定所,批号100503-200301,含量100%)、安替比林对照品(中国食品药品检定研究院,批号100508-201602,含量100%);实验用水(电阻率>18 MΩ·bcm,符合GB/T6682一级用水的规定);乙腈(色谱纯);甲醇(色谱纯);供试品均来自抽检样品,为检测合格的样品:双黄连口服液样品(批号:180301);双黄连注射液样品(批号20180107);黄芪多糖注射液(批号:91801302);益母多抗鱼腥草注射液(批号:180426);杨树花注射液(批号:20180202);柴胡注射液(批号:91906181),鱼腥草注射液(批号:20191001)。
2 方法与结果
2.1 色谱条件 色谱柱:CAPCELL PAK MGⅡ S5 C18 (4.6 mm × 150 mm,5 μm);流动相:磷酸盐缓冲液(磷酸氢二钠3.0 g,加水1000 mL,用磷酸调pH值至6.5)和乙腈(84:16,V1:V2);流速度:1.0 mL/min;柱温:30 ℃;进样体积:10 μl;检测器:二极管整列检测器(PDA),记录229 nm波长处的色谱图。取供试品溶液和对照品溶液在该色谱条件下进样分析,同时记录色谱图与光谱图。
2.2 液体的制备
2.2.1 供试品溶液的制备 精密量取供试品1 mL,置于100 mL容量瓶中,加入甲醇定容,经0.22 μm滤膜滤过,滤液作为供试品溶液。
2.2.2 对照品储备溶液 分别取对乙酰氨基酚、安乃近、氨基比林、安替比林对照品分别为58.68、50.73、55.80、60.40 mg 于50 mL容量瓶中,加甲醇溶解并稀释到刻度线,摇匀,作为对照储备溶液。
2.2.3 对照品工作溶液 精密量取2 mL对照储备溶液,置20 mL容量瓶中,用甲醇溶解并稀释至刻度线,摇匀,经0.22 μm滤膜滤过,滤液作为对照品工作溶液。另取上述四个对照品各2 mL,一同置于20 mL容量瓶中,用甲醇溶解稀释并定容,摇匀,经0.22 μm滤膜滤过,滤液作为混合对照品工作溶液。
2.2.4 建立光谱数据库的溶液 以对照品工作溶液作为建立光谱数据库的溶液,建立光谱数据库。
2.3 供试品的测定 按照2.1的色谱条件及2.2的溶液制备方法,将供试品溶液和对照品工作溶液注入高效液相色谱仪。按外标法以峰面积计算,即可得到对乙酰氨基酚、安乃近、氨基比林、安替比林的含量。
2.4 线性关系考察 分别精密量取“2.2”项下的对照品储备液,将对乙酰氨基酚、氨基比林、安替比林用甲醇稀释至10、12.5、25、50、100、200、500倍作为对照品溶液,安乃近则稀释为至5、6.5、10、20、100、200、500倍作为对照品溶液。按照上述色谱条件进样分析,以峰面积为纵坐标,对照品浓度为横坐标来建立线性回归方程,结果表明,对乙酰氨基酚、安乃近、氨基比林、安替比林浓度分别在1.17~117.28、2.03~202.92、5.58~111.60、2.42~120.80 μg/mL范围内呈现良好的线性关系。其线性关系分别为:
对乙酰氨基酚:y=42943x-5107.1,R2= 0.9986;安乃近:y=12590x-8787.7,R2= 0.9999;氨基比林:y=22107x-15671,R2= 0.9980;安替比林:y= 25211x-468.5,R2= 0.9993
2.5 专属性考察 取中兽药液体制样品,按照上述2.2的制备方法制得空白基质溶液。根据样品使用方式选择了比较有代表性的基质复杂的双黄连口服液和基质比较简单的鱼腥草注射液进行专属性实验。通过所选择的空白基质溶液以及对照品工作溶液进行专属性实验。结果表明,空白基质对四种解热镇痛类药物的出峰并没有干扰,不影响对其含量的测定。典型图谱图见图1~图3。

图1 A为双黄连口服液空白基质溶液的色谱图, B 为鱼腥草注射液空白基质溶液色谱图

图2 对乙酰氨基酚、安乃近、安替比林、氨基比林浓度为0.1 mg/mL对照品溶液色谱图

图3 对乙酰氨基酚(A)、安乃近(B)、安替比林(C)、氨基比林(D)的紫外光谱图(0.1 mg/mL)
2.6 精密度实验 取“2.1”项下的混合对照品溶液,连续进样6次,计算峰面积的RSD,结果表明,对乙酰氨基酚、安乃近、氨基比林、安替比林的峰面积RSD分别为0.66%、1.03%、0.03%、0.10%,说明该仪器的精密度良好。
2.7 稳定性实验 取“2.1”项下的混合对照品溶液,分别在0、1、6、9、12、24 h进样测定6次,计算峰面积RSD,对乙酰氨基酚、安乃近、氨基比林、安替比林峰面积的RSD分别为0.99%、2.82%、0.18%、0.42%。结果表明,混合溶液稳定性良好。
2.8 检测限 取中兽药液体制剂 1 mL,逐级加入对照品储备液2.5、2、1和0.5 mL,制成对乙酰氨基酚、氨基比林、安替比林添加量分别为2.35、1.17、0.59 g/L;2.23、1.12、0.56 g/L; 2.42、1.21、0.60 g/L;安乃近添加量为2.54、2.03、1.01 g/L的添加样品,同样根据样品使用方式选择了比较有代表性的基质复杂的双黄连口服液和基质比较简单的鱼腥草注射液进行检测限的考察。按照2.1的色谱条件以及2.2的处理方法进行测定。考虑到非法添加的成分含量大都较高,故选择光谱图失真的最大浓度作为本方法的检测限[10]。结果表明,对乙酰氨基酚、氨基比林、安替比林的检测限分别为1.17 g/L、1.12 g/L、1.21 g/L,安乃近的检测限为2.03 g/L。典型图谱见图4~图8。

图4 A、B 分别为鱼腥草注射液中添加(1.17 g/L、2.03 g/L、1.21 g/L、1.12 g/L)和(2.35 g/L、2.54 g/L、2.42 g/L、2.23 g/L)浓度的对乙酰氨基酚、安乃近、安替比林、氨基比林

图5 A、B 分别为双黄连口服液中添加(1.17 g/L、2.03 g/L、1.21 g/L、1.12 g/L)和 (2.35 g/L、2.54 g/L、2.42 g/L、2.23 g/L)浓度的对乙酰氨基酚、安乃近、安替比林、氨基比林
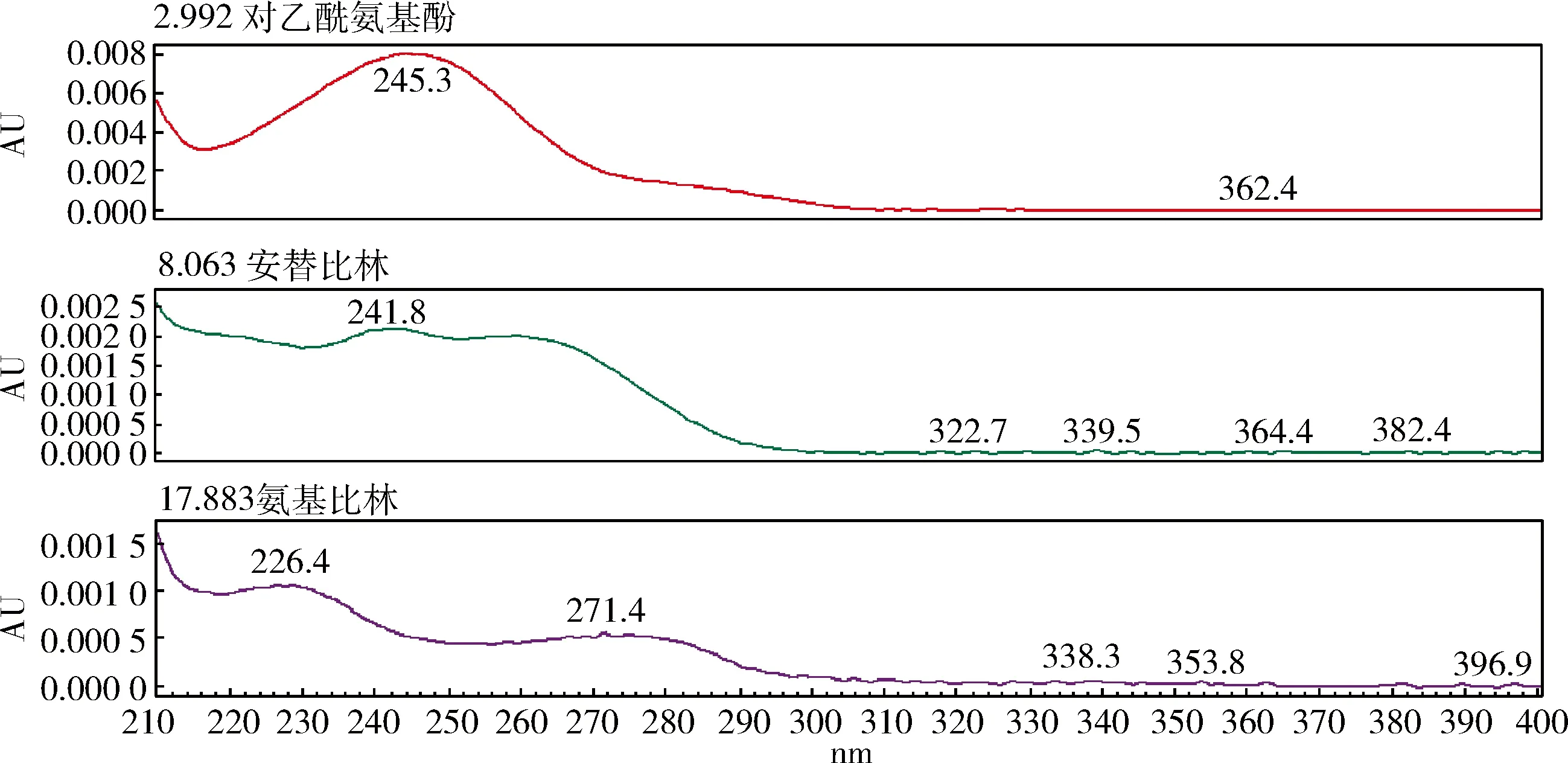
图6 鱼腥草注射液中添加的对乙酰氨基酚、安替比林、氨基比林的光谱图(1.17 g/L、1.21 g/L、1.12 g/L)

图7 双黄连口服液中添加的对乙酰氨基酚、安替比林、氨基比林的光谱图(1.17 g/L、1.21 g/L、1.12 g/L)

图8 为鱼腥草注射液(A)和双黄连口服液(B)中添加安乃近的光谱图(2.03 g/L)
2.9 样品加标回收实验 精密量取1.0 mL未检出上述四种解热镇痛药的供试品,置于100 mL容量瓶中,精密量取对乙酰氨基酚、安乃近、氨基比林、安替比林对照品储备液1.0、2.0、1.0、1.0 mL,将其加入装有供试品的100 mL容量瓶中。用甲醇稀释定容,(添加水平:对乙酰氨基酚、安替比林、氨基比林为1.17 g/L、1.21 g/L、1.12 g/L,安乃近为2.03 g/L)。每份供试品做5份平行样,按照外标法计算回收率,结果见表1,表明回收率良好。

表1 四种解热镇痛药在不同中兽药液体制剂中的回收率(n=5)
3 讨论与结论
3.1 溶剂条件的选择[11]在加标实验中,考察了甲醇,乙腈,和流动相分别稀释样品进样。结果表明,安乃近在用乙腈和流动相稀释的样品中回收率较差,可能是安乃近有降解。本次实验选用的液体制剂中兽药样品都能在甲醇中溶解,口服液中有析出的物质对回收率并无影响。综上,相比于流动相溶解,选择甲醇作为溶剂可以减少安乃近的降解。
3.2 色谱条件选择 参考了农业农村部公告第2448号上收载的阿莫西林可溶性粉中非法添加加热镇痛类药物检查方法的色谱条件,以及其他文献中的液相色谱条件[12-13],上述条件中,都能较好的将对乙酰氨基酚、安乃近、安替比林、氨基比林分离。但考虑到中药制剂中基质复杂,为了能更好的将基质中的杂质和目标峰分离,所以选择磷酸盐缓冲液(磷酸氢二钠3.0 g,加水1000 mL,用磷酸调pH值至6.5)和乙腈(84∶16,V1∶V2)为流动相,流速为1.0 mL/min等度进样。
3.3 检测波长的选择 农业部公告 第2448号[10]上收载的阿莫西林可溶性粉中非法添加解热镇痛类药物检查方法所选择的吸收波长为229 nm。故参考了该方法采取了229 nm作为定量波长。
上述实验结果表明,通过高效液相色谱法检测中兽药液体制剂中非法添加解热镇痛类药物的这一方法,具有操作方便,定量准确,重复性好的优点。为中兽药中非法添加解热镇痛类药物的监测提供了可靠的方法,为中兽药产品的质量监管提供了保障。
