灵芝三萜化合物的制备与药理活性研究进展
2021-04-16亓小妮谢苗吴杨洋张鑫杜秀菊
亓小妮 谢苗 吴杨洋 张鑫 杜秀菊

摘要 灵芝(Ganoderma lucidum)具有广泛的药理活性,灵芝三萜(G.lucidum triterpenes,GLTs)是灵芝中重要的活性成分之一,具有抗肿瘤、保肝护肝和增强免疫等生理功能,目前已经成为评价灵芝产品质量的重要指标之一。在参考最新研究的基础上,对灵芝三萜化合物的提取、分离纯化、检测方法以及药理活性等方面的研究进展进行了综述,旨在为灵芝三萜类化合物的进一步研究提供借鉴和参考,并更好地促进灵芝三萜类化合物资源的合理開发和利用。
关键词 灵芝;三萜类化合物;提取方法;分离纯化;质量控制;药理活性
中图分类号 R284.1文献标识码 A
文章编号 0517-6611(2021)05-0038-05
doi:10.3969/j.issn.0517-6611.2021.05.010
开放科学(资源服务)标识码(OSID):
Research Progress on Preparation and Pharmacological Activities of Ganoderma lucidum Triterpenes
QI Xiao-ni,XIE Miao,WU Yang-yang et al
(College of Life Sciences,Liaocheng University,Liaocheng,Shandong 252000)
Abstract Ganoderma lucidum has a wide range of pharmacological activities.G.lucidum triterpenes (GLTs) is a kind of important medicinal active ingredients,which has become one of the important indexes to evaluate the quality of G.lucidum,for it has lots of biological functions,such as anti-tumor,liver protection and so on.In this paper,with reference to the latest literature,research progress in the extraction,purification,detection and pharmacological activities of GLTs was reviewed,aiming to provide references for further research on GLTs,so as to better promote the rational development and utilization of G.lucidum triterpenes.
Key words Ganoderma lucidum;Triterpenes;Extraction process;Separation and purification;Quality control;Pharmacological activities
灵芝(Ganoderma lucidum),又名瑞草、神芝,隶属于多孔菌目(Polyporales)、灵芝科(Ganodermataceae)、灵芝属(Ganoderma),其味甘、性温,具有扶正固本、健脾补肾、保肝护肝和镇静安神等功效。临床上常用于慢性支气管炎、冠心病等症的治疗以及癌症化疗之后的辅助治疗[1]。现代研究表明,灵芝含有三萜类、多糖、氨基酸和生物碱等多种活性成分[2-3],其中三萜类化合物是重要的活性组分之一,具有抗肿瘤、保肝护肝、降血脂和抗病毒等多种药理功效,具有广泛的开发前景。
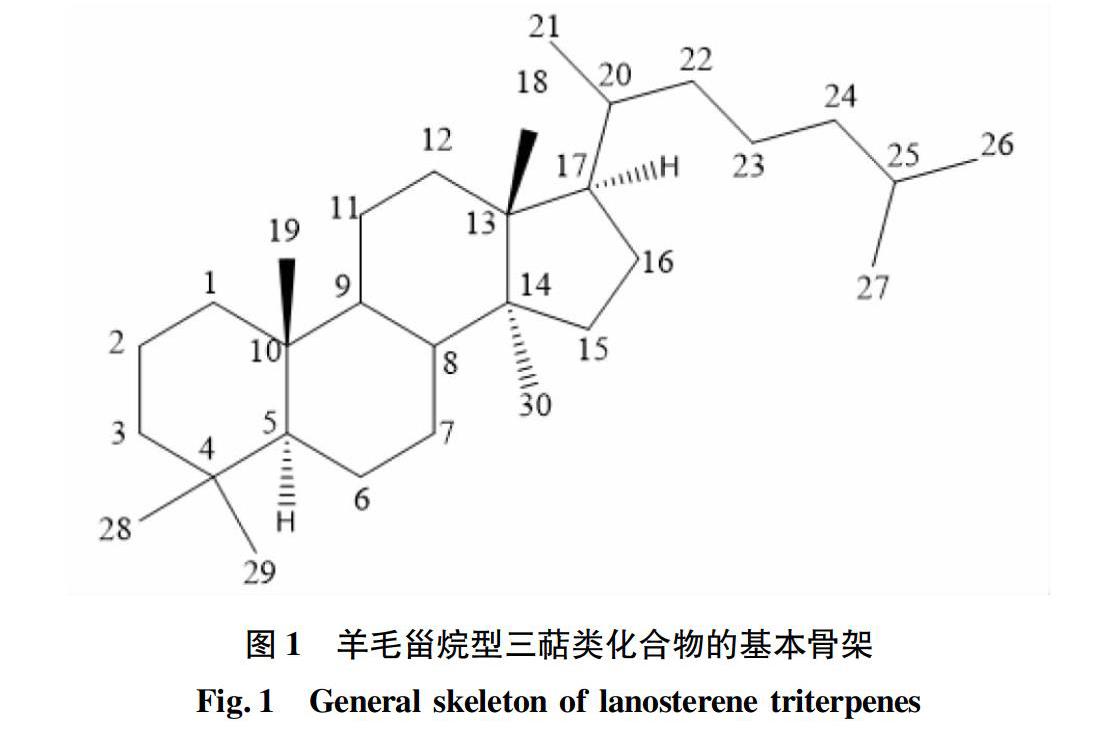
研究表明,灵芝三萜类化合物种类多、化学结构复杂。目前发现的主要是由异戊二烯单位构成的羊毛甾烷型(图1)。从灵芝中分离到的三萜类化合物目前有300多种[4]。按照碳原子数目不同,可分为C 30、C 24和C 27三大类;按照侧链和官能团不同,可分为灵芝酸类、灵芝醇类、灵芝醛类、和灵芝内酯类等,以前两类(灵芝酸类和灵芝醇类)为主[5-6]。灵芝三萜类化合物大多脂溶性较高,难溶于水,相对分子质量一般在400~600 Da[7]。
笔者对近年来灵芝三萜化合物的研究进展进行了总结和提炼,主要包括提取、分离纯化、质量检测与监控等方面,并针对现状进行了分析和展望,旨在为灵芝三萜类化合物的进一步研究提供借鉴和参考。
1 灵芝三萜的提取
灵芝三萜化合物的提取主要是基于目标产物的溶解度、吸附力、蒸汽压、超声空化作用和酶解作用等不同进行的,目前提取方法主要包括传统提取法[8-9]、超声提取法[10-12]、超临界萃取法[13-15]、微波提取法[16-17]和酶提取法[18-19]这5种(表1)。
1.1 传统提取方法
因为三萜类化合物易溶于有机溶剂,不易溶于水,传统提取法采用的溶剂大多为乙醇和氯仿,由于氯仿有毒,所以最常用为乙醇。郑士彬等[8]采用响应面法对灵芝三萜的提取工艺进行了优化,最佳条件为乙醇体积浓度73%、温度76 ℃、时间120 min、液料比16∶1,在此条件下的提取得率为6.91 mg/g。Ruan等[9]通过响应面法设计优化灵芝三萜的提取条件,其中参比三萜类灵芝酸H的产率从0.88 mg/g增加到2.09 mg/g。传统提取法提取相对更加简单,适合大量提取,但消耗溶剂较多,费用高。
1.2 超声波提取法
超声波是一种在传统提取法基础上的最常用的辅助技术,其原理是利用超声使细胞受到空泡冲击波的破坏,促进了传质,有利于溶质的溶出,与传统提取法相比较,作用时间短,溶剂用量少,节约能源。胡琼方等[10]采用超声波辅助法,以乙醇作为提取溶剂,获得灵芝三萜的最佳提取工艺为液料比42 mL/g,超声功率210 W,超声温度43 ℃,超声时间17 min,在此条件下的提取得率为0.61 mg/g。Zhang等[11]将RSM设计方法用于灵芝三萜超声辅助提取的优化,提取率为(7.338±0.150) mg/g。Oludemi等[12]对传统提取和超声辅助提取进行了比较,研究表明使用超声辅助可以显著提高三萜类化合物的得率,传统提取和超声辅助提取的得率分别为(285.7±31.2)、(435.6±21.1) mg/g。
1.3 超临界提取法 超临界提取技术是一种将超临界流体作为萃取剂,把一种成分从混合基质中分离出来的技术。二氧化碳(CO 2)是最常用的超临界流体,所以又称为超临界CO 2流体提取法。其原理是在临界点时,温度和压力微小的变化可导致溶解度发生极大突变,因此超临界CO 2流体提取法具有更大的优势。华正根等[13]采用此法提取灵芝三萜,并与采用传统乙醇回流提取法进行了同步比较,研究表明高压超临界CO 2 提取的灵芝三萜得率(1.35%)明顯高于后者(0.92%)。Li等[14]采用高压超临界CO 2法,从100 g破壁孢子粉中提取540.1 mg灵芝三萜。
1.4 微波提取法
采用微波辅助可促进水分蒸发,压力增大,使细胞破裂促进细胞内容物释放。微波辅助提取法所需时间最短,三萜产率最高,大大节省了提取时间,提高了工作效率。卢彦芳等[16]设计微波连续抽提的方法,并与其他传统提取方法进行比较,发现微波连续抽提和常规的微波提取分别需要14.5、10.0 min即可达到灵芝三萜类成分的最大提取量,而其他非微波提取的常规方法则需要几十分钟甚至上百分钟,且微波连续抽提所得产物的纯度远远高于其他方法。Chen等[17]采用微波辅助提取灵芝总三萜,并与传统提取法(得率为2.58%)、加热回流提取法(得率为2.22%)、超临界CO 2提取法(得率为1.52%)和超声辅助提取法(得率为1.72%)进行对比,表明微波辅助的提取得率最高(511%)。
1.5 酶提取法
酶反应破坏细胞壁的致密构造,减小传质屏障有效成分的溶出。酶辅助提取法相对于其他方法,提取条件更加温和,对环境无污染、提取效率高。刘晓艳等[18]采用酶辅助提取法,在最优提取条件下,三萜提取得率为099%。丁霄霄等[19]研究采用纤维素酶、半纤维素酶、木瓜蛋白酶等复合酶对灵芝三萜的工艺条件进行了优化,在最佳酶解提取工艺条件下,灵芝总三萜的提取得率为(1.29±004)%。但此法成本高,酶易失活。
综上所述,以上提取方法中,每种方法各有优劣,无论哪种方法都没有绝对的优势。超临界提取法能提高目标产物的溶解能力和提取得率,但设备要求较高。传统提取法,提取相对更加简单,适合大量提取,所以仍然是目前规模化、产业化提取的主要方式,但因为此法溶剂消耗较大,费用较高,一些辅助技术(超声辅助、微波辅助和微波辅助)提取法作为在传统提取方法之上的一种辅助技术,大大缩短了提取时间,提高了工作效率和提取得率。超声和微波设备的研究和酶制备技术的发展,将会使超声提取、微波提取和酶提取方法日益普及化和规模化。
2 灵芝三萜的分离纯化
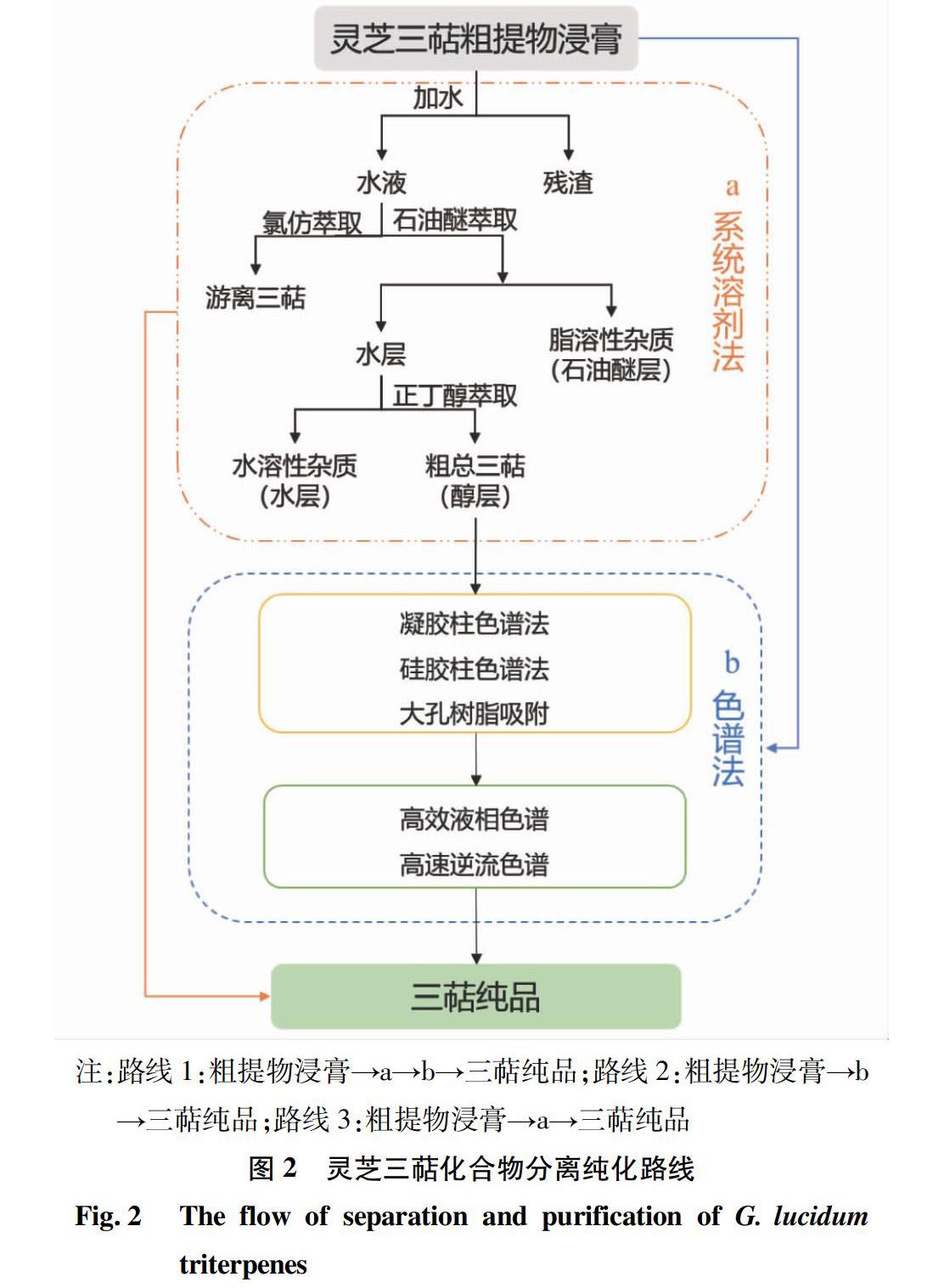
随着蛋白质和多糖类等大分子分离纯化技术的不断完善,灵芝三萜类化合物的分离纯化工艺也在不断创新和发展。目前灵芝三萜类化合物的分离纯化有多种途径,可以归纳为3种途径(图2)。
2.1 “乙醇粗提+系统溶剂法+色谱法”途径
这是目前最主要的一种途径,即对已经制备的粗提乙醇浸膏在系统溶剂法提取分离的基础上,再通过一种或多种层析法,有时还要利用结晶等技术达到最终分离纯化的效果(图2中路线1)。Feng等[20]用石油醚萃取乙醇提取物,通过再循环高速逆流色谱纯化萃取样品,分离得到灵芝酸S、灵芝酸T和灵芝酸 B,从300 mg粗制样品中分离出16.4 mg纯度为90.4%的灵芝B,采用再循环高速逆流色谱的循环洗脱模式,得到纯度分别为97.8%和83.0%的25.7 mg灵芝酸T和3.7 mg灵芝酸S。Zhang等[21]用乙酸乙酯对灵芝的乙醇提取物进行萃取。所得浸膏先后由硅胶柱和Sephadex LH-20凝胶柱富集纯化,最终将所得各组分经制备性HPLC进行色谱分离,得到19种三萜类化合物。
2.2 “乙醇粗提+色谱法”途径
先通过乙醇提取得到粗提乙醇浸膏,然后再选择合适的色谱方法得到纯品(图2中路线2)。如张春杰[22]依次应用硅胶柱色谱、葡聚糖凝胶色谱及高效液相色谱(HPLC)等色谱技术,并结合结晶与重结晶等分离手段,对南方灵芝子实体的次生代谢产物进行分离纯化,并从其乙醇提取物中分离到18个化合物。
2.3 “乙醇粗提+系统溶剂法”途径
经系列溶剂法萃取后,有时候也可以得到三萜类化合物的单品[23](图2中路线3)。经此途径分离得到的纯品大多为游离的三萜、三萜皂苷类及其混合物,但得到单品的机会不多。如冯娜等[24]用95%乙醇提取所收集的富含三萜类化合物的菌丝体,然后依次用石油醚、氯仿、乙酸乙酯和正丁醇萃取。从氯仿部分(抗肿瘤细胞增殖活性较好)中分离得到4个化合物,并测定各化合物的抗肿瘤活性。
由此可见,由第1、第2条途径得到的化合物通常纯度较高,这对后期其结构及其药理活性的研究有利。第3条途径得到的大多为三萜类化合物的混合物,不利于对灵芝三萜类单体的结构鉴定、构效关系及作用机制的研究,但可以从应用开发角度研究其药理功效。
3 灵芝三萜类化合物的检测与质量控制
灵芝三萜具有广泛的药理活性,其含量高低已经作为灵芝产品品质优劣的重要指标之一。因此,建立一个精确、便捷、高灵敏度的检测方法对于灵芝质量的监控显得尤为重要。目前,常用的检测方法主要有2种:化学比色法和高效液相色谱法(high performance liquid chromatography,HPLC)。
化学比色法可用于三萜化合物的定性测定,而不适宜用于精确的定量检测。由于所用的标准品齐墩果酸(或熊果酸)与灵芝三萜成分和结构存在很大差异,并且麦角甾醇和油酸等物质会干扰真实数据的获得,因此,往往导致化学比色法测定结果存在比较大的误差[25]。
相比于化学比色法,HPLC是一种比较精确的三萜含量的测定方法,具有快速、简便、灵敏、分离度好等特点,不受灵芝中干扰物质的影响,目前广泛用于灵芝三萜类化合物的检测与含量测定。由于标准品难获取,因此欲建立一种以三萜类化合物来控制灵芝质量的HPLC指纹图谱法存在很大困难[26-27]。目前,利用HPLC方法进行灵芝三萜类化合物含量检测虽有了一些研究,但还不够理想,一是HPLC分离效果不好,纯化出的标准品种类太少;二是建立的HPLC标准指纹图谱法还不够完善,所测的三萜成分种类还非常有限;另外,目前建立的HPLC指纹图谱法主要针对灵芝子实体三萜,针对灵芝发酵菌丝体三萜成分的检测方法鲜见报道,因此针对不同来源构建多种快速精确的三萜检测方法尤为重要。
4 灵芝三萜的药理活性
4.1 抗肿瘤
灵芝三萜具有较广泛的抗肿瘤活性,现已有研究报道了灵芝酸在前列腺癌、黑色素瘤、乳腺癌、脑膜瘤治疗中的作用,目前该化合物正在进行淋巴瘤治疗的临床前试验[28-30]。三萜通过下调细胞周期蛋白D1在G1期诱导细胞周期阻滞,在G2期通过抑制蛋白激酶C活性诱导细胞周期阻滞,并通过激活半胱氨酸的天冬氨酸蛋白水解酶级联,通过线粒体依赖通路促进癌细胞凋亡[31]。Feng等[32]发现通过抑制Wnt共受体LRP6的磷酸化来阻断Wnt/β-连环蛋白信号传导。在人(MDA-MB-231)和小鼠(4T1)乳腺癌细胞系中,灵芝显著降低LRP6的磷酸化并抑制Wnt3a激活的Wnt靶基因Axin2表达。灵芝的施用抑制了Wnt诱导的乳腺癌细胞的过度增殖和MDA-MB-231细胞迁移。研究结果证明,灵芝通过抑制Wnt/β-连环蛋白信号抑制乳腺癌细胞的生长和迁移,表明灵芝三萜可能是乳腺癌的潜在天然抑制剂。
4.2 保肝护肝
Peng等[33]研究报道了灵芝三萜类化合物4具有显著抑制由HSC-T6诱导的TGF-β的增殖活性,研究表明其具有抗肝纤维化作用。在一项以42名健康受试者为研究对象的研究中,Chiu等[34]证实了灵芝的抗氧化和保肝作用。Liu等[35]从茶病灵芝中提取分离的三萜类成分中有6类在细胞学试验中表现出了护肝作用,防止HL-7702细胞被DL-半乳糖胺诱导而产生细胞损伤。
4.3 抑制血管紧张素转化酶(ACE)
Rajasekaran等[36]报道称灵芝提取物在抗癌药物阿霉素诱导的心脏毒性试验中发挥了重要作用,其通过降低自由基的产生或通过提高谷胱甘肽含量和不同的抗氧化酶水平清除自由基。Daskaya等[37]研究说明灵芝酸F具有抑制血管紧张素转化酶ACE的作用。目前,合成血管紧张素转化酶抑制剂已广泛应用于临床高血压的防治。由于与合成药物有关的副作用和毒性,食品科学家和药物研究人员寻求天然药物资源,因此,基于灵芝酸F具有较高的血管紧张素自吸能力,迫切需要进一步深入的临床研究和产品开发。
4.4 抗炎作用 灵芝三萜通过抑制多种炎症介质的产生而介导细胞周期阻滞,可以作为一种抗炎、抗增殖的药物使用[38]。Hasnat等[39]通过免疫荧光法发现,灵芝三萜可抑制结肠炎小鼠的NF-kB通路;而通过免疫组织化学着色法发现了COX-2和IL-1β的表达,最后的动物学实验表明,这类灵芝的三萜类提取物可以显著缓解结肠炎小鼠的病情。Jiao等[40]发现,从灵芝中提取的羊毛甾烷三萜類化合物对LPS激活的BV-2小胶质细胞表现出显著的抗炎活性,同时有大量证据表明促炎介质(如NO)和小胶质细胞中神经炎症反应的进一步抑制可以减轻这些神经退行性疾病如帕金森氏症和阿尔茨海默病的严重程度或延缓其进展。
4.5 抗艾滋病毒
艾滋病毒是一种高度传染性的病毒,能导致后天免疫机能丧失,影响着全世界数百万人[41]。研究表明,灵芝具有抗HIV-1蛋白酶活性,可作为一种有效的抗HIV药物。从灵芝子实体中分离出的灵芝酸O和灵芝酸内酯,能抑制小牛DNA聚合酶-α、大鼠DNA聚合酶-β、HIV-1逆转录酶和其他化合物的活性;灵芝醇F和灵芝甘露醇对HIV-1有较强的抑制作用;灵芝酸B和灵芝醇B对HIV-1蛋白酶也有较强的抑制作用。其他灵芝三萜:灵芝酸C1、灵芝酸β、灵芝酸H和灵芝醇A对HIV-1蛋白酶的抑制作用较弱[42-43]。
4.6 其他 除上文所述的活性外,灵芝三萜的神经保护[44]、抑制α-葡萄糖苷酶[45]、抗疟原虫[46]、降血糖[47]和抗氧化[48]等作用也是现在研究的热点。
5 问题与展望
灵芝作为一种著名的食药兼用真菌,其药理活性早在《神农本草经》中就有记载,在远东地区的民间医学中也有着悠久的使用传统。随着现代科学技术的发展和对灵芝资源的不断研究与开发,其蕴含的价值将会越来越大。
目前对于灵芝三萜的研究还存在以下问题:第一,从开发功能食品和医药保健品来说,目前提取纯化工艺的优化大多是以提取得率的高低作为判断依据,很少以生物活性追踪作为进一步筛选依据的;第二,灵芝栽培规模和需求量不断增加,而目前建立的HPLC指纹图谱法对三萜类成分的分离度不高,所能检测的三萜种类太少,不利于灵芝活性成分的快速检测和质量控制;第三,目前虽然针对灵芝三萜类药理活性的文献报道很多,但试验样品大多为粗品,由于灵芝栽培环境、原料、品种等诸多因素影响,三萜类成分差异较大,质量不稳定,药理活性重现性不好,构效关系不清晰,作用机制不明确;第四,提取得率太低,纯化效果不理想,针对三萜单体药理学、药效学和毒理学等方面的深入研究难以展开。
为了更好地开发灵芝资源,深化三萜类化合物的研究,需要从以下几个方面着手:首先,三萜类化合物的提取优化和分离纯化工作应以生物活性作为追踪依据;其次,进一步加强优化提取分离流程,提高灵芝三萜类化合物高活性单品的提取率,加强三萜类单体的化学结构鉴定,丰富三萜类化合物的标品种类;再次,继续优化HPLC指纹图谱方法,加强质量控制;最后,加强三萜类单体成分的化学合成和衍生化,加强三萜化合物的药理学、药效学和毒理学研究,阐明构效关系,明确作用机制。
参考文献
[1]
苏保洲.灵芝的现代临床应用探索[J].现代中西医结合杂志,2019,28(5):567-570.
[2] SHIAO M S.Natural products of the medicinal fungus Ganoderma lucidum:Occurrence,biological activities,and pharmacological functions[J].The chemical record,2003,3(3):172-180.
[3] AHMAD M F.Ganoderma lucidum:Persuasive biologically active constituents and their health endorsement[J].Biomedicine & pharmacotherapy,2018,107:507-519.
[4] BABY S,JOHNSON A J,GOVINDAN B.Secondary metabolites from Ganoderma[J].Phytochemistry,2015,114:66-101.
[5] LIANG C Y,TIAN D N,LIU Y Z,et al.Review of the molecular mechanisms of Ganoderma lucidum triterpenoids:Ganoderic acids A,C2,D,F,DM,X and Y[J].European journal of medicinal chemistry,2019,174:130-141.
[6] 谭贻,唐传红,冯杰,等.灵芝三萜生物合成及调控研究进展[J].食用菌学报,2019,26(3):125-140.
[7] 刘维,虎虓真,朱莉,等.芝灵三萜的研究与应用进展[J].食品科学,2019,40(5):309-315.
[8] 郑士彬,韩阳,韩静,等.响应面法优化灵芝三萜回流提取工艺[J].中南药学,2015,13(4):378-382.
[9] RUAN W M,LIM A H H,HUANG L G,et al.Extraction optimisation and isolation of triterpenoids from Ganoderma lucidum and their effect on human carcinoma cell growth[J].Natural product research,2014,28(24):2264-2272.
[10] 胡琼方,董建生,高文庚.灵芝发酵粉中三萜化合物提取与测定[J].食品研究与开发,2018,39(10):104-109.
[11] ZHANG H,JIANG H J,ZHANG X J,et al.Development of global chemical profiling for quality assessment of Ganoderma,species by ChemPattern software[J].Journal of analytical methods in chemistry,2018,2018:1-12.
[12] OLUDEMI T,BARROS L,PRIETO M A,et al.Extraction of triterpenoids and phenolic compounds from Ganoderma lucidum:Optimization study using the response surface methodology[J].Food & function,2018,9(1):209-226.
[13] 華正根,王金亮,朱丽萍,等.高压超临界CO 2提取灵芝三萜和甾醇成分的研究[J].中国食用菌,2018,37(5):62-65,69.
[14] LI L,GUO H J,ZHU L Y,et al.A supercritical-CO 2 extract of Ganoderma lucidum spores inhibits cholangiocarcinoma cell migration by reversing the epithelial-mesenchymal transition[J].Phytomedicine,2016,23(5):491-497.
[15] ZHANG J S,ZHANG H,JIA W,et al.The inhibitory effect of triterpenoids of Ganoderma lucidum on prostate cancer and the mechanism of inhibition[C]//中国菌物学会.中国菌物学会2015年学术年会论文摘要集.北京:中国菌物学会,2015:161-162.
[16] 卢彦芳,安静,蒋晔.微波连续抽提用于灵芝三萜类成分的分析[J].中国中药杂志,2015,40(7):1296-1299.
[17] CHEN Y,XIE M Y,GONG X F.Microwave-assisted extraction used for the isolation of total triterpenoid saponins from Ganoderma atrum[J].Journal of food engineering,2007, 81(1):162-170.
[18] 刘晓艳,陈艺煊,吴林秀,等.响应面法优化灵芝总三萜酶辅助提取工艺及其抗氧化活性研究[J].食品科技,2017,42(8):225-230.
[19] 丁霄霄,李凤伟,余晓红.响应面法优化复合酶提取灵芝总三萜工艺[J].食品工业,2018,39(8):40-44.
[20] FENG N,WEI Y T,FENG J,et al.Preparative isolation of ganoderic acid S,ganoderic acid T and ganoderol B from Ganoderma lucidum mycelia by high-speed counter-current chromatography[J/OL].Biomedical chromatography,2018,32(10)[2020-03-25].https://doi.org/10.1002/bmc.4283.
[21] ZHANG J J,MA K,HAN J J,et al.Eight new triterpenoids with inhibitory activity against HMG-CoA reductase from the medical mushroom Ganoderma leucocontextum collected in Tibetan plateau[J].Fitoterapia,2018,130:79-88.
[22] 张春杰.南方灵芝、红平菇和红蜡蘑的次生代谢产物研究[D].绵阳:西南科技大学,2015.
[23] TENG X Q,ZHANG W Q,SONG Y Y,et al.Protective effects of Ganoderma lucidum triterpenoids on oxidative stress and apoptosis in the spleen of chickens induced by cadmium[J].Environmental science and pollution research international,2019,26(23):23967-23980.
[24] 冯娜,骆军鑫,贾薇,等.灵芝发酵菌丝体中活性物质的研究[C]//2012年中国菌物学会学术年会会议摘要.北京:中国菌物学会,2012.
[25] 张忠,张劲松,刘艳芳,等.分光光度法测定灵芝中总三萜含量方法探讨[J].上海农业学报,2016,32(1):61-65.
[26] 丁平,邱金英,梁英娇,等.灵芝三萜类化学成分指紋图谱研究[J].中国中药杂志,2009,34(18):2356-2359.
[27] 贾红岩,王亚涛,张芝华,等.高效液相色谱法测定不同产地及品种灵芝三萜类成分的含量[J].微生物学通报,2017,44(1):238-244.
[28] BORBIERI A,QUAGLIARIELLO V,DEL VECCHIO V,et al.Anticancer and anti-Inflammatory properties of Ganoderma lucidum extract effects on melanoma and triple-negative breast cancer treatment[J].Nutrients,2017,9(3):1-9.
[29] BRYANT J M,BOUCHARD M,HAQUE A.Anticancer activity of ganoderic acid DM:Current status and future perspective[J].Journal of clinical & cellular immunology,2017,8(6):1-15.
[30] ZHANG Y.Ganoderma lucidum (Reishi) suppresses proliferation and migration of breast cancer cells via inhibiting Wnt/β-catenin signaling[J].Biochemical and biophysical research communications,2017,488(4):679-684.
[31] SHARMA C,BHARDWAJ N,SHARMA A,et al.Bioactive metabolites of Ganoderma lucidum:Factors,mechanism and broad spectrum therapeutic potential[J/OL].Journal of herbal medicine,2019,17/18[2020-04-15].https://doi.org/10.1016/j.hermed.2019.100268.
[32] FENG Z H,WU R,LIN M H,et al.Tumor suppressor p53:New functions of an old protein[J].Frontiers in biology,2011,6(1):58-68.
[33] PENG X R,LI L,DONG J R,et al.Lanostane-type triterpenoids from the fruiting bodies of Ganoderma applanatum[J].Phytochemistry,2019,157:103-110.
[34] CHIU H F,FU H Y,LU Y Y,et al.Triterpenoids and polysaccharide peptides-enriched Ganoderma lucidum: A randomized,double-blind placebo-controlled crossover study of its antioxidation and hepatoprotective efficacy in healthy volunteers[J].Pharmaceutical biology,2017,55(1):1041-1046.
[35] LIU L Y,CHEN H,LIU C,et al.Triterpenoids of Ganoderma theaecolum and their hepatoprotective activities[J].Fitoterapia,2014,98:254-259.
[36] RAJASEKARAN M,KALAIMAGAL C.Cardioprotective effect of a medicinal mushroom,Ganoderma lucidum against adriamycin induced toxicity[J].International journal of pharmacology,2012,8(4):252-258.
[37] DASKAYA-DIKMEN C,YUCETEPE A,KARBANCIOGLU-GULER F,et al.Angiotensin-I-converting enzyme(ACE)-inhibitory peptides from plants[J].Nutrients,2017,9(4):1-19.
[38] DUDHGAONKAR S,THYAGARAJAN A,SLIVA D.Suppression of the inflammatory response by triterpenes isolated from the mushroom Ganoderma lucidum[J].International immunopharmacology,2009,9(11):1272-1280.
[39] HASNAT M A,PERVIN M,CHA K M,et al.Anti-inflammatory activity on mice of extract of Ganoderma lucidum grown on rice via modulation of MAPK and NF-κB pathways[J].Phytochemistry,2015,114:125-136.
[40] JIAO Y,XIE T,ZOU L H,et al.Lanostane triterpenoids from Ganoderma curtisii and their NO production inhibitory activities of LPS-induced microglia[J].Bioorganic & medicinal chemistry letters,2016,26(15):3556-3561.
[41] PAYDARY K,KHAGHANI P,EMAMZADEH-FARD S,et al.The emergence of drug resistant HIV variants and novel anti-retroviral therapy[J].Asian Pacific journal of tropical biomedicine,2013,3(7):515-522.
[42] SMITH D C,REDMAN B G,FLAHERTY L E,et al.A phase II trial of oral diethylstilbesterol as a second-line hormonal agent in advanced prostate cancer[J].Urology,1998,52(2):257-260.
[43] GAO Y H,ZHOU S F,HUANG M,et al.Antibacterial and antiviral value of the genus Ganoderma P.Karst.species (Aphyllophoromycetideae):A review[J].International journal of medicinal mushrooms,2003,5(3):235-246.
[44] CR D,KNEZ Zˇ,KNEZ HRNCˇICˇ M.Antitumour,antimicrobial,antioxidant and antiacetylcholinesterase effect of Ganoderma lucidum terpenoids and polysaccharides:A review[J].Molecules,2018,23(3):1-21.
[45] CHEN X Q,ZHAO J,CHEN L X,et al.Lanostane triterpenes from the mushroom Ganoderma resinaceum and their inhibitory activities against α-glucosidase[J].Phytochemistry,2018,149:103-115.
[46] OLUBA O M.Ganoderma terpenoid extract exhibited anti-plasmodial activity by a mechanism involving reduction in erythrocyte and hepatic lipids in Plasmodium berghei infected mice[J].Lipids in health and disease,2019,18(1):1-9.
[47] CHEN S D,LI X M,YONG T Q,et al.Cytotoxic lanostane-type triterpenoids from the fruiting bodies of Ganoderma lucidum and their structure-activity relationships[J].Oncotarget,2017,8(6):10071-10084.
[48] HSU P L,LIN Y C,NI H,et al.Ganoderma triterpenoids exert antiatherogenic effects in mice by alleviating disturbed flow-induced oxidative stress and inflammation[J].Oxidative medicine and cellular longevity,2018,2018:1-11.
