骨痹颗粒中桑寄生HPLC-PDA 指纹图谱建立
2021-03-09吴倩莲刘佳佳潘林梅朱华旭
吴倩莲 刘佳佳 潘林梅 朱华旭
(1.南京中医药大学药学院,江苏南京 210023;2.南京中医药大学江苏省植物药深加工工程研究中心,江苏南京 210023;3.南京中医药大学江苏省中药资源产业化过程协同创新中心,江苏南京 210023)
骨痹颗粒具有补肝肾、通经络的功效,临床上用于治疗骨关节炎[1-2]。骨痹颗粒[3]原方由桑寄生、川续断、骨碎补、鸡血藤等8 味中药组成。总黄酮为骨痹颗粒中的药效成分之一,课题组在研究膜技术精制骨痹颗粒的过程中将其保留率作为指标成分之一[4-5],并在研究骨痹颗粒质量标准中,对桑寄生黄酮类成分进行薄层鉴别[3]。为了更好地控制制剂质量,本研究针对骨痹颗粒原方中君药桑寄生展开。
本研究收集不同产地、寄主、生长状态及加工方式的桑寄生药材,建立指纹图谱并测定槲皮苷的含量,初步探究影响指纹图谱的药材信息与色谱峰因素,以期为桑寄生及骨痹颗粒质量提升研究提供参考。
1 材料
1.1 仪器 Waters e2695 高效液相色谱系统(含四元泵溶剂系统、在线脱气机和自动进样器、Waters 2998 型紫外检测器(PDA)(美国Waters 公司);BSA224S-CW 电子天平(赛多利斯科学仪器北京有限公司);HC-C6002 型电子天平(慈溪市华徐衡器实业有限公司);EPED-E2-20TS 实验室级超纯水器(南京易普易达科技发展有限公司);KH-250B 型超声波清洗器(昆山禾创超声仪器有限公司)。
1.2 试剂与药物 乙腈、甲醇(德国默克公司);水为超纯水;磷酸(分析纯,西陇科技股份有限公司)。原儿茶酸(南京良纬生物科技有限公司,批号lw18012207);(+)-儿茶素(上海源叶生物科技有限公司,批号PO2A9F57645);槲皮苷(批号111538-201606)、芦丁(批号100080-201810)、槲皮素(批号100081-201610),均购于中国食品药品检定研究院;萹蓄苷(金益柏生物科技有限公司,批号16060806);桑寄生药材,信息见表1。
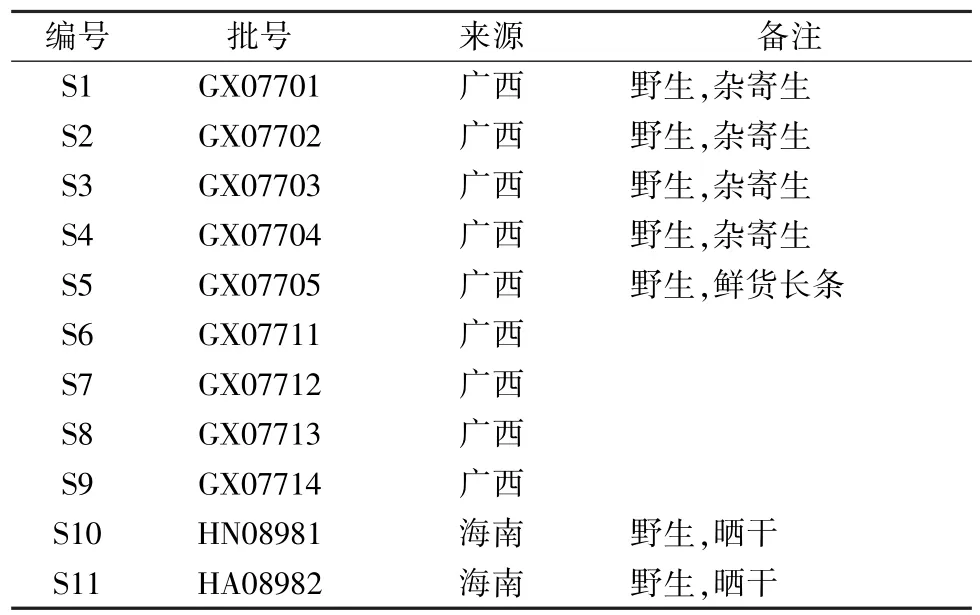
表1 桑寄生药材信息
2 方法
2.1 桑寄生指纹图谱建立
2.1.1 色谱条件 Agilent ZORBX SB-C18柱(4.6 mm×250 mm,5 μm);流动相乙腈(A)-0.2% 磷酸水溶液(B),洗脱梯度(0~6 min,2%~8%A;6~10 min,8%~10%A;10~15 min,10%~12%A;15~25 min,12%~16%A;25~45 min,16%~30% A;45~50 min,30%~36% A;50~53 min,36% A;53~55 min,36%~43% A;55~60 min,43%~56% A;60~62 min,56%~60% A;62~65 min,60%~2% A;65~70 min,2% A);检测波长225 nm;体积流量1.0 mL/min;柱温30 ℃;进样量10 μL。理论塔板数按槲皮苷峰计算应不低于10 000。
2.1.2 对照品溶液制备 分别取原儿茶酸、(+)-儿茶素、萹蓄苷、槲皮苷、槲皮素对照品适量,精密称定,各加甲醇制成每1 mL 含0.10 mg 的溶液,即得。
2.1.3 供试品溶液制备 精密称定1.0 g 药材粗粉,加入50%甲醇-水溶液30 mL,超声(200 W,40 kHz)提取30 min,离心,取上清液过0.45 μm 微孔滤膜,即得。
旅游纪念品长“同一张脸”,不仅会让游客产生审美疲劳,且不利于推广各个景区的独特旅游价值。尤其是同质化、低端化、地摊化的旅游纪念品会大大拉低国人的旅游购物消费。据统计,旅游购物在欧美国家占旅游业收入的50%到60%,在亚洲发达国家占40%以上,而在我国目前只占28%,国内外游客对旅游商品的满意度可见一斑。
2.1.4 方法学考察
2.1.4.1 精密度试验 取S9 供试品溶液,在“2.1.1”项条件下连续进样6 次,每次10 μL,记录色谱图。以槲皮苷色谱峰为参照,测得各共有峰的相对保留时间RSD 均小于0.5%,相对峰面积RSD 均小于3.0%,表明仪器精密度良好。
2.1.4.2 稳定性试验 取S9 供试品溶液,每隔3 h 进样一次,共测定18 h,分别进样10 μL,记录色谱图,以槲皮苷色谱峰为参照,测得各共有峰的相对保留时间RSD 均小于2.5%,相对峰面积RSD 均小于3.0%,表明供试品溶液在18 h 内稳定性良好。
2.1.4.3 重复性试验 取S9 样品,按“2.1.3”项下方法平行制备6 份供试品溶液,分别在“2.1.1”项条件下进样,记录色谱图,以槲皮苷色谱峰为参照,测得各共有峰相对保留时间RSD 均小于1.5%,相对峰面积RSD 均小于4.5%,表明该方法重复性良好。
2.1.5 指纹图谱建立 取11 批样品,按“2.1.3”项下方法制备供试品溶液,并在“2.1.1”项条件下进样,收集色谱图。图谱导入国家药典委员会推荐的中药色谱指纹图谱相似度评价系统2004A 版,设S9 样品图谱作为参照图谱,采用平均数法,时间窗宽度为0.1,经过多点校正后自动匹配,对11 批不同样品的指纹图谱及与生成的对照指纹图谱进行相似度分析。
2.2 槲皮苷含量测定
2.2.1 色谱条件与系统适应性试验 同“2.1.1”项下方法;检测波长254 nm。
2.2.2 供试品溶液制备 同“2.1.3”项下方法。
2.2.3 方法学考察
2.2.3.1 线性关系考察 对照品母液制备,取槲皮苷对照品约10 mg,精密称定,置于10 mL 量瓶中,用甲醇定容,制备成1 mL 含1 mg 槲皮苷对照品溶液。精密吸取对照品母液5.0 mL,置于10 mL 量瓶中,用甲醇定容,并逐级对半稀释,在“2.1.1”项条件下进样。以进样量为横坐标(X),峰面积为纵坐标(Y)进行回归,得槲皮苷回归方程Y=25 493 401X+181 920(r =0.999 9),在0.312 5~10.000 0 μg范围内线性关系良好。
2.2.3.2 精密度试验 取S9 供试品溶液与槲皮苷对照品,在“2.1.1”项条件下连续进样6 次,每次10 μL,记录色谱图,测得槲皮苷峰面积RSD 分别为0.47%、0.92%,表明仪器精密度良好。
2.2.3.3 稳定性试验 取S9 供试品溶液与槲皮苷对照品,在“2.1.1”项条件下,每隔3 h 进样1 次,共测定18 h,分别进样10 μL,记录色谱图,测得槲皮苷峰面积RSD 分别为0.33%、0.54%,表明供试品及对照品溶液中槲皮苷在18 h 内稳定性良好。
2.2.3.4 重复性试验 按“2.1.3”项下方法平行制备6份S9 供试品溶液,在“2.1.1”项条件下进样10 μL 分析,记录色谱图,测得槲皮苷峰面积RSD 为0.54%,表明该方法重复性良好。
2.2.3.5 加样回收率试验 平行精密称取6 份S9 样品,加入一定量槲皮苷对照品溶液按“2.1.3”项下方法制备供试品溶液,在“2.1.1”项条件下进样10 μL 分析,记录色谱图,测得槲皮苷的回收率分别为100.18%、99.64%、100.32%、102.12%、102.64%、102.84%,平均回收率101.29%。
3 结果
3.1 特征图谱建立 设S9 样品图谱作为参照图谱,采用平均数法,时间窗宽度为0.1,生成对照指纹图谱,见图1,在桑寄生药材特征图谱中建立24 个特征峰。与槲皮苷参照峰相应的峰为S 峰,计算各特征峰与S 峰的相对保留时间,其相对保留时间应在规定值的±5%之内。规定值为0.16(峰4)、0.30(峰9)、0.39(峰10)、0.43(峰11)、0.46(峰12)、0.48(峰13)、0.64(峰15)、0.66(峰16)、0.72(峰17)、0.74(峰18)、0.86(峰20)、0.90(峰21)、0.93(峰22)、0.98(峰23)。采用对照品比对法结合紫外吸收光谱可指认峰9 为原儿茶酸,峰12 为(+)-儿茶素,峰20 为芦丁,峰23 为萹蓄苷,峰24 为槲皮苷。
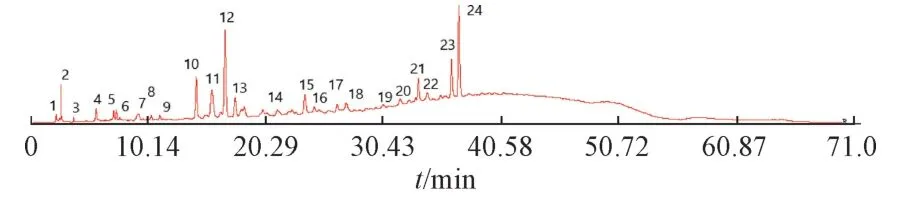
图1 桑寄生特征图谱
3.2 相似度评价 经多点校正后对11 批样品指纹图谱进行匹配,仅得到2 个共有峰,见图2,相似度见表2。
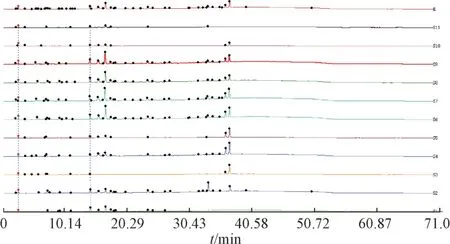
图2 11 批样品HPLC-PDA 指纹图谱
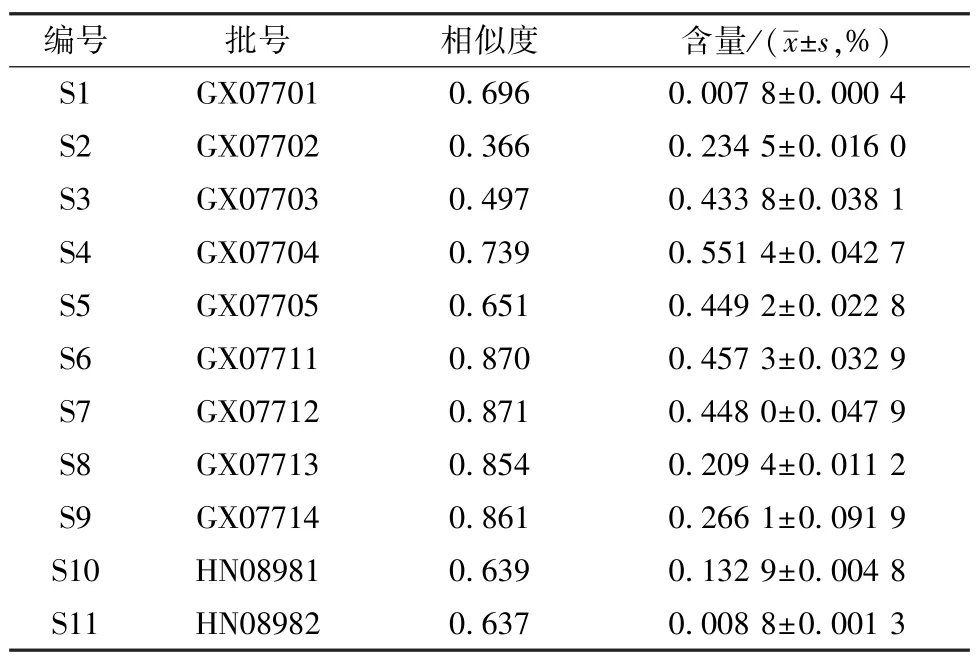
表2 桑寄生药材指纹图谱相似度与含量
11 批药材相似度为0.366~0.871,均小于0.9,表明药材差异大。11 批样品指纹图谱中,仅找到2 个共有峰,共有峰数目少,主要由个别样品引起,S3、S10 在0~25 min部分色谱峰较少,S1、3、11 在25~40 min 部分色谱峰较少。
3.3 槲皮苷含量 将11 批样品按“2.1.3”项下方法制备供试品溶液,在“2.1.1”项条件下(检测波长254 nm)进样分析,平行3 次,计算各批样品中槲皮苷的平均含量及RSD。表2 显示,槲皮苷含量最高达0.551 4%,最低0.007 8%,具有较大差异。采用SPSS 24.0 软件,经Explore 过程检验其平均含量正态分布,设置信区间为95%,依据ShapiroWilk 法检验,结果为P =0.237>0.05,具有统计学意义,表明各批槲皮苷含量呈正态分布。
4 讨论与分析
4.1 检测波长 采用二极管阵列在200~400 nm 范围内进行紫外全波长扫描,得到3D 峰形-时间图谱,从整体上看,225 nm 波长下整体色谱峰吸收强烈,色谱信息丰富,桑寄生中主要为黄酮类成分,360 nm 下槲皮苷成分色谱峰面积稳定。与水以及甲醇相比,桑寄生中成分用50%甲醇-水提取的效果更佳,基线噪音小,对色谱峰干扰小。
4.2 指标成分选择 桑寄生中多含黄酮类、生物碱、生物碱、氨基酸等成分,曾有报道含有儿茶类成分,寄主不同,糖苷类含量具有一定差异。本研究采用PDA 全波长扫描检测全程色谱峰紫外吸收光谱,60%以上色谱峰表现出黄酮类紫外吸收光谱特点。黄酮类成分主要为槲皮苷、萹蓄苷等,是桑寄生的主要活性成分,有研究表明槲皮苷是桑寄生归肝、肾经与祛风湿功效的重要物质基础[14-18],故将槲皮苷作为含量检测对象。另外,文献曾有报道桑寄生检测出槲皮素[11],曹越等[19]将槲皮素作为桑寄生指纹图谱的特征性成分之一,但本研究中仅S11 检测出少量槲皮素,大部分黄酮类以槲皮苷形式存在,与苏本伟等[18]报道一致。
4.3 聚类分析 将特征峰响应值导入SPSS 24.0,采用系统聚类法,方法组间联接,平均欧式距离为测量区间。聚类树状图分为2 个主支,S6~S9 为非野生品种,聚在一起,其余为另外一支,均为非野生品种。下支S3~S5 相聚,S1~S2、S10~S11 相聚,其中S5 为桑树寄主,而S3~S4 非桑树寄主,但S3 与S5 更为相似,表明寄主差异对桑寄生特征峰面貌影响较低;另外,S10~S11 产于海南,与产于广西的S1~S2 区分开,表明一定程度上可区分产地。初步推测影响桑寄生特征峰整体面貌的因素①生长状态(野生/非野生);②寄主(桑树寄主/杂寄生);③产地,且其影响程度可能为生长状态>产地因素>寄主因素。见图3。
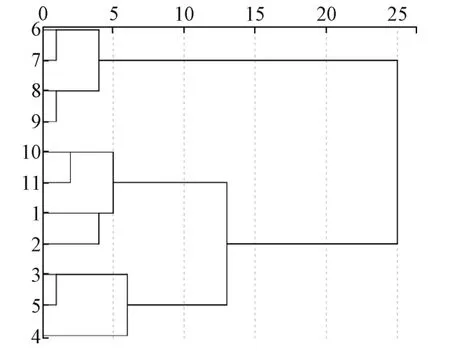
图3 聚类分析图
4.4 主成分分析 为研究影响桑寄生药材特征峰面貌的主要成分,将响应值数据采用SPSS 24.0 进行标准化处理。总方差解释结果见表3。
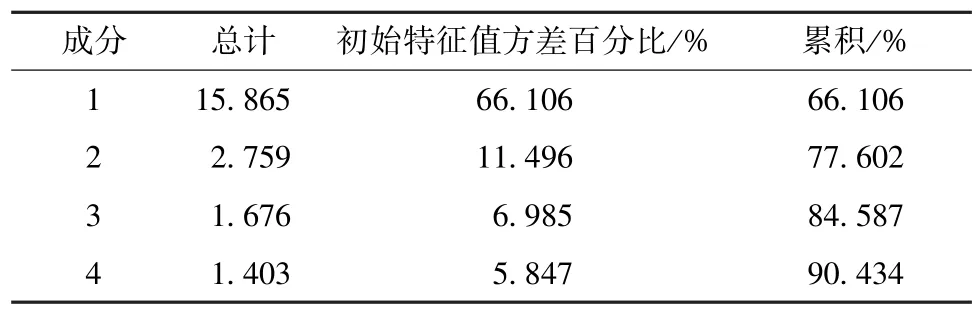
表3 总方差分析
前4 个主成分特征值均大于1,对总方差的贡献率达90.434%,即累积对桑寄生特征峰整体面貌的贡献为90.434%,因此选择前4 个主成分进行分析,将得到的成分矩阵进行标准化处理,经过方差最大正交旋转后,得到旋转后因子负荷矩阵。
将矩阵导入SIMCA 14,绘制椭圆得分图,见图4。以色谱峰为研究对象,以经过椭圆中心(0,0)点的两垂直坐标轴为基准,综合考察色谱峰对应点与两坐标轴的距离,垂直距离越远,代表其对区分不同批样品的贡献越大,即对桑寄生特征峰整体面貌的影响作用越大。结果见图4,表明9、6、24、23 号峰是影响桑寄生整体面貌的特征峰,其中原儿茶酸、槲皮苷及萹蓄苷的含量对表现桑寄生整体面貌具有意义。
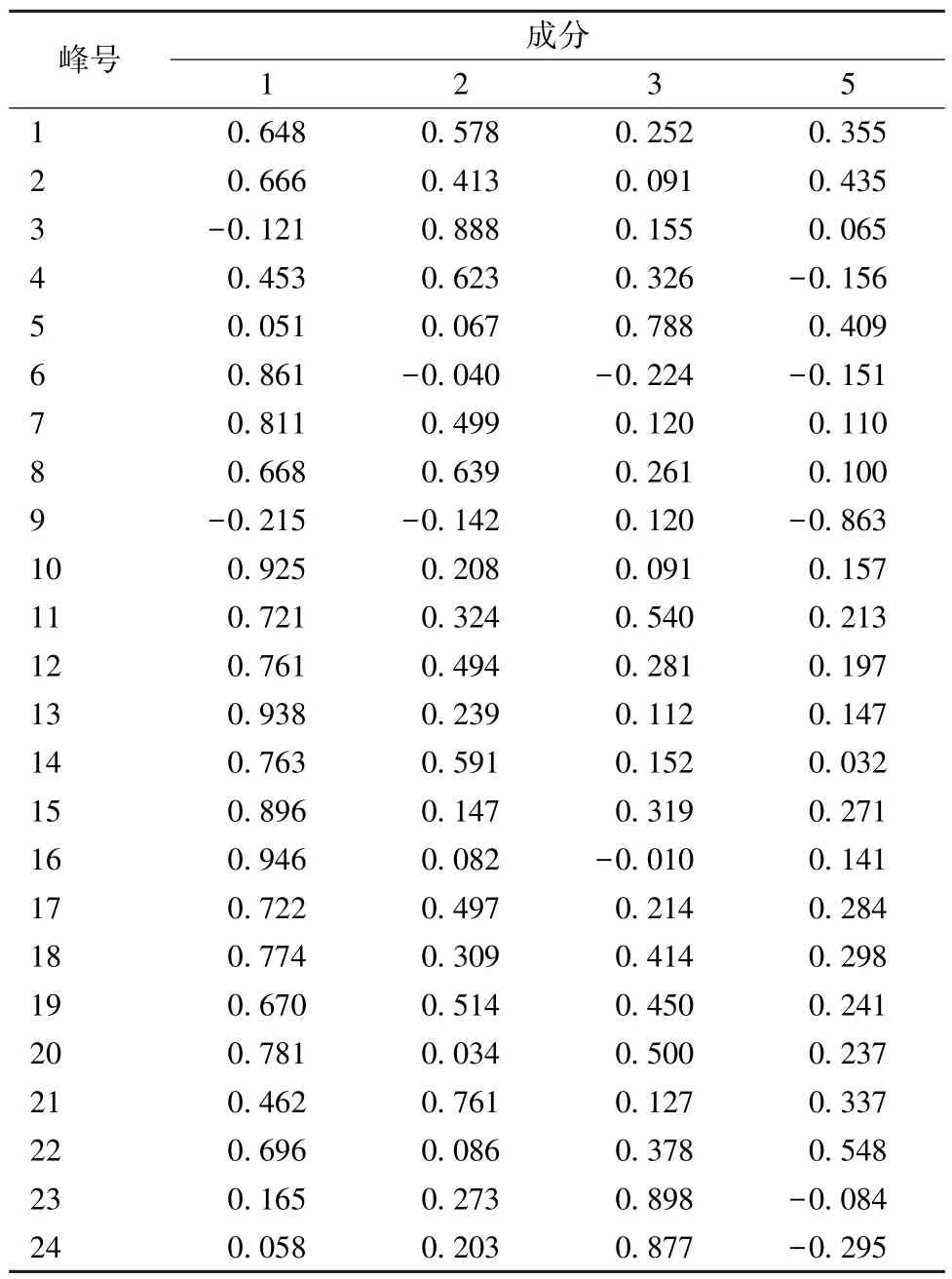
表4 旋转后因子负荷矩阵
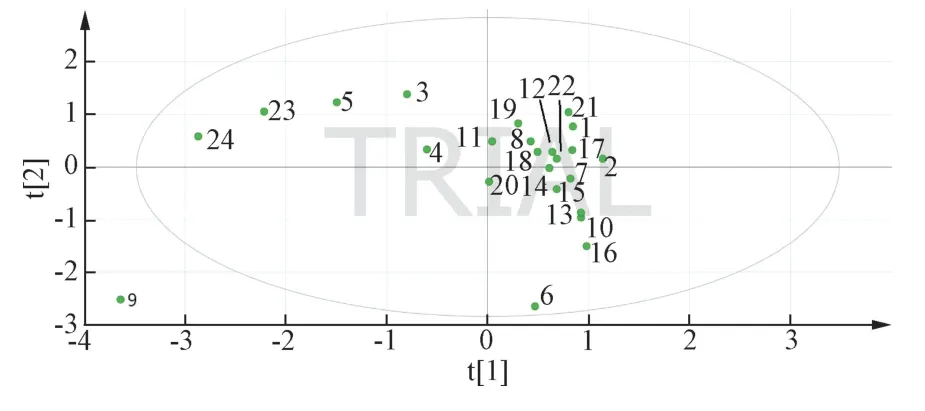
图4 22 批样品主成分分析图
5 结论与展望
本研究建立了桑寄生药材指纹图谱与含量测定方法,对主要色谱峰进行指认,通过聚类分析与主成分分析研究影响桑寄生特征峰面貌的因素(生长状态、产地、寄主)及主要色谱峰(原儿茶酸、槲皮苷、萹蓄苷),以期为研究桑寄生质量及骨痹颗粒成方制剂质量稳定提供基础。精制后的骨痹方药液能改善炎症并促软骨细胞增殖[19],桑寄生化学成分繁多复杂,药效成分众多,药理作用广泛,要建立全面的科学的药材质量评价体系,针对桑寄生单味药以及有效成分群进行细胞水平生物药效研究,以期为进一步提高骨痹颗粒质量与临床合理用药提供参考。
