柠檬酸交联处理对壳聚糖纤维的增强作用
2020-12-28胡天娇陆晔婷彭亚倩李蔚张祝辉侯秀良
胡天娇 陆晔婷 彭亚倩 李蔚 张祝辉 侯秀良

摘要: 为解决纯壳聚糖纤维力学性能较差的问题,文章采用柠檬酸溶液进行交联处理,探讨了交联处理条件(柠檬酸溶液质量分数、pH值、温度、时间)对壳聚糖纤维力学性能的影响。结果表明,在柠檬酸溶液质量分数20%、pH 6、交联温度50 ℃、交联时间2.5 h时,纤维力学性能达到最佳,干态断裂强度提高了36.36%,干态断裂伸长率提高了31%;湿态断裂强度提高了39.81%,湿态断裂伸长率提高了31%。通过对处理前后壳聚糖纤维自由氨基量与红外吸收光谱图的变化分析,表明柠檬酸与壳聚糖上的氨基产生离子交联和化学交联,从而提高了壳聚糖纤维的力学性能。
关键词: 壳聚糖;柠檬酸;交联;纤维;力学性能
中图分类号: TS102.6 文献标志码: A 文章编号: 10017003(2020)12001506
引用页码: 121103 DOI: 10.3969/j.issn.1001-7003.2020.12.003(篇序)
Effect of cross-linking treatment with citric acid on enhancement of chitosan fiber
HU Tianjiao, LU Yeting, PENG Yaqian, LI Wei, ZHANG Zhuhui, HOU Xiuliang
(Key Laboratory of Science & Technology of Eco-Textiles, Ministry of Education, Jiangnan University, Wuxi 214122, China)
Abstract: In order to improve the mechanical properties of pure chitosan fiber, citric acid solution was used for cross-linking treatment, and the effects of cross-linking treatment conditions(including mass fraction of citric acid solution, pH, temperature, and time) on mechanical properties of chitosan fibers were studied. The results showed that the fiber had the best tensile properties under the following conditions: mass fraction of citric acid solution 20%, pH 6, cross-linking temperature 50 ℃ and cross-linking time 2.5 h. Meanwhile, the dry breaking strength and breaking elongation increased by 36.36% and 31% respectively, while the wet breaking strength and breaking elongation of chitosan fiber increased by 39.81% and 31% respectively. By analyzing the changes of the free amino groups and FTIR spectra of chitosan fibers before and after the treatment, it was found that the ionic cross-linking and chemical cross-linking were generated between the amino groups of chitosan and citric acid, and therefore the mechanical properties of chitosan fibers improved.
Key words: chitosan; citric acid; cross-linking; fiber; tensile properties
殼聚糖是甲壳素脱乙酰化的产物,具有抑菌、除臭、吸附金属离子等多种优良性能[1],由壳聚糖制得的纤维在功能性纺织品、生物医用等领域具有潜在的应用价值[2-3],但纯壳聚糖纤维的力学性能较差,这是限制其进一步应用的关键因素。为提高壳聚糖纤维的力学性能,可采用醛类、环氧氯丙烷等交联剂[4-6]对壳聚糖进行交联处理,但是这些交联剂对生物系统具有较高毒性[7-8]。朱小颖等[9]采用天然多酚五倍子单宁对壳聚糖纤维进行改性整理,整理后的壳聚糖纤维力学性能得到一定提高。柠檬酸是一种有机三元羧酸,安全环保、来源广泛、价格低廉,已作为交联剂应用在蛋白质、淀粉等天然高分子材料中[10-11]。目前,已有研究使用柠檬酸交联壳聚糖制备膜[12]和凝胶[13]材料。
本文采用柠檬酸溶液对壳聚糖纤维进行后处理,研究了不同柠檬酸质量分数、pH值、温度、时间处理条件对壳聚糖纤维干态断裂强度和干态断裂伸长率的影响,并探究了壳聚糖与柠檬酸的交联机理,以改善壳聚糖纤维的力学性能。
1 实 验
1.1 材料与仪器
脱乙酰度95.7%、线密度1.97 dtex、长度50 mm的壳聚糖纤维(山东莱州市海力生物制品有限公司),无水柠檬酸、氢氧化钠(分析纯,国药集团化学试剂有限公司)。
GZX-9140 MBE电热鼓风干燥箱(上海博讯实业有限公司医疗设备厂),HH-4数显恒温水浴锅(荣华仪器制造有限公司),YG004型电子纤维强力机(常州德普纺织科技有限公司),Nicolet iS 10傅里叶变换红外光谱仪(美国THERMO FISHER),HITACHI SU 1510型扫描电子显微镜(日本日立株式会社)。
1.2 交联处理方法
将壳聚糖纤维在85℃条件下干燥24 h,干燥后的壳聚糖纤维浸泡于柠檬酸溶液中,在一定条件下处理一段时间,分别获得在不同柠檬酸溶液质量分数(0~25%)、不同柠檬酸溶液pH值(5~9)、不同温度(30~70 ℃)、不同时间(0~3 h)条件处理后的交联壳聚糖纤维。用氢氧化钠调节柠檬酸溶液到特定的pH值。处理后的纤维在去离子水中充分洗涤3次,并在85 ℃条件下干燥约3 h,然后放入温度20 ℃、相对湿度65%的恒温恒湿条件下平衡24 h。
1.3 性能测试及结果表征
1.3.1 壳聚糖纤维力学性能测试
根据化学纤维单纤维断裂强力和断裂伸长率的测定标准GB 9997—1988《化学纤维单纤维断裂强力和断裂伸长的测定》,在温度20 ℃、相对湿度65%环境中,将平衡后的纤维采用YG 004型电子纤维强力机进行力学性能测试。设定夹持距离20 mm,拉伸速率20 mm/min,分别得到纤维干态断裂强度和干态断裂伸长率,取50次数据的平均值。将纤维浸没在水中2 min后取出,再同上操作测试,得到纤维的湿态断裂强度和湿态断裂伸长率。
1.3.2 壳聚糖纤维形貌表征
采用HITACHI SU 1510扫描电镜观察壳聚糖纤维的表面形貌。将两种平衡后的纤维样品置于导电胶上,喷金后在加速电压5 kV的电镜下观察。
1.3.3 壳聚糖纤维自由氨基量测定
采用电导结合电位滴定法测定未交联壳聚糖纤维和交联壳聚糖纤维的自由氨基量。将壳聚糖纤维在85℃条件下干燥24 h,取0.3 g未交联壳聚糖纤维作为对照样,再取0.3 g壳聚糖纤维采用柠檬酸溶液进行交联处理,用去离子水充分洗涤3次并干燥,得到交联壳聚糖纤维。分别将两种纤维分散在50 g去离子水中,加入过量质量浓度0.1 mol/L HCl,将pH值调节至2左右,使得壳聚糖上的氨基完全质子化,此时壳聚糖全部溶解在体系中;再用0.1 mol/L NaOH溶液滴定壳聚糖溶液,每滴1 mL记录一次电导率和pH值,得到未交联壳聚糖纤维与交联壳聚糖纤维的电导滴定曲线和电位滴定曲线。两种纤维的滴定实验分别取3组做平行实验。
根据文献[14],可采用化学交联百分率(Y)计算壳聚糖自由氨基与柠檬酸化学交联的程度,其公式为:
式中:N1为未交联壳聚糖纤维的自由氨基量,N2为交联壳聚糖纤维的自由氨基量。
1.3.4 壳聚糖纤维化学结构测试
利用Nicolet iS 10傅里叶变换红外光谱仪对交联处理前后的壳聚糖纤维进行测试,分辨率4 cm-1,扫描范围500~4 000 cm-1。
2 结果与分析
2.1 交联处理条件优化
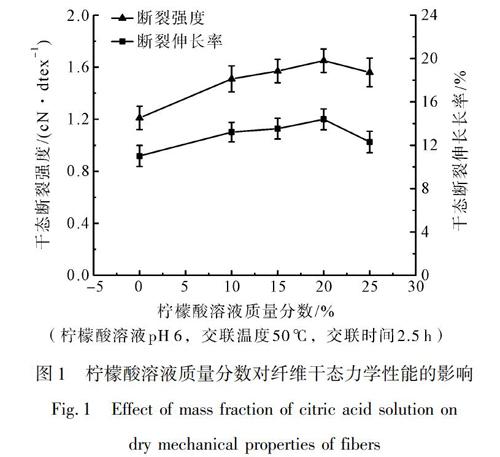
2.1.1 柠檬酸溶液质量分数对壳聚糖纤维干态力学性能的影响
柠檬酸溶液质量分数对壳聚糖纤维干态力学性能的影响如图1所示。由图1可知,未交联壳聚糖纤维的干态断裂强度为1.21 cN/dtex、干态断裂伸长率为11.01%。当柠檬酸质量分数小于20%时,随着质量分数的上升,交联壳聚糖纤维的干态断裂强度和干态断裂伸長率逐渐升高。当柠檬酸质量分数为20%时,交联纤维的干态断裂强度和干态断裂伸长率均达到最大值,分别为1.65 cN/dtex和14.39%,但随着柠檬酸质量分数继续升高,纤维的干态断裂强度和干态断裂伸长率下降。增大柠檬酸质量分数能使壳聚糖大分子接触更多柠檬酸分子,使得交联程度提高[15],但柠檬酸质量分数过高,过度交联反而使得壳聚糖大分子之间滑移难度增加,导致纤维的柔韧性变差,干态断裂强度和干态断裂伸长率下降。
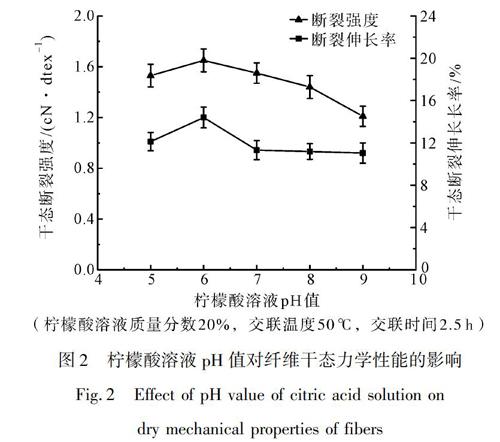
2.1.2 柠檬酸溶液pH值对壳聚糖纤维干态力学性能的影响
柠檬酸溶液pH值对壳聚糖纤维干态力学性能的影响如图2所示。当pH值为6时,交联壳聚糖纤维的干态断裂强度和干态断裂伸长率达到最大值1.65 cN/dtex和14.40%,但随着pH值继续升高,纤维的干态断裂强度和干态断裂伸长率下降。在酸性条件下,纤维干态力学性能提高较明显,交联溶液中的H+使壳聚糖上的NH2被质子化成NH+3,COO-与NH+3结合的机会增加,有利于离子交联的进行。交联液的酸性越大,纤维结构越不稳定,断裂强度和断裂伸长率提高较少;随着pH值的增大,壳聚糖的氨基质子化程度下降,COO-与NH+3结合的机会逐渐变少,交联程度逐渐下降。当pH值达到9时,交联纤维干态断裂强度为1.21 cN/dtex和干态断裂伸长率为11.04%,与未交联纤维干态断裂强度为1.21 cN/dtex和干态断裂伸长率为11.01%大致相同。
2.1.3 交联温度对壳聚糖纤维干态力学性能的影响
交联温度对壳聚糖纤维干态力学性能的影响如图3所示。随着温度的升高,纤维的干态断裂强度和干态断裂伸长率逐渐增大,当温度达到50 ℃时,纤维的干态断裂强度和干态断裂伸长率达到最大值1.65 cN/dtex和14.41%;随着温度的继续升高,纤维的干态断裂强度和干态断裂伸长率稍有下降。温度越高,分子活动能力增大,有利于增大壳聚糖上的氨基质子化程度,壳聚糖分子链上的NH+3增多,促进了柠檬酸和壳聚糖的离子交联;当温度超过50 ℃时且在酸性条件下,壳聚糖纤维降解的负作用大于交联产生的正作用,导致壳聚糖纤维降解加快[16],所以纤维的干态断裂强度和干态断裂伸长率稍有下降。由图3可知,温度对交联壳聚糖纤维干态力学性能没有明显影响。
2.1.4 交联时间对壳聚糖纤维干态力学性能的影响
交联时间对壳聚糖纤维干态力学性能的影响如图4所示。随着时间的增加,交联壳聚糖纤维干态断裂强度和干态断裂伸长率逐渐增大,当时间达到2.5 h时,纤维的干态断裂强度和干态断裂伸长率达到最大值1.64 cN/dtex和14.01%;随着交联时间继续增加,纤维的干态断裂强度和干态断裂伸长率略微下降。交联时间的增加,离子交联的程度也会随之上升,大分子之间的结合力变大,纤维的干态断裂强度和干态断裂伸长率提高。但是随着交联时间的继续增加,COO-与NH+3的结合已经达到平衡,因此纤维的干态断裂强度和干态断裂伸长率不会再继续增大。
2.2 交联处理后壳聚糖纤维的力学性能与形貌
如图5所示,壳聚糖纤维经柠檬酸溶液交联处理后,干态及湿态断裂强度和断裂伸长率均有所提高。图5(a)中,交联纤维干态断裂强度在柠檬酸质量分数为20%时达到最大值1.65 cN/dtex,但湿态断裂强度在柠檬酸质量分数为15%时达到最大值1.51 cN/dtex。湿态下的纤维会吸收水分子,使得大分子之间结合力变弱[17],所以纤维的湿态断裂强度低于干态断裂强度。壳聚糖纤维交联后,其亲水性氨基被柠檬酸封闭,但连接壳聚糖大分子的柠檬酸分子也具有亲水性,所以交联纤维的湿态断裂强度相比于干态断裂强度没有明显增大。交联在壳聚糖纤维上的柠檬酸越多,湿态下纤维结合的水分子越多,导致纤维湿态断裂强度降低更快。图5(b)中,在柠檬酸质量分数为20%时,交联纤维干态断裂伸长率达到最大值14.39%,由于柠檬酸上携带的羟基与壳聚糖大分子上的羟基容易形成氢键,而氢键是一种可移动的键型[18],所以能提高壳聚糖纤维的延伸能力,然后纤维的干态断裂伸长率由于过度交联开始下降;其湿态断裂伸长率也是同样的趋势,在柠檬酸质量分数为20%时达到最大值13.35%。
图6为交联前后壳聚糖纤维的表面形貌。由图6(a)可知,未交联纤维表面有凹槽,这是由于壳聚糖纤维是由湿法纺丝制得的,纺丝液在进入凝固浴后,凝固及牵伸过程中纤维表面受力不匀,导致纤维具有不规则的表面形态。由图6(b)可以看出,壳聚糖纤维经柠檬酸交联处理后,纤维表面的凹槽不明显,柠檬酸结合到纤维的表面,使得壳聚糖纤维的表面更加饱满光滑,在纤维拉伸过程中,分子间分担应力更加均匀,从而提高了纤维的力学性能。
2.3 柠檬酸与壳聚糖交联机理
2.3.1 自由氨基的电导与电位滴定分析
如图7所示,随着滴定过程中OH-的不断增加,滴定体系中电导率及pH值呈现出典型的转变。图7(a)中,未交联壳聚糖纤维的整个滴定过程可以分为三个部分:第一部分为OH-中和过量来自HCl的H+;第二部分为OH-与质子化壳聚糖的NH+3反应;第三部分为滴定体系中H+被OH-完全消耗,pH值随着OH-离子在体系中的过量滴入而迅速增加[19]。而图7(b)中,交联纤维比未交联纤维在第一部分和第二部分多一个部分,即因为经柠檬酸处理后的壳聚糖分子上连接着大量的柠檬酸分子,在滴定体系中,过量滴入H+会使柠檬酸上的COO-脱离壳聚糖大分子变成羧基。由于—COOH与—NH+3均为弱酸,—COOH表现出比—NH+3更高的酸性,因此柠檬酸上的—COOH先较于壳聚糖上的NH+3被OH-中和,同时也证明了柠檬酸分子已经通过静电相互作用连接在壳聚糖大分子上。
在电导与电位滴定曲线上,滴定的每个部分都有较清晰的转折点,这些转折点代表着一个过程到另一个过程的转变,通过线性回归拟合这些曲线确定这些转折点,其中r2>0.98。根据电导滴定曲线计算,未交联壳聚糖纤维的自由氨基量为(4.946±0.026) mmol/g,交联壳聚糖纤维的自由氨基量为(4.708±0.023) mmol/g,根据式(1)计算得到壳聚糖纤维化学交联百分率为4.81%。交联处理后的纤维中存在柠檬酸分子,氨基与羧基形成化學键而导致壳聚糖上的自由氨基减少。由于柠檬酸分子与壳聚糖大分子产生离子交联和少量化学交联,使得壳聚糖纤维的力学性能提高。
2.3.2 红外光谱分析
如图8所示,在3 550~3 050 cm-1的特征峰中,未交联纤维中心在3 293 cm-1左右,交联纤维的中心在3 234 cm-1左右,对应于O—H和N—H的伸缩振动峰。交联前后纤维的红外光谱差异主要在1 700~1 450 cm-1区域内,前者中出现了两个强度相近的峰,即在1 654 cm-1和1 577 cm-1处分别为酰胺Ⅰ带的CO伸缩振动峰和酰胺Ⅱ带的N—H平面变形峰。交联纤维在1 530 cm-1左右处出现较明显的峰(—NH+3对称弯曲拉伸),根据文献[20],壳聚糖与柠檬酸产生离子交联会出现此峰,所以可以推断壳聚糖质子化的—NH+3与柠檬酸的COO-形成了离子键而产生离子交联;并且在1 560 cm-1处出现了一个尖锐的吸收峰,分析认为是壳聚糖上的氨基与柠檬酸上的羧基形成化学键,使得壳聚糖中的氨基从伯胺转变为仲胺。
如图9所示,一个柠檬酸分子可电离出三个COO-,可以与不同壳聚糖大分子链上的NH+3发生静电相互作用产生离子交联,一部分壳聚糖的氨基与柠檬酸的羧基形成化学键,产生化学交联;交联使得壳聚糖大分子之间相互交错纠缠,纤维在拉伸过程中的应力增大,从而提高了纤维的力学性能。传统的醛类交联剂对壳聚糖纤维处理,虽然会提高材料的强度,但不会增加甚至会降低材料的延伸能力,而采用柠檬酸溶液处理,不仅可以提高纤维的断裂强度,还同时提高断裂伸长率。因此,使用柠檬酸作为壳聚糖材料的交联剂,是环保且有效的选择。
3 结 论
本文采用柠檬酸对壳聚糖纤维进行交联处理,使得壳聚糖纤维的干态及湿态力学性能提高,并探究了两者产生交联的机理,为壳聚糖纤维性能改善及应用提供参考价值。
1)柠檬酸溶液交联处理壳聚糖纤维的优化条件:柠檬酸溶液质量分数为20%、pH值为6、温度为50 ℃、时间为2.5 h。
2)壳聚糖纤维经上述优化条件交联处理后,干态断裂强度提高了36.36%,干态断裂伸长率提高了31%;湿态断裂强度提高了39.81%,湿态断裂伸长率提高了31%;纤维表面凹陷不再明显。3)壳聚糖纤维干、湿态力学性能得到改善是由于柠檬酸羧基与壳聚糖大分子上的氨基之间产生离子交联和化学交联。4)采用柠檬酸溶液对壳聚糖纤维进行交联处理是一种改善壳聚糖纤维力学性能的简单、有效、环保的方法。
参考文献:
[1]PILLAI C K S, PAUL W, SHARMA C P. Chitin and chitosan polymers: chemistry, solubility and fiber formation[J]. Progress in Polymer Science, 2009, 34(7): 641-678.
[2]王載利, 李达, 马建伟. 壳聚糖纤维的应用前景及其生产技术的新进展[J]. 现代纺织技术, 2011, 19(2): 52-54.
WANG Zaili, LI Da, MA Jianwei. Application prospect of chitosan fiber and new progress of production technology[J]. Advanced Textile Technology, 2011, 19(2): 52-54.
[3]彭孟娜, 马建伟. 生物基化学纤维的发展现状及其应用[J]. 合成纤维工业, 2018, 41(3): 55-59.
PENG Mengna, MA Jianwei. Development and application of bio-based chemical fibers[J]. China Synthetic Fiber Industry, 2018, 41(3): 55-59.
[4]徐德增, 苏丹, 程雪, 等. 戊二醛交联壳聚糖/PVA共混纤维的制备[J]. 大连工业大学学报, 2013, 32(3): 206-208.
XU Dezeng, SU Dan, CHENG Xue, et al. Preparation chitosan/PVA blend fibers crosslinked with glutaraldehyde[J]. Journal of Dalian Polytechnic University, 2013, 32(3): 206-208.
[5]杨庆. 高强度壳聚糖纤维的制备及结构性能研究[D]. 上海: 东华大学, 2005.
YANG Qing. Study on The Preparation Structure and Properties of Chitosan Fibers with High Tenacity[D]. Shanghai: Donghua University, 2005.
[6]LEE S H, PARK S Y, CHOI J H. Fiber formation and physical properties of chitosan fiber crosslinked by epichlorohydrin in a wet spinning system: the effect of the concentration of the crosslinking agent epichlorohydrin[J]. Journal of Applied Polymer Science, 2004, 92(3): 2054-2062.
[7]冯斌. 醛类化合物DNA化学损伤机制及生物标志物的研究[D]. 济南: 山东省医学科学院, 2006.
FENG Bin. A Study on DNA Damage and Biomarkers of Aldehydes[D]. Jinan: Shandong Academy of Medical Sciences, 2006.
[8]李若刚, 宋茂启, 王桂林. 环氧氯丙烷烧伤及其毒理作用探讨[J]. 河南外科学杂志, 2000(3): 305-306.
LI Ruogang, SONG Maoqi, WANG Guilin. Study on burn and toxicity of epichlorohydrin[J]. Henan Journal of Surgery, 2000(3): 305-306.
[9]朱小颖, 孙其松, 彭诗怡, 等. 五倍子单宁改性整理壳聚糖纤维[J]. 天然产物研究与开发, 2019, 31(11): 1960-1967.
ZHU Xiaoying, SUN Qisong, PENG Shiyi, et al. The modified finishing of chitosan fiber with gallnut tannins[J]. Natural Product Research and Development, 2019, 31(11): 1960-1967.
[10]REDDY N, LI Y, YANG Y Q. Alkali-catalyzed low temperature wet crosslinking of plant proteins using carboxylic acids[J]. Biotechnology Progress, 2009, 25(1): 139-146.
[11]REDDY N, YANG Y Q. Citric acid cross-linking of starch films[J]. Food Chemistry, 2010, 118(3): 702-711.
[12]GUERRERO P, MUXIKA A, ZARANDONA I, et al. Crosslinking of chitosan films processed by compression molding[J]. Carbohydrate Polymers, 2019, 206: 820-826.
[13]GHOSH P, RAMESHBABU A P, DHARA S. Citrate cross-linked gels with strain reversibility and viscoelastic behavior accelerate healing of osteochondral defects in a rabbit model[J]. Langmuir, 2014, 30(28): 8442-8451.
[14]MOURA M J, FANECA H, LIMA M P, et al. In situ forming chitosan hydrogels prepared via ionic/covalent co-cross-linking[J]. Biomacromolecules, 2011, 12(9): 3275-3284.
[15]温乐蛟, 侯秀良, 娄高源, 等. 谷朊纤维制备及其柠檬酸交联处理研究[J]. 化工新型材料, 2014, 42(8): 101-103.
WEN Lejiao, HOU Xiuliang, LOU Gaoyuan, et al. Preparation of gulten fibers and cross-linking treatment with citric acid[J]. New Chemical Materials, 2014, 42(8): 101-103.
[16]李丹. 改性壳聚糖纤维的研究[D]. 大连: 大连工业大学, 2009.
LI Dan. Study on Modified Chitosan Fiber[D]. Dalian: Dalian Polytechnic University, 2009.
[17]ZHU X Y, HOU X L, MA B M, et al. Chitosan/gallnut tannins composite fiber with improved tensile, antibacterial and fluorescence properties[J]. Carbohydrate Polymers, 2019, 226: 115311.
[18]CHEN P H, KUO T Y, LIU F H, et al. Use of dicarboxylic acids to improve and diversify the material properties of porous chitosan membranes[J]. Journal of Agricultural and Food Chemistry, 2008, 56(19): 9015-9021.
[19]XU H, SHEN L, XU L, et al. Low-temperature crosslinking of proteins using non-toxic citric acid in neutral aqueous medium: mechanism and kinetic study[J]. Industrial Crops and Products, 2015, 74: 234-240.
[20]杨上莹, 袁卉华, 易兵成, 等. 柠檬酸改性壳聚糖水凝胶的制备与性能[J]. 功能高分子学报, 2018, 31(3): 232-240.
YANG Shangying, YUAN Huihua, YI Bingcheng, et al. Fabrication and characterization of citric acid modified chitosan hydrogel[J]. Journal of Functional Polymers, 2018, 31(3): 232-240.
收稿日期: 20200322; 修回日期: 20201104
基金項目: 江苏省自然科学基金项目(BK20180624);江苏高校优势学科建设工程资助项目(苏政办发〔2014〕37号);中央高校基本科研业务费专项资金项目(JUSRP51907A)
作者简介: 胡天娇(1996),女,硕士研究生,研究方向为生物基纺织材料。通信作者:侯秀良,教授,houxiuliang@163.com。