烟雾暴露大鼠肺血管形态与压力变化的实验研究
2020-12-14邢爱萍胡晓芸武晓兰
邢爱萍 胡晓芸 武晓兰
1山西医科大学第二医院全科医学科,太原030001;2山西医科大学第一医院呼吸与危重症医学科,太原030001;3太原市中心医院呼吸与危重症医学科,太原030002
肺动脉高压是多种原因引起的严重的慢性肺循环疾病,肺血管重塑是肺动脉高压形成的重要病理基础。吸烟是支气管、肺疾病的主要危险因素[1]。目前,吸烟对肺血管的直接作用引起学术界的广泛关注。有研究表明,香烟烟雾可以直接作用于肺血管系统,导致肺血管重塑,进而发生肺动脉高压[2]。但其机制目前尚未明确。本实验通过建立烟雾暴露大鼠模型,观察肺血管形态及压力变化,并使用透射电镜观察肺小动脉的超微结构,探讨吸烟对肺血管损害的发生机制。
1 材料与方法
1.1 材料 实验用卷烟为上海卷烟厂产大前门牌卷烟,每支含焦油13 mg,烟碱1.0 mg,一氧化碳14 mg。小鼠α-平滑肌肌动蛋白 (α-smooth muscle actin,α-SMA)单克隆抗体购自美国Santa Cruz公司。
1.2 方法
1.2.1 动物分组及模型制备 清洁级雄性SD 大鼠40只,购自山西医科大学实验动物中心,体质量(200±30)g,随机数字表法分为对照(C)组、烟雾暴露1 个月 (S1m)组、烟雾暴露2 个月(S2m)组、烟雾暴露3个月 (S3m)组,每组10只,所有大鼠均按照实验动物管理和使用指南进行饲养和处理,于恒温环境中饲养,自由饮水和进食。参照文献[3]的方法制作大鼠实验性烟雾暴露装置,以有机玻璃、不锈钢丝及角钢、玻璃板、空气泵、压力表、胶皮管等制成体积为1 m×0.6 m×0.5 m 的熏箱,并连接体积为0.3 m×0.2 m×0.25 m的吸烟小室。烟雾暴露时将大鼠放入玻璃熏箱内,点燃的香烟烟雾由吸烟小室导入,熏烟时舱内氧浓度保持在21%。大鼠每周熏烟6 d,每天上、下午各1 次,每次15 支,每支香烟点燃15 min后换烟。每次点燃2支香烟放入,对照组大鼠不予熏烟。本研究符合 《赫尔辛基宣言》的原则。
1.2.2 平均右心室收缩压 (mean right ventricular systolic pressure,mRVSP)测定 各组大鼠于实验终点分别为:S1m 组、S2m 组、S3m组以25%的乌拉坦 (4 ml/100 g)腹腔注射麻醉,仰卧位固定于解剖台,切开右颈部皮肤,钝性分离皮下组织及肌层,暴露右颈外静脉,右颈外静脉斜切口,将与压力感受器连接并充满肝素盐水的PV-1肺动脉插管插入右颈外静脉,通过压力换能器与多导生理记录仪相连。插入时保持导管的弧形向下,当插管插入3~4 cm 时,将插管左旋并向前推进,并密切观察生理记录仪图形。当压力上升并出现右心室波形时,立即固定导管并描记该波形,则测得m RVSP。
1.2.3 动脉血气分析 测压完毕后,腹主动脉采血2 ml,2 h内采用全自动血气分析仪行PaO2测定。
1.2.4 透射电镜标本制备 取新鲜肺组织(1 mm×1 mm×1 mm)立即固定于预冷的3%戊二醛溶液,再用1%锇酸后固定,梯度脱水后用环氧树脂861包埋。半薄切片定位肺腺泡内肌型动脉后,再行超薄切片,用醋酸铀及枸橼酸铅双染色后在JEM-100CXⅡ型透射电镜下观察肺腺泡内肌型动脉内皮细胞,弹性纤维及平滑肌细胞的超微结构。
1.2.5 肺组织病理学观察和图像分析 石蜡切片常规做HE染色,显微镜下观察各组大鼠肺组织病理学变化。采用BI-2000医学图像分析系统进行肺小动脉管壁面积/管总面积 (wall area,WA%)的测量。选取直径为100~200μm 的5支肺小动脉测量并记录WA%。
1.2.6 α-SMA 免疫组织化学染色 采用链酶亲和素-过氧化物酶法,一抗为小鼠α-SMA 单克隆抗体(美国Santa Cruz公司,1∶100)。用PBS替代一抗作为阴性对照。石蜡切片脱蜡至水,用3%过氧化氢消除内源性过氧化物酶活性,微波修复抗原;用5%牛血清白蛋白封闭非特异性位点,依次滴加α-SMA、生物素化羊抗小鼠IgG、SABC 试剂,3,3,-二氨基联苯胺显色,苏木素复染,脱水、透明、封片。显微镜下观察,阳性表达为胞浆内有棕黄色颗状着色。随机选取5支肺小动脉直径100~200μm 的肺小动脉,测量平滑肌细胞平均吸光度值。
1.3 统计学分析 采用SPSS 12.0统计软件进行分析,实验数据以±s 表示,各组间差异显著性检验采用单因素方差分析 (one-way ANOVA),组内两两比较采用LSD 检验分析。相关性检验采用Spearman相关分析法。P <0.05为差异有统计学意义。
2 结果
2.1 肺组织病理改变 对照组大鼠肺泡结构完整,肺小动脉管腔正常,管壁及其周围无炎性细胞浸润。S2m 组和S3m 组肺泡结构紊乱,肺泡壁变薄,有不同程度的断裂,肺小动脉管壁增厚,管腔狭窄,周围均出现淋巴细胞、单核巨噬细胞和中性粒细胞浸润,以S3m 组为著。
2.2 烟雾暴露各组PaO2与m RVSP变化 C 组、S1m、S2m 及S3m 组PaO2分别为 (96.2±4.3)mm Hg(1 mm Hg=0.133 k Pa)、 (92.1±5.2)mm Hg、 (90.5±4.1)mm Hg、 (89.6±4.8)mm Hg,各组间比较,差异无统计学意义(F =2.004,P >0.05),见表1。各组大鼠m RVSP 检测结果分别为C 组 (14.07±4.18)mm Hg,S1m 组 (16.85±1.26)mm Hg,S2m 组(23.57 ± 4.51) mm Hg,S3m 组 (65.63 ±5.6)mm Hg,S3m 组大鼠mRVSP较C 组及S1m组升高,差异有统计学意义 (F =10.100,P <0.01,表1)。
2.3 烟雾暴露各组肺动脉超微结构观察 C 组内皮细胞扁平,小动脉内弹力膜规则,平滑肌细胞无扭曲变形,胶原纤维排列整齐。S1m 组肺小动脉内皮细胞形状不规则,内膜增厚,细胞内可见线粒体肿胀,弹力纤维增生,平滑肌细胞轻度增生。S2m 组内弹力膜厚薄不均,部分断裂,结构不清;平滑肌走向不规则,胶原纤维增生。S3m 组肺小动脉结构紊乱,内皮细胞严重变形,胞内线粒体损伤明显,肿胀、减少甚至消失,细胞器模糊不清。内膜增厚更为明显,胶原纤维大量增生(图1)。
2.4 肺血管形态及WA%分析结果 C 组大鼠肺动脉壁薄,烟雾暴露各组随烟雾暴露时间延长,肺动脉壁逐渐增厚。WA%呈时间依赖性增加,烟雾暴露各组WA%与C 组比较,差异均有统计学意义(P 值均<0.01);烟雾暴露各组间比较,差异有统计学意义 (F =251.690,P <0.01,表1,图2)。
2.5 肺小动脉α-SMA 的表达 C组血管壁仅见少许α-SMA 表达,随烟雾暴露时间延长,肺动脉壁α-SMA 表达量呈时间依赖性增加,烟雾暴露各组与C组比较,差异有统计学意义(F=23.100,P <0.01);烟雾暴露各组间比较,差异均有统计学意义(P 值均<0.01,表1,图3)。
2.6 相关分析Spearman相关分析结果显示 肺血管WA%与α-SMA表达呈正相关(r=0.703,P <0.05);肺血管WA%与m RVSP 无相关性(r=0.379,P >0.05)。
表1 各组大鼠PaO2、m RVSP、α-SMA、WA%比较 (±s)

表1 各组大鼠PaO2、m RVSP、α-SMA、WA%比较 (±s)
注:1 mm Hg=0.133 k Pa;m RVSP 为平均右心室收缩压;α-SMA 为α-平滑肌肌动蛋白;WA%为管壁面积占血管总面积的百分比;与对照组比较,a P <0.01;与烟雾暴露1个月组比较,b P <0.01;与烟雾暴露2个月组比较,c P <0.05
组别鼠数PaO2 (mm Hg)m RVSP (mm Hg)α-SMA (A 值)WA% (%)对照组10 96.2±4.3 14.07±4.18 37.5±7.5 30.1±4.1烟雾暴露1个月组10 92.1±5.2 16.85±1.26 52.6±14.3a 41.2±6.3a烟雾暴露2个月组10 90.5±4.1 23.57±14.51 72.2±13.6ab 52.0±7.1ab烟雾暴露3个月组10 89.6±4.8 65.63±0.93ab 98.1±15.6abc 62.1±6.9abc F 值2.004 10.100 23.100 251.690 P 值>0.05<0.05<0.01<0.01
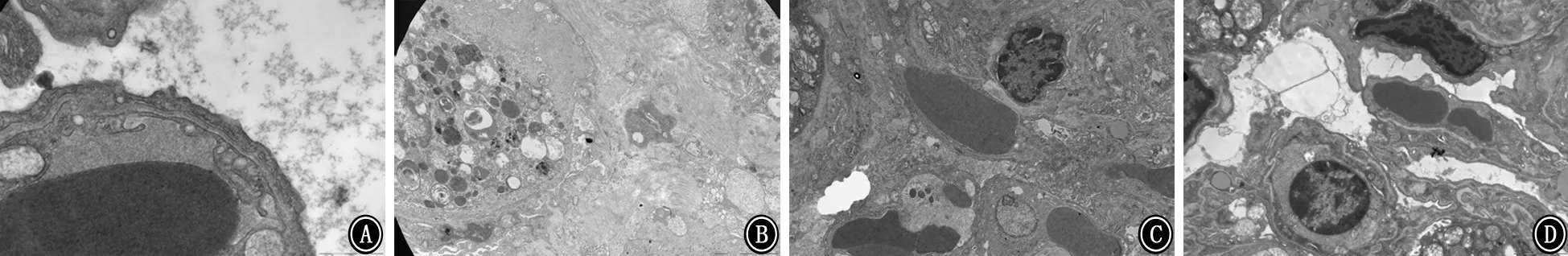
图1 各组大鼠肺小血管电镜观察结果 A:对照组 ×15 000;B:烟雾暴露1个月组 ×12 000;C;烟雾暴露2个月组 ×12 000;D:烟雾暴露3个月组 ×12 000
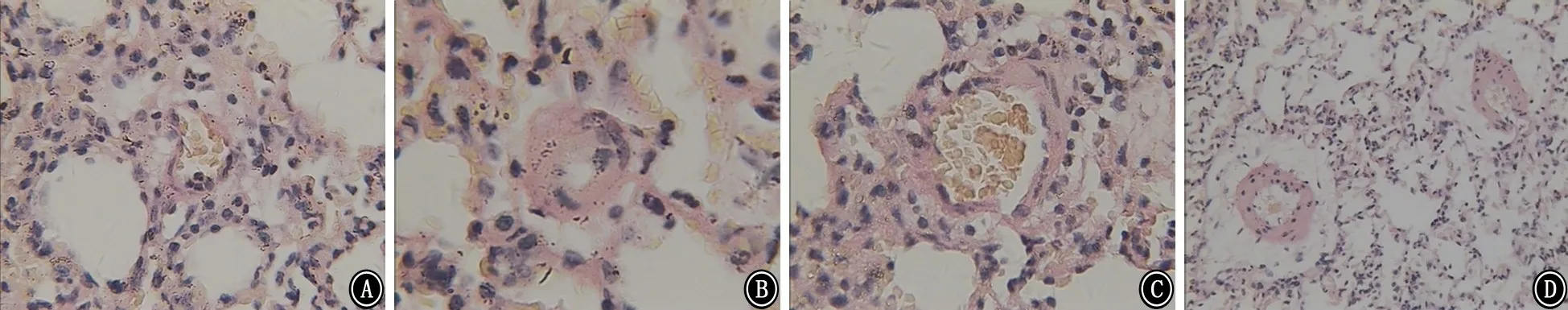
图2 各组大鼠肺动脉HE染色结果 HE ×100 A:对照组;B:烟雾暴露1个月组;C;烟雾暴露2个月组;D:烟雾暴露3个月组

图3 各组大鼠肺动脉α-SMA 免疫组化结果 免疫组织化学 ×400 A:对照组;B:烟雾暴露1个月组;C;烟雾暴露2个月组;D:烟雾暴露3个月组
3 讨论
肺动脉高压是一组由异源性疾病和不同发病机制引起的以肺血管阻力持续增加为特征的临床病理生理综合征,临床表现为右心室负荷增加,活动耐力下降,严重者可发生心脏衰竭而死亡。肺动脉高压的形成机制较为复杂,涉及多种因素的相互作用。血管收缩、血管重塑和血栓形成是导致肺循环血管阻力增加的主要原因[4]。肺血管重塑是肺动脉高压的病理学基础,其特点为内膜增厚,中膜平滑肌细胞增生和肥大,外膜成纤维细胞增殖和基质蛋白合成[5]。长期烟雾暴露可以导致肺血管重塑,且早于肺气肿的形成[6]。本研究在常氧下给予大鼠烟雾暴露,发现烟雾暴露3个月后右心室收缩压明显升高,而PaO2无下降,与Wright等[7]研究结果一致。反映了烟雾暴露所致肺动脉高压与低氧血症无直接关系,分析可能是香烟烟雾直接作用于肺血管系统而致肺血管重塑。
吸烟是一种较为严重的社会公共卫生问题,与许多疾病的发生、发展关系密切。香烟烟雾中含7 000多种化学物质,主要有尼古丁、焦油、一氧化碳、丙烯醛、一氧化氮、氢氰酸等6种,香烟中的主要成分尼古丁及其代谢产物有刺激平滑肌细胞增殖的作用。缺氧不是肺动脉高压的唯一因素,吸烟、炎症、氧化-抗氧化失衡等均可能参与肺动脉高压的形成[8]。本研究观察不同烟雾暴露时间对大鼠肺血管形态的影响,结果表明,烟雾暴露各组反映肺血管重塑的客观指标WA%均高于C 组,且随时间延长肺血管壁增厚渐明显,提示吸烟可致肺血管壁增厚。吸烟所致肺血管壁增厚的机制复杂,涉及血管舒缩功能失调、平滑肌增殖凋亡异常及血管重塑等多个环节[9-10]。本研究还发现烟雾暴露各组α-SMA 表达均高于C 组,而以S3m 组更为明显,提示吸烟导致无肌型动脉肌化,而这可能是肺循环阻力增大、肺动脉压升高的关键。
吸烟对肺血管的直接损害研究较少,烟雾暴露所致肺小血管超微结构病变尚属研究的薄弱环节。本实验发现与C 组相比,烟雾暴露后肺小动脉出现不同程度的内皮细胞肿胀,内弹力膜断裂,基底膜不完整及不规则增厚,胶原纤维在内膜下增生,中膜平滑肌细胞增生。与低氧研究结果类似但程度似有差别[11],表明吸烟可引起肺血管重塑,使肺微循环发生障碍,增加肺血管阻力,从而促进肺动脉高压的发生、发展。
总之,烟雾暴露可使肺血管形态发生明显改变,肺小动脉超微结构异常,导致肺血管重塑,肺血流阻力增加,右心室收缩压升高。
利益冲突所有作者均声明不存在利益冲突
