高镍三元正极材料的包覆与掺杂改性研究进展
2020-10-15柏祥涛班丽卿庄卫东
柏祥涛, 班丽卿, 庄卫东
高镍三元正极材料的包覆与掺杂改性研究进展
柏祥涛1, 班丽卿2, 庄卫东2
(1. 国联汽车动力电池研究院有限责任公司, 北京 101407; 2. 北京有色金属研究总院, 北京 100088)
随着新能源汽车的加速发展, 镍钴锰/铝酸锂三元正极材料、特别是高镍(镍含量大于50%)材料作为后起之秀, 由于其性能和成本的综合指标优于传统的钴酸锂和磷酸铁锂, 引起了学术界和产业界极大的研究兴趣。但是受其本身晶体结构和表面结构的限制, 三元正极材料也存在安全性较差、循环稳定性不足等缺点。近年来, 科研工作者为解决这些问题、并进一步提升三元材料的性能, 在材料改性技术方面开展了大量工作, 取得了令人瞩目的研究成果。本文从改性元素对三元正极材料结构以及对电化学性能改善的机理出发, 介绍了包覆和掺杂两种改性技术的研究进展, 并在此基础上对三元正极材料的发展方向做出展望。
镍钴锰酸锂; 包覆; 掺杂; 机理
新能源汽车产业是国家战略新兴产业, 随着车用动力电池需求的不断升级, 锂离子电池作为最有前途的储能介质受到了广泛关注[1]。与消费类电子用锂电池不同, 车用动力电池有更为严苛的要求, 如成本、能量密度、安全性、使用寿命等。研究[2]表明, 正极材料对这些性能有决定性作用。在众多正极材料中, 镍钴锰/铝酸锂三元正极材料(LiNiCoMn1–x–yO2/LiNiCoAl1–x–yO2, 简称NCM/NCA)、特别是高镍NCM/NCA(0.5≤<1)被寄予厚望[3-4]。在此类材料中, 其放电比容量随着镍含量的增加而升高[1], 但镍含量的增加也带来一系列新问题, 主要可分为表面问题和体相问题[2–7], 如表面残碱、过渡金属溶解、阳离子混排等。
在三元材料制备和存储过程中, 由于Ni3+的不稳定性, 其表面容易形成诸如LiOH和Li2CO3之类的碱性物质(可称为“残碱”), 残碱对三元材料的使用和性能均有不利影响[8]。LiOH使pH升高, 导致匀浆过程中容易形成“果冻”而无法涂布。Li2CO3造成水含量超标, 同时还导致电池循环过程产气, 影响安全性能。当Ni含量≤60%时, 通过一次烧结基本可以将残碱控制在可接受的范围内, 但是当Ni含量≥80%时, 则需对材料进行额外处理和多次烧结[9–11]。除残碱外, 活性材料与电解液之间的副反应也是影响NCM性能的重要因素。依据密度泛函理论(DFT)计算表明[12], 当电解液与正极材料接触时, 电解液中的碳酸乙烯酯(EC)与NCM的表面立即发生反应, 即此反应是化学反应而非电化学反应。在电解液中普遍存在的微量HF会侵蚀正极材料导致过渡金属溶解[13], 进而影响NCM的循环性能。
由于Li+(0.076 nm)与Ni2+(0.069 nm)的离子半径十分接近, 因此晶格中的Li、Ni很容易互换位置, 生成非化学计量比的结构, 即发生Li/Ni混排[14]。Ni2+进入锂离子层后能够阻断Li+的传输路径, 减少可以参加充放电循环的Li+的数量, 导致材料比容量降低。当Li+混排进入过渡金属层时, 由于其半径比过渡金属离子大, 过渡金属层会因空间效应和正电荷之间的互相排斥而膨胀, 导致层间距扩大并挤压相邻的锂离子层, 被压缩的锂离子层间距会降低锂离子的扩散系数, 影响材料的倍率性能。此外, Li/Ni混排还对正极材料性能有其他不利的影响, 如结构不稳定[14]、表面副反应增多[15-16]等。
三元材料主要由Ni2+/Ni3+和Ni3+/Ni4+氧化还原电对提供容量, 因此在充放电过程中, Ni通常处于不稳定的高价态(Ni3+、Ni4+), 容易通过失氧的方式向稳定的低价态转变, 对应层状相-尖晶石相-岩盐相的相转变过程[5,17]。层状和岩盐相中仅有一个八面体结构, 而尖晶石相中则同时有四面体和八面体结构。在由层状向尖晶石相转变的过程中, 需要部分金属离子由八面体结构迁移至四面体结构中, 处于不稳定状态的高价Ni离子优先发生迁移。但由于Ni3+和Ni4+分别有7个和6个d轨道电子, 根据晶体场理论, 其处于八面体位置比四面体位置更稳定, 因此当温度升高时, Ni离子更倾向于迁移至八面体位置, 即发生尖晶石向岩盐相的相转变, 同时释放氧气[18]。随着镍含量的增加, 第一次相转变温度逐渐降低, 当镍含量由40% (NCM433, 指Ni、Co、Mn的摩尔比为4 : 3 : 3, 如无特殊说明, 下同)增加到80% (NCM811)时, 温度由~250 ℃降低到~150 ℃ (图1)[19]。有研究表明, 充电过程中NCM523的相变主要发生在材料的表面, 生成岛状分布的尖晶石结构, 但是当截止电压较高时(4.8 V), 也会出现岩盐相(图2)[20]。
为解决以上问题, 包覆和掺杂是两种有效的手段。包覆改性一方面可以在材料表面沉积一层惰性物质, 隔离正极材料与电解液之间的接触, 减少副反应的发生; 另一方面也可以沉积一层活性材料, 减少残碱的同时还可以降低表面电阻。掺杂改性一方面可以通过改变材料的晶格常数或部分元素的价态来提高材料结构的稳定性, 另一方面也可以通过降低阳离子混排来提高材料的电子电导率和离子电导率。迄今为止, 已有不少文章[21–23]对三元材料的制备和改性进行了综述, 尽管这些综述很好地介绍了改性元素的种类和对电化学性能提升的效果, 但针对包覆和掺杂元素对其结构改善的原理以及对电化学性能提升机理的综述文章却较少。本文将从这两个方面系统介绍近年来三元正极材料包覆和掺杂改性研究的最新进展及其成果。

图1 时间分辨XRD(TR–XRD)测试过程中氧的质谱分析(O2, m/z=32) (上)及NCM相变温度区域(下)[19]

图2 NCM523高电压循环过程中的降解机制和相变[20]
1 包覆改性
电极材料与电解液之间的界面是电荷转移、Li+扩散和副反应的关键问题所在, 表面包覆改性是一种解决界面问题的有效方法。
1.1 HF清除剂
在锂离子电池中, 电解液作为传递锂离子的媒介, 主要由有机溶剂和电解质盐组成。现阶段商业化的电解液中, 使用最多的锂盐为LiPF6。有研究表明, 当温度超过50 ℃时, 电解液中的LiPF6会发生分解(式(1))[24-25]。在商业化的电解液中, 完全把水除去是不可能的, 微量水导致LiPF6分解(式(2, 3))生成HF[26]。HF侵蚀致使正极材料溶解加剧[13], 溶解后的金属离子聚集在正负极极片表面。随着电化学反应的进行, 负极表面的金属离子被还原为金属单质, 造成安全隐患。而正极附近的金属离子则有可能形成Ni–O、Co–O、Mn–O等非电化学活性物质, 不利于电子传输。此外, 腐蚀后的正极材料颗粒与导电剂等物质的接触变差, 引起循环过程中电压降低和阻抗上升。过渡金属溶解后, 正极材料表面出现岩盐相或尖晶石相, 且相变的种类与正极材料的组成有关。对于NCM523, 截止电压较高时(4.8 V)由于失氧, 表面重构主要生成岩盐相, 但是在正常的循环过程中则主要是尖晶石相[20]。NCM442恰好相反, 循环过程中表面主要是岩盐相[27]。有趣的是, 尽管NCM811的循环性能更差, 但循环过程中基本观察不到明显的结构变化, 其容量衰减主要来源于高脱Li表面和电解液之间的副反应[28]。
LiPF6→LiF↓+PF5(1)
PF5+H2O→POF3+2HF (2)
2POF3+3Li2O–→6LiF↓+P2O5↓(or LiPOF) (3)
选择合适的包覆剂隔绝正极材料与电解液是一种常见的保护思路, 常用包覆物质为氧化物。通过ALD (Atomic Layer Deposition, 原子层沉积)在NCM523表面沉积一层Al2O3之后, 可以显著减少NCM523与电解液的副反应[29]。Al2O3包覆对NCM811的初始性能没有明显影响, 但随着循环周数的增加, 包覆材料的优越性逐步得到体现[30]。这不仅与Al2O3“保护层”能够隔绝正极材料与电解液有关, 更重要的是改善了高镍材料的表面性质, 如降低表面转移电阻、提高离子导电率等。此外, 包覆层还能够降低正极材料的吸水性能, 而水含量与电池的长期性能紧密相关[31-32]。其他氧化物如SiO2[33]、WO3[34]、Y2O3[35]、Cr2O3[36]、Nb2O5[37]等也能改善循环和提高材料在空气中稳定性, 但Al2O3对材料性能的提升最有效[37-38]。
尽管氧化物包覆剂的作用十分明显, 但并不能完全阻止HF对正极材料的侵蚀[16]。使用Al2O3包覆后依然会检测到Ni–F、Mn–F, 即HF与除了与包覆剂Al2O3反应之外, 同样会与NCM本体反应[13,16]。这些副产物附着在正极的表面, 增加循环过程中的电阻。此外, 包覆效果与包覆方法及包覆层厚度紧密相关[39–41], 虽然包覆效果可以通过新型包覆手段(如ALD)实现, 但目前这些新型方法还难以大规模地商业化使用。再者, 尽管在这个过程中HF被消耗后形成更稳定的氟化物, 可以阻止其对正极材料的进一步侵蚀。但氧化物与HF的反应产物中有H2O, 会加剧电解液中HF的产生。
由于AlF3对HF更稳定, 且反应产物中没有H2O, 同时F的电负性高, 与正极材料表面氧的键合更强, 可以进一步抑制表面副反应, 因此是一个更好的选择[42-43]。包覆AlF3后, NCM523的晶格参数没有改变, 说明AlF3并没有进入晶格, 而仅仅是包覆在NCM表面[44]。由于循环过程中没有额外产生H2O, 因此AlF3包覆层可以减缓LiPF6的分解和Mn的溶解, 即可以增强材料的热稳定性和循环稳定性, 尤其是在脱锂量较大的情况。更重要的是, 经过60周循环后裸料的电荷转移阻抗增加了约25倍, 而包覆样品仅增加了约2.7倍[44]。CeF3在高温下呈现良好的电化学惰性, 在酸性环境下具有很好的稳定性[45], 并且室温时离子电导率很高[46-47], 符合包覆材料的各项要求。通过湿法工艺在NCM111表面沉积一层CeF3后[48], 能够有效防止HF对活性材料表面的持续侵蚀、延迟表面钝化层的生长; 同时还能起到稳定结构的作用, 提升材料的高电压(2.5~ 4.5 V)倍率性能和循环性能。不同的氟化物阳离子价态可以影响其包覆效果。例如, MgF2和LaF3均能提升NCM523的倍率和循环性能[49], 对高电压(3.0~ 4.8 V)循环过程中稳定晶体结构也有积极作用, 但LaF3包覆材料的高倍率性能(6)更优(图3), 而MgF2包覆更有利于提升热稳定性和高电压循环性能。两种包覆材料50周充放电循环后的XRD(X-ray Diffraction, X射线衍射)图谱也有所不同, LaF3包覆材料的(015)衍射峰强度明显降低, MgF2包覆材料的(110)衍射峰则出现轻微劈裂。这可能与氟化物的热力学稳定性有关, 详细的机理还有待进一步研究[50]。
1.2 残碱清除剂
研究结果显示, 残碱对材料的使用和性能发挥均有不利影响, 因此需要使用合适的方法将材料表面的残碱控制在一定的范围内。水洗是一种降低残碱的有效处理方式, 但水洗后材料的放电比容量明显降低, 存储稳定性变差, 阳离子混排也更严重。有研究[9]显示, 在空气中存储30 d后水洗样品的总碱量是未水洗样品的2倍多。包覆除了可以消耗HF之外, 也是一种有效降低残碱的方法[51]。
H2SiO3与NCM表面残余的LiOH/Li2CO3反应, 降低残碱的同时形成一层致密的Li2Si2O5包覆层[52]。当H2SiO3的添加量为1wt%时, 总碱量由0.46%降低到0.19%, 效果十分明显。消耗残碱有效改善了材料表面性能, 有利于提升放电容量和库仑效率; 而Li2Si2O5则提高了离子电导率、降低了极化, 有利于提升倍率性能。但是当添加量增加至2wt%时, 由于过量的H2SiO3分解形成惰性SiO2, 阻碍了Li离子脱嵌, 包覆效果反而有所下降(表1)。值得注意的是, 采取这种思路进行包覆处理时, 对正极材料的保护和性能提升往往是多维度的。H3PO4与残碱反应生成Li3PO4(图4), 除降低残碱提高离子电导率外, 还能吸收电解液中的H2O和HF, 减少活性物质与电解液的副反应, 改善材料的循环性能[53–55]。此种思路可以扩展至其他类型的正极材料, 如可利用(NH4)2SO4对固溶体材料进行表面处理, 形成Li2SO4包覆层[56]。使用氧化物进行包覆时, 虽然氧化物主要起“保护层”的作用, 但文献[57]报道显示, 当热处理温度合适时, 氧化物包覆剂也可能与正极材料表面的残碱发生反应。

图3 NCM523裸样和包覆样的第5周放电曲线(3.0~4.6 V)[49]
(a) 1; (b) 3; (c) 6

表1 不同包覆量时锂离子电池的放电比容量[52]
* After cycling at 10
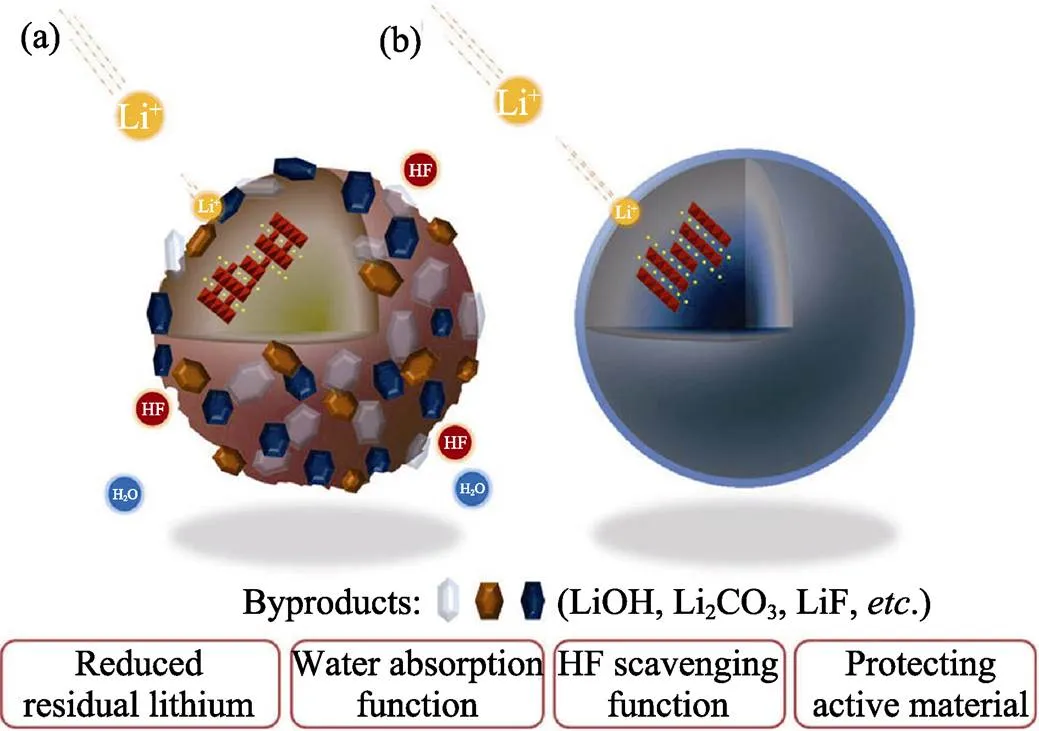
图4 循环150次后(a)裸样和(b) Li3PO4包覆的NCM622 (1wt%)的表面副产物示意图[53]
除无机化合物外, 有机物也可以用于正极材料的包覆。Xu等[58]使用质子化聚苯胺(PANI)的NMP (1-methyl-2-pyrrolidinone, 1-甲基-2-吡咯烷酮)溶液对NCM811进行洗涤, PANI中的H+可以与残碱反应、降低总碱量, 同时由于PANI在NMP中是弱酸, 因此不会与NCM本体反应。残碱减少和PANI包覆的双重作用有利于改善材料的倍率、循环和高温性能。石墨烯具有优异的电学和热学性能, 在锂离子电池中是一种理想的添加剂[59], 但缺点也很明显: 其二维平面结构很难与活性材料表面紧密结合, 在充放电过程中容易脱落。使用环氧官能化硅烷(KH650)和还原氧化石墨烯(RGO)对NCM811进行双包覆[60], KH650同时起到消耗–OH、降低残碱和固化RGO的作用, 两者结合可以促进电子的传递, 并在循环过程中保护活性物质不受侵蚀, 降低初始不可逆容量损失, 减少电解质与电极的副反应。同理, 以聚乙烯吡咯烷酮(PVP)诱导剂在NCM811表面包覆一层聚苯胺, 也可达到相同的效果[61]。正极材料通常是由一次颗粒堆积形成的球形二次颗粒, 仅在二次颗粒表面包覆, 对材料内部导电率的提升有限。借助球磨、喷雾干燥工艺, 将碳材料包覆在一次颗粒表面并填充在一次颗粒之间, 可形成更优良的导电网络, 从而更好地改善正极材料的倍率性能和循环性能[62–64]。
传统的包覆方式通常是在材料生产过程中完成, 最近有研究组[65]采用新方法, 将包覆过程与电池制备时的匀浆过程相结合, 取得了不错的效果。正极匀浆时加入一定量的S将Ni3+还原为Ni2+, S被氧化为Li2S2O3, 并在首次充电时继续氧化形成Li2SO4。其作用机理如式(4~8)所示。这种处理方式对材料的循环性能没有明显影响, 但是可以显著提升倍率性能。类似地, 在匀浆过程中加入LiPF6也可以起到相同的效果, 反应产物为更稳定的Li3PO4和LiF, 提升材料循环性能的同时还可以降低表面电阻, 提升材料的倍率性能[66]。
4LiMO2+2S→4MO+Li2S2O3+Li2O (4)
Li2S2O3+5Li2O-8e→2Li2SO4+8Li+(5)
Li2S2O3+5Li2CO3-8e→2Li2SO4+5CO2+8Li+(6)
2LiMO2+S+2Li2O-4e→2MO+Li2SO4+4Li+(7)
2LiMO2+S+2Li2CO3-4e→
2MO+Li2SO4+2CO2+4Li+(8)
1.3 结构稳定剂
高镍三元正极材料循环性能不佳, 除了副反应之外, 还与充放电过程中的表面结构变化和二次颗粒破碎有关[27,67-68]。某些特定的包覆剂在隔绝电解液、减少副反应的同时, 也能起到稳定表面结构和抑制微裂纹的作用。如硅酸盐和磷酸盐, 较强的Si=O、P=O键使过渡金属与SiO3、PO4聚阴离子间的共价键更强; 同时, 硅酸盐/磷酸盐比金属氧化物具有更高的热力学与电化学稳定性, 因此能够提升正极材料结构稳定性, 提升高电压或高温性能。Li2SiO3包覆层能有效地隔绝高电压下电极–电解液界面上的副反应, 更重要的是, 当锂离子在高压下发生深度脱层时, 包覆层增强了正极材料的结构稳定性[69]。此外, Li2SiO3还可以增强锂离子在电极/电解质界面的扩散, 防止正极材料颗粒在循环过程中的粉化[70]。Li3PO4在提升材料的倍率性能的同时, 又可以阻止HF和POF3的侵蚀, 提升材料的循环性能[71]。有证据表明, Li3PO4还能够减缓高温下的相转变, 正极材料的初始热分解温度和放热量均明显下降, 相转变温度提升, 并且可以抑制尖晶石和岩盐结构之间的相转变。LiFePO4(LFP)正极材料得益于其无机性质和化学稳定性, 具有优异的循环性能, 作为包覆剂使用时能够提升三元材料的高温循环稳定性, 同时又不会降低首周放电比容量[72]。但是, LFP的导电性较差, 需要通过工艺严格控制颗粒大小和包覆层厚度[73]。为尽量提高三元材料的放电容量, 需要提升其充放电截止电压, 但高电压下副反应和不可逆相变加剧, 影响循环性能和安全性能。在以LFP包覆的NCM523为正极组装的5 Ah软包电池中, LFP包覆层抑制了层状—尖晶石—岩盐相的相转变, 因此该电池能够耐受4.5 V的高电压, 且在满电状态下不会发生热失控[74-75], 其他磷酸盐也有类似报道[76-77]。自从索尼公司首次推出LiCoO2/C二次电池以来, LiCoO2作为正极材料取得了巨大的成功。有鉴于此, 研究者将LiCoO2用于三元材料的包覆, 发现其可以减少三元材料表面的NiO结构, 提升电化学性能[78-79]。此外, 由于LiCoO2的结构稳定性, 同时还能提升三元材料在空气中的存储性能, 减少表面镍价态、水分、残碱含量以及降低电化学性能受暴露时间的影响[80]。
除材料本身的结构稳定性之外, 循环过程中二次颗粒内部产生的微裂纹也是导致正极材料循环性能下降的原因之一: 产生微裂纹后, 电解液即会浸入, 并在颗粒内发生不可逆分解, 分解产物沿晶间裂纹的积累加速了容量衰减(图5)[81]。在Li2SiO3包覆的NCM523中, 富硅区不仅集中在颗粒的表面, 在晶界处、甚至在400 nm深处也有Si元素分布[82]。富硅区抑制了裂纹的形成, 阻止了电解质溶液在颗粒内的侵入和分解。LBO(硼酸锂)材料具有良好的离子电导率和高氧化稳定性, 更重要的是在提升三元材料的高电压性能的同时[83], 也能够抑制循环过程中微裂纹的产生, 将NCM811在4.6 V循环时微裂纹的出现周数由106周延长至211周[84]。

图5 100周循环(4.7 V)后正极材料颗粒内部微裂纹的(a~d)SEM照片及其(e)形成示意图[81]
1.4 小结
由于在活性材料表面引入了其他物质, 并且绝大多数包覆物不具有电化学活性, 因此尽管包覆改性能够提升材料的性能, 但往往也会带来新的问题。比如, 传统的包覆剂如Al2O3、SiO2、TiO2、AlPO4、CoPO4等离子电子传导率低, 容易导致包覆后材料的极化增加、容量降低、倍率降低等, 而选用快离子导体则可避免相应问题[54,69–71,85]。Zr对提升循环保持率有益处, 但对初始容量和残碱作用不明显, P则相反。使用Zr/P双包覆, 借助Zr和P的协同作用, 可以同时提升样品的初始容量和循环性能, 残碱的降低也较为可观[86]。包覆剂中的高价态金属离子(如Ti4+)容易进入晶格, 加剧Li/Ni混排, 使用纳米Li2TiO3进行包覆则可避免[87]。Cr8O21包覆NCM523的结果表明, 虽然包覆量为2.5wt%时不可逆容量有所增加(15.6 mAh/g), 但却拥有最优的循环性能[88]。三元正极材料首次库伦效率普遍不高, 这与循环初期氧空位的形成有关[89], 包覆改性能够限制氧空位产生, 降低首周不可逆容量。Kalaiselvi课题组[90]的研究结果显示, 在Al2O3、Bi2O3、In2O3三种包覆物中, Bi2O3包覆料的不可逆容量最低, 同时也具有最好的结构稳定性, 甚至可以耐受5.2 V的高电压。
综上, 包覆剂的物化性质、包覆量、包覆方式、混合方式等对正极材料性能的影响是多方面的、复杂的, 且在改善某一方面性能的同时, 经常需要以牺牲其他性能为代价。而通过对包覆剂的选择和包覆工艺的优化, 则可减少负面作用。这就要求研究者综合考虑, 开展横向(如: 不同类型包覆剂)和纵向(如: 相同类型不同阳离子价态包覆剂)的对比研究, 全面提升NCM材料的性能。
2 掺杂
包覆对解决材料表面问题效果显著, 但对晶体结构的作用却十分有限, 而体相结构也是影响材料性能的关键所在, 因此需要借助掺杂改性进一步提升材料的性能。
2.1 减少不稳定元素
三元材料中普遍存在锂镍混排现象, 造成Li–O层间距减小和扩散阻力增大。锂位的过渡金属离子也会阻碍锂离子传导, 导致锂离子扩散能垒增高, 倍率性能下降。文献[91]报道了多种控制锂镍混排的方法, 由于锂镍混排不仅发生在材料制备阶段, 也发生在电池的循环过程中, 因此除了需要严格控制高温合成条件之外, 体相掺杂也是一种必要的手段, 可以有效地改善高镍三元材料的电化学性能。
由于离子半径相当(Li+=0.076 nm, Mg2+=0.072 nm, Ni2+=0.069 nm), 当掺杂量<2wt%时, Mg2+主要占据Li位[92], 在脱锂量逐渐增加、电压逐渐增高的过程中, Mg2+的支柱作用能够减轻各向异性的晶格变 化[93]。较小的轴变化率和稳定的电压平台均表明掺杂样具有良好的结构可逆性[94]。值得注意的是, Mg掺杂进入Li层会导致Li/Ni混排加剧(1.8%→2.3%), 但对倍率性能影响不大, 且200周循环后掺杂样的Li/Ni混排则明显小于裸样(4.0%→7.8%)。当脱锂量较大时, 相邻过渡金属层间O2–—O2–的强斥力导致层状结构坍塌和不可逆相变, 造成NCM高电压循环性能不佳。Mg2+掺杂可以降低O2–—O2–之间的斥力、提高O–M–O的键能, 增强层状结构的稳定性, 有效抑制充放电过程中的相转变[95]。Aurbach课题组[96]研究了Mo6+掺杂的NCM523, 认为Mo6+与Mg2+不同, 倾向于在表面富集, 并且在晶格中处于Ni位。掺杂对样品的放电比容量和循环性能均有有益影响: 1~4倍率放电比容量提升20%~30%; 截止电压在4.3~4.6 V 范围内时常温(30 ℃)和高温(45 ℃)循环容量衰减率均有所减缓(图6)。
除取代金属离子外, 也可进行阴离子(O)掺杂[97]。第一性原理计算和中子粉末衍射(NPD)表明[98], F原子取代O原子可以促使相邻的Li、Ni互换位置, 诱导形成稳定的局部卤化物八面体(LOSH)。NPD和XRD结果显示, 通过改变F掺杂量可以调整这种“反位”缺陷的比例, 而缺陷比例与材料的性能密切相关。拥有5.7%缺陷的掺杂样具有良好的高温循环性能(55 ℃)和倍率性能, 原因是LOSH使轴增大, 更有利于Li离子的迁移。缺陷还可以提高材料的热稳定性, 5.7%缺陷可以将热分解温度由179.51 ℃提高到226.96 ℃。可能原因有2个: 1)Ni迁移到Li层诱导LOSH的产生; 2)反位缺陷反过来阻止更多的Ni迁移到Li层, 抑制层状结构的相变。Li等[99]通过对NCA进行氟掺杂改性, 也得到类似结论。由于Li–F键强于Li–O键, 氟会部分替代氧的位置。因此在氟掺杂之后, 材料表面的Ni2+数量有所增加, 而活性的Ni3+数量有所减少, 加剧锂镍混排, 首次放电比容量有所下降; 但是材料表面的活性Ni3+减少, 有利于减少界面副反应, 抑制极化以及避免循环过程中阻抗升高, 提升材料的循环性能、倍率性能、高温性能和过充性能等。

图6 在(a) 45 ℃ (4.3、4.4、4.5、4.6 V, C/3)和(b) 30 ℃ (2.8~4.3 V, 不同倍率)条件下NCM523裸样和Mo掺杂样的循环曲线[96]
2.2 降低Li/Ni混排
锂镍混排对NCM材料的电化学性能和结构稳定性均有不利影响, 有必要进行控制。但如2.1中所言, 某些掺杂元素(如Mg)会加剧Li/Ni混排, 因此对材料进行掺杂改性提高结构稳定性的同时, 还需要考虑对混排的影响。
Nb掺杂主要以+5价形式占据NCM111的3b位置[100], 可以有效减少阳离子混排。当掺杂量为2wt%时, Ni3a/(Ni3a+Li3a)由裸样的5.73%减少到3.13%, 相应的0.1放电比容量(2.7~4.3 V)由151.9 mAh/g提高到200.4 mAh/g。掺杂后/值更高, 更有利于锂离子的脱嵌, 有助于提升倍率性能。由于Nb–O的键能大于M–O (M=Ni、Co、Mn), 因此在循环过程中结构更稳定。同时为保证价态平衡, 部分Mn4+被还原形成局部富Mn3+区域, 可以起到增加电导率、稳定循环的作用。掺杂量是一个很重要的参数, 1wt%的Nb掺杂有助于抑制循环过程中的相转变、降低电化学极化[101]; 当掺杂量超过2wt%时, Nb5+不会完全进入晶格, 而是在表面形成Nb2O5杂相, 导致材料的循环性能下降[102]。除影响Li/Ni混排外, Ni2+的迁移还是导致层状结构到尖晶石结构相转变的原因[20,103]。Zr4+离子的强静电作用使Ni2+迁移阻力增加, 可以抑制层状结构到尖晶石结构的相变[104](图7)。同时Jahn−Teller活性Ni3+离子的减少, 也能够提高结构稳定性和循环稳定性(表2)。另一方面, 更多的Ni2+被氧化为Ni3+, 降低了锂镍混排[105]。Zr掺杂NCM523中活性氧(指Li2CO3/LiOH中的氧)的含量有所减少而晶格氧含量有所增加, 说明Zr进入了晶格[106]。表面的Ni3+/Ni2+比例增加, 说明锂镍混排降低, 结构稳定性有所增强。当再加入Ti时,(003)/(004)比值进一步升高(1.25→1.31), 说明Zr/Ti双掺杂存在协同作用。单独掺杂Ti可以将NCM811的(003)/(004)由1.35增加到1.40左右, 并且随着掺杂量的增加, Li/Ni混排逐渐降低[107]。掺杂后更完美的晶体结构提升了材料的高电压倍率性能和循环性能, 原因是Ti增大了晶胞参数, 有利于Li+的脱嵌。而充放电过程中的体积变化率变小, 能够减少循环过程中二次粒子的破碎。但当掺杂量过多时材料的放电比容量有所降低, 这一方面是由于Ti不具有电化学活性, 另一方面是因为掺杂Ti增加了充放电过程中的极化。

图7 可能的Ni2+迁移形成尖晶石相机制[104]
Red: oxygen atoms; Grey: Ni atoms; Violet: Mn atoms; Blue: cobalt atoms

表2 不同物质掺杂NCM622的循环和倍率性能[104]
* 200 cycles at 1rate
2.3 稳定氧原子
充放电过程中高镍材料结构不稳定[108], 容易发生层状相–尖晶石相–岩盐相的相转变, 期间伴 随氧气的释放[109-110]。失氧反应是锂离子电池热失控的一个重要原因, 因此, 可以通过抑制氧气释放来提高电池安全性, 亦即需要改善正极材料的热稳定性。
脱锂过程伴随着氧空位的产生, 氧空位形成后Ni原子将迁移到Li位, 即氧空位加剧了阳离子混排, 反之亦然。理论计算结果表明[111], Al掺杂可以抑制氧空位的形成, 即增强了氧稳定性。而Mg可以阻止Ni的迁移并减少阳离子混排, 增强结构稳定性。同时, 即使已有氧空位存在, Al和Mg掺杂也可以阻止Ni原子的迁移[112]。有研究表明, Al可以有效地将电子转移到O中, 而氧电荷的增加使其结合能更大[113], 即Al–O键能更大, 掺杂Al之后的NCM结构更稳定[114]。与上述机理不同, Kim等[115]发现, W掺杂NCM的表面会生成一层岩盐相, 通常这种岩盐相出现在多次循环后或因其他原因被破坏的NCM表面, 在新制备的材料中很少出现。计算结果表明, 岩盐相中的O结合能比层状相中更高, 即表面的岩盐相可以减少失氧。此外, 受价态平衡的限制, 部分Ni3+被还原为Ni2+, 减少了Jahn–Teller活性点, 对稳定结构有积极作用。掺杂1mol% W的LNO (LiNiO2)、NC8911(LiNi0.89Co0.11O2)、NCM900505和NCM801505的循环性能均得到不同幅度的提升(图8(a))。高镍正极材料掺杂W之后热稳定性显著提升, 最高可超过25 ℃, 并且这些热反应释放的总热量也有不同程度的降低(图8(b))。
使用Mo掺杂时, Mo6+倾向于占据Mn4+位, 为保持电荷平衡, Ni2+/Ni3+的比值会增加, 进而导致锂镍混排的加剧[116], 但Mo掺杂可以极大地提高材料的热稳定性。Li0.2Ni0.8Mn0.1Co0.1O2发生尖晶石相向岩盐相转变的相转变温度为250 ℃, 而4mol% Mo掺杂可将此温度提高到350 ℃以上, 同时氧气释放量大幅减少。原因是Mo6+没有d轨道电子, 根据晶体场理论, 不存在八面体位置稳定能。因此当温度升高时, Mo6+很容易由八面体位置前移至四面体位置, 即发生层状向尖晶石结构的相转变。但由于Mo6+在四面体中更稳定, 即含Mo的尖晶石结构更稳定, 因此当温度继续升高时, 由尖晶石向岩盐相的相转变很难发生。Mo掺杂增大了NCM622的晶胞参数, 可以增强阳离子有序度并拓宽锂离子迁移通道[117]。此外, Mo6+/Mo4+电对能够提升部分放电比容量, 而较强的Mo–O键可以抑制晶格氧的流失并稳定材料的表面。因此, Mo掺杂是提高材料理化性能的有效方法, 可提高NCM622在高压下的电化学性能。

图8 不同正极材料的(a)循环性能和(b) DSC曲线[115]
2.4 小结
不同掺杂元素占据的晶格点位有所区别, 而取代不同点位对NCM性能的改善也有所不同。Ta对NCM811的高温(45 ℃)放电比容量和循环性能提升、电压滞后降低等有益处; Zr、Mg掺杂时材料的轴变化率更小, 循环性能更佳, 但倍率较差; 使用Al、Ti、Si进行掺杂时循环性能也有一定程度的提高, 但提升效果不如Ta、Zr、Mg[118]。必要时, 可以采用多元素共掺杂的方式。取代Li位的Na在扩大锂层层间距的同时, 也有加强结构稳定性的作用, 而掺杂在O位的F则有利于增强晶型和界面稳定性, 同时进行Na和F掺杂时, 两者的协同作用能够全面提升NCM622的性能, 如首周库仑效率、倍率、循环等[119]。Mg–Al–B共掺杂[120]时, Mg2+可以增加层间距, 稳定晶体结构; B起到抑制不稳定相的作用, 同时又不影响Li+的迁移。Mg–Al–B共掺杂能够降低阳离子混排, 提高材料高电压下的界面稳定性。综上, 在对NCM进行掺杂改性, 需要综合考虑掺杂元素对材料性能的影响, 根据不同的需求选择掺杂元素, 必要时需考虑不同掺杂元素的协同作用。
3 掺杂包覆改性
表面包覆主要是利用惰性物质隔离正极材料表面与电解液之间的副反应、抑制金属离子的溶解、优化材料的循环性能, 或使用能够与Li2CO3/LiOH反应的物质降低残碱、提高材料的安全性能, 但基本不会改变材料的晶体结构, 锂镍混排等缺陷依然存在。掺杂主要是利用外加元素的离子半径和价态等性质与过渡金属(Ni、Co、Mn)不同, 改变材料的晶格参数和过渡金属价态, 提高正极材料的稳定性、循环性能或倍率性能等, 但对材料表面的改善有限, 正极材料仍然直接暴露在电解液中。因此, 有必要将掺杂和包覆结合, 全面提升材料的性能。
3.1 自发形成的掺杂包覆
事实证明, 在进行掺杂或包覆处理时, 两种改性往往同时起作用[121]。例如, Li等[122]在使用Zr对NCM811进行掺杂改性时发现, 材料表面会形成一层1~2 nm的Li2ZrO3包覆层。Zr的掺杂和包覆双重作用使NCM811具有更优的倍率性能和循环性能[123]。由于低镍材料具有更好的稳定性, 因此可以设计内部富Ni表面富Co、Mn的梯度材料, 同时提升电性能和结构性能[124–126]。有意思的是, 自发形成掺杂/包覆双重效果时, 掺杂元素在体相中往往呈梯度分布, 梯度分布的Ge元素能够抑制阳离子混排, 同时还有利于改善Li+离子传输通道[127]。阴离子掺杂时也有类似效果, Ran等[128]使用NH4H2PO4改性NCM622时, 得到了PO43–梯度掺杂和Li3PO4包覆的材料, 极大地提升了NCM622的高温高电压循环性能。这是因为PO43–掺杂进入氧层稳定了晶体结构, 表面的Li3PO4包覆层一则可以阻止过渡金属溶解, 二则作为快离子导体改善了离子传输。使用Al、Y、Si、Cd、V等元素进行改性时, 也有类似效果[70,129–132]。梯度掺杂还能够在正极材料的表面形成一层无序的层状结构(图9), 这种结构比岩盐相更有利于锂离子的传输, 掺杂元素又进一步提高了氧骨架的坚固性, 形成了特殊的掺杂/包覆结构[133-134]。
3.2 控制制备工艺形成掺杂包覆
除自发形成的掺杂包覆效果外, 不同的后处理工艺可以控制改性方式。通过湿法在NCM811表面沉积一层包覆物, 当焙烧温度<700 ℃时, 形成ZrO2包覆; >700 ℃时, 则是ZrO2包覆和Zr掺杂[135]。使用Ti对NCM811进行改性时, 将表面沉积有无定形TiO2的前驱体直接进行配锂焙烧, 得到Ti掺杂和Li2TiO3包覆的NCM811。如将同样的前驱体进行480 ℃预处理后再配锂焙烧, 则得到Li2TiO3包覆的NCM811[136]。Ce4+很容易将Ni2+氧化为Ni3+, 可以降低锂镍混排, 并且较强的Ce–O键对高脱锂态下的层状结构有很好的稳定作用; 当热处理温度高于500 ℃时, 表面生成CeO2包覆层, 可以隔离电解液侵蚀, 降低循环过程中表面电阻的增加速度[137]。焙烧气氛对改性效果也有影响[138]: 在空气气氛下焙烧时, Li2ZrO3仅存在于NCM622的表面, 呈岛状结晶分布; 而当使用氧气气氛时, 得到的是无定型Li2ZrO3包覆层, 且Zr扩散进入体相, 可以同时实现包覆和掺杂的双重效果。虽然高镍材料中含有Mn元素, 但使用Mn化合物对高镍材料进行处理形成梯度高镍材料, 能够显著提升材料的倍率及循环性能[139]。

图9 无序层状相包覆层的示意图[133]
掺杂和包覆也可选用不同的元素。聚吡咯(PPy)是一种典型的导电聚合物, 包覆后能够形成一层导电网络, 有利于电子/离子扩散, 并可用作正极材料和电解质之间的保护层。文献[140]报道, Zr掺杂可以改善结构稳定性, 提升NCM523的常温循环容量保持率, 再进行PPy包覆, 可以提高界面导电性并抑制界面副反应, 表现出更好的循环性能。研究表明, Ti元素相对于La更容易进入NCM晶格, 因此将Ti和La与NCM811一起热处理时, 得到的是Ti掺杂和La4NiLiO8包覆的材料[141]。取代Ni2+位的Ti4+可以降低Li/Ni混排、抑制循环过程中的相变和微裂纹的形成, La4NiLiO8除能够抑制循环期间活性材料表面的结构恶化外, 其优异的电子导电性则有利于快速电子传输。更重要的是, 由于Ti和La4NiLiO8降低相变和增强表面稳定性的协同效应, 成功抑制了NCM811内部微裂纹的形成和表面结构恶化。由于包覆层是通过表面残余添加剂与残锂反应后生成的, 因此大多情况下是不完全包覆, 为实现完全包覆, 可再用其他类型的添加剂进行二次包覆[142]。
3.3 小结
与单独进行包覆或掺杂改性相同, 掺杂/包覆双改性并不一定能全面提升材料性能。Al2O3包覆/Mg2+掺杂的NCA, 由于Al3+和Mg2+并不具有电化学活性, 因此其首周放电比容量明显下降, 但这种改性方式对提升材料结构稳定性十分有效[143]。Ge梯度掺杂和Li2GeO3包覆NCM821206则能同时提升其循环性能和倍率性能[127]。原因是Li2GeO3包覆层能够抑制界面副反应以增强正极材料的表面结构稳定性, Ge梯度掺杂则不仅可以通过增加相变能垒抑制层状向尖晶石状或岩盐相的相转变, 而且还可以通过降低扩散阻力促进Li+的快速扩散, 减缓电压衰减。因此, 选择掺杂和包覆元素需十分慎重, 选择双改性路线时不应只是简单地选择文献报道的掺杂物和包覆物, 或是简单地单独考虑包覆或掺杂效果, 而是应从掺杂和包覆物的协同作用入手, 选择两种相辅相成的材料, 既实现掺杂和包覆的双重优点, 又不至于严重降低活性材料的某些性能[144]。
4 总结与展望
随着国家新能源汽车补贴新标准对能量密度要求的不断攀升, 高镍、特别是镍含量超过80%的三元材料被认为是现阶段最有希望的正极材料。但高镍材料本身的缺点严重制约了其在动力电池中的应用。各国的研究者们在提高高镍材料的安全性能、循环性能等方面开展了大量工作, 包覆、掺杂等改性手段也取得了不同程度的进展。但距离实现镍含量超过80%的三元材料在动力电池中大规模应用, 在提升材料性能方面还需进行更深入的探索。
由于正极材料的性能(如粒度分布、元素组成等)继承自前驱体, 因此前驱体的各项技术指标尤为重要, 但现阶段研究工作对正极材料的设计和合成工艺优化关注较多, 而对前驱体与正极材料性能之间的关系研究较少, 因此需要结合前驱体的制备技术和残碱产生的原理设计正极材料及制备工艺, 从根本上解决正极材料的某些问题(如残碱)。
高镍三元正极材料具有高能量密度, 可大规模应用于新能源汽车领域, 但阳离子混排导致了结构不稳定和锂离子扩散缓慢, 影响其循环稳定性和倍率性能。尤其是高度脱锂状态下的结构不稳定性, 更是安全问题的关键所在。除体相结构外, 稳定的界面, 如材料表面与电解液的副反应及表面失氧问题, 对于提升NCM/NCA的电化学性能与安全性能也至关重要。此外, 实际应用还要考虑体积能量密度, 需进一步解决该问题以增加受限空间中的能量密度。在过去的研究中, 科学家基于对结构—性能关系的理解, 通过整合不同的元素降低阳离子混排、提高结构稳定性, 通过惰性包覆层减少与电解液的副反应。事实证明, 采用包覆/掺杂改性的手段, 结合对一次粒子形貌的控制(如单晶、特殊结晶取向等), 能够全方位提高NCM/NCA在反复充放电循环中的稳定性, 加快高能量密度正极材料的发展步伐。
目前对改性结果的讨论较多, 而对包覆/掺杂元素的理论研究不足, 从而导致使用同一种元素进行改性时, 可能会得到完全不同的效果, 由此带来相左的机理解释。因此需要研究者系统研究不同价态、不同半径的元素改性不同镍钴锰比例的三元材料时的规律, 以及不同热处理工艺对包覆/掺杂效果的影响规律。更重要的是, 需要将包覆和掺杂两种改性工艺有机结合, 全面提升高镍正极材料的性能, 而不是以牺牲其他性能为代价来提升某方面性能。例如, Xu等[145]利用氧化化学气相沉积(oCVD)在一次颗粒和二次颗粒表面同时包覆一层聚乙撑二氧噻吩(PEDOT), 不仅增强了锂离子和电子传输, 还能够显著抑制层状到尖晶石/岩盐的相变和失氧、减轻晶间/晶内裂纹产生, 并有效稳定活性材料—电解质界面, 全面提升高镍NCM高电压下的电化学性能和热稳定性。改性元素种类选择、改性工艺优化, 包覆厚度/掺杂深度控制等对于正极材料性能的提升至关重要, 需要进一步的理解, 并开发新颖的方法和工艺。
成分梯度有望成为下一步的技术解决方案, 梯度元素的选择和梯度分布有待进一步优化, 以平衡能量密度和循环稳定性。虽然很容易得到浓度梯度的 NCM 材料, 并在循环中保持, 但梯度分布的NCA却很难制备, 在高温时前驱体的浓度梯度趋于消失。因此在主体材料的选择和制备工艺研究方面, 还需给予更多的关注。对于梯度掺杂而言, 循环过程中梯度元素的演变规律, 以及对正极材料性能的影响, 也需要进行更为深入的研究。
此外, 正极材料的性能最终要体现在全电池中, 相同性质的NCM/NCA材料匹配不同负极时会面临不同的失效机制。因此有必要将各种改性的NCM/NCA材料组装成商品化电池, 并研究其性能和失效机制, 这有助于为正极材料的改进提供指导。对于负极材料而言, SEI (Solid Electrolyte Interface固体电解质界面相)膜的发现和引入极大地推进了石墨负极的商业化应用。虽然对正极CEI (Cathode Electrolyte Interface正极电解质中间相)膜的讨论由来已久, 但由于CEI膜的形成受众多因素影响且在高电压下不稳定, 不同研究人员关于CEI膜的研究结果之间存在差异。特别是对高镍材料的研究, 则更为不足。因此, 在CEI膜的形成机制和组成、正极材料本征性质对CEI膜的影响规律、高电压充放电过程中的稳定性与变化规律、以及CEI与SEI膜之间的相互影响机制等方面, 需要开展更为深入和广泛的研究。
最后, 更重要的是在以上研究基础之上, 开发适合工业生产的工艺, 再配合电池技术的进步, 实现动力电池性能的全面提升。相信在学术界和工业界的合作努力下, 高安全性能、高能量密度的动力电池将会推动新能源汽车的持续发展。
[1] CHOI N S, CHEN Z, FREUNBERGER S A,. Challenges facing lithium batteries and electrical double-layer capacitors.., 2012, 51(40): 9994–10024.
[2] LIU W, OH P, LIU X,. Nickel-rich layered lithium transition- metal oxide for high energy lithium-ion batteries.., 2015, 54(15): 4440–4457.
[3] SCROSATI B, GARCHE J. Lithium batteries: status, prospects and future., 2010, 195(9): 2419–2430.
[4] 柏祥涛, 孙学义, 庄卫东, 等. 氢氧化物前驱体制备LiNi0.5Co0.2Mn0.3O2的机理. 电池, 2014, 44(5): 260–263.
[5] LEE K S, MYUNG S T, AMINE K,. Structural and electrochemical properties of layered Li[Ni1−2xCoMn]O2(=0.1–0.3) positive electrode materials for Li-ion batteries.., 2007, 154(10): A971–A977.
[6] JOUANNEAU S, MACNEIL D D, LU Z,. Morphology and safety of Li[NiCo1−2xMn]O2(0≤≤1/2).., 2003, 150(10): A1299–1304.
[7] MACNEIL D D, LU Z H, CHEN Z H,. A comparison of the electrode/electrolyte reaction at elevated temperatures for various Li-ion battery cathodes., 2002, 108(1/2): 8–14.
[8] KIM J, LEE H, CHA H,. Nickel-rich cathodes: prospect and reality of Ni-rich cathode for commercialization.., 2018, 8(6): 1702028.
[9] XIONG X H, WANG Z X, YUE P,. Washing effects on electrochemical performance and storage characteristics of LiNi0.8Co0.1Mn0.1O2as cathode material for lithium-ion batteries., 2013, 222: 318–325.
[10] XU S, WANG X, ZHANG W,. The effects of washing on LiNi0.83Co0.13Mn0.04O2cathode materials., 2019, 334: 105–110.
[11] LI J, CHEN B R, ZHOU H M. Effects of washing and heat-treatment on structure and electrochemical charge/discharge property of LiNi0.8Co0.15Al0.05O2powder.., 2016, 31(7): 773–778.
[12] XU S Z, LUO G F, JACOBS R,.modeling of electrolyte molecule ethylene carbonate decomposition reaction on Li(Ni, Mn, Co)O2cathode surface., 2017, 9: 20545−20553.
[13] MYUNG S T, IZUMI K, KOMABA S,. Role of alumina coating on Li-Ni-Co-Mn-O particles as positive electrode materialfor lithium-ion batteries.., 2005, 17(14): 3695–3704.
[14] YU H J, QIAN Y M, OTANI M,. Study of the lithium/nickel ions exchange in the layered LiNi0.42Mn0.42Co0.16O2cathode material for lithium ion batteries: experimental and first-principles calculations.., 2014, 7: 1068–1078.
[15] AURBACH D. Electrode-solution interactions in Li-ion batteries: a short summary and new insights., 2003, 119–121: 497–503.
[16] MYUNG S T, AMINE K, SUN Y K. Surface modification of cathode materials from nano- to microscale for rechargeable lithium- ion batteries.., 2010, 20: 7074–7095.
[17] YOON W S, HANSON J, MCBREEN J,. A study on the newly observed intermediate structures during the thermal decomposition of nickel-based layered cathode materials using time-resolved XRD.., 2006, 8: 859–862.
[18] KONISHI H, YUASA T, YOSHIKAWA M. Thermal stability of Li1−yNiMn(1−x)/2Co(1−x)/2O2layer-structured cathode materials used in Li–ion batteries., 2011, 196: 6884–6888.
[19] BAK S M, HU E Y, ZHOU Y N,. Structural changes and thermal stability of charged LiNiMnCoO2cathode materials studied by combinedtime-resolved XRD and mass spectroscopy., 2014, 6(24): 22594–22601.
[20] JUNG S K, GWON H, HONG J,. Understanding the degradation mechanisms of LiNi0.5Co0.2Mn0.3O2cathode material in lithium ion batteries.., 2014, 4: 1300787.
[21] 邵奕嘉, 黄斌, 刘全兵, 等. 三元镍钴锰正极材料的制备及改性. 化学进展, 2018, 30(4): 410–419.
[22] MANTHIRAM A, KNIGHT J C, MYUNG S T,. Nickel-rich and lithium-rich layered oxide cathodes: progress and perspectives.., 2016, 6(1): 1501010.
[23] CHEN Z, CHAO D, LIN J,. Recent progress in surface coating of layered LiNiCoMnO2for lithium-ion batteries.., 2017, 96(4): 491–502.
[24] AURBACH D. The electrochemical behavior of lithium salt solutions ofbutyrolactone with noble metal electrodes., 1989, 136(4): 906–913.
[25] EDSTROM K, GUSTAFSSON T, THOMAS J. The cathode- electrolyte interface in the Li-ion battery., 2004, 50(2/3): 397–403.
[26] AURBACH D. Identification of surface films formed on lithium surfaces inbutyrolactone solutions II. contaminated solutions.., 1989, 136(6): 1611–1614.
[27] LIN F, MARKUS I M, NORDLUND D,. Surface reconstruction and chemical evolution of stoichiometric layered cathode materials for lithium-ion batteries.., 2014, 5: 3529.
[28] LI J, LIU H, XIA J,. The impact of electrolyte additives and upper cut-off voltage on the formation of a rocksalt surface layer in LiNi0.8Mn0.1Co0.1O2electrodes.., 2017, 164(4): A655–A665.
[29] SHI Y, ZHANG M H, QIAN D N,. Ultrathin Al2O3coatings for improved cycling performance and thermal stability of LiNi0.5Co0.2Mn0.3O2cathode material., 2016, 203(10): 154–161.
[30] NEUDECK S, STRAUSS F, GARCIA G,. Room temperature, liquid-phase Al2O3surface coating approach for Ni-rich layered oxide cathode material.., 2019, 55: 2174–2177.
[31] VETTER J, NOVAK P, WAGNER M R,. Ageing mechanisms in lithium-ion batteries., 2005, 147(1/2): 269–281.
[32] AURBACH D, MARKOVSKY B, SALITRA G,. Review on electrode-electrolyte solution interactions, related to cathode materials for Li-ion batteries., 2007, 165(2): 491–499.
[33] LIANG L W, HU G R, JIANG F,. Electrochemical behaviours of SiO2-coated LiNi0.8Co0.1Mn0.1O2cathode materials by a novel modification method.., 2016, 657: 570–581.
[34] GAN Z G, HU G R, PENG Z D,. Surface modification of LiNi0.8Co0.1Mn0.1O2by WO3as a cathode material for LIB.., 2019, 481: 1228–1238.
[35] LI Y P, YAN G J, LUO L M,. Enhanced electrochemical performance of LiNi0.4Co0.2Mn0.4O2cathode materialsY2O3coating., 2019, 6(10): 105533.
[36] LOGHAVI M M, MOHAMMADI-MANESH H, EQRA R. LiNi0.8Co0.15Al0.05O2coated by chromium oxide as a cathode material for lithium-ion batteries.., 2019, 23(8): 2569–2578.
[37] MYUNG S T, IZUMI K, KOMABA S,. Functionality of oxide coating for Li[Li0.05Ni0.4Co0.15Mn0.4]O2as positive electrode materials for lithium-ion secondary batteries., 2007, 111(10): 4061–4067.
[38] ZUO D X, WANG C P, TIAN G L,. Comparative study of Al2O3, SiO2and TiO2-coated LiNi0.6Co0.2Mn0.2O2electrode prepared by hydrolysis coating technology.., 2019, 9(2): 85–97.
[39] ZHU W C, HUANG X, LIU T T,. Ultrathin Al2O3coating on LiNi0.8Co0.1Mn0.1O2cathode material for enhanced cycleability at extended voltage ranges., 2019, 9(2): 92.
[40] NEUDECK S, MAZILKIN A, REITZ C,. Effect of low-temperature Al2O3ALD coating on Ni-rich layered oxide composite cathode on the long-term cycling performance of lithium- ion batteries.., 2019, 9: 5328.
[41] CUI X L, AI L, MAO L P,. Enhanced electrochemical properties of LiNi0.6Co0.2Mn0.2O2cathode material by the diffusional Al2O3coating layer., 2019, 25(2): 411–419.
[42] YANG K, FAN L Z, GUO J,. Significant improvement of electrochemical properties of AlF3-coated LiNi0.5Co0.2Mn0.3O2cathode materials., 2012, 63: 363–368.
[43] LEE S H, YOON C S, AMINE K,. Improvement of long-term cycling performance of Li[Ni0.8Co0.15Al0.05]O2by AlF3coating., 2013, 234: 201–207.
[44] CHO Y, OH P, CHO J. A new type of protective surface layer for high-capacity Ni-based cathode materials: nanoscaled surface pillaring layer.., 2013, 13(3): 1145–1152.
[45] HAN B L, LU X C. Effect of nano-sized CeF3on microstructure, mechanical, high temperature friction and corrosion behavior of Ni-W composite coatings.., 2009, 203(23): 3656–3660.
[46] KUMAR D A, SELVASEKARAPANDIAN S, NITHYA H,. Structural and conductivity analysis on cerium fluoride nanoparticles prepared by sonication assisted method.., 2012, 14(5): 626–634.
[47] KUMAR D A, SELVASEKARAPANDIAN S, NITHYA H,. Influence of substrate temperature on CeF3thin films prepared by thermal evaporation.., 2014, 143(2): 765–772.
[48] XIE Y, GAO D, ZHANG L L,. CeF3-modified LiNi1/3Co1/3Mn1/3O2cathode material for high-voltage Li-ion batteries.., 2016, 42(13): 14587–14594.
[49] SONG H G, KIM S B, PARK Y J. Enhanced electrochemical properties of Li[Ni0.5Co0.2Mn0.3]O2cathode by surface coating using LaF3and MgF2.., 2012, 29(2): 163–169.
[50] DAI S C, YAN G J, WANG L,. Enhanced electrochemical performance and thermal properties of Ni-rich LiNi0.8Co0.1Mn0.1O2cathode materialCaF2coating.., 2019, 847: 113197.
[51] LIM Y J, LEE S M, LIM H,. Amorphous Li-Zr-O layer coating on the surface of high-Ni cathode materials for lithium ion batteries., 2018, 282: 311–316.
[52] LIU S J, WU H, HUANG L,. Synthesis of Li2Si2O5-coated LiNi0.6Co0.2Mn0.2O2cathode materials with enhanced high-voltage electrochemical properties for lithium-ion batteries.., 2016, 674: 447–454.
[53] JO C H, CHO D H, NOH H J,. An effective method to reduce residual lithium compounds on Ni-rich Li[Ni0.6Co0.2Mn0.2]O2active material using a phosphoric acid derived Li3PO4nanolayer.., 2015, 8(5): 1464–1479.
[54] ZHU J, LI Y J, XUE L L,. Enhanced electrochemical performance of Li3PO4modified Li[Ni0.8Co0.1Mn0.1]O2cathode materiallithium-reactive coating.., 2019, 773: 112–120.
[55] FAN Q L, YANG S D, LIU J,. Mixed-conducting interlayer boosting the electrochemical performance of Ni-rich layered oxide cathode materials for lithium ion batteries., 2019, 421: 91–99.
[56] BAN L Q, YIN Y P, ZHUANG W D,. Electrochemical performance improvement of Li1.2[Mn0.54Ni0.13Co0.13]O2cathode material by sulfur incorporation., 2015, 180: 218–226.
[57] HUANG Y Q, HUANG Y H, HU X L. Enhanced electrochemical performance of LiNi0.8Co0.15Al0.05O2by nanoscale surface modification with Co3O4., 2017, 231: 294–299.
[58] XU S, DU C Y, XU X,. A mild surface washing method using protonated polyaniline for Ni-rich LiNi0.8Co0.1Mn0.1O2material of lithium ion batteries., 2017, 248: 534–540.
[59] HE X S, HAN G K, LOU S F,. Improved electrochemical performance of LiNi0.8Co0.15Al0.05O2cathode material by coating of graphene nanodots.., 2019, 166(6): A1038–A1044.
[60] YANG H, WU K P, HU G R,. Design and synthesis of double- functional polymer composite layer coating to enhance the electrochemical performance of the Ni-rich cathode at the upper cutoff voltage., 2019, 11: 8556–8566.
[61] GAN Q M, QIN N, ZHU Y H,. Polyvinylpyrrolidone-induced uniform surface-conductive polymer coating endows Ni-rich LiNi0.8Co0.1Mn0.1O2with enhanced cyclability for lithium-ion batteries., 2019, 11(13): 12594–12604.
[62] 尹艳萍, 庄卫东, 王忠, 等. 一种锂离子电池用含镍层状正极材料/碳复合材料及其制备方法. 中国, CN108232153A. 2018.06.29.
[63] 王忠, 庄卫东, 尹艳萍, 等. 一种石墨烯改性锂镍钴锰氧化物正极材料及其制备方法. 中国, CN109244448A. 2019.01.18.
[64] 王忠, 庄卫东, 尹艳萍, 等. 一种纳米碳材料改性锂镍钴锰氧化物正极材料及制备方法. 中国, CN109473642A. 2019.03.15.
[65] ZHANG S S, CHEN J, WANG C S. Elemental sulfur as a cathode additive for enhanced rate capability of layered lithium transition metal oxides.., 2019, 166(4): A487–A492.
[66] ZHANG S S, FAN X L, WANG C S. Enhanced electrochemical performance of Ni-rich layered cathode materials by using LiPF6as a cathode additive., 2019, 6(5): 1536–1541.
[67] LI J, DOWNIE L E, MA L,. Study of the failure mechanisms of LiNi0.8Mn0.1Co0.1O2cathode material for lithium ion batteries.., 2015, 162(7): A1401–A1408.
[68] LIU H, WOLF M, KARKI K,. Intergranular cracking as a major cause of long-term capacity fading of layered cathodes.., 2017, 17(6): 3452–3457.
[69] ZHAO E Y, CHEN M M, HU Z B,. Improved cycle stability of high-capacity Ni-rich LiNi0.8Mn0.1Co0.1O2at high cut-off voltage by Li2SiO3coating., 2017, 343: 345–353.
[70] PENG Z J, YANG G W, LI F Q,. Improving the cathode properties of Ni-rich LiNi0.6Co0.2Mn0.2O2at high voltages under 5by Li2SiO3coating and Si4+doping.., 2018, 762: 827–834.
[71] LEE S W, KIM M S, JEONG J H,. Li3PO4surface coating on Ni-rich LiNi0.6Co0.2Mn0.2O2by a citric acid assisted Sol-Gel method: improved thermal stability and high-voltage performance., 2017, 360: 206–214.
[72] KIM S B, LEE K J, CHOI W J,. Preparation and cycle performance at high temperature for Li[Ni0.5Co0.2Mn0.3]O2coated with LiFePO4.., 2010, 14: 919–922.
[73] WU Z Z, JI S P, LIU T C,. Aligned Li+tunnels in core-shell Li(NiMnCo)O2@LiFePO4enhances its high voltage cycling stability as Li-ion battery cathode.., 2016, 16(10): 6357–6363.
[74] ZHU L, YAN T F, JIA D,. LiFePO4-coated LiNi0.5Co0.2Mn0.3O2cathode materials with improved high voltage electrochemical performance and enhanced safety for lithium ion pouch cells.., 2019, 166(3): A5437–A5444.
[75] KIM W S, KIM S B, JANG I C,. Remarkable improvement in cell safety for Li[Ni0.5Co0.2Mn0.3]O2coated with LiFePO4.., 2010, 492(1/2): L87–L90.
[76] DIAO R J, NAYAKA G P, ZHU C Y,. CePO4coated LiNi0.6Co0.2Mn0.2O2as cathode material and its electrochemical performance.., 2019, 14: 8070–8079.
[77] TONG H, DONG P Y, ZHANG J F,. Cathode material LiNi0.8Co0.1Mn0.1O2/LaPO4with high electrochemical performance for lithium–ion batteries.., 2018, 764: 44–50.
[78] LIU W M, HU G R, DU K,. Surface coating of LiNi0.8Co0.15Al0.05O2with LiCoO2by a molten salt method.., 2013, 216: 267–272.
[79] LIU W M, HU G R, DU K,Synthesis and characterization of LiCoO2-coated LiNi0.8Co0.15Al0.05O2cathode materials.., 2012, 83: 11–13.
[80] LIU W M, HU G R, DU K,. Enhanced storage property of LiNi0.8Co0.15Al0.05O2coated with LiCoO2., 2013, 230: 201–206.
[81] YAN P F, ZHENG J M, GU M,. Intragranular cracking as a critical barrier for high-voltage usage of layer-structured cathode for lithium-ion batteries.., 2017, 8: 14101.
[82] HASHIGAMI S, KATO Y, YOSHIMI K,. Influence of lithium silicate coating on retarding crack formation in LiNi0.5Co0.2Mn0.3O2cathode particles., 2018, 291: 304–310.
[83] DU M L, YANG P, HE W X,. Enhanced high-voltage cycling stability of Ni-rich LiNi0.8Co0.1Mn0.1O2cathode coated with Li2O-2B2O3.., 2019, 805: 991–998.
[84] HASHIGAMI S, YOSHIMI K, KATO Y,. Improvement of cycleability and rate-capability of LiNi0.5Co0.2Mn0.3O2cathode materials coated with lithium boron oxide by an antisolvent precipitation method., 2019, 4(29): 8676–8681.
[85] ZHANG J Y, CAO Y, OU X,. Constituting the NASICON type solid electrolyte coated material forming anti-high voltage system to enhance the high cut-off voltage performance of LiNi0.6Co0.2Mn0.2O2charge attracts electrostatic assembly., 2019, 436: 226722.
[86] PARK K, PARK J H, HONG S G,. Enhancement in the electrochemical performance of zirconium/phosphate bi-functional coatings on LiNi0.8Co0.15Mn0.05O2by the removal of Li residuals.., 2016, 18: 29076–29085.
[87] HE X S, XU X, WANG L G,. Enhanced electrochemical performance of LiNi0.8Co0.15Al0.05O2cathode materialLi2TiO3nanoparticles coating.., 2019, 166(2): A143–A150.
[88] YANG J, YU Z Y, YANG B,. Electrochemical characterization of Cr8O21modified LiNi0.5Co0.2Mn0.3O2cathode material., 2018, 266: 342–347.
[89] GAO T P, WONG K W, FUNG K Y,. A rational three-step calcination strategy for synthesizing high-quality LiNi0.5Mn0.3Co0.2O2cathode materials: the key role of suppressing Li2O formation., 2018, 288: 153–164.
[90] BHUVANESWARI D, BABU G, KALAISELVI N. Effect of surface modifiers in improving the electrochemical behavior of LiNi0.4Mn0.4Co0.2O2cathode., 2013, 109: 684–693.
[91] WANG D, LI X H, WANG Z X,. Role of zirconium dopant on the structure and high voltage electrochemical performances of LiNi0.5Co0.2Mn0.3O2cathode materials for lithium ion batteries., 2016, 188: 48–56.
[92] POUILLERIE C, CROGUENNEC L, BIENSAN P,. Synthesis and characterization of new LiNi1−yMgO2positive electrode materials for lithium-ion batteries.., 2000, 147(6): 2061–2069.
[93] XIE Q, LI W D, MANTHIRAM A. A Mg-doped high-nickel layered oxide cathode enabling safer, high-energy-density Li-ion batteries.., 2019, 31(3): 938–946.
[94] POUILLERIE C, CROGUENNEC L, DELMAS C. The LiNi1−yMgO2(=0.05, 0.10) system: structural modifications observed upon cycling., 2000, 132(1/2): 15–29.
[95] HUANG B, LIN X H, WANG Z X,. Synthesis of Mg-doped LiNi0.8Co0.15Al0.05O2oxide and its electrochemical behavior in high-voltage lithium-ion batteries.., 2014, 40(8): 13223–13230.
[96] BREUER O, CHAKRABORTY A, LIU J,. Understanding the role of minor molybdenum doping in LiNi0.5Co0.2Mn0.3O2electrodes: from structural and surface analyses and theoretical modeling to practical electrochemical cells., 2018, 10(35): 29608–29621.
[97] WOO S U, PARK B C, YOON C S,. Improvement of electrochemical performances of Li[Ni0.8Co0.1Mn0.1]O2cathode materials by fluorine substitution.., 2007, 154(7): A649–A655.
[98] LI C L, KAN W H, XIE H L,. Inducing favorable cation antisite by doping halogen in Ni-rich layered cathode with ultrahigh stability.., 2019, 6(4): 1801406.
[99] LI X, XIE Z W, LIU W J,. Effects of fluorine doping on structure, surface chemistry, and electrochemical performance of LiNi0.8Co0.15Al0.05O2., 2015, 174: 1122–1130.
[100] LÜ C J, YANG J, PENG Y,. 1D Nb-doped LiNi1/3Co1/3Mn1/3O2nanostructures as excellent cathodes for Li-ion battery., 2019, 297: 258–266.
[101] YANG Z G, XIANG W, WU Z G,. Effect of niobium doping on the structure and electrochemical performance of LiNi0.5Co0.2Mn0.3O2cathode materials for lithium ion batteries.., 2017, 43(4): 3866–3872.
[102] WU J F, LIU H G, YE X H,. Effect of Nb doping on electrochemical properties of LiNi1/3Co1/3Mn1/3O2at high cutoff voltage for lithium-ion battery.., 2015, 644: 223–227.
[103] BREGER J, MENG Y S, HINUMA Y,. Effect of high voltage on the structure and electrochemistry of LiNi0.5Mn0.5O2: a joint experimental and theoretical study.., 2006, 18(20): 4768–4781.
[104] SCHIPPER F, DIXIT M, KOVACHEVA D,. Stabilizing nickel-rich layered cathode materials by a high-charge cation doping strategy: zirconium-doped LiNi0.6Co0.2Mn0.2O2., 2016, 4: 16073–16084.
[105] DONG S D, ZHOU Y, HAI C X,. Ultrathin CeO2coating for improved cycling and rate performance of Ni-rich layered LiNi0.7Co0.2Mn0.1O2cathode materials.., 2019, 45(1): 144–152.
[106] CHEN Y X, LI Y J, LI W,. High-voltage electrochemical performance of LiNi0.5Co0.2Mn0.3O2cathode materialthe synergetic modification of the Zr/Ti elements., 2018, 281: 48–59.
[107] DU R, BI Y, YANG W,. Improved cyclic stability of LiNi0.8Co0.1Mn0.1O2Ti substitution with a cut-off potential of 4.5 V.., 2015, 41(5): 7133–7139.
[108] PARK S H, OH S W, SUN, Y K. Synthesis and structural characterization of layered Li[Ni1/3+xCo1/3Mn1/3−2xMo]O2cathode materials by ultrasonic spray pyrolysis., 2005, 146(1/2): 622–625.
[109] YANG J, XIA Y Y. Suppressing the phase transition of the layered Ni-rich oxide cathode during high-voltage cycling by introducing low-content Li2MnO3., 2016, 8(2): 1297–1308.
[110] BAK S M, NAM K W, CHANG W,. Correlating structural changes and gas evolution during the thermal decomposition of charged LiNi0.8Co0.15Al0.05O2cathode materials.., 2013, 25(3): 337–351.
[111] MIN K, SEO S W, SONG Y Y,. A first-principles study of the preventive effects of Al and Mg doping on the degradation in LiNi0.8Co0.1Mn0.1O2cathode materials.., 2017, 19: 1762–1769.
[112] DIXIT M, MARKOVSKY B, AURBACH D,. Unraveling the effects of Al doping on the electrochemical properties of LiNi0.5Co0.2Mn0.3O2using first principles.., 2017, 164(1): A6359–A6365.
[113] XIAO P H, DENG Z Q, MANTHIRAM A,. Calculations of oxygen stability in lithium-rich layered cathodes., 2012, 116(44): 23201–23204.
[114] AURBACH D, SRUR–LAVI O, GHANTY C,. Studies of aluminum-doped LiNi0.5Co0.2Mn0.3O2: electrochemical behavior, aging, structural transformations, and thermal characteristics.., 2015, 162(6): A1014–A1027.
[115] KIM U H, JUN D W, PARK K J,. Pushing the limit of layered transition metal oxide cathodes for high-energy density rechargeable Li ion batteries.., 2018, 11: 1271–1279.
[116] KONISHI H, YOSHIKAWA M, HIRANO T. The effect of thermal stability for high-Ni-content layer-structured cathode materials, LiNi0.8Mn0.1−xCo0.1MoO2(=0, 0.02, 0.04)., 2013, 244: 23–28.
[117] LIU Q, ZHAO Z K, WU F,. The effects of molybdenum doping on LiNi0.6Co0.2Mn0.2O2cathode material., 2019, 337: 107–114.
[118] WEIGEL T, SCHIPPER F, ERICKSON E M,. Structural and electrochemical aspects of LiNi0.8Co0.1Mn0.1O2cathode materials doped by various cations.., 2019, 4(2): 508–516.
[119] XIANG W, ZHU C Q, ZHANG J,. Synergistic coupling effect of sodium and fluorine co-substitution on enhancing rate capability and cycling performance of Ni-rich cathode for lithium ion battery.., 2019, 786: 56–64.
[120] HU G, ZHANG M, LIANG L,. Mg-Al-B co-substitution LiNi0.5Co0.2Mn0.3O2cathode materials with improved cycling performance for lithium-ion battery under high cutoff voltage., 2016, 190: 264–275.
[121] CHANG S H, CHEN Y X, LI Y J,. Improvement of the high-voltage electrochemical properties of Li[Ni0.5Co0.2Mn0.3]O2@ ZrO2cathode materials with liquid phase modification.., 2019, 781: 496–503.
[122] LI X, ZHANG K J, WANG M S,. Dual functions of zirconium modification on improving the electrochemical performance of Ni-rich LiNi0.8Co0.1Mn0.1O2., 2018, 2: 413–421.
[123] HE T, LU Y, SU Y F,. Sufficient utilization of zirconium ions to improve the structure and surface properties of nickel-rich cathode materials for lithium-ion batteries., 2018, 11(10): 1639–1648.
[124] SUN Y K, KIM D H, YOON C S,. A novel cathode material with a concentration-gradient for high-energy and safe lithium- ion batteries.., 2010, 20(3): 485–491.
[125] XU X, JIAN J Y, XIANG L Z,. Enhancing high-voltage performances of nickel-based cathode materialaluminum and progressive concentration gradient modification., 2019, 317: 459–467.
[126] SHI J L, QI R, ZHANG X D,. High-thermal- and air-stability cathode material with concentration-gradient buffer for Li-ion batteries., 2017, 9(49): 42829–42835.
[127] TANG M J, YANG J, CHEN N T,. Overall structural modification of a layered Ni-rich cathode for enhanced cycling stability and rate capability at high voltage., 2019, 7: 6080–6089.
[128] RAN Q W, ZHAO H Y, WANG Q,. Dual functions of gradient phosphate polyanion doping on improving the electrochemical performance of Ni-rich LiNi0.6Co0.2Mn0.2O2cathode at high cut-off voltage and high temperature., 2019, 299: 971–978.
[129] ZHANG M L, ZHAO H Y, TAN M,. Yttrium modified Ni-rich LiNi0.8Co0.1Mn0.1O2with enhanced electrochemical performance as high energy density cathode material at 4.5 V high voltage.., 2019, 774: 82–92.
[130] TANG W J, CHEN Z X, XIONG F,. An effective etching- induced coating strategy to shield LiNi0.8Co0.1Mn0.1O2electrode materials by LiAlO2., 2019, 412: 246–254.
[131] YU H F, LI Y G, HU Y J,. 110th anniversary: concurrently coating and doping high-valence vanadium in nickel-rich lithiated oxides for high-rate and stable lithium-ion batteries.., 2019, 58(10): 4108–4115.
[132] CHEN Y X, LI Y J, TANG S Y,. Enhanced electrochemical properties of the Cd-modified LiNi0.6Co0.2Mn0.2O2cathode materials at high cut-off voltage., 2018, 395: 403–413.
[133] KONG D F, HU J T, CHEN Z F,. Ti-gradient doping to stabilize layered surface structure for high performance high-Ni oxide cathode of Li-ion battery.., 2019, 9: 1901756.
[134] HAN B, XU S, ZHAO S,. Enhancing the structural stability of Ni-rich layered oxide cathodes with a preformed Zr-concentrated defective nanolayer., 2018, 10(46): 39599–39607.
[135] SCHIPPER F, BOUZAGLO H, DIXIT M,. From surface ZrO2coating to bulk Zr doping by high temperature annealing of nickel-rich lithiated oxides and their enhanced electrochemical performance in lithium ion batteries.., 2018, 8(4): 1701682.
[136] MENG K, WANG Z X, GUO H J,. Improving the cycling performance of LiNi0.8Co0.1Mn0.1O2by surface coating with Li2TiO3., 2016, 211: 822–831.
[137] WU F, LI Q, CHEN L,. Use of Ce to reinforce the interface of Ni-rich LiNi0.8Co0.1Mn0.1O2cathode materials for lithium-ion batteries under high operating voltage., 2019, 12(4): 935–943.
[138] ZHAN X W, GAO S, CHENG Y T. Influence of annealing atmosphere on Li2ZrO3-coated LiNi0.6Co0.2Mn0.2O2and its high-voltage cycling performance., 2019, 300: 36–44.
[139] 李宁, 李文进, 张宇宙, 等. 一种梯度高镍正极材料及其制备方法和锂离子电池. 中国, CN107528060A. 2017.12.29.
[140] WANG D, LI X H, WANG Z X,. Co-modification of LiNi0.5Co0.2Mn0.3O2cathode materials with zirconium substitution and surface polypyrrole coating: towards superior high voltage electrochemical performances for lithium ion batteries., 2016, 196: 101–109.
[141] YANG H P, WU H H, GE M Y,. Simultaneously dual modification of Ni-rich layered oxide cathode for high-energy lithium- ion batteries.., 2019, 29(13): 1808825.
[142] RAN Q W, ZHAO H Y, SHU X H,. Enhancing the electrochemical performance of Ni-rich layered oxide cathodes by combination of the gradient doping and dual-conductive layers coating.., 2019, 2(5): 3120–3130.
[143] SUN S M, LIU T, NIU Q H,. Improvement of superior cycle performance of LiNi0.8Co0.15Al0.05O2cathode for lithium-ion batteries by multiple compound modifications.., 2019, 838: 178–185.
[144] 任志敏, 王振尧, 高敏, 等. 一种磷镁协同掺杂改性的富锂锰基正极材料及其制备方法和锂离子电池.中国, CN107591534A. 2018.01.16.
[145] XU G L, LIU Q, LAU K K S,. Building ultraconformal protective layers on both secondary and primary particles of layered lithium transition metal oxide cathodes., 2019, 4: 484–494.
Research Progress on Coating and Doping Modification of Nickel Rich Ternary Cathode Materials
BAI Xiangtao1, BAN Liqing2, ZHUANG Weidong2
(1. China Automotive Battery Research Institute Co., Ltd, Beijing 101407, China; 2. General Research Institute for Nonferrous Metals, Beijing 100088, China)
In recent years, the development of new energy vehicles industry is accelerating. Lithium nickel cobalt manganese/aluminum oxide ternary cathode materials (NCM/NCA), especially with the nickel content ≥50%, has aroused great interest in both academia and industry. This is mainly due to the fact that the aggregative parameters of performance and cost of NCM/NCA are superior to those of traditional cathode materials, such as LiCoO2and LiFePO4. However, the application of NCM/NCA is affected by a number of drawbacks, including poor safety and insufficient cycle stability and so on, which are mainly attributed to its crystal and surface structure. Researchers have carried out various efforts to solve these problems and further improve the performance of NCM/NCA. Some remarkable results have been achieved in the past few years. In this review, the latest research progress on coating and doping of Ni-rich ternary cathode materials is summarized from the view on the mechanism of structural and electrochemical improvement of NCM/NCA. Finally, the perspective for the development of NCM/NCA cathode materials is also prospected.
lithium nickel cobalt manganese oxide; coating; doping; mechanism
O646
A
2019-11-07;
2020-01-14
国家重点研发计划—新能源专项(2016YFB0100400)
The National Key R&D Program of China-New Energy Special Project (2016YFB0100400)
柏祥涛(1983–), 男, 博士研究生, 高级工程师. E-mail: baixt@glabat.com
BAI Xiangtao (1983–), male, PhD candidate, senior engineer. E-mail: baixt@glabat.com
1000-324X(2020)09-0972-15
10.15541/jim20190568
