乳腺MRI簇环样强化的影像与病理对照研究
2020-09-08谭非易刘梅程流泉李平杨宇李少波
谭非易,刘梅,程流泉,李平,杨宇,李少波
1.解放军总医院第六医学中心放射科,北京 100048;2.湖南中医药大学第一附属医院放射科,湖南长沙 410021;3.解放军总医院第一医学中心病理科,北京 100853;*通讯作者 程流泉 13910209982@139.com
簇环样强化是2013年第5 版乳腺影像报告和数据系统(breast imaging reporting and data system,BIRADS)新增的非肿块强化(non-mass enhancement,NME)的内部强化特征。有学者认为,簇环样强化是导管周围基质强化形成的多个薄壁小环形强化簇集样分布的一种特征性表现[1-2]。Tozaki 等[3]于2006年提出簇环样强化的概念,并认为其对恶性肿瘤的阳性预测值为67%~100%;随后部分文献报道了类似的研究成果[4-8],但这种增强模式的总体阳性预测值目前尚存在争议。临床工作中观察到,簇环样强化不仅见于NME 表现的乳腺恶性肿瘤,如乳腺导管原位癌、浸润性导管癌、浸润性小叶癌等;也可见于乳腺良性病变,如硬化性腺病、不典型导管增生、乳腺纤维囊性病变、导管内乳头状瘤、簇集的小囊肿、乳管扩张、乳腺炎性疾病等,甚至在增强延迟期背景实质强化中常见到簇环样强化的表现[9-12]。这些评估簇环样强化对恶性肿瘤的阳性预测值的文献多数在第5 版BIRADS 之前发表,成像的空间分辨率有限,样本量较小,并且判断簇环样强化的标准并未统一。随着MRI空间分辨率的提高,在诊断乳腺病变时更容易观察到内部增强模式,尤其是簇环样内部增强模式[2]。本研究利用1 mm×1 mm×1 mm 的高空间分辨率成像方式,分析簇环样强化的病理基础,以探讨其诊断价值。
1 资料与方法
1.1 研究对象 回顾性分析解放军总医院第一医学中心放射科2017年10月—2019年10月经活检或手术病理证实的簇环样强化女性患者103 例共105 个病灶,年龄24~72 岁,平均(46.1±9.5)岁。105 个病灶中57 个为恶性,包括浸润性乳腺癌(invasive ductal carcinoma,IDC)33 例、单纯导管内原位癌(ductal carcinoma in situ,DCIS)17 例、DCIS 伴微浸润5 例、黏液癌1 例、乳头状癌1 例;48 个病灶为良性,包括导管内乳头状瘤11 例、乳腺腺病21 例(其中硬化性腺病10 例)、纤维囊性增生2 例、不典型增生3 例、炎性病变7 例、纤维腺瘤4 例。同一病灶病理上报告的多种类型均以危险级别偏高的病变论述,如腺病合并不典型增生,则以不典型增生计算。排除MRI 检查前病灶接受穿刺活检或其他治疗干预的患者。
1.2 仪器与方法 采用 GE 3.0T MR 扫描仪(Discovery750 或750W),8 通道乳腺线圈。患者取俯卧位双乳自然悬垂。检查序列[13]包括,①FSE-T2WI:IDEAL 脂肪抑制,TR 5247 ms,TE 68 ms,矩阵320×224。②EPI-DWI:STIR 脂肪抑制,TR 5400 ms,TE 60 ms,IR 250 ms,b=0、1000 s/mm2,矩阵128×128。FSE-T2WI 和EPI-DWI 均为二维采集,横轴位匹配定位,视野34 cm×34 cm,层厚4 mm,间距1 mm,扫描层数36。③T1WI 序列用动态增强VIBRANT 序列去除脂肪抑制选项并将TE 设置为最小,其余扫描参数与下述动态增强一致。④动态增强VIBRANT 序列:TR 7.7 ms,TE 4.3 ms,视野32 cm×32 cm,脉冲角100;调节并行采集(ASSET)因子和部分K 空间填充方式达到实际采集空间分辨率1 mm×1 mm×1 mm,192 层,每个时相的时间分辨率为120 s,连续采集6 个时相,按照1+5 模式,即第1 时相为预扫描,第2 时相扫描开始的同时以2 ml/s 注射0.5 mmol/L 钆对比剂,总量按照0.1 mmol/kg 计算,对比剂注射后以同样的速度注入20~25 ml 生理盐水冲洗。
1.3 簇环样强化的判定与图像测量 以下特征表现为簇环样强化[2,5,11,14]:①在增强图像上表现为中心低信号的小环,小环直径1~3 mm;②在一定范围内小环的数量≥5 个,各小环空间相连呈蜂窝状;③分布符合乳腺小叶或终末导管小叶单位(terminal ductal lobular unit,TDLU)的解剖形态。其中,增强扫描第1 时相出现的簇环样强化定义为早期簇环样强化,增强扫描第4时相出现的簇环样强化为延迟期簇环样强化,记录为“1”,否则记录为“0”,两者均是本研究的纳入标准。簇环样强化的动态增强时间-信号曲线(TIC)测量ROI 大小包括3~5 个小环,出现平台型TIC 时则用增强第1 时相减去增强第4 时相,若结果为正值则归为流出型(Ⅲ型),若结果为负值则归为流入型(Ⅰ型)。由1 名主治医师和1 名主任医师判读图像并达成一致意见。按照簇环强化出现的时机和曲线类型组合成不同的增强模式。
1.4 簇环样强化的病理对照 在连续的病理切片中选取MRI 图像上在位置、范围和病理大小可以互相匹配解释的病理图片,标本大小从玻片的2~3 cm 到放大2~6 倍视野,HE 染色后,由病理科医师和放射科医师进行一对一比较和归类分析。由于标本不同程度萎缩,经病理科医师认定,选择直径500~2000 μm的病灶单位与MRI 上直径1~3 mm 的小环对应解释。将MRI 簇环样强化划分为3 个部分,中心表现为低于簇环强化幅度或无强化的低信号、小环表现为强化幅度高于中心和周围的高信号部分、周围表现为小环外围部分,由病理科医师对其中的病理成分进行分类。
1.5 统计学方法 采用SPSS 19.0 软件,对增强早期、延迟期是否有簇环样强化、TIC 类型与病理良恶性的关系进行分析。通过χ2检验进行单变量分析,筛选出病变良、恶性组差异有统计学意义的自变量,再对其进行二分类Logistic 回归分析,使用“向前似然比”法,筛选出有统计学差异的诊断模式,得出其似然比(OR)及95%CI。以P<0.05 为差异有统计学意义。
2 结果
2.1 簇环样强化的影像-病理对照 在MRI 上,簇环强化的直径约1~3 mm,强化的小环取决于中心和环周组织的低信号衬托形成的对比,簇环样强化出现的时机可以在增强早期(对比剂注射后2 min)表现为中心不强化,或延迟期(对比剂注射后8 min)表现为中心廓清。在组织病理图上对应大小的结构为肿瘤的瘤巢或TDLU,直径在0.5~4.0 mm 之间;腺泡直径为50 μm,扩张的TDLU 间导管的直径约0.5~2.0 mm。因此认为,簇环样强化的组织单位为瘤巢与周围的纤维基质、扩张的导管与周围基质以及正常或增生的TDLU 与纤维包囊。
MRI 上中心低信号部分可见到下列3 种成分:①扩张的导管内无细胞的坏死出血或分泌物,早期和延迟期均无强化,对应的病理类型包括IDC、DCIS、腺病或乳腺炎;②瘤巢中心的癌细胞团,早期强化幅度低于周围的环结构,或早期与环同期强化而延迟期廓清凸显,对应病理包括IDC、DCIS、导管内乳头状癌或包裹型乳头状癌;③纤维血管基质与增生的上皮细胞,早期弱强化并持续强化,对应导管内乳头状瘤、不典型增生、旺炙增生的TDLU、复杂腺病(图1)。

图1 女,58 岁。低-中级别大汗腺型导管原位癌并周围腺病改变。MRI 增强早期示病灶呈局灶性分布的簇环样强化(A);延迟期示病灶仍呈簇环样强化,病灶中央部分小环延迟期廓清、周围部分小环延迟期渐进强化(B);病理镜下示病灶大体形态与MRI 相应截面所示相似,所测得瘤巢直径大小与MRI 小环接近(箭头,HE,×0.4,C);测量单个腺泡直径约48 μm(箭),与MRI 上簇环的大小不匹配(HE,×24.4,D)
MRI 上强化的小环对应组织病理上2 种成分:①以较大的或扩张的导管壁轮廓为基础的导管周围基质,包括基底膜内外的肿瘤或非肿瘤细胞成分,可观察到显著或不显著的血管内皮细胞提示血供丰富。②瘤巢周围的纤维包囊、TDLU 纤维包囊,也可见于黏液癌黏液湖周围富含毛细血管的纤维分隔,也见于腺病、纤维腺瘤和乳腺炎等良性病灶(图2)。
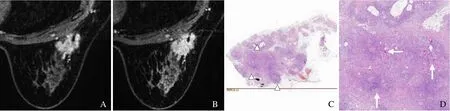
图2 女,32 岁,右侧肉芽肿性乳腺炎。MRI 增强早期示病灶呈局灶性簇环样强化(A);延迟期簇环样强化特征更明显,呈渐进性强化(B);病理镜下示病灶大体形态与MRI 相应截面所示相似(HE,×0.4),被破坏的小叶结构呈类圆形(箭头)对应MRI 图上的小环(C);放大病理图示大量炎症细胞浸润,周围血供丰富(箭),可解释MRI 图像上持续渐进性强化的簇环样强化灶(HE,×1.5,D)
MRI 环周组织对应病理上3 种组织成分:①癌细胞成分,主要是IDC,可以观察到新生的血管结构,早期明显强化且延迟期廓清,周围离心扩展小;②炎症细胞成分,以淋巴细胞和中性粒细胞为主,可以观察到丰富的血管结构,早期明显强化且延迟期持续强化,延迟期范围扩展;③周围基质成分,包括富含黏液的基质、淀粉样或玻璃样变性的纤维基质,其中黏液基质表现为持续的延迟期强化,淀粉样或玻璃样变性的基质表现为无强化或轻度强化(图3)。
2.2 簇环样强化的诊断价值 恶性组和良性组簇环样强化出现在增强早期或延迟期差异无统计学意义(表1)。单因素分析和Logistic 回归分析(表2)共同提示廓清型曲线(Ⅲ型)是独立预测因素(P<0.05)。在不同的组合模式中,组合A 除1 例浸润性导管癌并黏液癌外,其余8 例为腺病且其中2 例合并纤维腺瘤,2 例为纤维囊性疾病,2 例为肉芽肿性小叶性乳腺炎;模式C 中1 例为黏液腺癌,4 例均为腺病,其中2 例硬化性腺病;模式E 的6 例病变均为良性,除1 例为导管内乳头状瘤外,其余均为腺病、不典型增生并腺病、或腺病并纤维腺瘤形成,这些也共同提示流入型曲线(Ⅰ型)是良性诊断的独立预测因素。
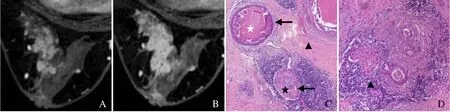
图3 女,38 岁,高级别DCIS。增强早期(A)簇环样强化,延迟期(B)环周组织强化显著,簇环样强化中心与病理图(HE,×2.4,C)的扩张导管中心对应,可以为细胞填充或坏死分泌物(星号),强化的小环对应导管壁周围细胞丰富组织(箭),环周的间质部分延迟期均强化凸显簇环特征,病理图(HE,×4.6,D)环周癌性间质水肿、疏松,有大量淋巴细胞浸润,血供极丰富(箭头)
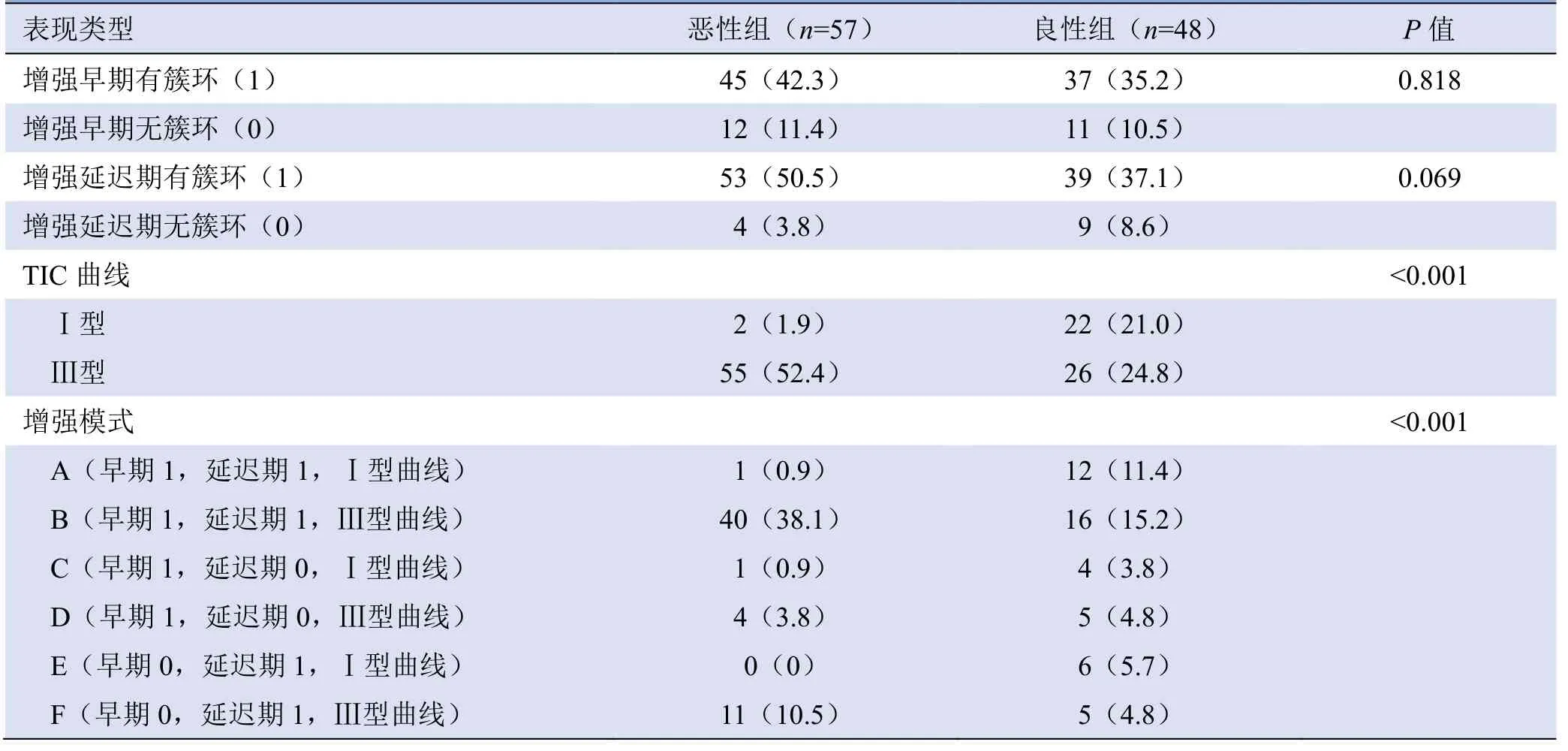
表1 两组患者病变性质和簇环样强化判断模式比较[例(%)]
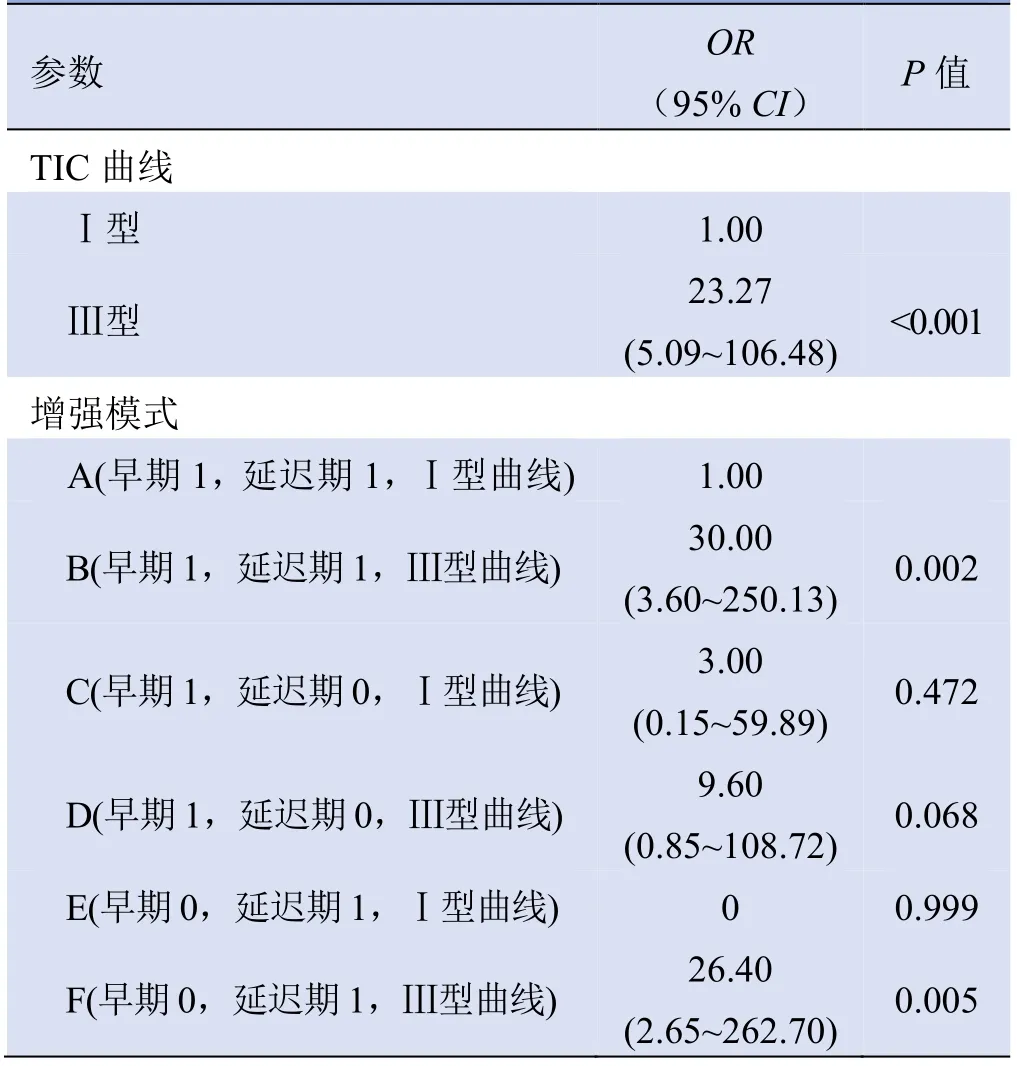
表2 Logistic 回归分析病变良恶性判断模式
3 讨论
3.1 簇环样强化的病理基础 2013 版BI-RADS 词汇对簇环样强化进行了定义,指出它是导管周围基质的强化,认为相当于导管周围间质或导管壁的强化[14]。Tozaki 等[3]于2006年首次提出簇环样强化的概念时,就已将簇环样强化病变与病理对照分析,认为增强早期观察到的簇环样强化其病理显示为导管周围间质,但不能排除导管内癌细胞参与增强;部分纤维囊性疾病呈现的簇环样强化对应于伴有微钙化的扩张导管。Chikarmane 等[4]研究表明由于簇环样强化总是与不均质强化和簇集样强化存在交叉,很难将簇环与其他强化模式分开。Uematsu 等[10]研究显示,部分病例横断面可见成簇小环,部分病例仅矢状面可见成簇小环。从组织病理测量看,乳腺腺体每个腺叶输乳管直径约2 mm,每个TDLU 的平均直径约0.5 mm,腺泡的直径约(44.8±8.2)μm,而目前MRI 的空间分辨率设置多数在1.2~1.6 mm,无法分辨直径<1 mm 的细微结构,并不足以显示腺泡的周围基质。本研究使用1 mm×1 mm×1 mm 分辨率显示的簇环样强化直径在1~3 mm,当各种原因导致TDLU 增大或导管扩张时,即可在MRI 上凸显为簇环样强化,在重建图像上如果平行于导管则表现为轨道样强化,如果垂直于导管则表现为小环样强化。
在这种各向同性高空间分辨率下将簇环分成中心、小环和环周3 个部分。从簇环样强化的大小,根据与病理图片的一一对照测量,认为凸显强化的小环对应的是扩张导管周围的基质、瘤巢或TDLU 周围的纤维包囊。凸显强化的小环厚度大约1 mm,病理医师解读此区域可见血管内皮细胞增多,可解释凸显强化的小环,向内的中心部分主要是通过渗透,向外的环周部分则取决于组织细胞成分与血供。
3.2 簇环样强化的影像特征 簇环的形成取决于中心部分的低信号与小环及环周组织的动态增强对比差异,确切地说,环的凸显取决于中心部分的低信号,而决定动态增强曲线类型的主要是小环和环周组织,这是病灶的主体部分,为了避免ROI 测量的平均容积效应,本研究对呈现为平台型曲线的病灶采用减影的方式进行再划分。当中心部分是扩张乳管内的出血或分泌物时,呈现为不强化的低信号可以理解;如果中心是富血供的瘤巢或导管内乳头状瘤血管纤维束,则呈现早期簇集样强化,延迟期廓清呈簇环样强化,见于浸润性癌和浆细胞乳腺炎脓肿形成前期,这在早期版本的BI-RADS 被描述为分隔样强化。在黏液癌、腺病或纤维腺瘤,簇环样强化出现在早期而延迟期被填平,主要是黏液湖或纤维间质的渐进性强化消除了对比差异[15]。
因此,本研究显示单独根据增强早期或延迟期有无簇环样强化判断病变的良恶性差异无统计学意义,但是将其与TIC 类型结合后,即显示差异有统计学意义。Logistic 回归分析显示,无论簇环样强化何时出现,廓清型TIC 对恶性预测的OR 值均有统计学意义。相关研究[16]认为,DCIS 存在管周型和基质型2 种不同的血管生成类型,管周型表现为导管基底膜周围大量环状、网状微血管生成;基质型表现为DCIS 病灶周围基质内大量新生血管;而浸润性导管癌亦分为癌细胞团周围大量微血管生成,及癌细胞团内部基质内大量新生血管。多数恶性病变边缘区微血管密度明显高于中央区,中央区为坏死组织或低微血管密度区的结缔组织。当恶性病变表现为模式B 时,其血管生成多为管周型,增强早期管周DCIS 或瘤巢周围强化明显,表现为簇环样强化;延迟期癌细胞供血血管对比剂廓清,而周围间质持续强化,表现为小环壁较早期变薄的簇环样强化。当恶性病变血管生成为基质型时,则表现为早期呈簇集样强化(非簇环样强化)、延迟期癌细胞团内部对比剂廓清、周围间质持续强化,呈簇环样,与Tozaki 等[3]和Chikarmane 等[4]的观点一致,Tozaki 等[3]认为这种强化模式是簇环样强化的两种类型之一,也称为集丛样强化的子集,可以解释增强模式F。
流入型曲线的簇环样强化包括模式A、C、E,这种或早期或延迟期出现的簇环样强化,多数对应良性病变,包括导管内乳头状瘤、腺病、不典型增生并腺病、或腺病并纤维腺瘤形成。这种流入型的簇环强化,除1例黏液癌解释为中心黏液的持续强化导致延迟期簇环强化消失外,其余均可用不同程度强化的小环和持续强化的环周组织的对比差异进行解释,对良性预测的提示意义很明确。良性病灶管腔中央为分泌物或无细胞结构物质在增强早期及延迟期均不强化,或者中心为渐进强化的组织;决定流入型曲线的持续强化的主要是小环和环周组织,这些良性病灶组织以渐进性强化为主。
本研究的不足之处在于完全空间匹配的影像-病理对照仍然存在技术上的困难,尽管本研究在影像和病理之间寻求了最合理的解释,但这仅是典型层面的典型表现,对强化的机制尚缺乏药代动力学和病理生理的解释。在不同强化模式的分组中,部分组别的样本量小而不均衡可能会导致统计误差。
总之,MRI 上的簇环样强化是较大的导管周围基质或TDLU 周围基质的强化,簇环样强化的性质主要由小环和环周组织的动态增强曲线决定,廓清型曲线的簇环样强化对恶性病灶有诊断价值。
