4例COVID-19患者不同类型标本的SARS-CoV-2核酸及抗体检测结果分析
2020-08-04卢婷陈雨欣沈瀚南京大学医学院附属鼓楼医院检验科南京210009
卢婷,陈雨欣,沈瀚(南京大学医学院附属鼓楼医院检验科,南京 210009)
新型冠状病毒(SARS-CoV-2)具有高传染性、高隐匿性和高致病性的特点[1],引发的新型冠状病毒肺炎(COVID-19)主要症状为发热、咳嗽和呼吸困难,重症患者多发展成呼吸窘迫综合征、脓毒症、多功能器官衰竭等[2],早发现、早治疗是控制疫情的关键。临床上主要采用商品化的试剂盒进行核酸检测和血清学抗体检测。实时荧光RT-PCR检测是诊断SARS-CoV-2的确诊方式[2],但是目前核酸检测假阴性率较高,与部分患者临床症状不符,给临床诊治带来困扰。本研究通过留取确诊患者多种样本(包括鼻咽拭子、粪便、尿液、血液)进行病毒核酸检测及病毒血清抗体检测,旨在提高患者病毒检出率,尽快确诊。
1 资料和方法
1.1研究对象 患者1,男,35岁,主诉“咽部不适”,2020年2月3日出现头疼、恶心欲吐,2月4日入本院发热门诊就诊,当日检测咽拭子SARS-CoV-2核酸阳性,2月5日复检咽拭子SARS-CoV-2核酸阳性,结合影像学、临床症状和核酸检测结果确诊为COVID-19,2月5日转入定点医院治疗。
患者2,男,56岁,主诉“咳嗽、发热1 d”,2020年1月30日曾与武汉返宁人员有接触史,2月1日出现咳嗽、发热症状,2月2日入本院发热门诊治疗,温度38.2 ℃,当日检测咽拭子SARS-CoV-2核酸阳性,2月3日复检咽拭子SARS-CoV-2核酸阳性,结合临床表现、接触史及核酸检测结果确诊为COVID-19,2月3日转入定点医院治疗。
患者3,男,27岁,主诉“发热2 d”,2020年1月28日与武汉返宁人员有接触史,1月29日出现发热,2月1日入发热门诊就诊,温度38.0 ℃,当日检测咽拭子SARS-CoV-2核酸阳性,2月2日咽拭子SARS-CoV-2核酸复检阳性,结合临床表现、接触史及核酸检测结果确诊为COVID-19,2月2日转入定点医院治疗。
患者4,女,62岁,主诉“发热5 d”,2020年2月2日入发热门诊就诊,温度38.5 ℃,当日咽拭子SARS-CoV-2核酸检测阳性,2月3日咽拭子SARS-CoV-2核酸复检阳性,结合临床表现、影像学及核酸检测结果确诊为COVID-19, 2月3日转入定点治疗医院治疗。
1.2标本采集 采集咽拭子SARS-CoV-2核酸检测阳性的4名COVID-19患者的不同类型标本,包括鼻拭子、粪便、尿液、血液,所有标本在咽拭子SARS-CoV-2核酸检测阳性后的24 h内采集完毕。咽拭子、鼻拭子、尿液保存在病毒采样管(包含生理盐水和RNA酶抑制剂)内;粪便标本取花生米大小量放入病毒采样管,涡旋震荡2次,每次15 s,2 000 r/min离心5 min;空腹状态下抽取患者5 mL血液保存在有分离胶的采血管内,3 000 r/min离心5 min,分离血清后备用。
1.3仪器与试剂 Cobas LightCycler480实时荧光定量PCR仪(瑞士Roche公司),新型冠状病毒(2019)核酸检测试剂盒和配套核酸提取液(硕世公司),i Flash 3000-H化学发光免疫分析仪以及配套新型冠状病毒免疫球蛋白IgM和IgG抗体化学发光法检测试剂盒(深圳亚辉龙公司)。
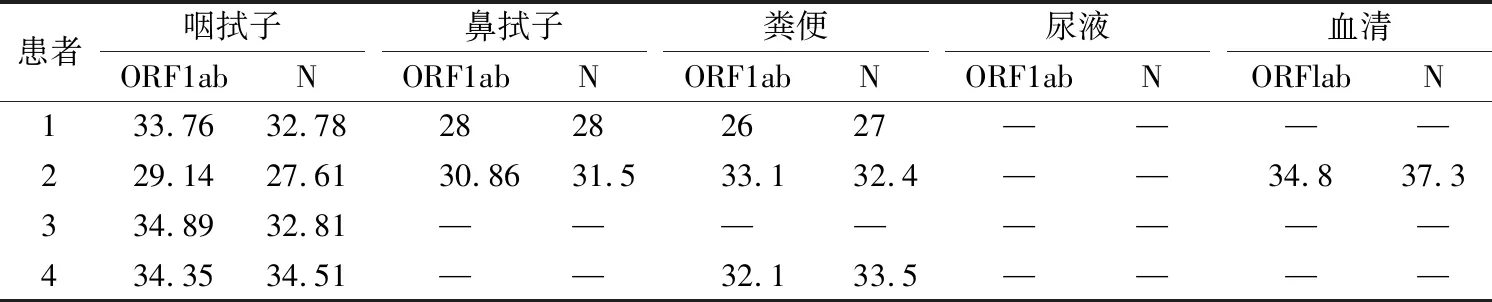
1.4核酸提取和扩增 上述标本采用核酸提取和检测试剂盒进行RNA提取和扩增,按试剂盒说明书进行操作。将反应管放入Cobas LightCycler480实时荧光定量PCR仪扩增,扩增参数:50 ℃逆转录30 min;95 ℃预变性5 min;95 ℃变性10 s,55 ℃ 40 s退火、延伸及检测荧光,45个循环。结果判断:FAM、VIC通道分别对应SARS-CoV-2的ORFlab基因和N基因;阳性:2个通道同时满足待测样本循环阈值(Ct)≤35,扩增曲线呈S型;阴性:2个通道结果Ct>38或未检出;可疑:有一个通道结果Ct≤35,其他一个通道35 1.5化学发光法检测病毒IgM/IgG 定点医院将4名患者血清送本院检测SARS-CoV-2抗体。用i Flash 3000-H化学发光免疫分析仪及配套新型冠状病毒IgM和IgG抗体检测试剂盒检测。结果<10 AU/mL为阴性,≥10 AU/mL为阳性。 2.1不同类型标本SARS-CoV-2核酸检测结果 4名患者中咽拭子全部为阳性,2名鼻拭子阳性,3名粪便标本阳性,尿液标本均未检出病毒,1名血清标本可疑,见表1。 表1 患者不同部位采集标本的核酸Ct值 2.2血清SARS-CoV-2抗体检测结果 患者3在2月4日检测结果为IgM 14.36 AU/mL,IgG 82.29 AU/mL,2月7日检测结果为IgM 61.96 AU/mL,IgG 152.67 AU/mL。其余患者一周内IgM和IgG检测均为阴性。 本文通过4名COVID-19确诊患者的咽拭子、鼻拭子、粪便、尿液、分离血清中的核酸以及血清抗体检测发现:患者的咽拭子检出率最高,其次是粪便、鼻拭子,1名患者血清核酸结果可疑,尿液标本均未检出病毒核酸。本研究中咽拭子检出率最高,粪便标本中病毒同样也有较高的阳性率,说明患者在感染早期肠道内也易携带病毒[3];其他样本类型阳性率不高。可能由于患者处于病程早期,病情较轻,病毒潜伏期长且病毒载量低,核酸检测试剂盒的灵敏度对于低载量病毒的检出率低;不同部位存在的病毒载量有所不同,导致不同部位的标本病毒检出率不同[4]。 在本研究中,患者1粪便标本中病毒载量高于鼻咽拭子,可能该患者的肠道病毒受体多于呼吸道受体,与个体差异有关。患者2的鼻、咽拭子、粪便核酸检测结果均为阳性,分离血清标本也可以检出低载量的病毒,可能与患者男2的病情相对较重,病毒载量高有关,有文献指出血液和肛拭子中病毒的检出与重症出现呈正相关,应注意监测患者病情,警惕患者病情加重[5]。患者3在2月1日咽拭子核酸检测阳性,尿液标本和粪便标本均阴性,2月4日化学发光法定量检测患者血清IgM、IgG阳性,2月7日IgM、IgG进一步升高,说明患者血清中开始出现抗体,抗体的动态检测可以确定患者是否感染及观察治疗效果,可运用于流行病学调查。由于以上患者确诊后转入定点传染病医院进行治疗,我们无法获得更多的血清学抗体动态数据。总之,SARS-CoV-2检测时可以采取多种类型标本联合检测,提高病毒的检出率,对于有临床症状但核酸阴性的患者可以采用血清学抗体检测作为补充,共同提高病毒检测的阳性率,为病情的确诊和疫情的控制提供支持。2 结果
3 讨论
