慢性颈动脉闭塞的血管再通治疗
2020-07-03吴祥波蔡权黄子纯康志明聂创孙冬李华钢刘煜敏梅斌
吴祥波 蔡权 黄子纯 康志明 聂创 孙冬 李华钢 刘煜敏 梅斌
慢性颈动脉闭塞(CCAO)是缺血性卒中的主要 原因之一[1⁃2]。根据文献报道,既往有短暂性脑缺血发作(TIA)或轻型脑卒中病史的慢性颈动脉闭塞患者脑卒中年复发率为5%~6%[3],其中伴脑血流动力学障碍者缺血性卒中复发风险更高,是无血流动力学障碍者的2 ~4 倍[4⁃5]。慢性颈动脉闭塞易引起动脉⁃动脉栓塞事件或慢性脑低灌注(CCH),因此开通慢性闭塞血管、改善脑灌注,理论上可以显著降低缺血性卒中复发之风险、改善患者远期预后。颅内外血管搭桥术可以部分改善脑血流动力学,但颈动脉闭塞外科研究(COSS)结果显示其对缺血性卒中远期预防效果并不理想[6]。近年来,血管再通治疗是慢性颈动脉闭塞研究的热点和难点,尤其是何时开通血管、如何开通血管,以及如何处理围手术期并发症等问题,仍是目前争议的焦点。武汉大学中南医院神经内科对近年在该院施行血管再通治疗的部分慢性颈动脉闭塞患者的临床资料进行回顾分析,拟通过文献复习,总结血管再通治疗的影响因素和围手术期并发症,以期提高临床对慢性颈动脉闭塞血管再通治疗的认识。
对象与方法
一、研究对象
1.纳入标准 (1)CTA 或DSA 提示单侧颈动脉闭塞,包括颈内动脉(ICA)和颈总动脉(CCA)闭塞。(2)存在与责任血管相应的脑缺血症状,经过内科保守治疗缺血症状始终未得到缓解。(3)CTP 或PWI 提示患侧脑组织存在明显低灌注区域。(4)发病至血管再通治疗时间≥2 周。(5)所有患者及其家属均对手术方案和风险知情,并签署知情同意书。
2.排除标准 (1)无症状性颈动脉闭塞。(2)存在抗血小板药物禁忌证。(3)麻醉药或碘剂过敏。(4)存在活动性出血或已知有出血倾向。(5)合并严重心脏、肺、肾脏等疾病。
3.一般资料 选择2018 年8 月至2019 年7 月在武汉大学中南医院神经内科接受血管再通治疗的慢性颈动脉闭塞患者共12 例,男性10 例,女性2 例;年龄28 ~71 岁,中位年龄58 岁;发病至血管再通治疗时间2 ~104 周,中位时间为4 周。既往史包括高血压(8 例)、冠心病(2 例)、糖尿病(2 例)、高脂血症(3 例),以及短暂性脑缺血发作史(2 例)、缺血性卒中病史(6 例)和吸烟(4 例);临床主要表现为侧肢体偏瘫(8 例)、反复短暂性脑缺血发作(2 例)、视野缺损(1 例)或慢性血管性头痛(1 例)。
二、研究方法
1.血管再通治疗 本组因动脉炎(1 例)或动脉夹层(3 例)所致慢性颈动脉闭塞患者均行单纯球囊扩张术,由大动脉粥样硬化(8 例)引起的慢性颈动脉闭塞患者则接受球囊扩张术+支架植入术。患者平卧位,于局部麻醉下以Seldinger 法穿刺股动脉,置入8F 动脉鞘,行全脑血管造影;全身肝素化,在超滑泥鳅导丝引导下将导引导管置于闭塞近端,选择支撑力较强的微导丝(Pilot 150,美国Abbott 公司或Transend 300,美国Boston Scientific 公司)和微导管(Excelsior SL⁃10,美国Stryker 公司或Echelon⁃10,美国Medtronic 公司),旋转微导丝并配合微导管输送,轻柔突破闭塞纤维帽,小心通过闭塞段,经微导管造影确认微导管远端进入血管真腔。在路径图引导下,将微导丝置于闭塞远端,撤出微导管;沿微导丝 将 小 球 囊(2 mm × 20 mm Maverick 球 囊,美 国Boston Scientific 公司或2 mm×9 mm Gateway 球囊,美国Stryker 公司)置入闭塞远端,由远及近依次扩张闭塞段;将栓子保护装置(EV3 保护伞Spider FX,美国Medtronic 公司)沿微导丝输送至颈内动脉C1段远端固定并释放;必要时选择较大球囊(4 mm×30 mm Maverick 球 囊,美国Boston Scientific 公司 或4 mm×20 mm Gateway 球囊,美国Stryker 公司)由远及近再次扩张闭塞段。根据球囊扩张后管径,选择类型和尺寸适宜的支架(Wallstent 颈动脉支架,美国Boston Scientific 公司;RX Acculink 颈动脉支架,美国Abbott 公司;或Xact 颈动脉支架,美国Abbott 公司),准确定位后释放,缓慢回收保护伞和导引导管,即刻复查造影评估支架贴壁和前向血流情况。
2.围手术期处理 术前均常规服用阿司匹林100 mg/d 和氯吡格雷75 mg/d,连续治疗3 ~5 d。术后转入神经重症监护病房监测生命体征24 h,密切观察神经系统症状与体征以及穿刺点情况,同时予下述治疗:据血压情况经静脉泵入不同剂量的乌拉地尔,使收缩压维持在110 ~120 mm Hg(1 mm Hg=0.133 kPa),疗程为2 ~3 d;皮下注射低分子量肝素4000 U/12 h,连续3 d;继续服用阿司匹林100 mg/d和氯吡格雷75 mg/d 双联抗血小板治疗,共治疗3 ~6 个月改为阿司匹林100 mg/d 或氯吡格雷75 mg/d长期维持,若基因检测提示患者对阿司匹林或氯吡格雷治疗不敏感,可更换为替格瑞洛180 mg/d;服用阿托伐他汀10 ~20 mg/d 或瑞舒伐他汀5 ~10 mg/d进行长期调脂治疗。
3.评价指标 (1)术前经多模态影像学[CTA、MRA 或DSA,CTP 或PWI,高分辨率磁共振血管壁成像(HR⁃VWI)]检查观察闭塞部位、闭塞节段、闭塞血管近端残端形态和血管壁病变性质。(2)血管再通:术后即刻行全脑血管造影检查,采用脑梗死溶栓血流分级(TICI)评价血管再通程度,TICI 分级≥2b 级为血管再通成功,≤2a 级血管再通失败。(3)围手术期并发症:记录栓子脱落、血管痉挛、脑高灌注综合征(CHS)、低血压等并发症发生情况。(4)随访:分别采用电话、门诊或住院的方式进行定期随访,记录缺血性卒中复发事件;术后1 和3 个月行颈部血管超声检查,术后6、12 个月行CTA 或DSA 检查,明确再通血管有无再狭窄或闭塞。
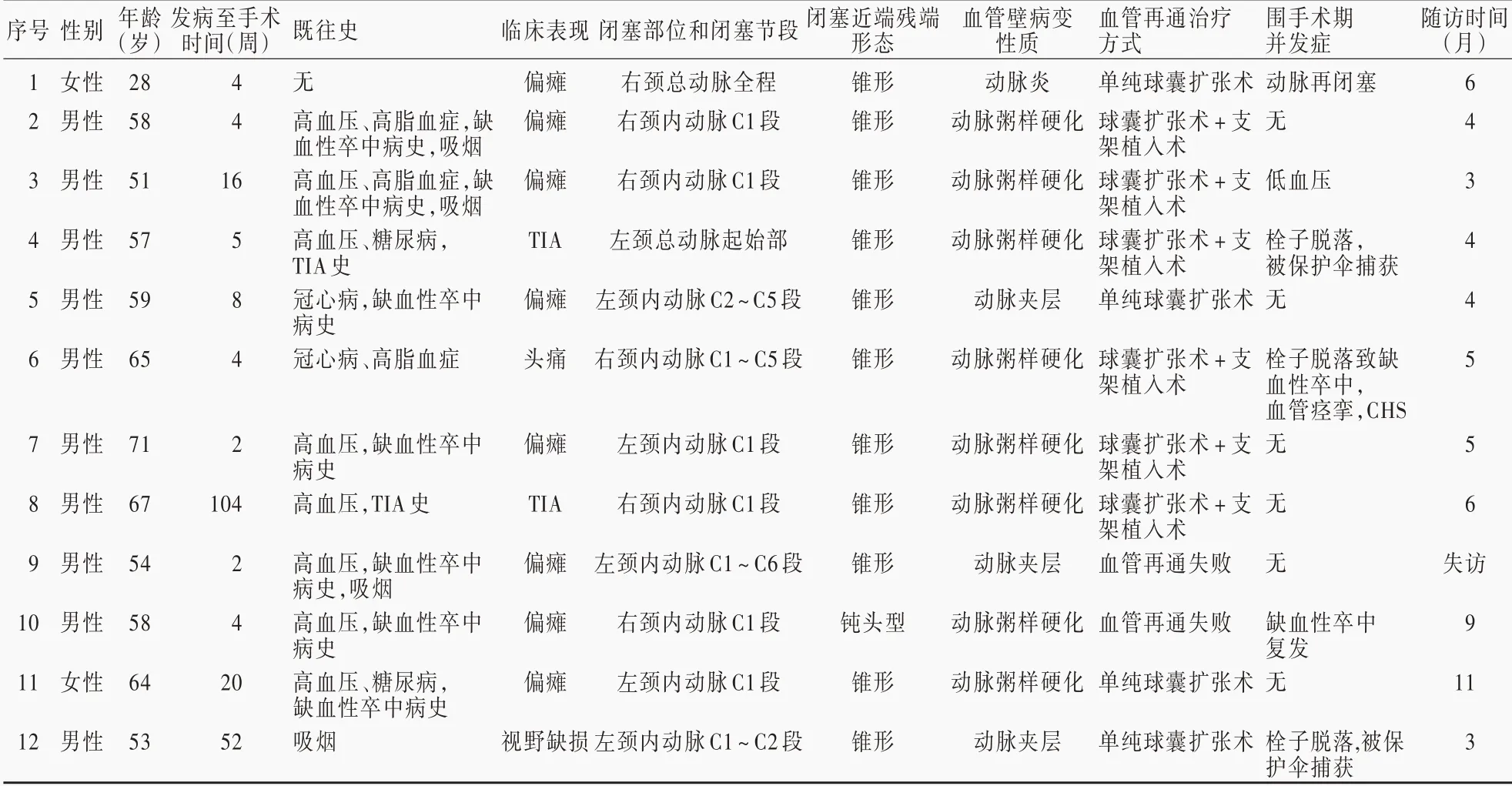
表1 12 例慢性颈动脉闭塞患者的临床资料Table 1. Clinical data of 12 patients with CCAO
结 果
本组12 例患者颈动脉闭塞部位和闭塞节段分别位于右颈总动脉全程(1 例),左颈总动脉起始部(1 例),右颈内动脉C1 段(4 例)和C1 ~C5 段(1 例)以及左颈内动脉C1 段(2 例)、C1 ~C2 段(1 例)、C2 ~C5 段(1 例)和C1 ~C6 段(1 例);闭塞血管近端残端形态为锥形(11 例)或钝头型(1 例);管壁病变性质分别呈现大动脉粥样硬化(8 例)、动脉夹层(3 例)和动脉炎(1 例)。
本组共有10 例患者获得血管再通,再通成功率为10/12,其中4 例行单纯球囊扩张术、6 例行球囊扩张术+支架植入术。其余2 例患者血管再通失败,其中1 例为左颈内动脉C1 ~C6 段闭塞,考虑动脉夹层形成,术中选择3 mm×20 mm 球囊扩张后未能开通血管,放弃手术;1 例闭塞血管近端残端呈钝头型,微导丝经多次尝试仍无法通过纤维帽,遂转至神经外科行颈动脉内膜切除术。12 例患者中6 例出现围手术期并发症,其中3 例术中发生栓子脱落(导致缺血性卒中1 例、脱落的栓子被栓子保护装置捕获2 例);1 例术中发生严重血管痉挛,手术结束撤出微导丝后症状即得到缓解;1 例术后即刻出现严重低血压(80/50 mm Hg),经升压、补液等对症治疗后缓解;1 例术后第2 天出现脑高灌注综合征(头痛、轻度烦躁),复查CT 排除颅内出血后予以乌拉地尔严格控制血压、小剂量甘露醇脱水降低颅内压等治疗,4 d 后症状缓解。
本组患者术后随访仅1 例失访,其余11 例均顺利随访3 ~11 个月(中位时间5 个月)。在血管再通成功的10 例患者中,1 例动脉炎患者术后4 个月发生颈总动脉再闭塞,再次行单纯球囊扩张术;2 例血管再通失败患者中1 例失访,1 例术后9 个月缺血性卒中复发,予内科保守治疗后遗留严重神经功能障碍[改良Rankin 量表(mRS)评分3 分]。
典型病例
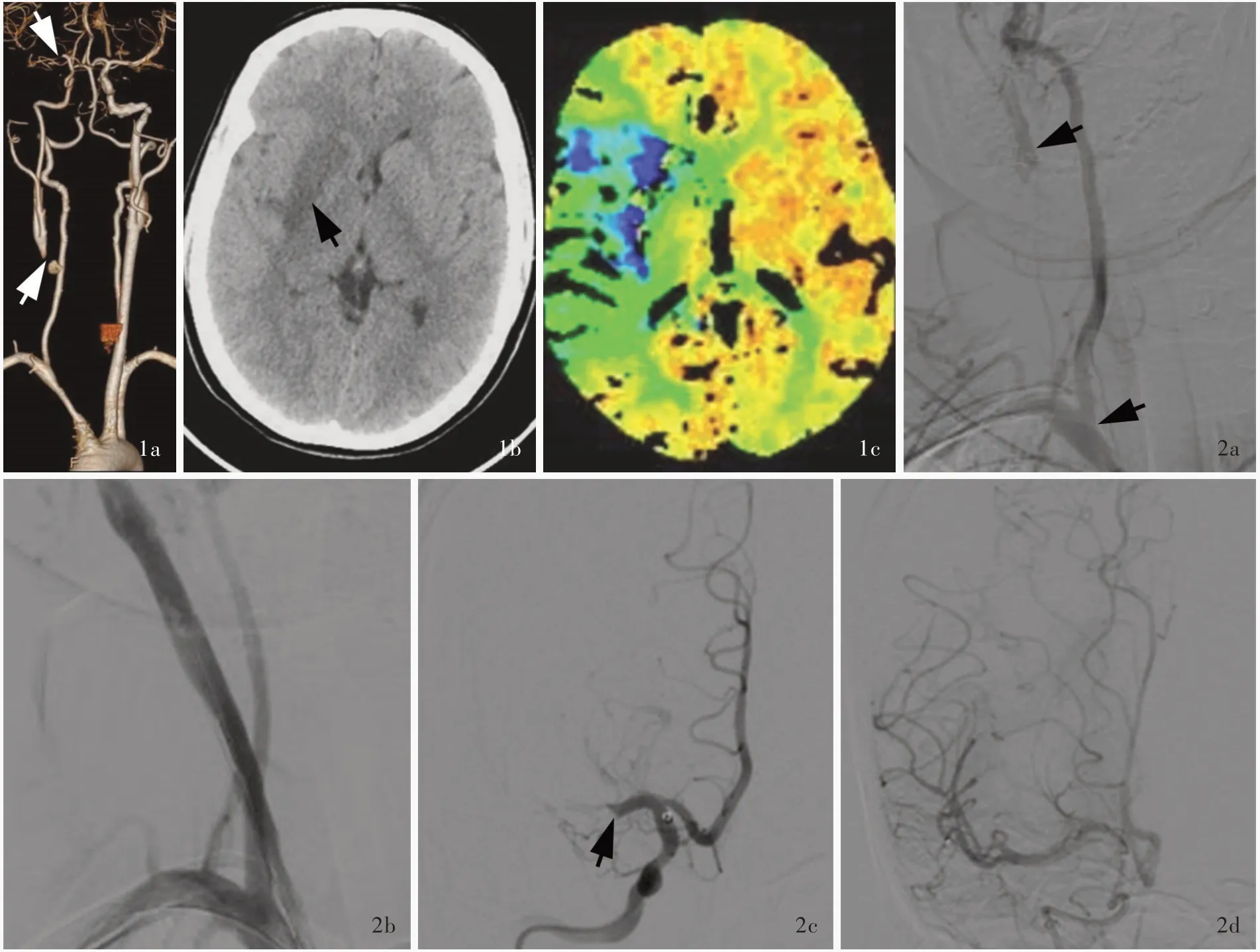
图1 例1 患者首次手术前影像学所见 1a CTA 显示右颈总动脉和大脑中动脉闭塞(箭头所示) 1b 横断面CT 显示右侧基底节区梗死灶(箭头所示) 1c 横断面MTT 图显示右侧大脑半球灌注较对侧降低(绿色区域所示) 图2 例1 患者首次手术中影像学所见 2a DSA 显示右颈总动脉近端呈线样狭窄、远端闭塞(箭头所示) 2b 单纯球囊扩张术开通右颈总动脉,恢复前向血流 2c DSA 显示右大脑中动脉M1 段近端闭塞(箭头所示) 2d Solitaire FR 支架取栓后恢复前向血流,TICI 分级2b 级Figure 1 The first preoperative imaging findings of Case 1 CTA showed the occlusion of the right CCA and MCA (arrows indicate,Panel 1a). Axial CT showed infarction in the right basal ganglia region (arrow indicates, Panel 1b). Axial MTT showed decreased perfusion in the right cerebral hemisphere (green areas indicate, Panel 1c). Figure 2 Intraoperative imaging findings of Case 1 DSA showed the proximal severe stenosis and distal occlusion of the right CCA (arrows indicate, Panel 2a). Balloon dilatation successfully opened the occlusion of the right CCA and restored the forward blood flow (Panel 2b). DSA showed the occlusion of the proximal M1 segment of the right MCA (arrow indicates, Panel 2c). After mechanical thrombectomy with Solitaire FR stent, the forward blood flow was restored, and the TICI grade was 2b (Panel 2d).
患者(例1) 女性,28 岁。因发作性左侧肢体无力2 天,于2019 年4 月4 日首次入院。入院前2 天在工作中突发左侧肢体无力,言语不清,伴头晕、恶心呕吐,休息片刻后缓解,入院前1 天再次出现左侧肢体无力,无法抬举,并伴言语不清、口角偏斜,症状呈进行性加重,当地医院头部CT 检查排除颅内出血后转入我院。患者入院前1 个月反复出现头晕,未予重视。入院后体格检查:嗜睡,反应迟钝,构音障碍,左侧鼻唇沟浅,口角向右歪斜,伸舌左偏,左侧肢体肌力0 级、肌张力降低,感觉与共济运动不配合,左侧病理征阳性。美国国立卫生研究院卒中量表(NIHSS)评分12 分。CTA 显示,无名动脉中度狭窄,右侧颈总动脉和大脑中动脉闭塞(图1a)。CT 可见右侧基底节区梗死灶(图1b);CTP 显示,右侧大脑半球灌注降低[平均通过时间(MTT)延长],梗死核心19ml、缺血半暗带153 ml(图1c)。急诊行右侧颈总动脉血管成形术+右侧大脑中动脉机械取栓术(图2a ~2d)。术后组织形态学观察栓子为红色血栓(图3)。术后恢复良好,共住院2 周,出院时NIHSS 评分6 分。术后7 周(2019 年5 月24 日)复查NIHSS 评 分3 分、mRS 评 分2 分;DSA 显 示,无 名 动脉、右侧颈总动脉轻度狭窄(图4a)。术后4 个月因头晕、耳鸣伴听力下降2 周,于2019 年8 月5 日再次入院。CTA 显示,无名动脉、右侧颈总动脉闭塞(图4b)。MRI 可见右侧基底节区陈旧性梗死灶(图4c);PWI 显示,右侧基底节区和颞叶灌注降低(MTT延长,图4d)。增强HR⁃VWI 显示,右颈总动脉闭塞、颈内动脉C1 ~C7 段中度狭窄伴炎症性改变(图4e)。2019 年8 月15 日施行无名动脉+右侧颈总动脉血管再通术。术中脑血管造影可见无名动脉重度狭窄,右颈总动脉呈线样狭窄,远端经同侧椎动脉和后交通动脉代偿(图4f)。以2 mm × 9 mm Gateway 球囊由远及近依次扩张闭塞段,术后即刻复查全脑血管造影,再通良好,残留狭窄率约为20%,TICI 分级3 级(图4g)。术后予以阿司匹林100 mg/d 和氯吡格雷75 mg/d 抗血小板治疗、泼尼松(初始剂量30 mg/d,连续3 ~4 周后逐渐减量,每2 周减5 mg,直至5 ~10 mg/d,维持1 ~2 年)抗炎症治疗,以及环磷酰胺600 mg/2 周免疫抑制治疗。患者共住院2 周,出院后随访至术后2 个月,头晕、耳鸣症状改善,mRS 评分2 分。
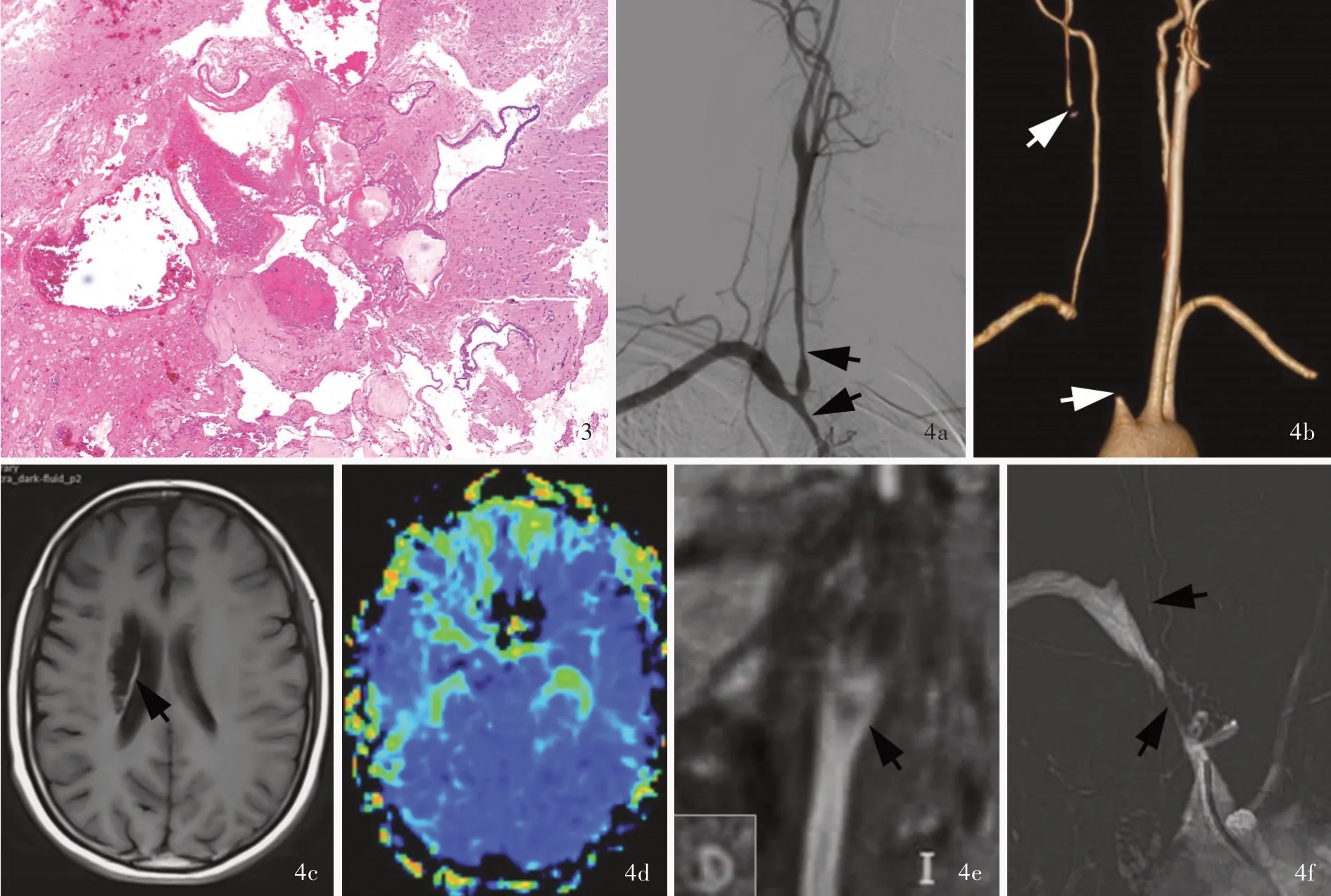
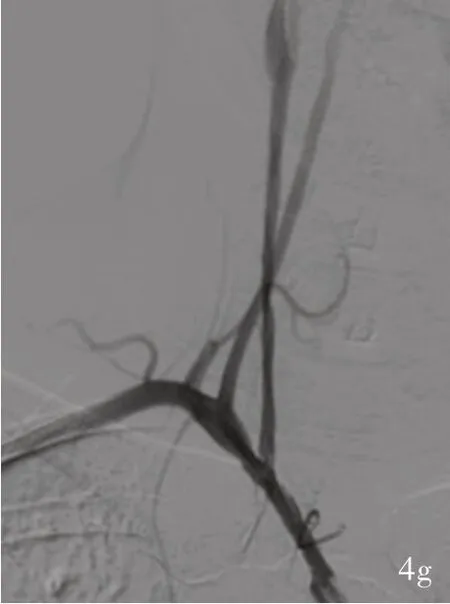
图3 例1 患者首次手术后组织学形态观察,栓子为红色血栓 HE 染色 ×20 图4 例1 患者二次手术前后影像学检查所见 4a 首次手术后7 周随访,DSA 显示无名动脉、右颈总动脉轻度狭窄(箭头所示) 4b 二次手术前CTA 显示无名动脉、右颈总动脉闭塞(箭头所示) 4c 二次手术前横断面T1WI 显示右侧基底节区陈旧性梗死灶(箭头所示) 4d 二次手术前横断面MTT图显示右侧基底节区和颞叶灌注降低(绿色区域所示) 4e 二次手术前矢状位增强HR⁃VWI 显示右颈总动脉管壁呈明显环形强化(箭头所示) 4f 术中DSA 显示,头臂干重度狭窄,右颈总动脉线样狭窄(箭头所示) 4g 单纯球囊扩张术开通无名动脉和右颈总动脉,前向血流恢复Figure 3 The first postoperative histologic appearance of Case 1 suggested that the embolus was a red thrombus. HE staining × 20 Figure 4 Image findings of Case 1 before and after the second operation Seven weeks after the first operation, DSA showed slight stenosis of the innominate artery and the right CCA (arrows indicate, Panel 4a). The second preoperative CTA showed occlusion of the innominate artery and the right CCA (arrows indicate, Panel 4b). The second preoperative axial T1WI showed an old infarct at the right basal ganglia region (arrow indicates, Panel 4c). The second preoperative axial MTT showed decreased perfusion in the right basal ganglia region and temporal lobe (green areas indicate, Panel 4d). The second preoperative sagittal enhanced HR⁃VWI showed the obvious annular enhancement of the vessel wall of the right CCA (arrow indicates, Panel 4e). Intraoperative DSA showed severe stenosis of the innominate artery and right CCA (arrows indicate,Panel 4f). Balloon dilatation was performed again to open the occluded vessels and restore the forward blood flow (Panel 4g).
患者(例3) 男性,51 岁。因头晕伴左侧肢体无力4 个月,于2019 年7 月1 日入院。患者4 个月前无明显诱因突发头晕,左侧肢体无力、抬举困难、无法行走,当地医院诊断为右侧基底节区缺血性卒中、右侧颈内动脉起始部闭塞,经内科保守治疗效果欠佳,转入我院。既往有高血压病史1 年,规律服用氨氯地平5 mg/d,血压控制尚可。入院后体格检查:血压140/80 mm Hg,语言流利,左上肢近端肌力3+级、远端2 级,左下肢近端肌力4 级、远端3 级,肌张力均正常,左侧病理反射未引出。头部MRI 可见右侧基底节区和侧脑室旁陈旧性梗死灶(图5a);MRA 显示右颈内动脉C1 段近端呈“鼠尾”样改变(图5b);PWI 检查右侧基底节、侧脑室旁,以及部分岛叶、额叶和枕叶灌注较对侧明显降低[脑血流量(CBF)减少,MTT 延长;图5c,5d]。HR⁃VWI 显示,血管腔呈混杂高信号,增强后管腔明显强化;C2 段水平段可见管腔断续显影伴腔内环形增厚、狭窄,增强扫描狭窄段血管腔呈明显不均匀强化(图5e)。遂于2019 年7 月9 日行右颈内动脉血管再通术。术中脑血管造影显示,右颈内动脉起始部锥形残端(图6a),闭塞远端开放,经同侧颈外动脉代偿,后交通动脉开放。以2 mm×20 mm Maverick 球囊由远及近扩张闭塞段,将EV3 保护伞Spider FX 栓子保护装置(4 mm)输送至右颈内动脉C4 段固定并释放,再以4 mm×30 mm Maverick 球囊再次扩张狭窄血管,最后于右颈内动脉起始部植入1 枚8 ~6 mm×40 mm Xact 颈动脉支架(图6b ~6e)。术后即刻全脑血管造影显示,支架贴壁良好,TICI 分级3 级(图7)。术后出现严重低血压,最低约80/50 mm Hg,以平衡盐溶液1000 ml/d 补液、多巴胺5 μg/(kg·min)静脉泵入(药物剂量根据血压剂量)升压治疗,2 天后血压趋于稳定。患者共住院2 周,出院后随访至术后3 个月,未再发生缺血性卒中,复查颈动脉超声显示支架贴壁良好,血流通畅。
讨 论
症状性慢性颈动脉闭塞具有较高的缺血性卒中复发风险[4],并可能伴发血管性认知损害(VCI)[7]等病变,目前国内外尚无统一的治疗规范。抗血小板治疗是缺血性脑血管病二级预防的基础,氯吡格雷联合阿司匹林减少症状性颈动脉狭窄栓子研究(CARESS)显示,症状性颈动脉狭窄患者予以双联抗血小板治疗可以降低发病后90 天无症状性缺血性卒中发生率[8],而长期疗效则随着发病时间的延长而逐渐降低[9],且出血风险增加[10]。颈部血管病变的手术方法主要包括颅内外血管搭桥术、颈动脉内膜切除术(CEA)和颈动脉支架成形术(CAS)。颅内外血管搭桥术是改善脑灌注的直接方法,可以有效降低脑卒中复发风险[11],但2011 年发表的多中心、前瞻性、随机对照临床试验——COSS 研究证实其疗效并不优于单纯药物治疗[6]。颈动脉内膜切除术对颅外局限性血管闭塞有较好的疗效;而对于累及岩骨段以上的长节段病变,颈动脉支架成形术则可能是唯一治疗方法。然而,无论是颈动脉内膜切除术还是颈动脉支架成形术均存在手术难度较大、术中不可预知因素较多和术后并发症发生率较高的问题。
能否开通闭塞血管是神经介入医师进行治疗决策时所面临的首要问题。在本研究纳入的12 例患者中,2 例血管再通失败,其中1 例为闭塞近端残端呈钝头型,另1 例为累及岩骨段以上的长节段动脉夹层。2018 年,Hasan 等[12]提出了慢性颈 内 动 脉闭塞(COICA)新的脑血管它造影分型方法:A 型,颈内动脉近端为锥形残端、远端管腔开放;B 型,颈内动脉近端呈钝头型残端、远端管腔开放;C 型,颈内动脉近端无残端、远端管腔开放;D 型,颈内动脉无残端,远端管腔闭塞至颈内动脉分叉部。按照新的造影分型方法,Hasan 等[12]对32 例慢性颈内动脉闭塞患者施行了闭塞血管的再通治疗,其结果显示:总体血管再通成功率为68.75%(22/32),其中A 型8/8、B 型8/8、C 型4/8、D 型2/8;围手术期并发症发生率为6/32,A 型0/8、B 型1/8、C 型3/8、D 型2/8;因此该作者认为闭塞近端无残端、远端管腔未开放的患者,血管再通成功率较低、围手术期并发症发生风险较高、远期疗效欠佳,其结论是此类患者血管再通治疗获益十分有限。对于单纯血管内介入治疗开通困难的患者,充分评估手术风险与获益后,可以在有条件的医疗中心进行复合手术。目前,采用复合手术治疗慢性颈动脉闭塞尚处于探索阶段,近年陆续有文献资料报道慢性颈动脉闭塞患者经复合手术成功开通、临床获益的病例[13⁃14]。
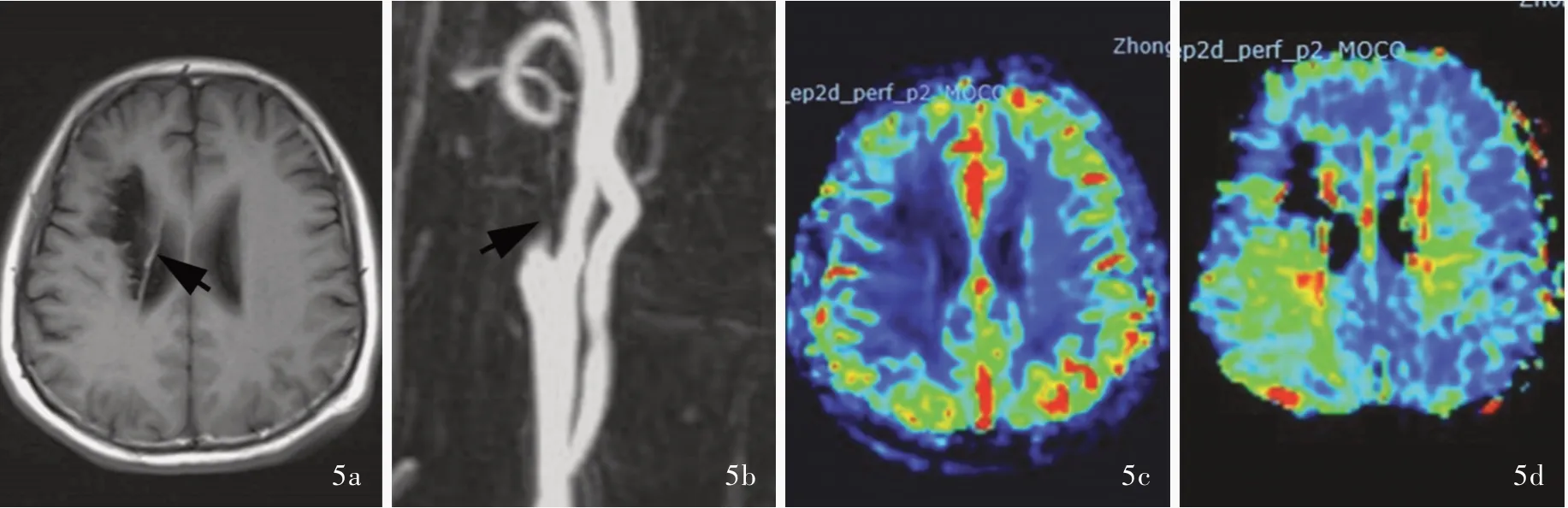
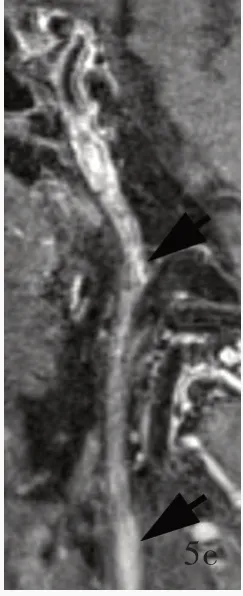
图5 例3 患者手术前影像学检查所见 5a 横断面T1WI 显示右侧基底节区陈旧性梗死灶(箭头所示)5b MRA 显示右颈内动脉C1 段残端呈“鼠尾”样改变(箭头所示) 5c 横断面CBF 图显示,右侧基底节、侧脑室旁软化灶区无灌注,右侧部分岛叶、额叶和枕叶灌注降低(蓝色区域所示) 5d 横断面MTT 图显示,右侧基底节、侧脑室旁软化灶区无灌注,右侧部分岛叶、额叶和枕叶灌注降低(绿色区域所示) 5e 矢状位增强HR⁃VWI 显示,右颈内动脉C1 段混杂高信号,狭窄段血管明显强化(箭头所示)Figure 5 Preoperative imaging findings of Case 3 Axial T1WI showed an old infarct in the right basal ganglia region (arrow indicates, Panel 5a). MRA showed a "rat tail" shape at the stump of C1 segment of the right ICA (arrow indicates, Panel 5b). CBF map showed reduced perfusion in the right basal ganglia region,the lateral ventricles, and part of the insula, frontal and occipital lobes (blue areas indicate, Panel 5c). The MTT map showed reduced perfusion in the right basal ganglia region, the lateral ventricles, and part of the insula, frontal and occipital lobes (green areas indicate, Panel 5d). Sagittal enhanced HR⁃VWI showed C1 segment of the right ICA was mixed with high signals, and obvious enhancement (arrows indicate, Panel 5e).
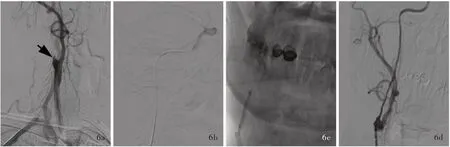
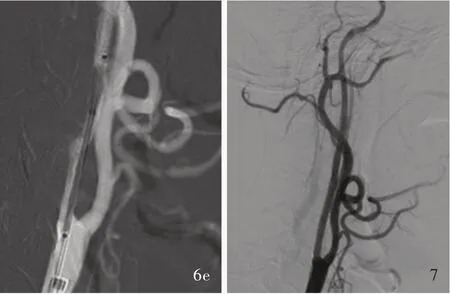
图6 例3 患者手术中影像学检查所见 6a DSA 显示右颈内动脉C1 段近端闭塞,残端呈锥形(箭头所示) 6b微导管配合微导丝小心通过闭塞段,进入血管真腔 6c,6d Maverick 球囊由远及近扩张闭塞段,开通右颈内动脉 6e 于右颈内动脉起始部植入1 枚8 ~6 mm×40 mm Xact 颈动脉支架 图7 例3 患者手术后即刻复查DSA 显示,支架贴壁良好,前向血流通畅,TICI 分级3 级Figure 6 Intraoperative imaging findings of Case 3 DSA showed that the proximal C1 segment of the right ICA was occluded, with tapered stump (arrow indicates, Panel 6a).The microcatheter was carefully passed through the occluded segment with the microfilament and located in true cavity (Panel 6b). Maverick balloon successfully opened the occlusion of the right ICA distally to proximally by dilating the occluded vessels (Panel 6c, 6d). An 8-6 mm × 40 mm Xact carotid stent was implanted at the proximal C1 segment of the right ICA (Panel 6e). Figure 7 Immediately postoperative DSA of Case 3 showed the stent was well adherent to the wall and the forward blood flow was unobstructed. TICI grade was 3.
术中栓子脱落致缺血性卒中是血管再通治疗无法回避的难题。本研究有3 例患者于术中发生栓子脱落,其中1 例诱发缺血性卒中事件,2 例脱落的栓子被栓子保护装置捕获而避免了缺血性卒中事件的发生。De Martino 等[15]认为,术前对患者进行规范的抗血小板治疗和他汀类药物调脂治疗,可有效降低围手术期缺血性卒中的风险和发病后30 天病死率;术中应用栓子保护装置亦可降低颈动脉支架成形术围手术期缺血性卒中发生率[16],因此对于医疗条件较好的医疗中心,应推荐血管再通术中常规应用栓子保护装置[17]。支架对管壁的压力可造成粥样硬化斑块破裂以及动脉内膜和内膜下损伤,从而诱发血小板聚集和急性血栓形成[18],鉴于此,对于长节段闭塞的患者,尤其是术中应用支架较多或术后即刻复查全脑血管造影显示血管壁欠光滑的患者,建议术后静脉应用替罗非班1 ~2 天[19]。此外,如果术中发生远端大血管栓塞事件,及时施行机械取栓术可能是一种有效的补救措施。
脑高灌注综合征和低血压是血管再通治疗的重要围手术期并发症。脑高灌注综合征是颈动脉支架成形术后原低灌注区脑血流量显著增加并超出脑组织代谢需求而引起的严重并发症,发生率为0.44%~1.70%,其危险因素包括术后血压不稳定、短期内发生过患侧缺血性卒中病史、对侧动脉狭窄>70%和冠状动脉病变等[20];患者主要表现为意识障碍和头痛,严重时可导致脑出血、癫发作甚至死亡。血管再通治疗后出现的血压降低可能通过以下机制发挥作用:(1)闭塞血管再通有效改善脑灌注,无需机体自身调节代偿机制维持脑灌注压(CPP)[12]。(2)颈动脉支架对管壁的径向支撑力使颈动脉窦压力感受器承受持续的机械性压力,压力感受器处于持续兴奋、无疲劳状态[21]。(3)颈动脉成形术使管腔直径增大、管壁顺应性增加,导致颈动脉窦压力感受器的敏感性增强[22]。因此,血管再通治疗应重视围手术期血压波动,包括术中开通血管前,需维持血压不低于术前之基础值;术后若不合并其他脑血管重度狭窄,可将血压降至术前基础值的20%或收缩压<120 mm Hg[19]。
血管痉挛也是血管再通治疗的常见围手术期并发症,可能与微导管或微导丝对脑血管的机械刺激有关,若血管痉挛时间较长即可导致缺血性卒中事件。Ishihara 等[23]发现,诊断性脑血管造影期间发生血管痉挛、手术入路血管弯曲度(>30°)和焦虑是脑血管再通治疗后发生血管痉挛的危险因素。术前2 小时静脉微量泵入尼莫地平可在一定程度上预防血管痉挛。术中轻柔操作微导管和微导丝,尽量不要进入血管过深,栓子保护装置位置不可过高或进入颅内,避免其来回移动,亦具有一定的预防血管痉挛作用。一旦发生脑血管痉挛,及时回撤微导管和微导丝,通常可迅速缓解症状,必要时可予以扩血管药物或行球囊扩张术。血管再通治疗的其他并发症还包括动脉夹层、动脉穿孔或血管壁撕裂、动脉再狭窄、支架塌陷、支架移位等,但发生率相对较低。
规范的术前评估对血管再通治疗具有重要指导意义。目前有多种方法,如颈动脉超声、CTA、MRA、DSA、CTP、PWI、HR⁃VWI 等,不同的影像学检查方法各具优势和局限性。其中,HR⁃VWI 在评估血管壁病变性质和程度方面具有独特的优势,可以获得闭塞部位、闭塞节段、闭塞段是否存在潜在真腔、血管壁病变性质(动脉粥样硬化、动脉夹层或动脉炎)等信息。本研究结果显示,慢性颈动脉闭塞的血管壁病变性质可以影响血管再通的成功率,动脉夹层致慢性颈动脉闭塞患者血管再通成功率较低,而动脉炎患者术后缺血性卒中复发率较高。因此,通过多模态影像学评估血管内血栓特征、血管壁病变性质、脑灌注状态等,对严格掌握手术适应证、指导治疗具有重要价值。
综上所述,累及岩骨段以上的长节段闭塞、闭塞近端残端形态和血管壁病变性质均可影响慢性颈动脉闭塞患者血管再通成功率,栓子脱落、脑血管痉挛、脑高灌注综合征和低血压是主要的围手术期并发症。术前多模态影像学评估有助于筛选手术病例、指导术中决策和预防围手术期并发症。由于本研究样本量较小,期待未来开展前瞻性大样本随机对照临床试验,以指导临床决策。
利益冲突无