肝脏遗传性出血性毛细血管扩张症影像学表现
2020-06-23冯汝静马隆佰毛一朴周和秀
冯汝静,马隆佰,毛一朴,周和秀
遗传性出血性毛细血管扩张症(heredittary hemorrhagic telangiectasia,HHT)又名Rendu-Osler-Weber综合征,是一种以毛细血管扩张及动静脉畸形为病理基础,累及粘膜、皮肤及多发器官的常染色体显性遗传性疾病,发病率约1/1万~1/5000,8%~31%的患者可累及肝脏[1-5]。肝脏遗传性出血性毛细血管扩张症通常无症状,但可有高输出型心衰、肝功能衰竭、门脉高压等严重并发症[6],因此,对其准确诊断对临床具有重要的意义。MSCT、MR等影像检查作为临床常用的检查,是诊断肝脏HHT的重要手段。因此,本研究通过结合文献回顾性分析11例肝脏HHT患者的临床和影像资料,旨在提高对肝脏HHT的影像诊断水平。
材料与方法
1.临床资料
回顾分析2012年4月-2018年10月经临床诊断的11例HHT患者资料,其中男4例,女7例,年龄14~88岁,平均年龄(50.5±18.2)岁。临床表现及就诊原因主要包括鼻出血及皮肤毛细血管扩张、功能性腹痛、腹胀、消化不良、便秘、腹股沟疝等,其中1例超声心动图发现左心扩大及门脉高压。
2.诊断标准
参照2000年国际HHT基金科学顾问委员会制定的临床标准(也称Curaco诊断标准)[7]。①鼻出血:表现为自发性、反复发生鼻出血;②皮肤黏膜毛细血管扩张:如嘴唇、舌头、手指、鼻部等处的多发毛细血管扩张;③内脏受累:肺动静脉瘘、肝动静脉分流、脑动脉畸形、脊髓动静脉畸形和伴或不伴有胃肠道出血的胃肠道毛细血管扩张;④家族史:根据上述诊断,直系亲属中至少有一位诊断HHT。符合上述4项中3项或以上即可为确诊病例。
3.检查方法
CT扫描:采用Siemens sensation 64层螺旋CT扫描仪或Philips Brilliance 256 CT扫描仪,管电压120 kV,管电流200~300 mAs,螺距1.4/0.993,准直64×0.6 mm/128×0.625 mm,扫描层厚1 mm,层间隔0.8 mm。患者均为仰卧位。腹部扫描范围为膈顶至髂前上棘,胸部扫描范围为胸腔入口到肺下界膈面。增强扫描用70~80 mL非离子对比剂(优维显,300 mg I/mL)经肘静脉注射,注射流率为3.0 mL/s,开始注射后35 s、60 s及120 s分别行动脉期、门脉期及平衡期扫描。薄层图像传至Philips EBW(Extended Brilliance Workspace)及Siemens SyngoMMWP(Syngo MultiModality Workplace)工作站上行多平面重组(multiplannar reconstruction,MPR)、最大密度投影(maximum intensity projection,MIP)。
MRI扫描:采用Siemens Avanto 1.5T及Siemens Skyria 3.0T,线控阵体部线圈。一次性屏气成像完成肝脏扫描,自旋回波序列T1加权成像(T1WI:TR 520 ms,TE 15 ms)及快速自旋回波序列T2加权成像(T2WI:TR 3500 ms,TE 93 ms)。采用3D T1-VIBE(volumetric interpolated breath-hold examination)序列进行动态增强扫描,15 mL钆对比剂(马根维显,0.1 mg/mL)经肘静脉推注,注射流率为2.0 mL/s,注射对比剂后15 s开始动脉期扫描, 每隔8 s扫描一次,扫描3次后,嘱患者换气15 s,再进行门脉期扫描,扫描方式同动脉期,注射对比剂120 s后行延迟期扫描。
结 果
1.平扫表现
11例患者的CT平扫图像上,1例病例有数目<3个的囊性病灶并胆管轻度扩张,1例病例有数目大致10个左右的大小不等的囊性病灶(图1),其余病例肝实质为等密度。1例病例有类肝硬化表现即各叶比例失常、肝裂增宽、肝缘欠光整(图2a),其余病例肝脏外形正常。2例磁共振病例肝实质T1WI信号均为等信号,T2WI见斑片云雾状稍高信号(图2b)。
2.增强表现
肝脏异常灌注:11例患者10例出现雪花样或棉絮样异常灌注,表现为动脉期、门脉期图像上散在小斑点、小结节强化(图2c、d)或弥漫性斑片状、片状强化。
肝脏血管畸形:①肝动脉畸形4例,表现为动脉期图像上肝总动脉、肝固有动脉、左右肝动脉及分支增粗、迂曲,左肝动脉相对更为明显,管径达0.5 cm以上(图3);②肝动脉-静脉瘘2例,表现为肝动脉增粗、迂曲,肝静脉于动脉期早显,肝静脉分支增粗,动脉与静脉直接相通(图4a、b);③肝动脉-门脉瘘2例,肝动脉增粗、迂曲,门脉于动脉期早显,动脉脉分支与门脉直接相通(图1c);④肝门脉-静脉瘘1例,表现为肝门脉分支与肝静脉分支直接相通,相应的血管分支增粗。
11例病例肝脏HHT CT增强表现具体如表1。
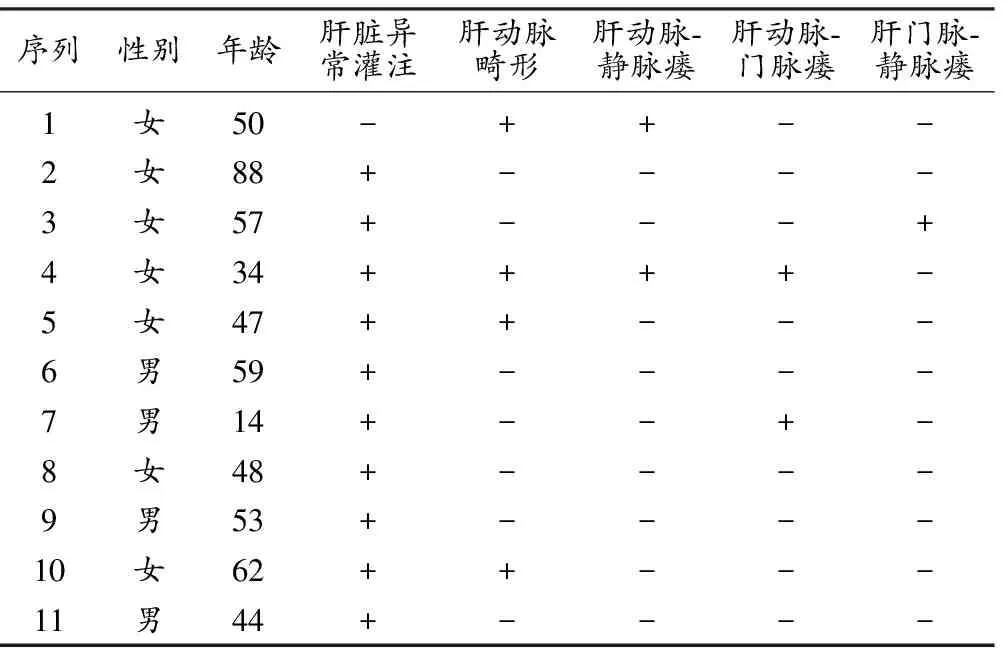
表1 11例肝脏HHT CT增强影像表现
3.肝外病变CT表现
4例病例同时肺部CT检查发现肺内动静脉畸形(arteriovenous malformation,AVM)病灶,均表现为单支肺动脉与肺静脉相通(图5、6)。2例单发,分别发生于右肺中叶内侧段、左肺下叶后基底段;2例多发,均为两个病灶,1例发生在左肺下叶背段和右肺中叶内侧,1例发生在右肺上叶尖后段和左肺上叶前段。
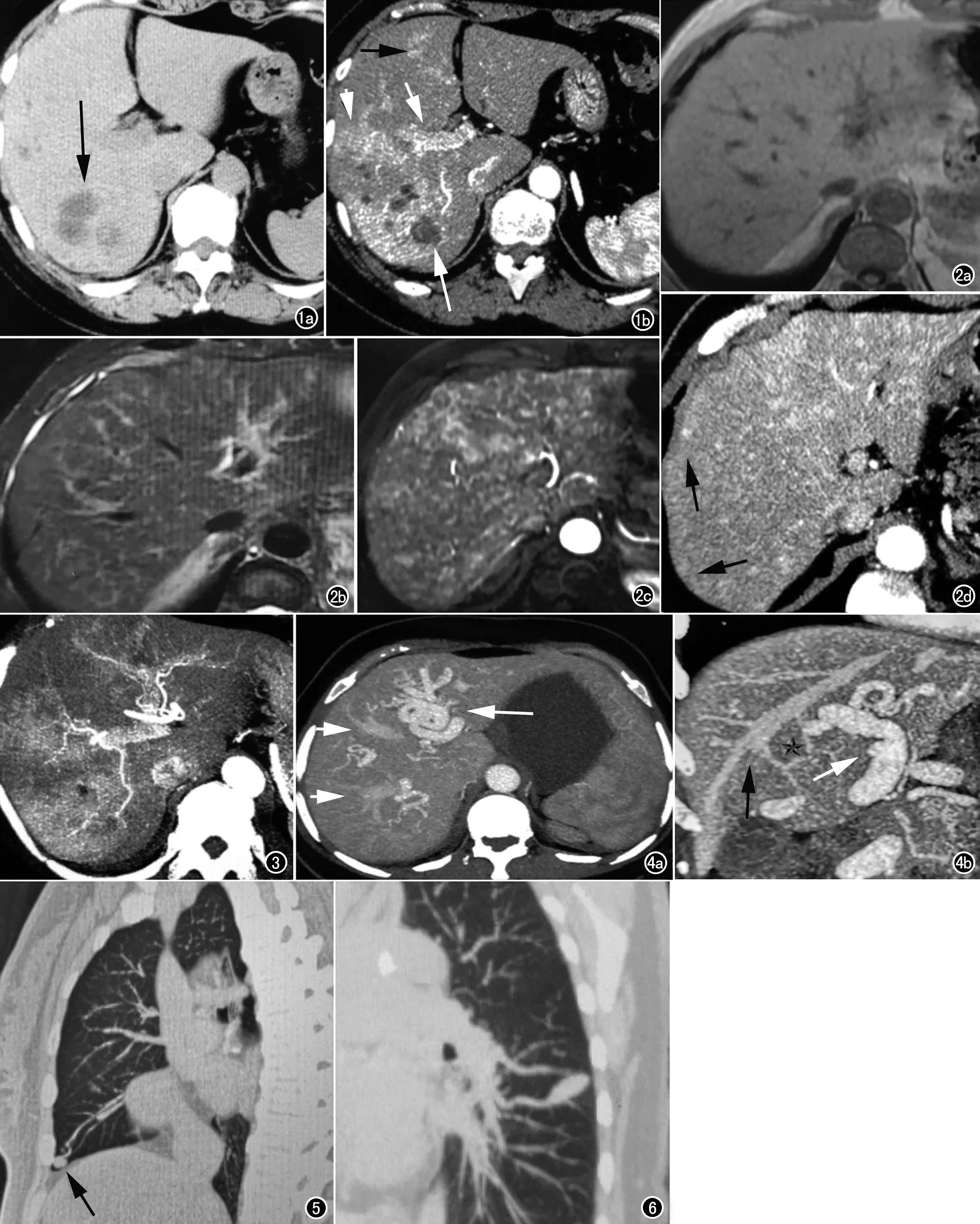
图1 a)CT平扫图像,除了囊性病灶(箭)外其余实质为等密度;b)CT动脉图像显示无强化的囊性病灶(箭)、门静脉(短箭)早显、斑片状及片状(箭头)异常灌注。 图2 a)T1WI图像示肝实质为等信号,肝缘不光整; b)T2WI图像部分病灶呈斑片状稍高信号(箭);c)T1WI增强动脉期图像,病灶呈小斑点、小结节强化;d)CT动脉期图像,肝实质内弥漫多发结节样强化。 图3 CT动脉期MIP图像,显示肝动脉及其分支增粗、门静脉早显、血管周围斑片状、片状异常灌注。 图4 a)轴面MIP图像示肝动脉增粗(箭)及肝动脉-静脉瘘(短箭); b)冠状面MIP图像示肝动脉(箭)-肝右静脉(黑箭)瘘。 图5 肺部CT平扫MIP图像示中叶单一型AVM。 图6 肺部CT平扫MIP图像示左肺下叶背段单一型AVM。
讨 论
遗传性出血性毛细血管扩张症的病理生理机制主要是HHT基因突变引起的血管生成调节异常,目前发现的突变基因有5种,最常见的是ENG(HHT1型)和ALK-1(HHT2型)。肝脏受累的遗传出血性毛细血管扩张症中HHT2型更为常见[1-3,6]。遗传性出血性毛细血管扩张症的临床表现和预后差异很大,这取决于毛细血管扩张的数量、类型和位置。鼻出血是HHT最常见的临床症状,经常容易被忽视。而大部分肝脏HHT是无症状的,仅有8%的肝脏HHT患者可出现轻微症状[3,5-6]。随着腹部CT、MR检查及不断增加,偶然发现的肝脏遗传性出血性毛细血管扩张症病例也在增加。在回顾性研究中,肝脏受累的HHT发生率估计为HHT的8%至31%,但在一项大型前瞻性研究中,这一比例更高,在41%~78%之间[8-9]。肝脏HHT常存在多种血管异常分流,随着病程的进展可引起高输出型心衰、肝功能衰竭、门脉高压、胆道坏死等严重并发症,这些肝脏血管异常相关的并发症以及死亡的发生频率是3.6和1.1每100个人年数[6,10]。本组病例中有1例出现左心扩大的心衰表现。因此,提高对肝脏HH影像表现的认识,可以提高临床对HHT的诊断率,及早监测、及早处理,可以防止严重并发症的发生。
肝脏HHT病变主要是血管不同程度的扩张,可以从小的毛细血管扩张发展到大的动静脉畸形,通常伴随肝内异常分流,主要有肝动脉-门静脉分流,肝动脉-肝静脉分流、门静脉-肝静脉分流3种类型。CT平扫图像上肝脏HHT通常无异常表现,多期增强扫描可因肝脏血管扩张程度不同而出现不同的影像表现。小的毛细血管扩张可以是局灶性或弥漫性,主要表现为肝脏的灌注不均。小的局灶性病灶表现为仅在动脉期小结节状、小斑片状强化,边界模糊,直径一般为数毫米,较大的局灶性病灶(直径在10mm以上)则在动脉期及肝实质期均呈相对略高密度的强化,有文献称大病灶门脉期显示更清晰[11]。弥漫性病变则表现为弥漫斑片状、片状动脉期异常强化,分布主要沿门脉或肝静脉分布,通常在肝实质期上呈等密度,病灶范围不同而表现为雪花样、棉絮样或地图样灌注。动静脉畸形及其三种肝内异常分流在CT增强图像上表现更为清晰、直接,即肝动脉、门静脉、肝静脉的增粗、走行迂曲,血管与血管之间相通沟通形成瘘。肝动脉-门脉瘘常伴随肝动脉-静脉瘘出现,门脉-静脉瘘比较少且多在静脉期显示[5,12]。本组病例的CT表现与文献[11-14]报道基本一致。阮志兵等[12]搜集的病例中以大血管畸形为主,故其认为肝动脉扩张、纡曲是诊断肝脏HHT最可靠的标志。本组病例有5例主要表现为肝脏的异常灌注,大血管畸形表现不明显,与文献报道不符,考虑为该5例病例主要受累的是肝内毛细血管所致,有待更大样本的进一步分析。
MR具有更高的软组织分辨率,因此能更为准确的显示肝脏HHT肝实质的异常。Milot等[15]认为肝脏HHT在MR图像上肝实质异常表现有3种不同的类型:毛细血管扩张、灌注障碍和结节性增生(NH)。毛细血管扩张是指毛细血管前动脉与后静脉直接相通、扩张,表现为T1WI低信号、T2WI高信号的结节灶。灌注障碍主要是由于肝内血管不同程度发育障碍引起的各肝小叶血供差异所致,表现增强扫描动脉期结节样、斑片样甚至片样的高信号,而门静脉表现为等信号。肝内动静脉畸形导致血流不均可引起肝细胞的损伤与修复,发生结节性增生,MR图像上表现为与正常肝实质相比T1WI略低信号、T2WI略高信号的结节灶,这些结节在增强扫描的动脉期明显强化。此类再生结节因其周围没有纤维间隔而有别于肝硬化中所见的肝细胞再生结节,被称为假性肝硬化[16]。本组病例中2例MR病例有灌注障碍及结节性增生的表现,与文献报道所见一致。
肝脏HHT在影像上需要与引起肝血管异常增粗的疾病、引起肝脏灌注异常的疾病及引起胆道坏死的疾病进行鉴别。肝硬化通常可以有门脉高压引起的门脉增粗、各肝叶纤维化程度不同而引起的灌注不均及肝硬化增生结节,与肝脏HHT在影像表现上有一定的相似性,故应注意鉴别。肝硬化通常为肝炎性或酒精性肝硬化,临床上有肝炎、酗酒等相关病史,晚期可以有门脉增粗或门脉海绵样变表现,但一般肝动脉无增粗,肝脏灌注不均通常以肝段分布,表现动脉期大片状异常强化,与肝脏HHT结节状、雪花状灌注不均不同;但肝硬化增生结节与肝脏HHT增生结节鉴别有困难。总之,存在肝血管畸形或肝实质异常灌注的病例,特别是两种征象共存的情况下,要考虑到HHT的可能。
肺部是HHT另一较为常见的受累器官,可与肝脏同时受累。文献报道[16]肺部HHT的发生率约为HHT的20%~50%,肺部HHT的AVM病灶可分为单纯型和复杂型,病灶直径≥3 cm会出现呼吸困难、紫绀、咯血等症状。大约8%的肺部HHT患者有显著的肺动脉高压,进而继发高输出性心衰,特别是与肝脏同时受累的病例[17]。本组病例中4例/11例病例同时肺部CT检查发现肺内AVM病灶,病灶均为单纯型——单支动脉与静脉相通,交通血管呈瘤样扩张,其中1例出现了左心扩大的心衰症状。因此,笔者认为当发现肝脏HHT时应进行肺部CT检查,能及时发现肝肺同时受累的HHT,从而提示临床关注并预防心衰等较严重并发症的发生。
综上所述,肝脏遗传出血性毛细血管扩张症影像学具有雪花样或棉絮样异常灌注及血管畸形的特征性表现,认识并准确诊断对临床具有重要的临床意义,特别是对肝肺同时受累病例的准确诊断,可以预防心衰等严重并发症的发生。
