基于低共熔溶剂的涡旋辅助悬浮固化-分散液液微萃取/高效液相色谱法测定水中三氯生与三氯卡班
2020-05-09陈梦轩吴友谊周韫璐许梦琪
陈梦轩,吴友谊*,周韫璐,许梦琪
(1.苏州科技大学 环境科学与工程学院,江苏 苏州 215009;2.江苏省环境科学与工程重点实验室,江苏 苏州 215009)

TCS和TCC已有的分析方法主要为高效液相色谱法(HPLC)、高效液相色谱-质谱法(HPLC-MS)、气相色谱法(GC)和气相色谱-质谱法(GC-MS)。但由于环境水体中的TCS和TCC含量很低,在检测前需进行富集。常用的富集方法为液-液萃取(LLE)和固相萃取(SPE),但存在需大量有毒有机溶剂[7]、耗时长、重复利用率低、成本高等不足[8]。其他基于固相萃取的小型化技术(如搅拌棒吸附萃取、固相微萃取、微固相萃取)也存在萃取及解吸耗时长[9-11]、选择性差[12]的缺点。分散液液微萃取(DLLME)具有重复性好、萃取时间短、回收率高、富集倍数高、溶剂用量少等优点而广受关注,但大多数萃取剂有毒,对环境不友好。即使作为传统溶剂替代的离子液体(ILs),也往往存在合成工艺复杂且毒性大、价格高的问题。因此,寻找一种绿色环保的DLLME萃取剂极为必要。
低共熔溶剂(DES)是由两种或两种以上化合物,即氢键供体(HBD)和氢键受体(HBA)的自缔合作用生成的物质[13-14]。DES是一种可替代传统萃取溶剂的绿色溶剂,可用于从各种基质中分离和预浓缩分析物[15],具有低挥发性、水溶性、无毒性、生物相容性、可生物降解性以及可设计和调整的特点。但现有报道的DES多与水混溶,难以作为水相萃取溶剂。Ferrone等[16]合成亲水性DES,用以萃取橄榄油、大豆油等食用油中的羟丙烯基苯丙素。TCS和TCC属于弱极性化合物(logKOW分别为4.8、4.9)[17],理论上,采用较为疏水的DES萃取效果更佳,但尚无将疏水性DES用于检测环境水体中TCS和TCC的文献报道。
DLLME通常使用密度比水大、凝固点高的萃取剂,而目前合成的疏水性DES大多密度低于水、凝固点接近室温。本实验借鉴漂浮有机液滴固化分散液液微萃取(DLLME-SFO)技术[18-19],在低温下,将疏水性DES萃取剂由液态转化成固态,以降低萃取相分离收集的难度,进而提高萃取效率。合成了几种新型疏水性DES,并筛选出以薄荷醇作为HBA,十二醇作为HBD的绿色、低凝固点的DES。基于上述DES建立了涡旋辅助悬浮固化-分散液液微萃取/高效液相色谱(VA-DLLME-SFDES/HPLC)检测环境水体中三氯生和三氯卡班的方法,并成功应用于实际湖水的检测。
1 实验部分
1.1 仪器与试剂
Shimadzu LC-20AT液相色谱仪(日本岛津公司);Sk-1型快速混合器(金坛市科析仪器有限公司);0406-1型离心机(上海外科器械厂);85-2B双数显控温磁力搅拌器(金坛市文华科教实验仪器厂);UV-2450型紫外分光光度计(日本岛津公司);HY-4调速多用振荡器(金坛市恒丰仪器制造有限公司);T6新世纪紫外可见分光光度计(北京普析通用仪器有限公司);AL204电子分析天平(梅特勒-托利多仪器上海有限公司)。
三氯生(99.0%)、三氯卡班(98.0%)均购于J&K百灵威科技有限公司;甲醇(色谱纯,美国 Sigma 公司);十二醇(>99.0%)、十四醇(>98.0%)均购于上海阿拉丁试剂有限公司;薄荷醇(≥98.0%,美国 Sigma 公司);三辛基甲基溴化铵、三辛基甲基氯化铵(>98.0%,阿达玛斯试剂有限公司)。
1.2 标准溶液的配制
分别准确称取25 mg三氯生和三氯卡班标准品,用甲醇溶解并定容至50 mL棕色容量瓶中,配制成500 mg/L的单标储备液,于冰箱4 ℃避光保存。使用时以甲醇稀释成所需浓度的标准工作液。
1.3 DES的制备
按照1∶2的摩尔比分别称取氢键受体(HBA)和氢键供体(HBD),放入50或100 mL圆底烧瓶中混合,并加入磁搅子,75 ℃下水浴加热搅拌(转速1 000 r/min),直至得到透明澄清的均一液体。
1.4 DES理化性质的测定
1.4.1 密度与熔点室温下(20 ℃),用电子天平测定1.00 mL DES的准确质量,平行5次,均值代入公式ρ=m/V计算密度。
将DES冷冻成固体后,水浴加热,观察DES的融化温度,记录熔点。
1.4.2 辛醇-水分配系数采用摇瓶法测定辛醇-水分配系数,主要参考文献[20]并稍作改动。室温下(20 ℃),将装有20 mL正辛醇与200 mL水的锥形瓶在振荡器上振荡24 h,使两者相互饱和,静置分层后两相分离,分别保存备用。用乙醇将DES制备成400 μL/L的标准储备液备用。采用紫外分光光度计测定并绘制每种DES的标准曲线。移取400 μL DES于10 mL具塞比色管中,用上述经处理的被水饱和的正辛醇定容配成4×104μL/L的储备液。各移取1.0 mL上述溶液于6个10 mL离心管中,用上述经处理的被正辛醇饱和的水定容至10 mL。将离心管置于振荡器上振荡3 h后取出并离心。重复测定3次下相(即水相)中DES的吸光度。根据下式计算辛醇-水分配系数的对数值(logKOW):logKOW=log(COVO-CWVW)/CWVO。式中:CO为平衡时DES在正辛醇相中的浓度(μL/L);CW为平衡时DES在水相中的浓度(μL/L);VW、VO分别为正辛醇相和水相的体积(mL)。
1.5 样品前处理
准确移取10 mL经0.45 μm滤膜过滤后的环境水样于15 mL塑料离心管中,用盐酸调至pH 5.0,加入70 μL DES,涡旋1 min后,以4 000 r/min离心10 min。萃取完成后将离心管置于冰箱冷冻15~20 min。待DES凝固,倾去水相。离心管在室温下放至DES融化后,以4 000 r/min离心5 min。用微量进样针将DES转移至玻璃进样衬管中,待HPLC分析。
1.6 液相色谱条件
色谱柱:Agilent ZORBAX Eclipse XDB-C8(4.6 mm×150 mm,5 μm);柱温:30 ℃;进样体积:10 μL;检测波长:280 nm;流速:1.0 mL/min;流动相:A为甲醇,B为水。梯度洗脱程序:0~2 min,70% A;2~10 min,70%~90% A;10~15 min,90%~70% A;15~20 min,70%A。
2 结果与讨论
2.1 萃取剂的选择
在悬浮固化-分散液液微萃取中,萃取剂的选择至关重要。萃取剂必须密度比水小,凝固点接近或略低于室温,在水中溶解度小,对目标物有较高的亲和力且不干扰目标物[21]。按照表1和“1.3”方法制备6种DES,结果表明,6种新合成的疏水性DES的密度均小于或接近水(1.0 g/mL)。DES 6的熔点最高,为35 ℃;DES 3的熔点最低,只有23 ℃(表1)。6种DES的熔点基本均高于室温,可通过冷冻实现凝固,符合悬浮固化-分散液液微萃取对萃取剂的要求。另外,合成的DES熔点均低于HBA或HBD,这主要是由于母体化合物的化学结构(离子或中性)存在差异所致。其中DES 1~4的熔点降低幅度比DES 5、6大,是氢键受体的不同所致。上述6种DES均有一定的疏水性,因此有季铵盐参与时,熔点才会有较大的下降。以薄荷醇作为氢键受体时,其母体本身为中性物质,所得DES熔点降幅小[22]。
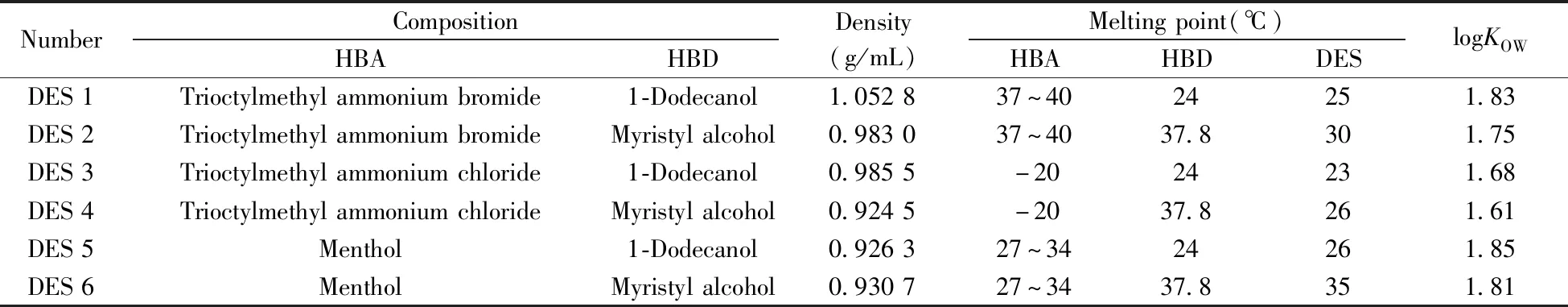
表1 DES及合成原料的理化性质Table 1 Physical and chemical properties of DES and its raw materials
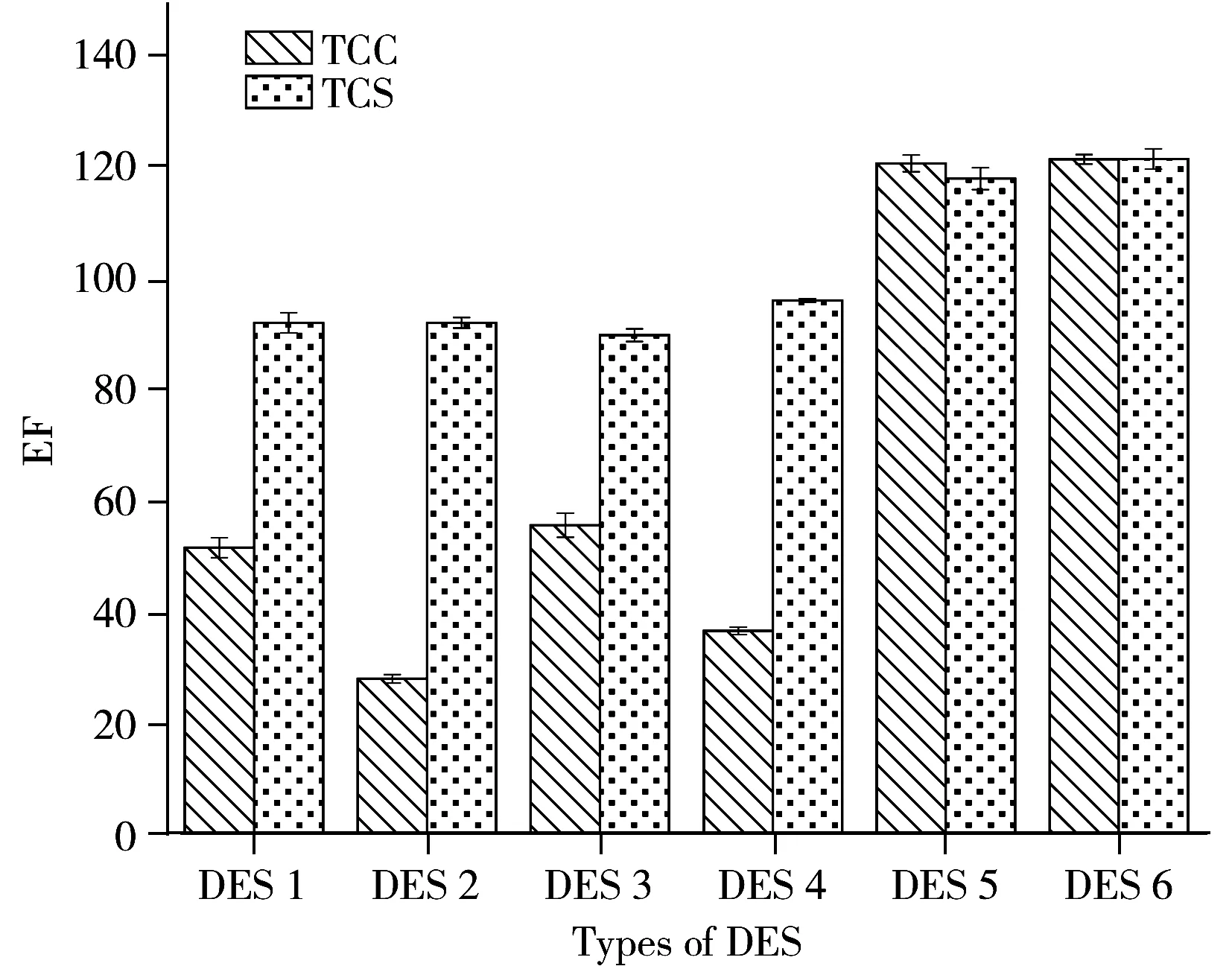
图1 DES类型对TCS和TCC萃取的影响Fig.1 Effect of type of DES on extraction of TCS and TCC water sample volume:10 mL;HBA∶HBD=1∶2;volume of extractant:80 μL;pH=4.0;vortex time:1 min
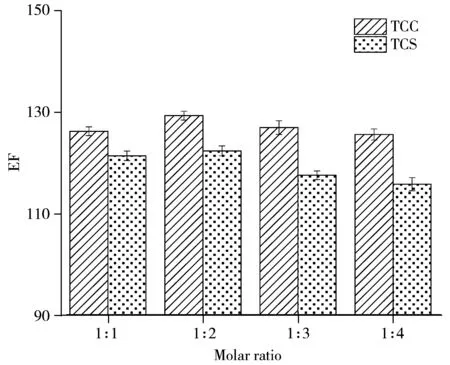
图2 薄荷醇与十二醇的摩尔比对TCS和TCC萃取的影响Fig.2 Effect of molar ratio of menthol to 1-dodecanol on extraction of TCS and TCC
TCS和TCC均为脂溶性化合物,辛醇-水分配系数较高(logKOW分别为 4.8、4.9)[17],其更易溶于长链脂肪醇或脂肪烃类物质。因此,合成时选择十二醇或十四醇为HBD组分。考察了DES类型对TCS和TCC萃取效率的影响,结果显示6种DES对2种分析物均有一定的萃取效率(图1)。以三辛基甲基溴化铵和三辛基甲基氯化铵作为HBA(即DES 1~4)时,富集效果较差,而以薄荷醇作为HBA(DES 5、6)时,富集倍数(EF)大于100。根据相似相溶原理,DES 2~4 3种萃取剂的logKOW均偏小,与目标物的极性差异较大,且其作为萃取剂时色谱干扰峰较多,因而富集效果不理想。DES 1、DES 5和DES 6的极性偏弱,理论上对2种目标物有较好的富集效果。此3种DES的logKOW接近,但DES 1的密度与水相近,萃取离心后只有部分悬浮于样品溶液上层,损失较大,富集倍数低于其它2种DES(图1)。而DES 6 作为萃取剂时,色谱峰展宽较大。因此最终选择富集倍数高、干扰峰少的DES 5作为萃取剂(薄荷醇、十二醇分别作为HBA和HBD)。
2.2 HBA与HBD摩尔比的选择
分别以薄荷醇和十二醇作为HBA和HBD,考察了两者不同摩尔比(1∶1、1∶2、1∶3、1∶4)对2种目标物萃取效果的影响。由图2可见,薄荷醇和十二醇的摩尔比为1∶2时TCS和TCC的富集倍数最高,随着十二醇的比例增加,富集倍数呈下降趋势。这可能是因为萃取剂中十二醇增多,使得DES的熔点低于室温,不利于其在水相中的分散,导致萃取效率低。同时,摩尔比为1∶1的DES由于其熔点高于室温,冷冻时间过长,且易于融化,所以DES损失较大。最终确定薄荷醇和十二醇的摩尔比为1∶2。
2.3 HBA与HBD用量的选择
萃取剂的用量会直接影响萃取效率,足量的萃取剂可确保分析物完全萃取,并获得良好的回收率,但过量的萃取剂可能会导致萃取效率下降。考察了萃取剂用量(50、60、70、80、90、100、120 μL)对2种目标物萃取效果的影响,结果表明,在10 mL水样中,当萃取剂DES的用量由50 μL增至70 μL时,TCS和TCC的回收率增加;当DES用量在70~90 μL时(TCS为70~80 μL),目标分析物的回收率基本不变;当DES用量大于90 μL时,目标分析物的回收率下降。综合考虑回收率和富集倍数,选择萃取剂用量为70 μL。
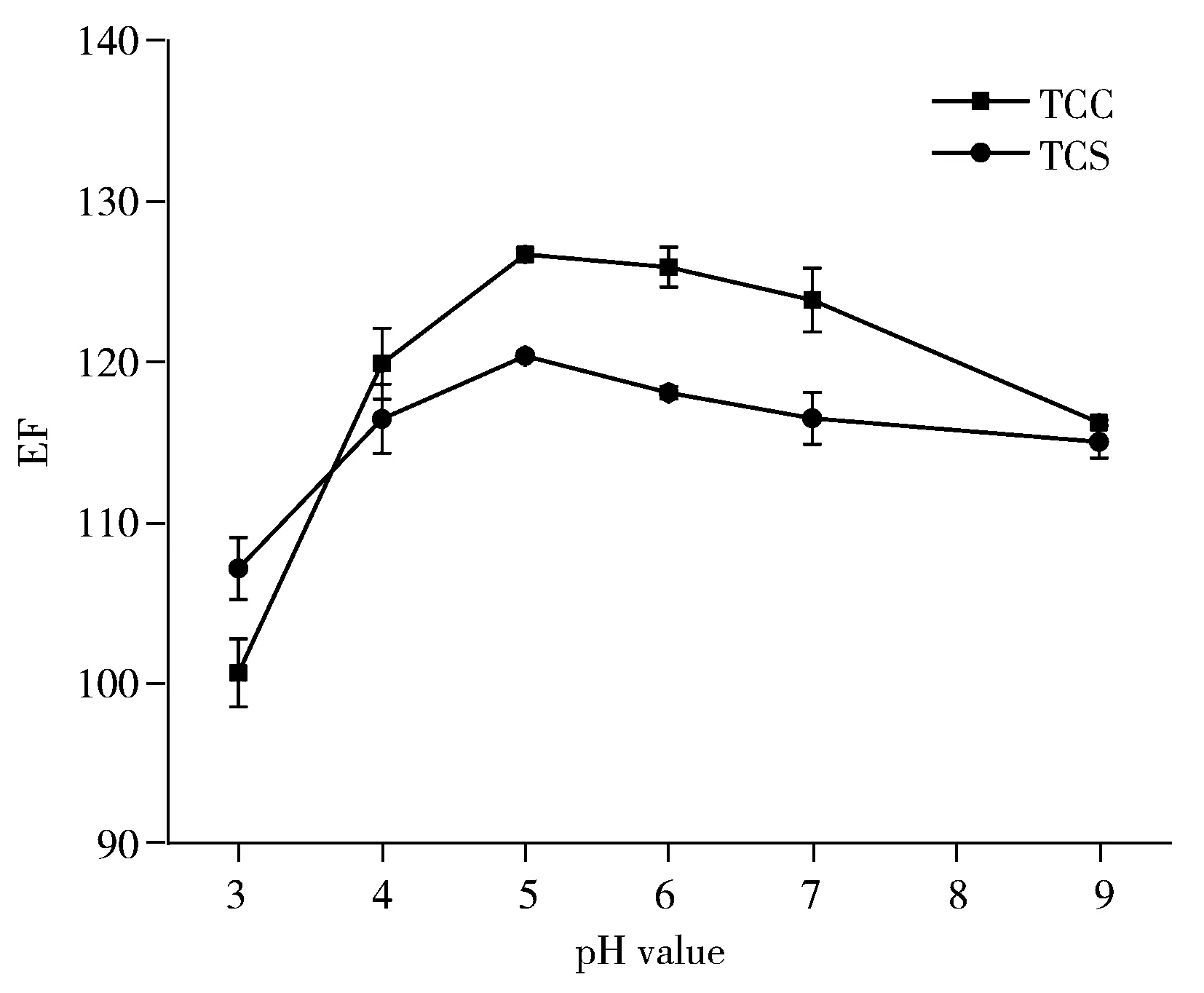
图3 pH值对TCS和TCC萃取的影响Fig.3 Effect of sample pH value on extraction of TCS and TCC
2.4 pH值的选择
样品的pH值会影响分析物在样品溶液中的存在形式。考察了不同pH值条件下,DES对TCS和TCC的萃取效果。如图3所示,TCS和TCC在弱酸性条件下的富集倍数较高,在碱性条件下的富集倍数下降。pH 5.0时,两种目标物的富集倍数最高。这是由于非两性化合物的存在状态通常与酸解离常数(pKa)相关。当样品溶液的pH值低于化合物的pKa 2个单位时,该化合物主要以非电离的中性分子存在;反之,则主要以负离子形式存在[23]。TCS和TCC的pKa分别为7.9和12.7[24],加入0.1 mol/L 盐酸调至弱酸性,可确保TCS和TCC处于非电离状态,有利于被萃取到有机相中[25]。因此选择最佳pH值为5.0。
2.5 涡旋时间及盐的影响
以涡旋代替分散剂,在涡旋作用下,DES可充分分散到样品溶液中,因此涡旋时间会影响乳化过程和两相之间的平衡。考察了不同涡旋时间(0.5、1、2、3、4、5 min)对TCS和TCC萃取效果的影响。结果表明,过长的涡旋时间并不能提高萃取效果,涡旋时间为1 min时2种目标物的富集倍数最高,且分析物由水相到萃取剂的转移很迅速。为方便操作,选择涡旋时间为1 min。
盐的加入可以降低分析物在含水样品中的溶解度,并增强其在有机相的分配。考察了样品中加入不同量NaCl(0~20%)对TCS和TCC萃取效果的影响,发现盐浓度对两种目标化合物具有不同的影响。随着NaCl加入量的增加,TCS的萃取效率降低,但TCC的萃取效率基本不变。因此实验选择不添加盐。
2.6 方法验证
用空白样品基质溶液配制TCS和TCC的质量浓度分别为0.5、1、2、4、10、50、100 μg/L的标准溶液,在最佳萃取条件下测定,绘制出两种目标物的工作曲线。结果表明,TCS和TCC的线性范围分别为0.59~100、0.26~100 μg/L,相关系数(r2)均为0.999 8;分别按3倍信噪比(S/N=3)计算检出限(LOD)为0.08~0.18 μg/L,以10倍信噪比(S/N=10)计算定量下限(LOQ)为0.26~0.59 μg/L;TCS和TCC的富集倍数分别为141和148倍(表2)。
通过在空白样品中分别加标3种不同浓度(2、10、50 μg/L)的混合标准溶液以评估方法的精密度。同1天内,对样品进行前处理后,重复测定6次所得结果的相对标准偏差即为日内精密度(Intra-RSD);连续6 d,同一时间下对样品进行前处理后,所得结果的相对标准偏差即为日间精密度(Inter-RSD)。TCS和TCC的日内精密度和日间精密度均不大于5.4%(表2)。

表2 VA-DLLME-SFDES/HPLC方法的分析性能Table 2 Analytical performance of the proposed VA-DLLME-SFDES/HPLC method
2.7 方法比较
将本文建立的VA-DLLME-SFDES/HPLC法与其他文献方法进行比较(见表3)。结果显示,本方法的LOD略高于Micro-SPE-HPLC法,与IL-DLPME-LC-MS/MS法相当,均优于其他3种方法。但Micro-SPE-HPLC需耗时2 h以上且样品用量大。
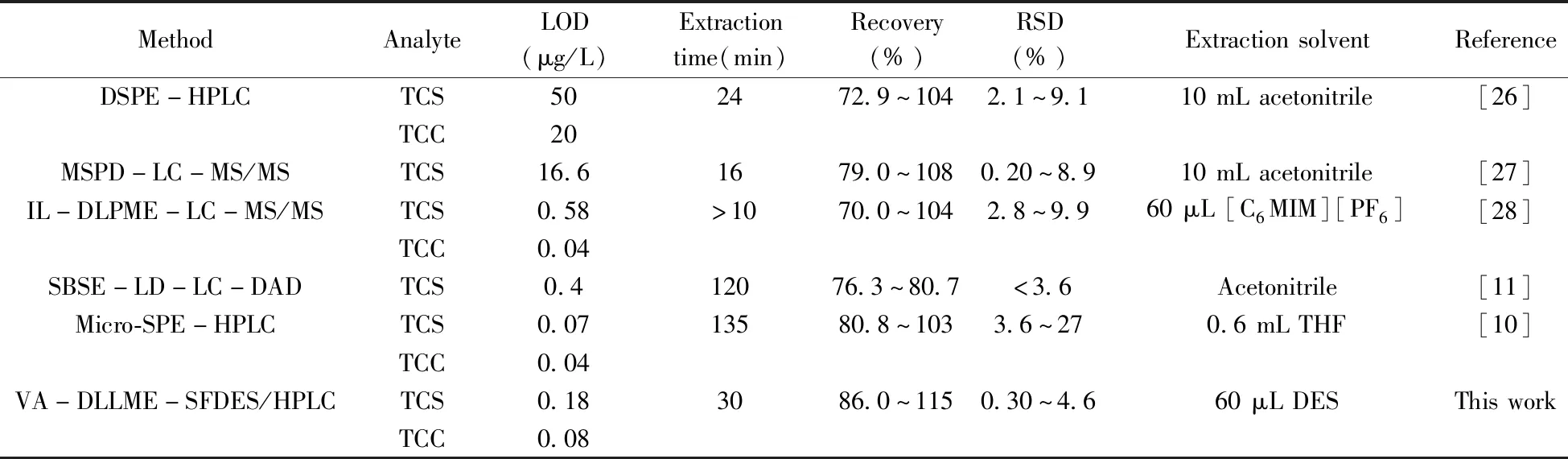
表3 本方法与其他方法的比较Table 3 Comparison of the proposed method with other methods
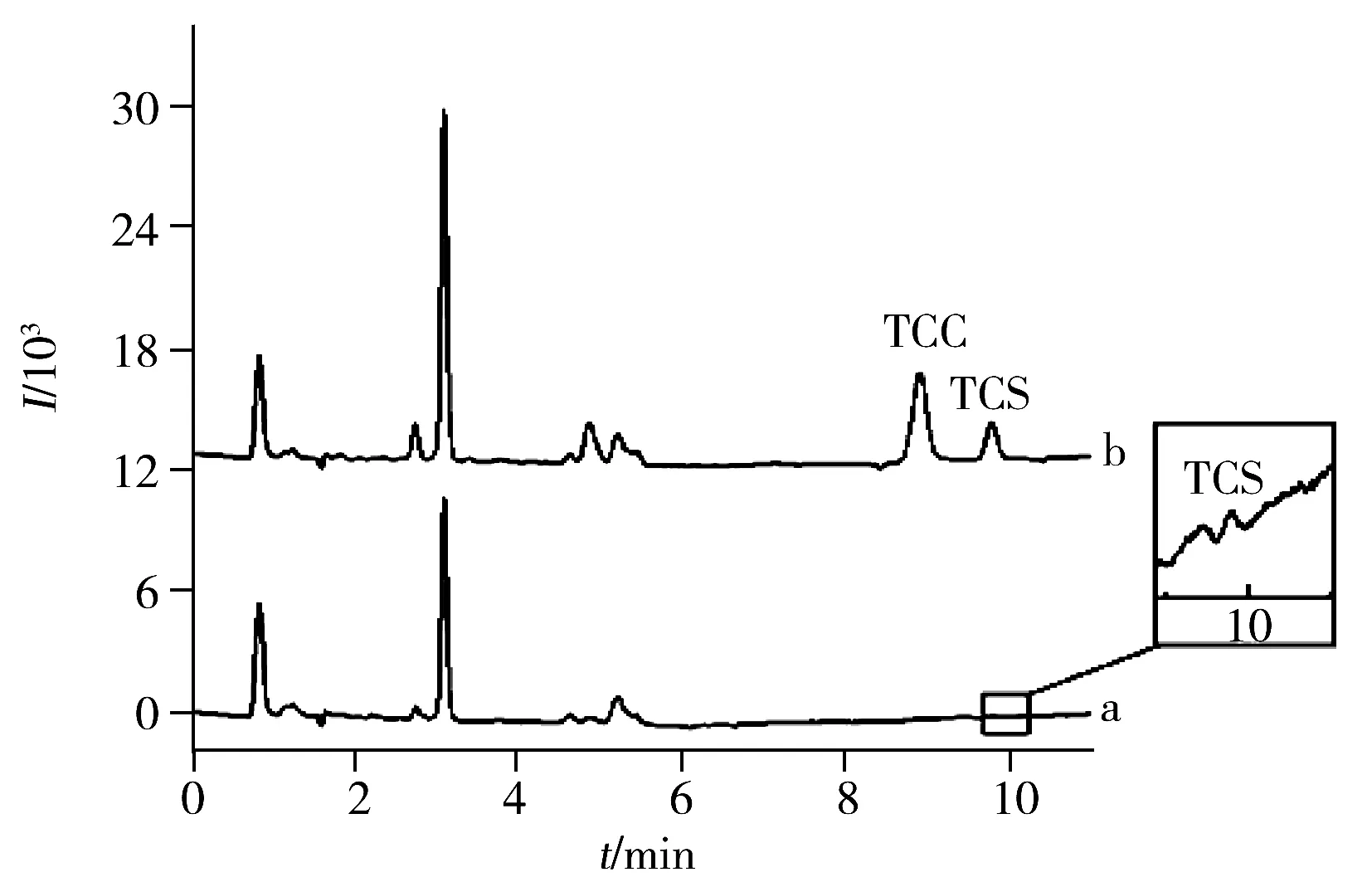
图4 实际样品和加标样品的色谱图Fig.4 HPLC chromatograms of actual and spiked samplesa.water sample 13#;b.spiked water sample 13# (10 μg/L TCS+TCC)
2.8 实际样品分析
采用本方法对太湖水域周边3个点位(4#、12#和13#)的实际环境水样进行测定。结果表明,在4#、12#水样中均未检出TCS和TCC,13#水样中出现TCS峰(图4),但无法准确定量。对上述3个水样进行低、中、高3个水平的加标实验(n=3),加标回收率为86.0%~115%(表4)。
3 结 论
本文建立了基于疏水性DES的涡旋辅助悬浮固化-分散液液微萃取结合高效液相色谱测定环境水样中TCS和TCC的新方法。以薄荷醇和十二醇为原料合成疏水性DES,避免了有毒有机溶剂的使用,降低了分析成本,且减少对人类和环境的污染影响。提取过程无需使用分散剂,利用涡旋加速DES的分散和萃取;利用冷冻固化降低了萃取相分离收集的难度。在简化操作的同时,大大提高了提取效率,缩短了萃取时间。在最佳萃取条件下,分析物的富集倍数为141~148。该方法具有良好的回收率和重复性,线性范围宽,检出限较低,适用于环境水体中TCS和TCC的测定。
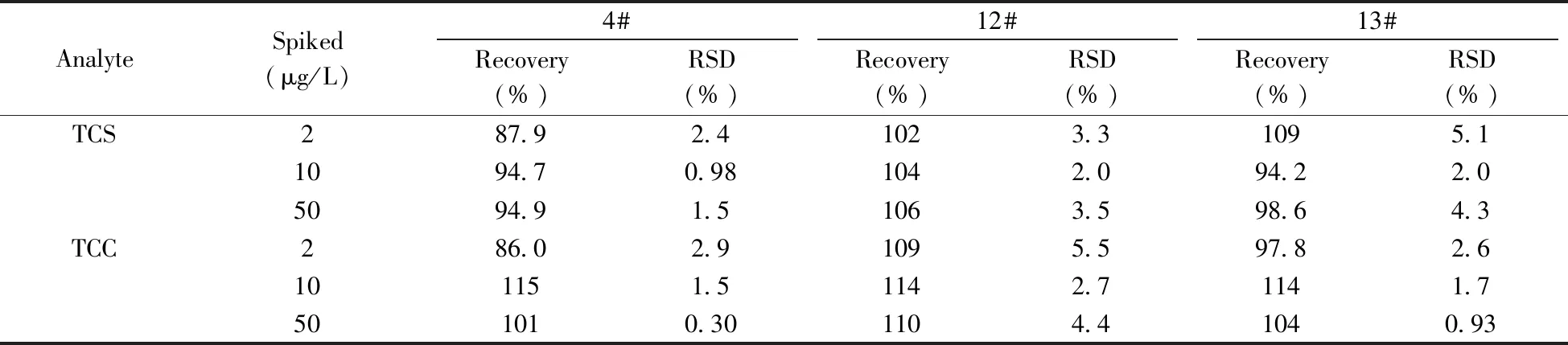
表4 太湖水样中TCS和TCC的加标回收率(n=3)Table 4 Spiked recoveries of TCS and TCC in Taihu lake water(n=3)
