液相色谱-串联质谱法测定固体及液体药物中27种新型毒品芬太尼类物质
2020-05-09张建莹黄昌雄卞学海梁淑雯
罗 耀,张建莹,黄昌雄,卞学海,李 颖,梁淑雯
(深圳海关 食品检验检疫技术中心,广东 深圳 518045)
芬太尼(Fentanyl)是从阿片(罂粟)中提取的生物碱及衍生物,是一种强效麻醉性镇痛药,其麻醉效力比海洛因强50倍,比吗啡强100倍。但其也是一种成瘾性毒品,2 mg的药量足以致命。而且这类化学非法合成毒品易出现各种变体,例如芬太尼目前已知的变体有130多种。芬太尼类物质是指化学结构与芬太尼相比,符合以下1个或多个条件的物质:①使用其他酰基替代丙酰基;②使用任何取代或未取代的单环芳香基团替代与氮原子直接相连的苯基;③哌啶环上存在烷基、烯基、烷氧基、酯基、醚基、羟基、卤素、卤代烷基、氨基及硝基等取代基;④使用其他任意基团(氢原子除外)替代苯乙基。图1为5种典型芬太尼类物质的化学结构式。芬太尼类物质(Fentanyl analogs and metabolites)是新精神活性物质(New psychoactive substances,NPS)的重要组成部分。新精神活性物质又称“策划药”或“实验室毒品”,是继传统毒品、合成毒品后全球流行的第3代毒品。
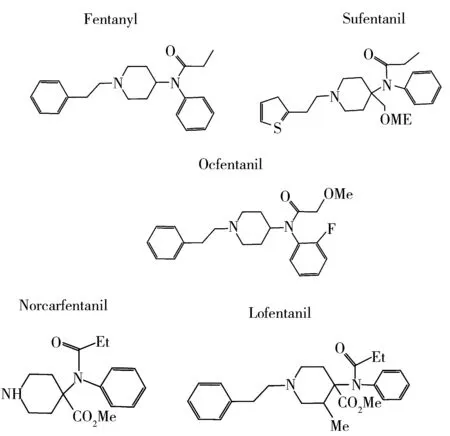
图1 5种典型芬太尼类物质的化学结构式Fig.1 Chemical structures of typical fentanyl analogs and metabolites
据报道,自2013年以来,海洛因和假药配方中分别发现了非法芬太尼及其类似物,随后缉获的药物材料和毒理学案例中发现的此类物质数量急剧增加,2016年芬太尼及其类似物的致死人数超过海洛因[1]。由于该类物质的毒性强、品种多、变异快、缉查难,已成为当前国际禁毒领域面临的一大难题。我国禁毒主管部门对芬太尼类物质采取非常严格的监管措施,列管品种达25种,超过了联合国规定管制的21种。2019年4月我国首次将芬太尼整类物质列入《非药用类麻醉药品和精神药品管制品种增补目录》,按类纳入毒品管制范畴。为满足新形势下芬太尼类物质的列管要求,助力海关打击毒品犯罪,急需建立芬太尼类物质的定性定量方法。
目前,芬太尼类物质的检测方法有酶联免疫吸附测定法(ELISA)、气相色谱-质谱法(GC-MS)[1]、高效液相色谱法(HPLC)及液相色谱-串联质谱法(LC-MS/MS)[2-15],主要针对芬太尼、瑞芬太尼、舒芬太尼等单一物质进行分析,涉及血液、乳汁、尿液、唾液等生物基质。联合国毒品与犯罪问题办公室推荐的方法中,GC-MS法仅涉及3种芬太尼类物质[1],液相色谱-高分辨质谱法(LC-HRMS)亦只涉及10多种芬太尼类物质的筛查检测[1]。针对广泛的非法和处方芬太尼类物质的LC-MS/MS检测方法报道较少,导致处方芬太尼类药物的过量流行和非法芬太尼类药物的出现。本研究通过75%乙腈水结合乙腈提取固、液体药物中的芬太尼类物质,两类药物分别采用HLB固相萃取小柱及QuEChERS法净化,液相色谱-串联质谱测定,建立了固体和液体药物中27种新型毒品芬太尼类物质(包括芬太尼及26种类似物或代谢物)的分析方法。
1 实验部分
1.1 仪器与试剂
TSQ Endura LC-MS/MS液相色谱-串联质谱仪(配Ultimate 3000超高效液相色谱仪,Thermofisher公司),Rax top涡旋振荡仪(德国Heidolph公司);3K18高速冷冻离心机(德国Sigma公司);高纯水发生器(Milli-Q Integral 10+,美国Millipore公司);0.22 μm 亲水PTFE有机滤膜(上海安谱公司)。 甲醇、乙腈、甲酸、乙酸铵(色谱纯,德国Merck公司);实验用水为Milli-Q超纯水;Oasis HLB固相萃取柱(60 mg/3 mL,美国Waters公司);N-丙基乙二胺吸附剂(PSA,美国Supelco公司)。27种芬太尼类物质标准溶液(化合物名称见表1,质量浓度100 mg/L,美国Cerilliant公司),使用乙腈稀释为1.00 mg/L和100 μg/L的混合标准工作溶液,于-18 ℃避光存放。
1.2 样品处理
1.2.1 固体药物粉末称取固体试样0.100 g,加入2 mL 75%乙腈水,涡旋溶解,再加入2 mL 乙腈,涡旋30 s,超声提取15 min。9 500 r/min 离心5 min后,吸取全部上清液于HLB固相萃取柱(预先用5 mL乙腈活化)中,待上清液全部流出,再加入4 mL乙腈淋洗。收集所有流出液,40 ℃水浴氮吹至低于0.5 mL,加入0.5 mL水,再以乙腈定容至1.00 mL,涡旋振荡30 s,9 500 r/min 离心5 min。取上清液,过0.22 μm有机滤膜后,上机测定。
1.2.2 液体药物称取液体试样0.100 mL,加入2 mL 75%乙腈水,涡旋溶解,再加入2 mL 乙腈,涡旋30 s,超声提取15 min。加入25 mg PSA,涡旋1 min,9 500 r/min 离心5 min。吸取所有上清液,40 ℃水浴氮吹至低于0.5 mL,加入0.5 mL水,再用乙腈定容至1.00 mL,涡旋振荡30 s,9 500 r/min 离心5 min。取上清液,过0.22 μm有机滤膜后,上机测定。
1.3 色谱条件
色谱柱:Eclipse Plus Phenyl-Hexyl(150 mm×2.1 mm,3.5 μm,美国Agilent公司)。流动相:A为0.005 mol/L乙酸铵溶液(含0.1%甲酸);B为甲醇(含0.1%甲酸)。梯度洗脱程序:0~1.0 min,5% B;1.0~40 min,5%~55% B;40~45 min,55% B;45~45.5 min,55%~5% B;45.5~50 min,5% B。流速:0.3 mL/min;进样量:2 μL。
1.4 质谱条件
离子化模式:电喷雾离子源(ESI),温度:150 ℃;正离子模式;质谱扫描方式:多反应监测(MRM);毛细管温度:350 ℃;雾化器温度:350 ℃;鞘气压力:35 Arb(Arbitrary units);辅助气压力:8 Arb;分辨率:单位分辨率;驻留时间:30 ms。其它质谱参数见表1。
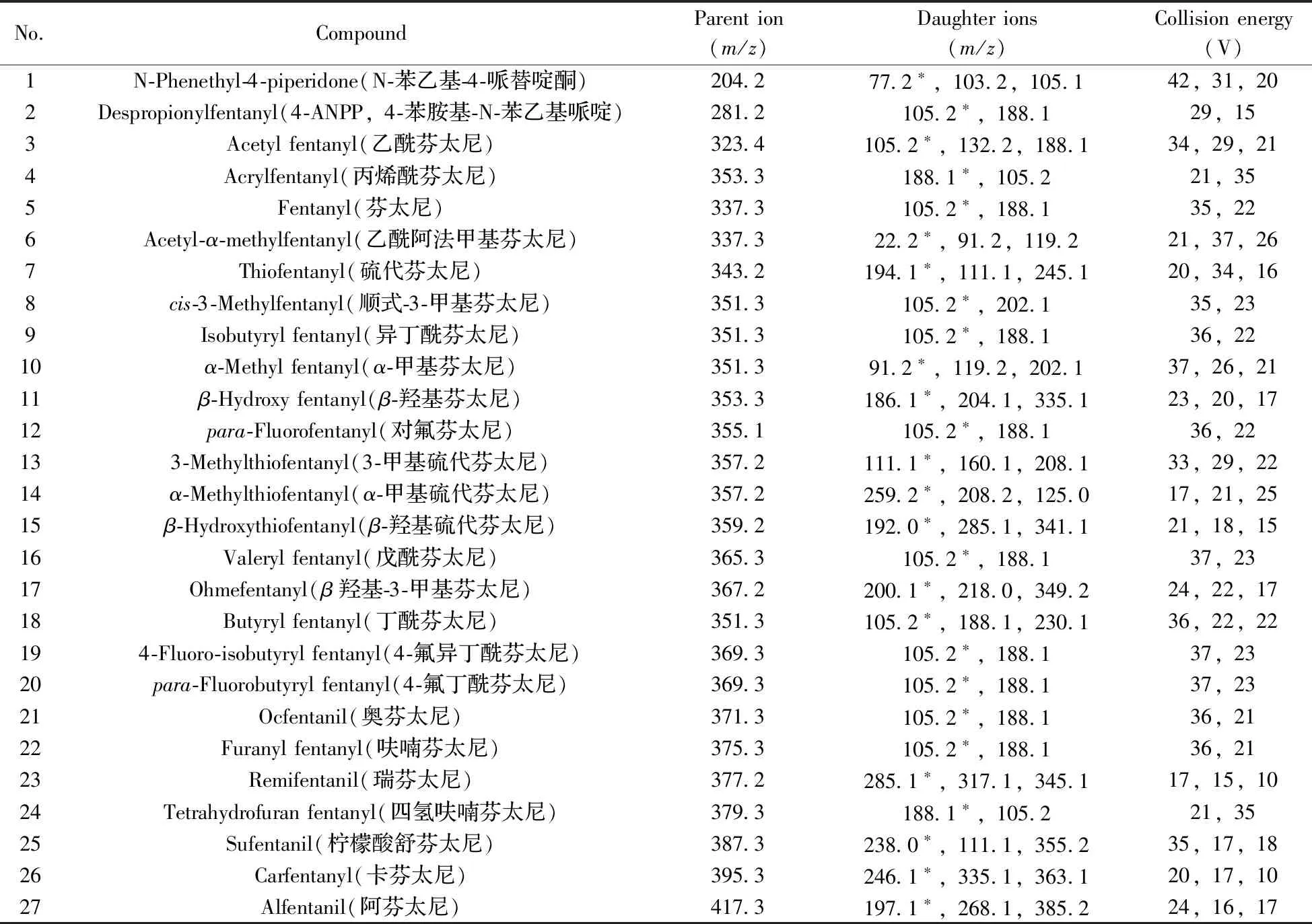
表1 27种化合物的质谱参数Table 1 MS parameters for the detection of 27 compounds
*quantitative ion
2 结果与讨论
2.1 色谱柱的选择
由于芬太尼类物质含有苯基、烷基和酰胺等基团,化学性质差异较大,且同时存在部分同分异构体,因此本方法采用苯基-己基色谱柱Eclipse Plus Phenyl-Hexyl(150 mm×2.1 mm,3.5 μm),当使用含甲醇的流动相时,对极性胺类化合物和芳香族化合物有显著的选择性。结果表明,27种芬太尼类物质均得到较好的分离和保留,其中包括2对同分异构体(4-氟异丁酰芬太尼和4-氟丁酰芬太尼,丁酰芬太尼和对氟芬太尼)。
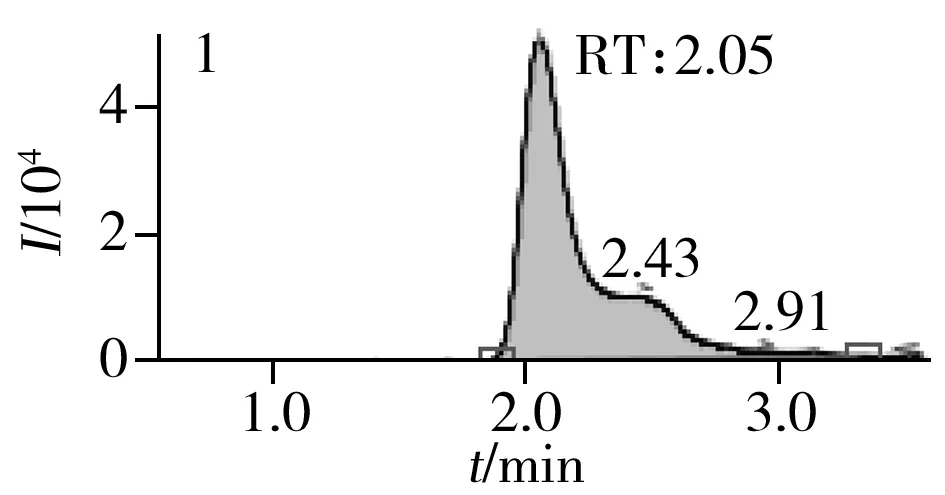
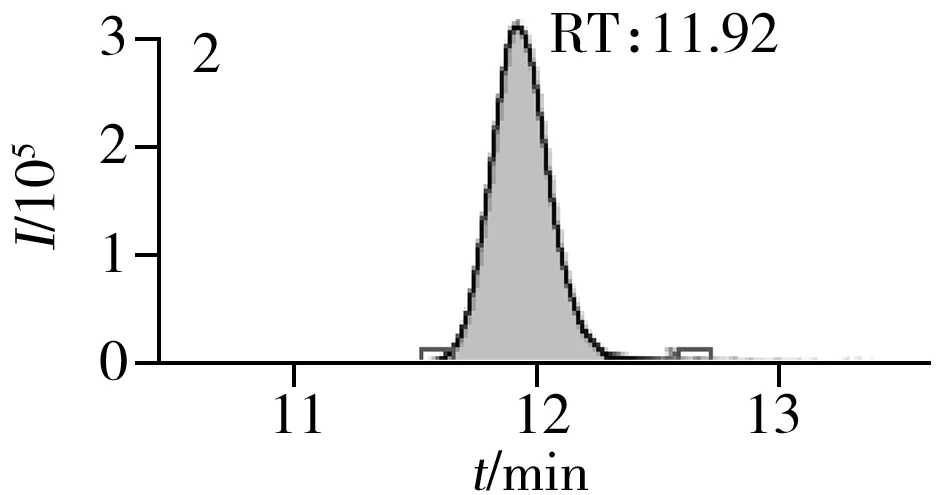
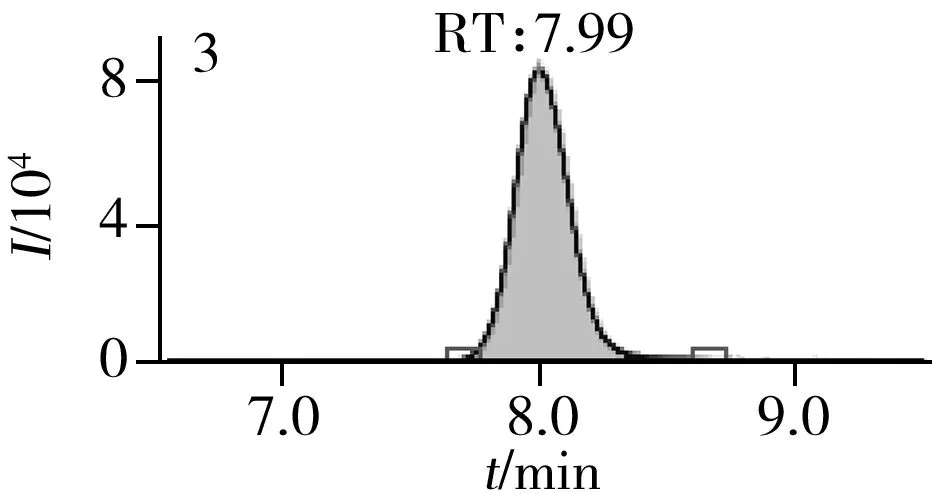
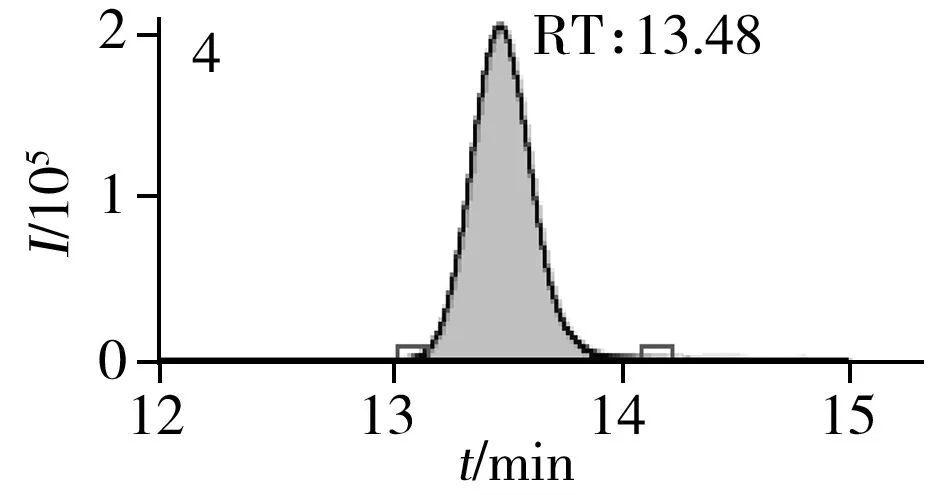
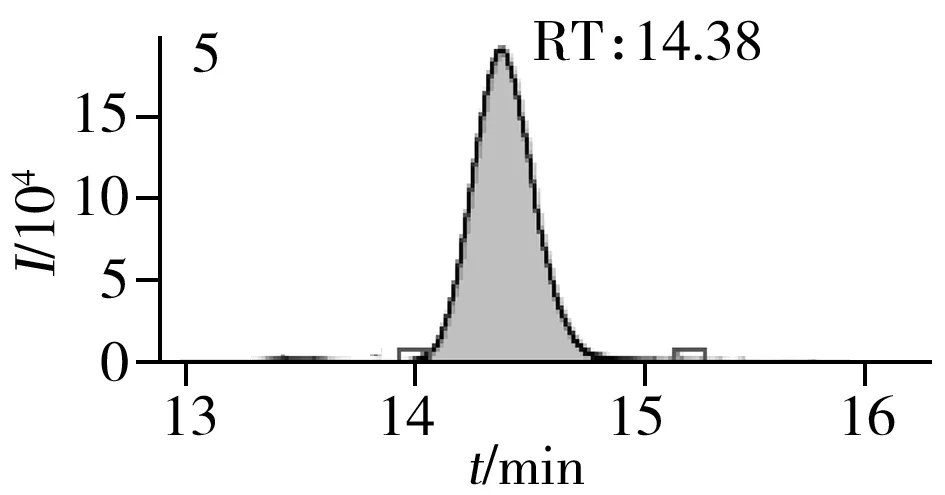
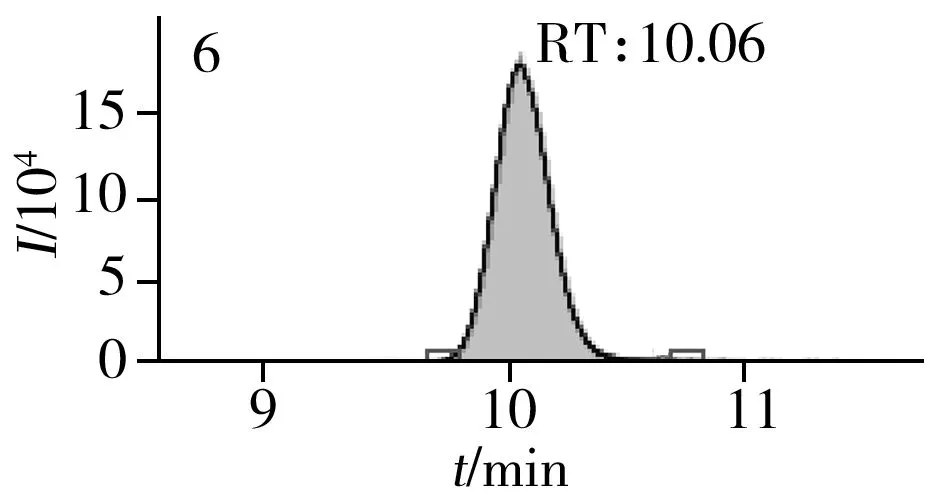
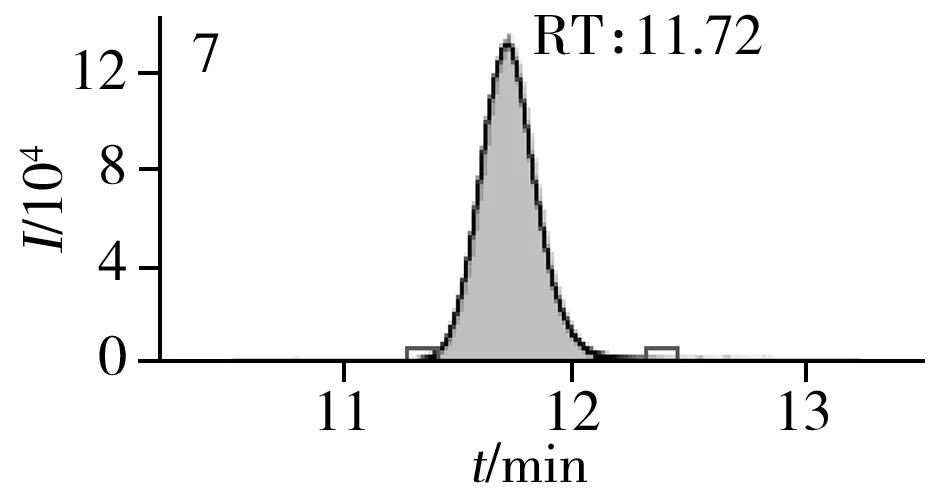
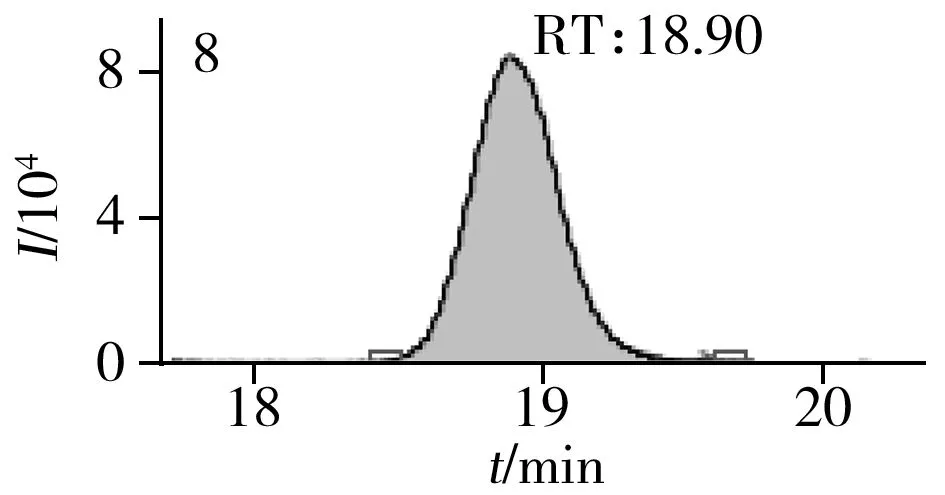
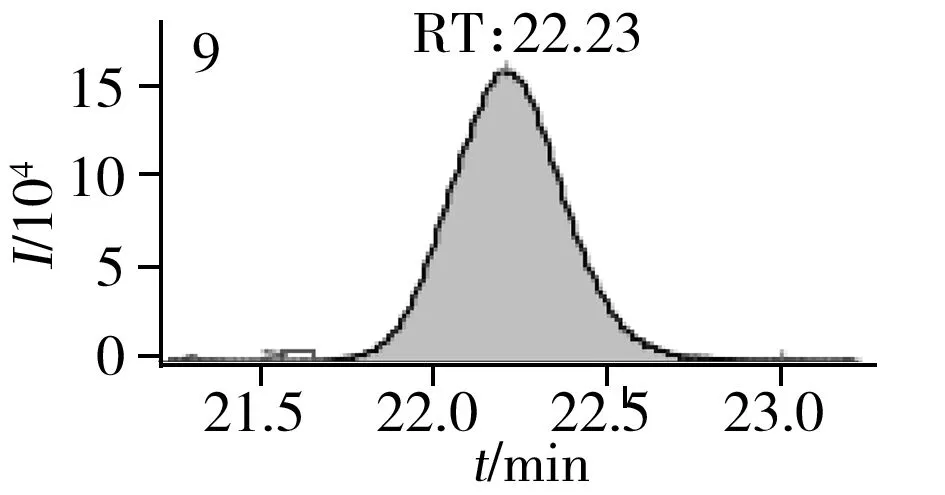
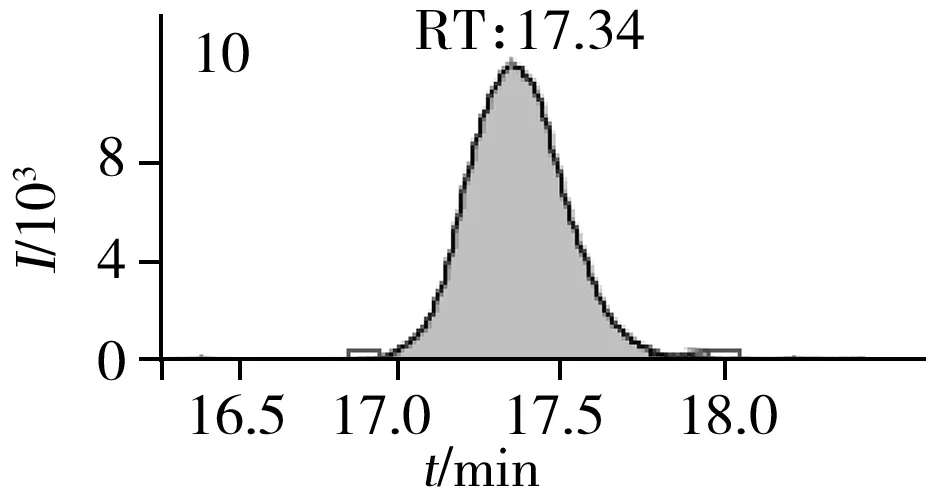
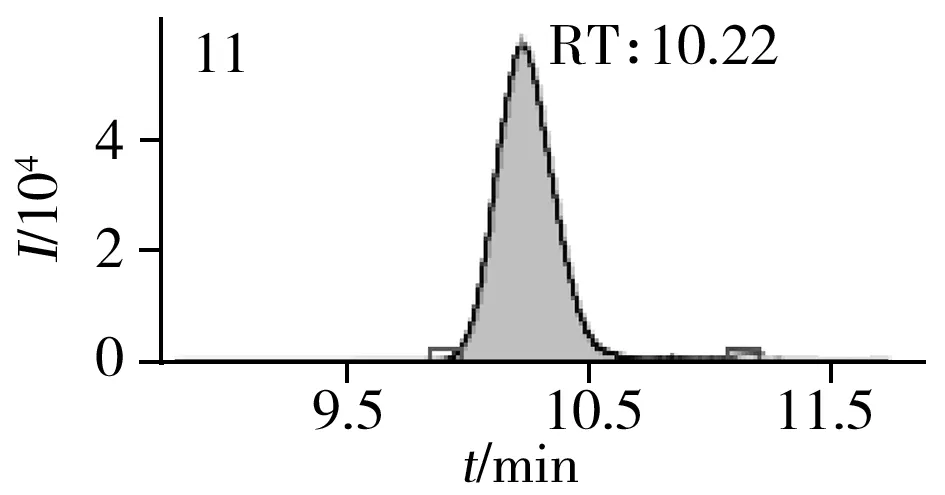
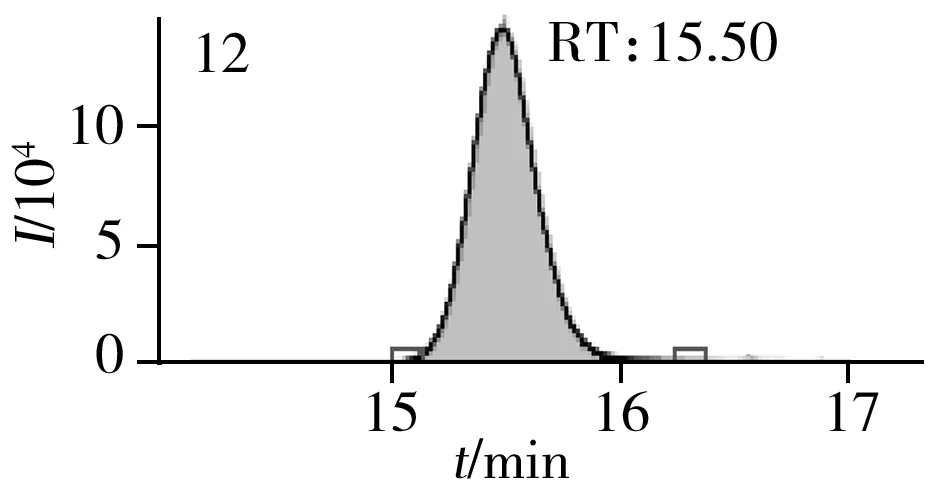
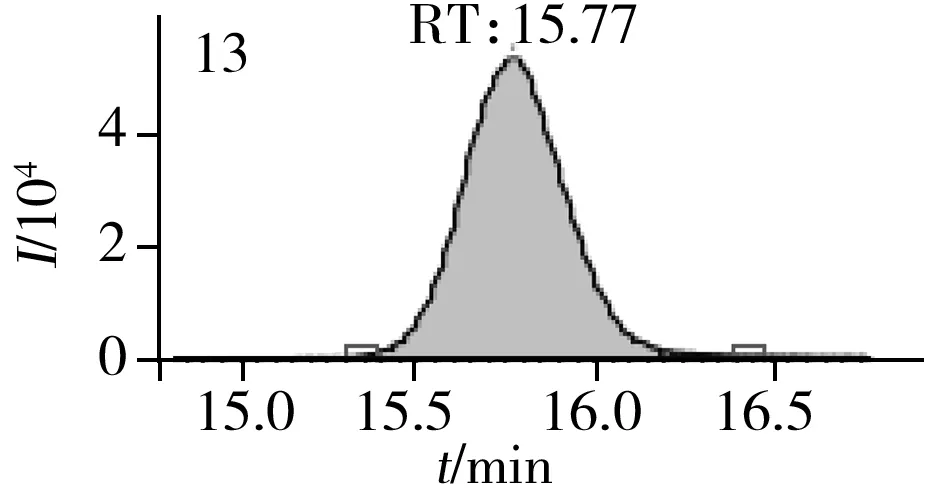
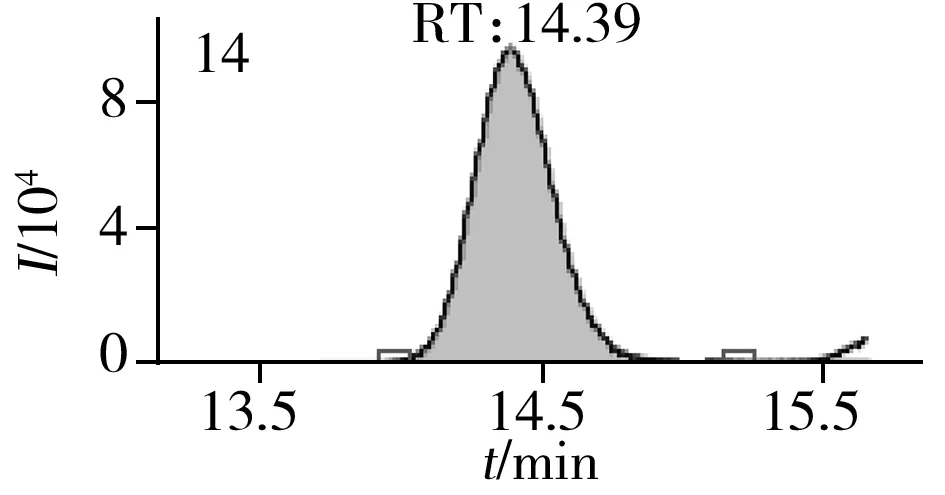
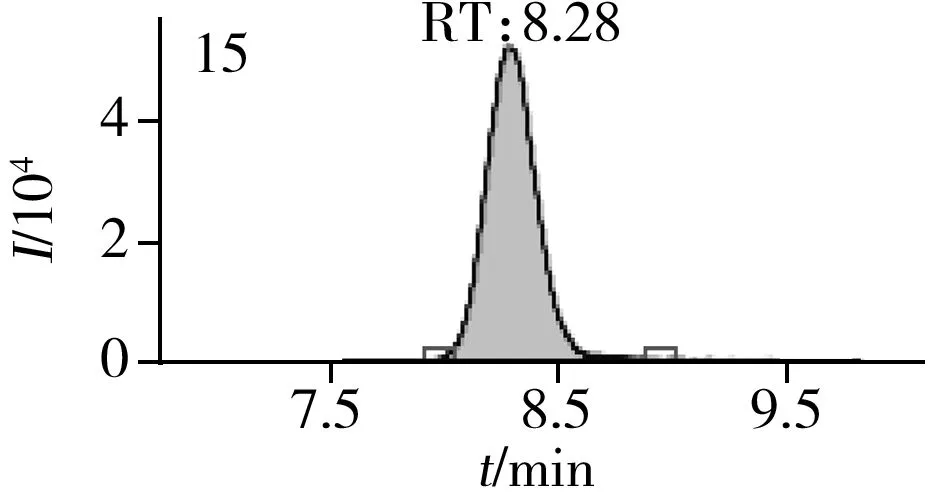
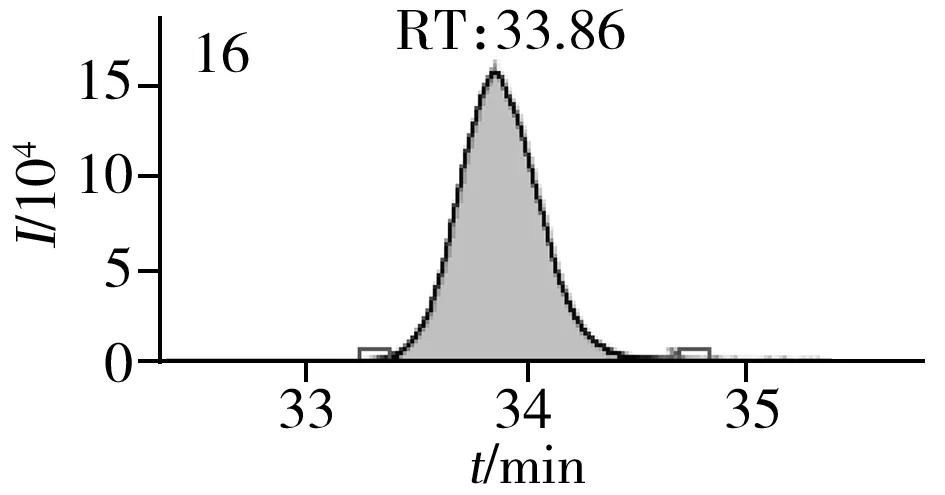
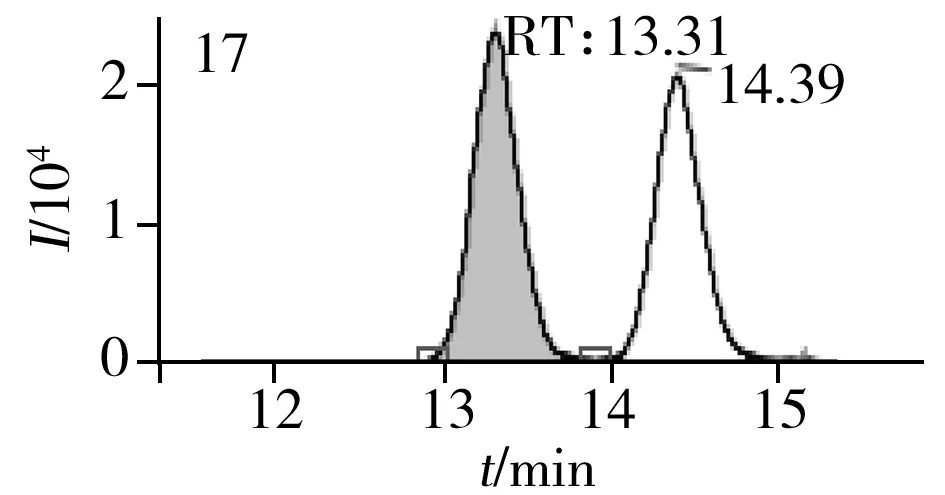
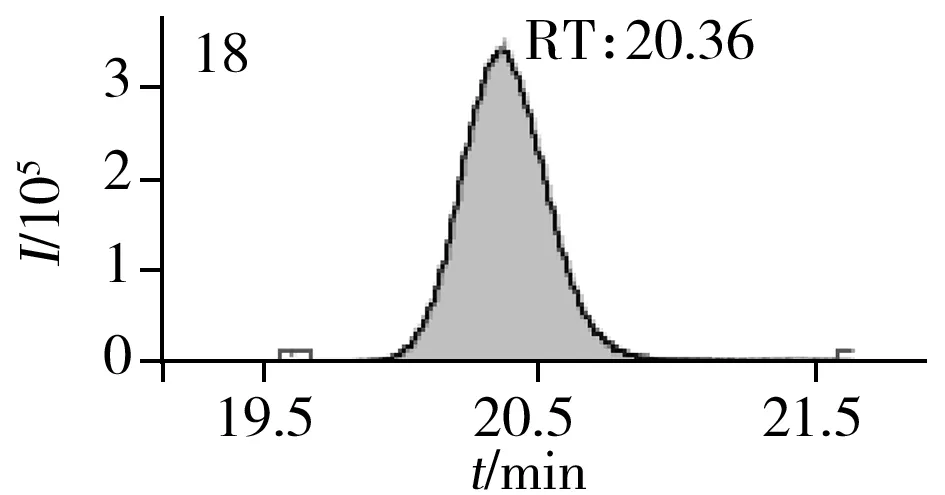
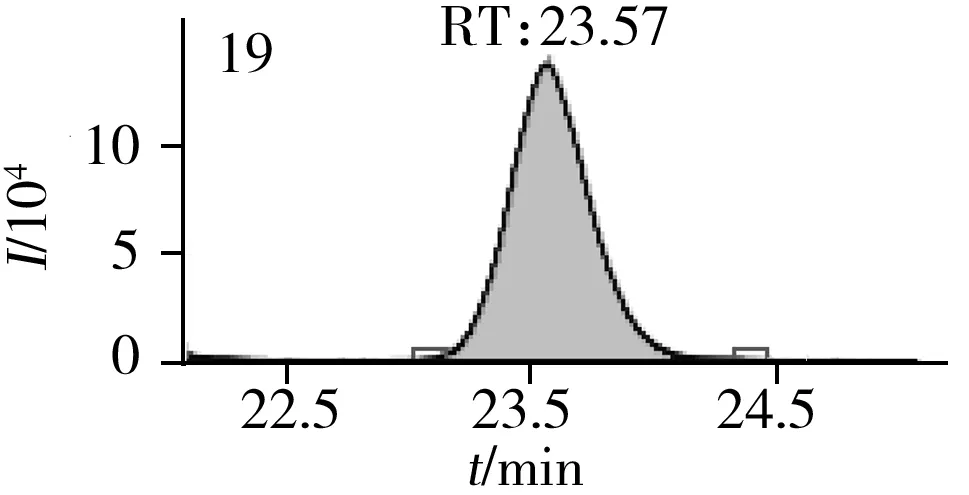
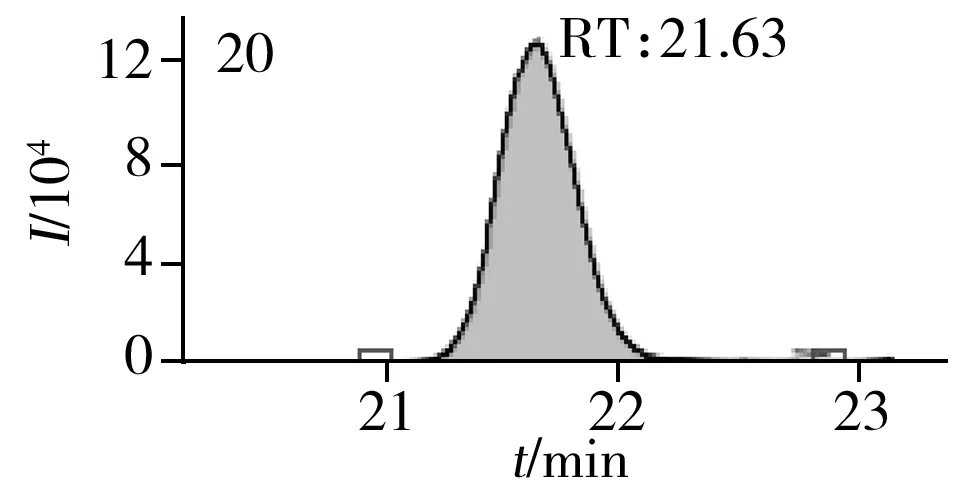
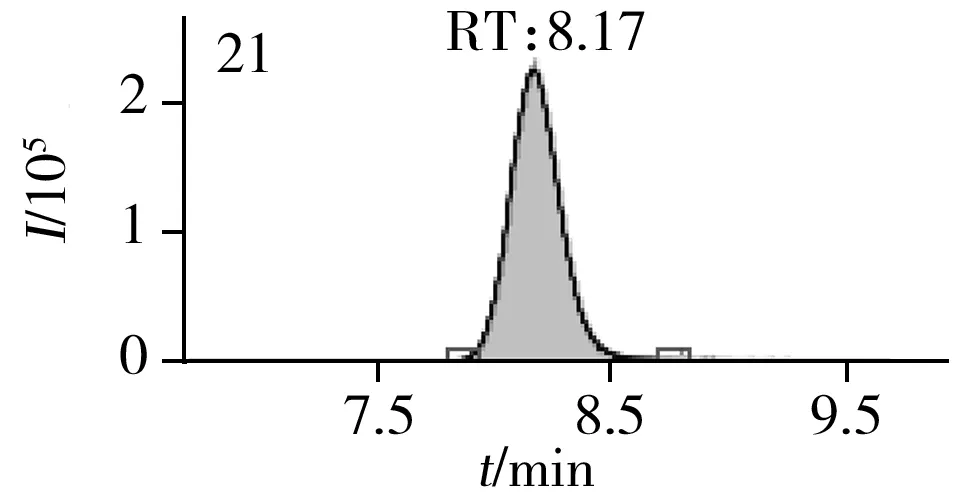
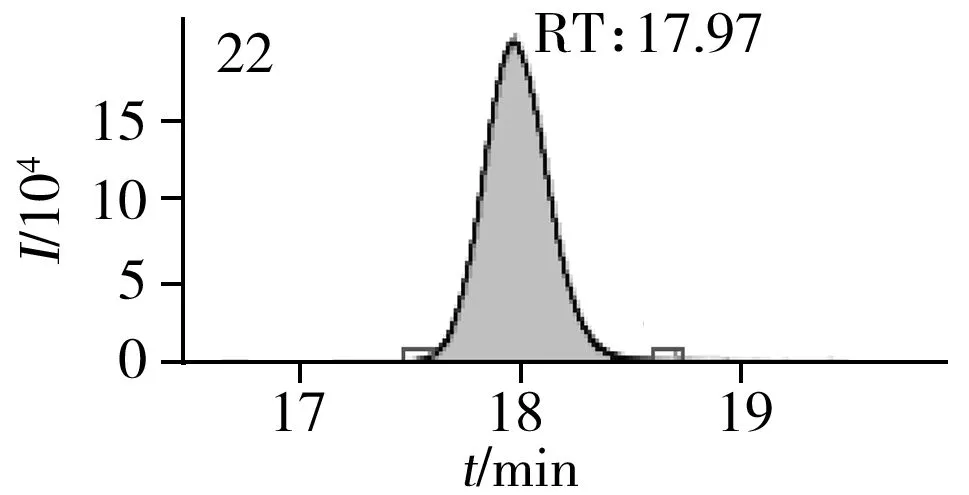
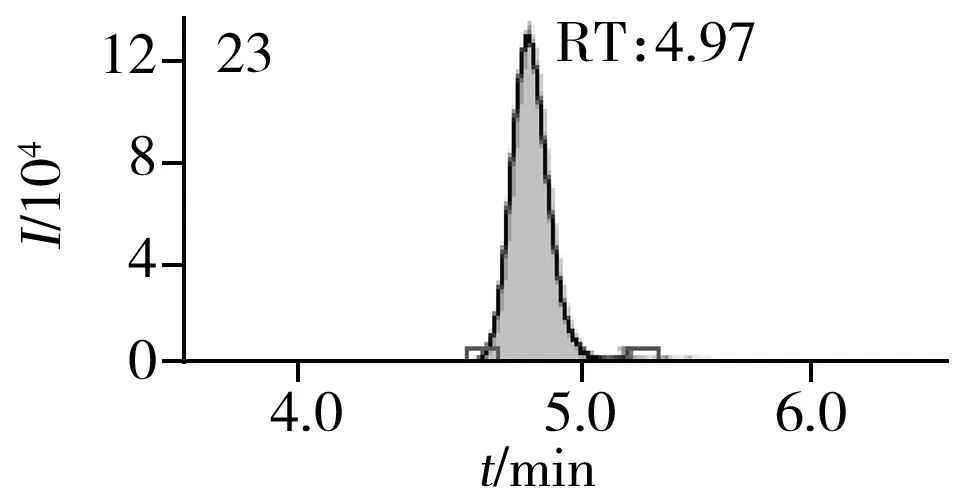
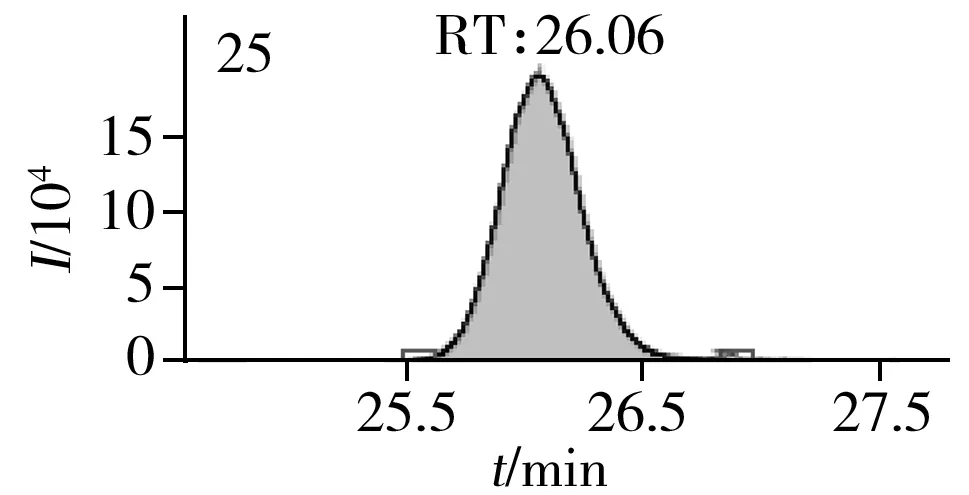
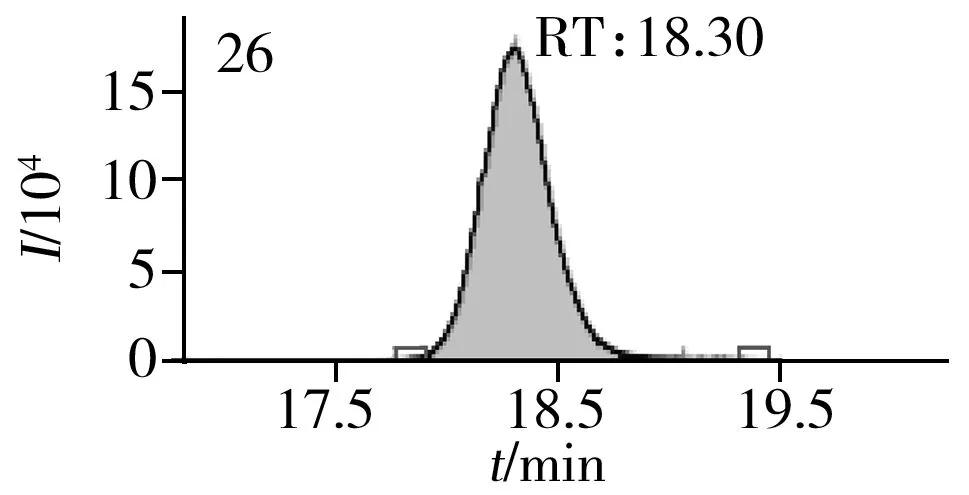
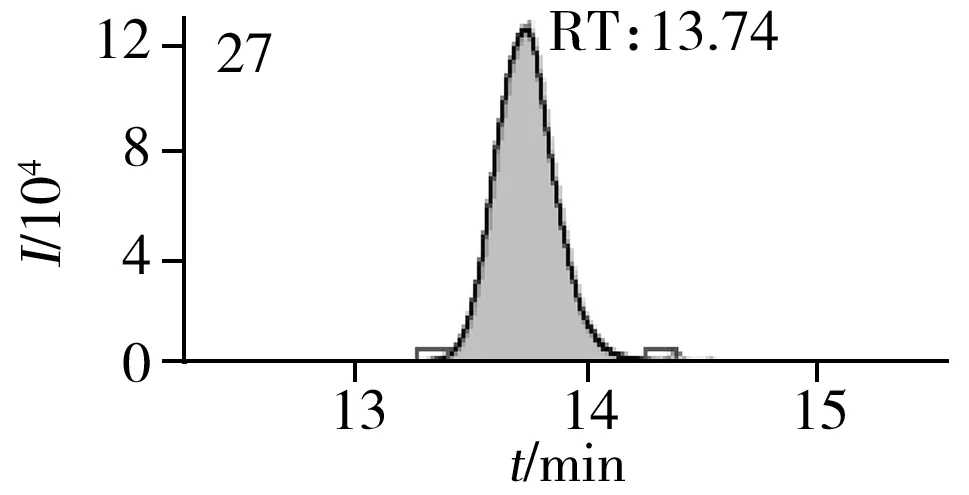
图2 止咳水基质加标样品(10.0 μg/L)的MRM色谱图Fig.2 MRM chromatograms of the spiked(10.0 μg/L) cough syrup samples the peak numbers denoted were the same as those in Table 1
2.2 流动相的选择
实验对比了甲醇(含0.05%甲酸)-0.005 mol/L乙酸铵(pH 3.0)、甲醇(含0.1%甲酸)-0.005 mol/L乙酸铵(含0.1%甲酸)、乙腈(含0.1%甲酸)-0.005 mol/L乙酸铵(含0.1%甲酸)、甲醇(含0.1%甲酸)-0.1%甲酸水、乙腈(含0.1%甲酸)-0.05%甲酸水5种流动相的色谱分离效果。结果显示,相较于在流动相中加入0.05%甲酸,加入0.1%甲酸有利于提高分析物的离子化效率并改善色谱峰形,而加入乙酸铵可起到缓冲盐的作用。由于乙腈的洗脱能力较强,不利于4种同分异构体的分离,最终实验确定以甲醇(含0.1%甲酸)-0.005 mol/L乙酸铵(含0.1%甲酸)作为流动相,并优化了最佳洗脱程序。在“1.3”条件下,27种目标化合物均可得到较好的分离度和峰形。止咳水基质加标样品(质量浓度为10.0 μg/L)中27种目标化合物的MRM色谱图见图2。
2.3 样品前处理方法的优化
2.3.1 提取溶剂的选择根据溶剂性质、芬太尼类物质性质、样品基质特点和检测灵敏度的要求及浓缩需要,本方法选择乙腈水溶液作为提取溶剂。分别考察了50%乙腈水、75%乙腈水、100%乙腈作为提取溶剂时,固体、液体药物样品中27种目标化合物的回收率。结果表明,乙腈中加适量水可增加固体药物的溶解度,提高目标化合物的提取效率;但加入过多水分不利于样液的浓缩。综合考虑,选取2 mL 75%乙腈水+2 mL 乙腈为提取溶剂。
2.3.2 HLB净化柱洗脱液用量的选择HLB固相萃取柱填料是亲脂性二乙烯苯和亲水性N-乙烯基吡咯烷酮单体按一定比例组成的大孔共聚物。芬太尼类物质大多为弱极性,而固体类试样干扰物一般为淀粉、糊精、纤维素、色素以及固体赋型颗粒。本实验采用HLB固相萃取柱作为正相柱,吸附弱极性至中等极性的酸性、中性、碱性化合物以净化固体样品。
分别比较了洗脱液乙腈的不同用量(1、2、3、4、5 mL)对27种目标化合物回收率的影响。结果表明,乙腈洗脱量为4 mL时,27种目标化合物的总体回收率较好(为73.3%~83.3%),因此选择洗脱液乙腈的用量为4 mL。
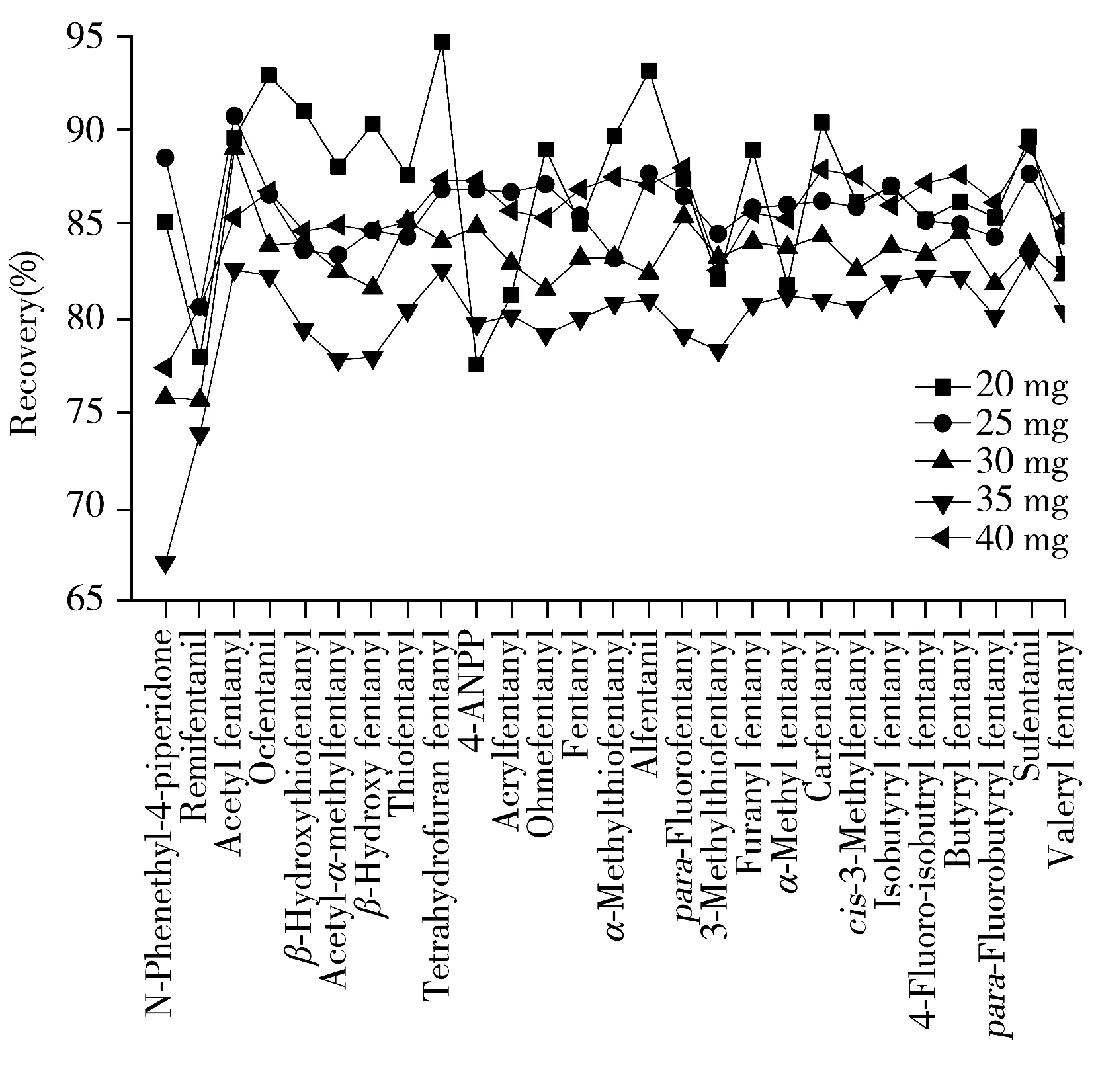
图3 PSA用量对目标化合物回收率的影响Fig.3 Effect of PSA dosage on recoveries of analytes
2.3.3 PSA吸附剂用量的选择PSA是在高纯硅胶基质上键合N-丙基乙二胺的极性吸附剂,无端基封尾,主要保留机理为弱阴离子交换(水溶性基质)、极性吸附(非极性有机基质)、螯合作用,能有效去除基质中的许多极性物质(如色素、有机酸、糖等)。液体类试样主要为有机酸、糖分、色素、维生素等,因此液体药物采用PSA净化。
分别比较了不同PSA用量(20、25、30、35、40 mg)对27种目标化合物回收率的影响。结果表明,在上述PSA用量下,除了N-苯乙基-4-哌替啶酮、4-苯胺基-N-苯乙基哌啶(4-ANPP)等的回收率略有偏差外,绝大部分化合物的回收率均大于70%(见图3)。综合考虑,选取PSA添加量为25 mg。
2.4 基质效应
基质效应(ME)是指不同的样品基质在质谱检测(特别是使用电离源)时由于离子化效应而产生的离子增强或抑制作用。其计算公式为ME=Ka/Kb,其中Ka为样品基质的校准曲线斜率,Kb为溶剂校准曲线的斜率。当ME接近100%时,表明无明显的基质效应;大于100%时,表明存在基质增强效应;小于100%,则说明存在基质抑制效应。实验考察了头痛粉、止咳水样品的基质效应,分别采用纯溶剂和基质提取液配制标准曲线工作溶液,按照本方法进行测定得到目标物的溶剂和样品基质匹配标准曲线方程,并计算基质效应。结果显示,头痛粉和止咳水样品的ME值为105%~130%,存在较低的基质效应。因此,本方法采用溶剂配制标准工作曲线溶液。
2.5 方法学验证
2.5.1 线性方程与定量下限在优化实验条件下,以50%乙腈水溶液稀释混合标准储备溶液,配成质量浓度为0.5、1.0、2.5、5.0、10.0、25.0、50.0 μg/L的混合标准工作溶液,采用本方法进行测定,并以峰面积对各组分的质量浓度绘制工作曲线。结果表明,27种目标化合物的质量浓度在0.5~50.0 μg/L范围内与其定量离子的响应峰面积呈良好线性关系,相关系数(r2)均大于0.99(见表2)。
基于回收率和相对标准偏差(RSD)满足欧盟SANTE/11813/2017要求的最低加标水平[16],以及加标样品的定量离子对色谱峰信号10倍信噪比(S/N)的要求,并结合国内外的残留限量要求,确定27种目标化合物在固体药物中的定量下限均为10.0 μg/kg,液体药物中均为10.0 μg/L。
2.5.2 准确度与精密度采用空白的头痛粉和止咳水作为验证基体,加标水平为10.0、20.0、50.0 μg/kg(μg/L),每个水平做6个平行。按本方法进行测定,外标法定量,计算每种化合物的平均回收率及RSD。结果表明,27种芬太尼类物质在头痛粉中3个加标水平下的平均回收率为84.8% ~106%,RSD为1.1% ~7.8%;在止咳水中的平均回收率为86.9% ~109%,RSD为0.86% ~8.5%(见表2)。
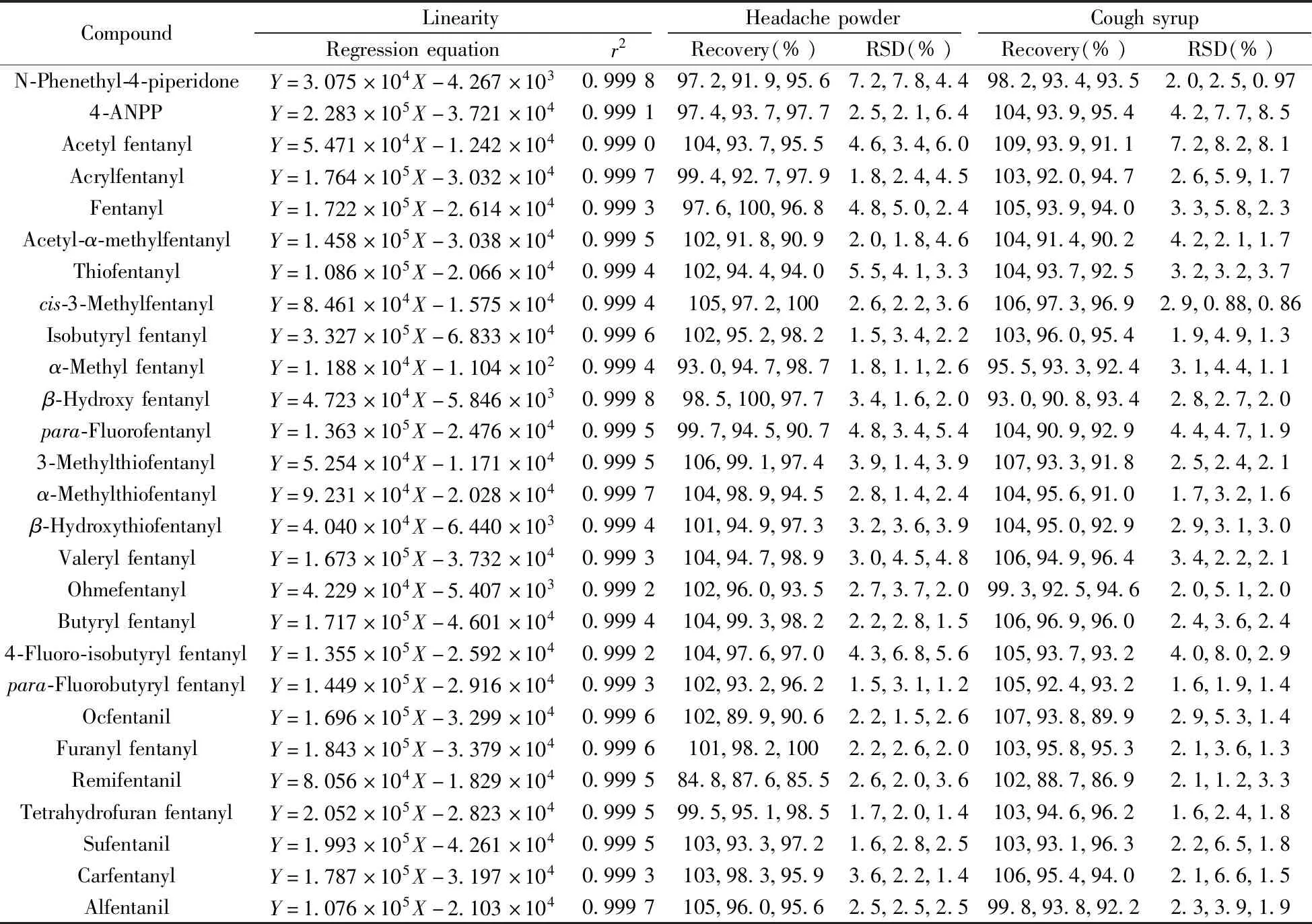
表2 27种芬太尼类物质的线性方程、相关系数、回收率及相对标准偏差(n=6)Table 2 Regression equations,correlation coefficients(r2),recoveries and relative standard deviations of 27 compounds(n=6)
Y:peak area;X:mass concentration,μg/L
2.6 实际样品检测
应用所建立的分析方法对3份芬太尼注射液样品进行检测,均检出高浓度芬太尼,质量浓度分别为47.1、47.8、48.1 mg/L。
3 结 论
本文采用75%乙腈水溶液结合乙腈提取固体和液体药物中27种芬太尼类物质,固体药物提取液经HLB固相萃取柱净化,液体药物提取液经QuEChERS法净化后,采用液相色谱-串联质谱测定。该法操作简便,耗时短,溶剂用量少,灵敏度高,稳定性好;具有较高的回收率、良好的精密度和较低的定量下限,适用于头痛粉、止咳水等药物中芬太尼类物质的定性及定量检测,满足公安缉毒、刑侦及相关检测部门对芬太尼监控的检测技术要求,具有迫切的现实应用价值。
