原发性肝肉瘤样癌误诊为肝脓肿1例报告
2020-02-08钱晓晖高炳强王伟林
钱晓晖,高炳强,王伟林
浙江大学医学院附属第二医院 肝胆胰外科,杭州 310009
原发性肝肉瘤样癌(primary hepatic sarcomatous carcinoma, PHSC)是一种原发于肝脏的罕见恶性肿瘤,其组织学形态类似于梭形细胞肉瘤,其发病率约占肝脏恶性肿瘤的0.2%[1]。临床上常因对该疾病认识不足而误诊,导致延误患者治疗。
1 病例资料
患者男性,56 岁,因“上腹部隐痛伴反复发热1个月” 于2019年2月18日在本院第1次就诊住院。患者于1个月余前无明显诱因出现右上腹部隐痛,不伴腰背放射痛,反复发热,最高39.2 ℃。患者至当地医院就诊,肝脏平扫CT示脓肿较囊肿可能性大。当地医院予抗感染治疗,患者发热症状缓解,仍偶有上腹部隐痛,为求进一步诊治,遂至本院治疗。门诊拟“肝脓肿”收入本院。既往史: 乙型肝炎病史1年余,口服拉米夫定片1次/d,每次1片抗病毒治疗。查体: 肝区压痛,无反跳痛,其余查体无阳性体征。实验室检查: WBC 10.1×109/L,中性粒细胞百分比 91%,肝功能指标及肿瘤标志物无异常。肝脏超声造影示:右肝高回声团块,增强后病灶周边不均匀增强,中央不规则无增强区。考虑肝脓肿,不除外肝细胞癌。肝脏增强MRI示:肝Ⅳ段见较大异常信号肿块影,T1像呈不均匀低信号,T2像呈不均匀高信号,见包膜,病灶周围肝实质片状略长T2信号水肿带,弥散部分受限,增强肿块内未见明显强化,包膜呈渐进性强化,可见分隔(图1)。考虑肝脓肿,不除外胆管细胞癌。遂行第1次肝活组织检查术, B超引导下未见明显液化, 未穿出脓液。病理回报:肝组织见凝固性坏死,并见假小叶形成,小叶间纤维组织增生,伴小胆管增生,未见肿瘤细胞。建议再次穿刺。遂行第2次肝活组织检查术, B超引导下见肝内明显液化灶,予置管引流出乳白色浓稠脓液,留取5 ml脓液细菌培养未见细菌生长。病理回报:见明显增生纤维组织,并见灶状急性慢性炎症细胞浸润,小胆管增生显著。患者在住院期间接受二线抗菌药及保肝治疗, 腹痛症状缓解, 体温降至正常。因患者目前无明确肿瘤证据,遂予出院。出院后20余日后,患者再次发烧,最高39.2 ℃,遂再次入本院。实验室检查:WBC 12.5×109/L,中性粒为主;C反应蛋白32 mg/L;降钙素原正常。待高热时行血培养阴性。肝脏增强CT可见:肝Ⅴ~Ⅷ 段多房样低密度灶,增强后边缘轻度延迟强化,门静脉右支栓塞(图2)。考虑肝脓肿;胆管细胞癌待排查;门静脉右支栓塞,怀疑菌栓。遂行第3次肝活组织检查术,病理示:低分化癌。免疫组化示: CK(AE1/AE3)弥漫弱阳性、Vimentin弥漫阳性、CK7阴性、hepPar-1阴性、AFP阴性、GPC3阴性、Arginase-1阴性、CD34阴性(图3)。患者最终诊断为PHSC,经科室讨论,患者目前暂无手术机会,予白蛋白紫杉醇+吉西他滨方案化疗。患者接受4次化疗后复查AFP 65 ng/ml,CEA 6.1 ng/ml, CA125 57 U/ml。肝脏MRI示:肝Ⅴ~Ⅷ 恶性肿瘤,较前片病灶增大。因患者化疗效果不佳且出现化疗不良反应,遂改予特瑞普利单抗免疫治疗+安罗替尼靶向治疗。2周后再次随访,患者死亡。
2 讨论
PHSC是由恶性上皮性成分和梭形细胞肉瘤样成分构成的罕见肝脏原发性恶性肿瘤,其本质是一种特殊类型的癌而非肉瘤或癌肉瘤, 其组织学来源一直存有争议。目前,多数文献认为PHSC的肉瘤成分由癌细胞转化而来,并非真正的上皮和间叶组织[2]。既往研究[3-5]表明,复发性介入治疗如经导管动脉化疗栓塞术、射频消融术和经皮乙醇注射可能是主要的癌向肉瘤样转化的原因。
PHSC在临床诊断中主要与肝癌及肝脓肿鉴别[3,6]。PHSC与肝细胞癌的发生在年龄和性别的分布上无显著差异,且多数PHSC患者也存在与HCC类似的肝炎肝硬化病史,但PHSC患者血清中AFP和CA19-9水平往往不高,肝功能也无明显损害,这些特征可与常见的肝癌进行鉴别。PHSC的临床表现不具特异性,腹痛和发热为常见两大表现,部分PHSC表现为囊性病灶,导致其与肝脓肿难以鉴别,而耽误诊治。PHSC中包含肉瘤与癌2种成分,影像学上因两者所占比例不同呈现多种表现。多数情况下,肿瘤呈巨块状,其中心常常坏死和出血,而外周为具有纤维基质的存活的癌组织。CT表现为多囊性混杂密度包块,增强时实质部分强化,多在分隔处强化,中心坏死区不强化,延迟期外周继续增强。MRI示,T1呈现低信号,中心坏死区呈现更低信号,T2以高信号团块为主,增强表现与CT类似[7]。而普通肝细胞癌CT平扫时显示病灶以低密度为主,坏死部分表现更低密度,增强时病灶具有典型的“快进快出”特点。
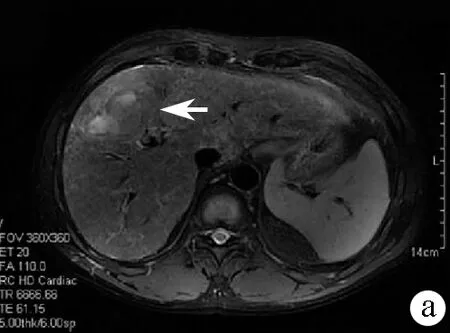
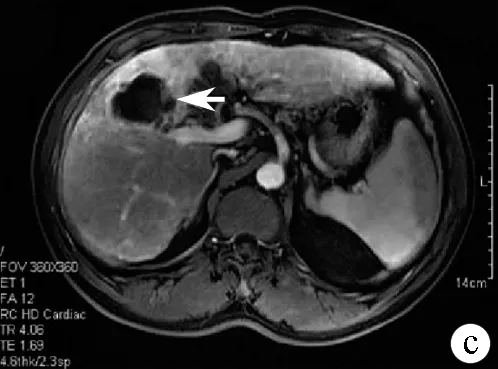
注:a,肝内病灶呈混杂略高信号(箭头);b,增强后动脉期呈边缘增强中心坏死区低信号(箭头);c,静脉期呈边缘增强中心坏死区低信号(箭头)。
图1MRI检查结果(T2WI)
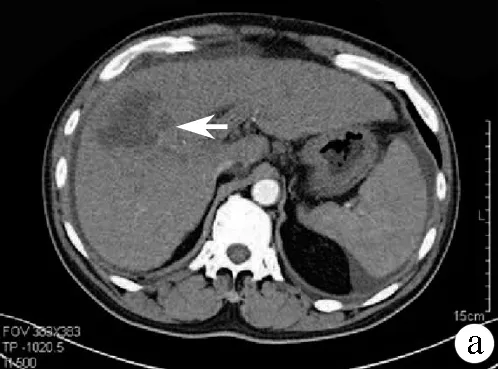


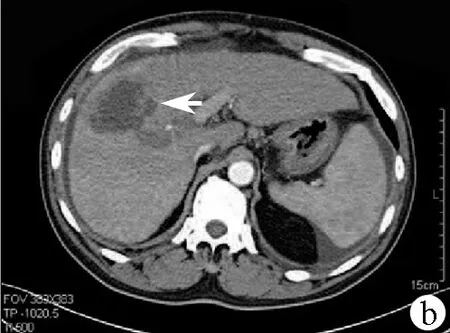
注:a,增强动脉期示肝内病灶呈不均匀强化(箭头);b,静脉期示病灶呈边缘强化,门静脉右支栓子(箭头);c,延迟期示病灶呈边缘强化,门静脉右支栓子(箭头)。
图2CT检查结果
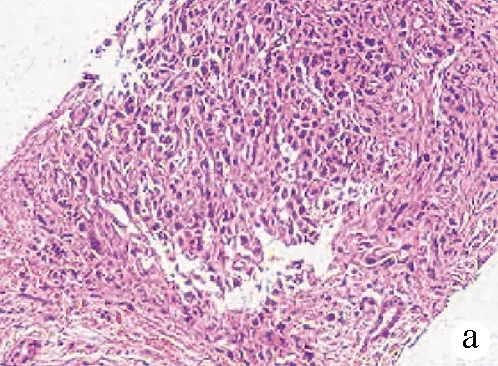
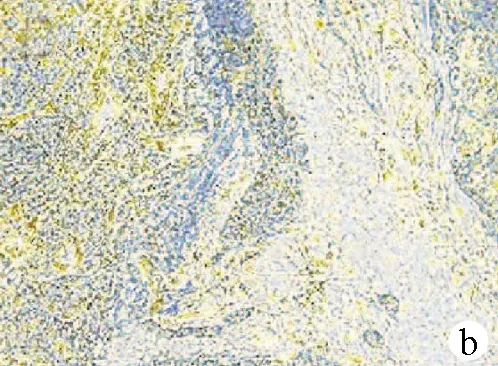
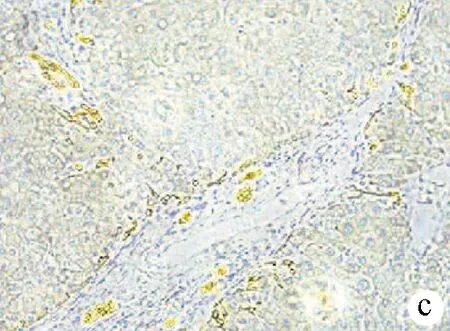
注:a,梭形细胞肉瘤样成分,伴有核分裂(HE染色,×100); b,CK(AE1/AE3)弥漫弱阳性(免疫组化,×100); c,Vimentin弥漫阳性(免疫组化,×100)。
图3病理结果
病理学检查是确诊 PHSC的主要方法,在组织学中可见标本中明确的恶性上皮成分和梭形细胞肉瘤样成分及2种成分的移行区;且肿瘤中肉瘤样细胞应该>50%,否则诊断相应癌伴肉瘤样变更为准确;免疫组化中,肿瘤上皮细胞性标记阳性表达,同时肉瘤样成分标志物 Vimentin 阳性[8]。本例患者诊断为PHSC 的主要依据: (1)无抗肿瘤治疗经历;(2)肝脏病灶在抗感染治疗下进展,且影像学检查显示门静脉栓子;(3)病理组织学检查见恶性上皮性及梭形细胞肉瘤样成分,且两者形态之间存在移行过渡;(4)免疫组化示CK(AE1/AE3) 弥漫弱阳性,Vimentin呈弥漫阳性。
结合袁俊清等[9]的研究,总结本次将PHSC误诊为肝脓肿的原因主要有以下几点:(1)该例患者早期影像学检查提示病灶为囊性病变,考虑到囊腔壁量少,而其囊腔内为坏死后液化的组织,无法用来穿刺活组织检查,导致其比实性组织的穿刺更难判断[10];(2)PHSC囊壁内肉瘤细胞和癌细胞分布具有不均匀性,不同部位的肿瘤间变程度有差异,穿刺活组织检查中囊壁组织量较少,难以发现典型的肉瘤细胞、病理性核分裂等明确肿瘤证据;(3) PHSC无特异性的临床表现,肿瘤标志物未见异常,影像学检查考虑肝脓肿可能性大。
目前,关于PHSC的治疗均为个案报道或病例系列报道,现一般认为肝脏部分切除和肝移植是PHSC的首选方式[11]。PHSC患者术后比普通肝癌的患者更有可能发生局部复发和远处转移,对于Ⅲ~Ⅳ期PHSC患者,死亡均发生在确诊后的2~5个月内[11]。对于首次发现即失去手术机会的患者,目前无一线推荐的非手术治疗方案[12]。Tsuji等[3]报道1例手术切除术后的患者接受辅助性依托泊苷、表柔比星和顺铂化疗,患者获得12个月的无瘤生存期。本例患者由于早期诊断为肝脓肿,而PHSC进展快,侵袭性强,患者得到确诊时已不适合手术,遂接受化疗,患者病情仍未获得有效控制,最后尝试免疫治疗及靶向治疗,仍未获得明显的生存期延长,最终患者在发病后4个月死亡。在治疗过程中发现,患者初诊时水平正常的肿瘤标志物(如AFP、CEA)出现异常上升。这可能与肿瘤的进展、转移有关,表明PHSC治疗过程中,患者血清肿瘤标志物的变化具有判断患者预后的潜能。
本例报告的不足之处在于患者在抗肿瘤治疗后,肿瘤标志物水平上升的情况下,未能再次探究患者目前的病理情况,观察肿瘤组织成分的变化,以此来探究PHSC肿瘤组织成分变化与血清学肿瘤标志物的联系。
