ZnFe2O4/NG光催化同时脱除亚硝态氮与氮氨的研究
2019-11-25叶嘉刘守清
叶嘉,刘守清
(苏州科技大学化学生物与材料工程学院,江苏苏州215009;江苏省环境功能材料重点实验室,江苏苏州215009)
传统的脱氮技术是利用微生物的硝化与反硝化作用处理污水。硝化法是在厌氧条件下通过硝化细菌将氨氮(Ammonia-N,NH3-N,简称为AN)转化为亚硝酸根和硝酸根;反硝化法是在好氧条件下将亚硝酸根和硝酸根转化为氮气放出,从而实现脱氮。但由于微生物受环境温度、泥年、营养成分等因素影响较大,当废水水质无法满足微生物正常生长条件时,比如重金属废水[1]、高浓度氨氮废水[2]、无碳源污水[3]及含抗生素的废水等均不适于生物脱氮,需要开发新的脱氮技术。笔者曾经报道了光催化氧化氨氮脱氮的方法[4-8],但光催化同时脱除亚硝态氮(Nitrite-N,NO2--N,简称为NN)和氨氮的研究则很少报道[9]。笔者用ZnFe2O4作为主体催化剂,通过负载氮杂石墨烯(NG)制备得到了铁酸锌/氮杂石墨烯(ZnFe2O4/NG)杂化光催化剂。利用该杂化光催化剂,开展了光催化同时脱除亚硝酸根和氨氮的研究,优化了同时脱除亚硝态氮与氨氮的工艺条件。
1 实验部分
1.1 化学试剂
Fe(NO3)3·9H2O购自天津市大茂化学试剂厂;Zn(NO3)2·6H2O和KMnO4购自南京化学试剂厂;NaOH和石墨粉购自中国上海试剂总厂;CO(NH2)2购自上海埃彼化学试剂有限公司。
1.2 氧化石墨烯的制备
首先采用改进的Hummers法合成氧化石墨烯(GO)[10],准确称量1.0 g石墨粉(用5%稀盐酸洗涤2-3次,再用去离子水洗至中性,烘干得到)于500 mL烧杯中,置入水浴锅中,在冰水(0℃)环境下持续搅拌。准确量取浓硫酸15.0 mL缓慢滴加至石墨粉悬浊液中,混合均匀。准确称取高锰酸钾3.0 g,缓慢加入上述混合液中。搅拌30 min,控制温度不超过20℃。准确量取去离子水45 mL,缓慢滴加入上述混合液,待搅拌均匀,再缓慢滴加过氧化氢溶液(10%,150 mL),室温下搅拌24 h。静置,洗涤至中性,取下层混合液,在60℃真空干燥箱中干燥24 h,即得GO。
1.3 NG的制备
准确称取80 mg的GO,超声分散于50 mL去离子水中。准确称取24.0 g尿素加入到上述溶液,混合均匀后加水至80 mL,超声溶解60 min移至高压水热反应釜中,在170℃下密闭加热12 h。待样品冷却到室温,用去离子水洗涤、过滤,在60℃真空干燥箱中干燥24 h,即得NG。
1.4 ZnFe2O4/NG的合成
准确称取1.785 0 g Zn(NO3)2·6H2O(6 mmol)和4.848 0 g Fe(NO3)3·9H2O(12 mmol)磁力搅拌下溶于20.0 mL去离子水中。称量72.3 mg NG(ZnFe2O45.0 wt%)溶于10 mL去离子水中超声分散1 h,将锌盐与铁盐混合液加入到NG悬浮液中,磁力搅拌1 h。准确称量2.40 g氢氧化钠溶于10 mL去离子水中,缓慢滴加到上述悬浮液中,持续搅拌1.5 h。最终,溶液总体积控制在60 mL左右,将悬浮液转移到100 mL不锈钢高压反应釜中,置于烘箱升温至180℃保持8 h。自然冷却样品到室温,然后洗涤、过滤,在60℃真空干燥箱中干燥24 h,即得ZnFe2O4/NG杂化光催化剂。类似地,可制得ZnFe2O4。
1.5 催化剂表征
X-射线粉末衍射法(XRD,X-射线粉末衍射仪,型号:D/max 2500 pC型)表征催化剂的晶相结构。X射线源是Cu-Kα,辐射波长为0.154 nm,管电压和管电流分别为40 kV、40 mA。透射电子显微镜(TEM,型号:TecnaiG220型,美国FEI公司)用于表征催化剂形貌和颗粒大小。紫外-可见漫反射光谱法(UV-Vis DRS,紫外-可见漫反射光谱仪,型号:岛津UV 3600plus型)测定样品的漫反射光谱。在633 nm激光激发下测定样品的拉曼光谱(拉曼光谱仪,型号:LabRam HR800型)。
1.6 光催化脱氮实验
首先通过N2鼓泡30 min去除水中溶解氧形成厌氧环境,加入50 mg·L-1NO2--N和100 mg·L-1NH3-N后,经1 mol·L-1NaOH调节反应液的pH=9.5左右,再加入0.375 g催化剂。以300 W汞灯作为光源,光催化实验在光催化反应仪(BL-GHX-V,上海比郎仪器有限公司)中进行,如图1所示,通过石英冷阱维持反应温度在25℃左右。第一阶段厌氧光催化反应3 h,隔30 min,取3 mL溶液测定亚硝态氮、氨氮与硝态氮的浓度。检测过程中,亚硝态氮、硝态氮、氨氮三种物质分别检测,避免相互干扰。亚硝态氮的分析测定采用N-(1-奈基)乙二胺光度法,硝态氮的分析测定采用紫外分光光度法,氨氮采用国标纳氏试剂比色法。为了实现亚硝态氮与氨氮的完全脱除,将剩余的氨氮溶液曝气30 min形成好氧环境,进行第二阶段的光催化反应,同时用氢氧化钠维持pH=9.5左右,脱除残余的氨氮,以实现总氮的完全脱除。
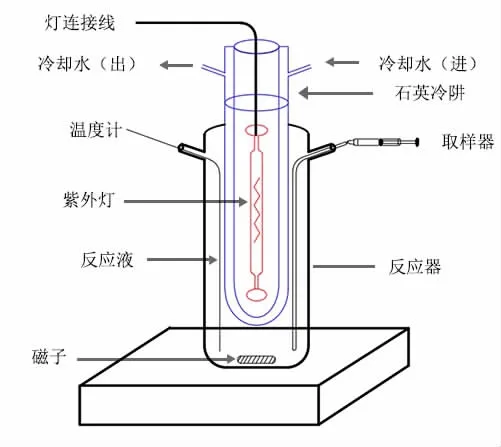
图1 光催化同时脱除亚硝态氮与氨氮的实验装置
2 结果与讨论
2.1 X-射线粉末衍射表征
图2为NG、ZnFe2O4、ZnFe2O4/NG的XRD衍射图谱。曲线a为NG的衍射图,曲线b在2θ=29.84、35.14、42.77、53.06、56.59、61.98、70.13、73.58和78.35°处的衍射峰分别对应ZnFe2O4的衍射面(220)、(311)、(400)、(422)、(511)、(440)、(620)、(533)和(444),与ZnFe2O4标准图谱(JCPDS22-1012)一致。比较曲线(b)和(c)可以看出,ZnFe2O4/NG的衍射图谱与ZnFe2O4基本一致,同时在ZnFe2O4/NG衍射图中在26.2°处观察到NG的(002)面衍射峰,表明NG较好地分散于催化剂中。
根据曲线b和c中(311)晶面衍射峰的半峰宽,按照Scherrer公式

可以计算出ZnFe2O4/NG、ZnFe2O4的粒径大小。其中D为晶粒的平均粒径;K为晶粒形状因子,取0.89;λ为X射线波长,取0.154 nm;W为衍射峰的半峰宽;θ为衍射角。通过计算得到ZnFe2O4/NG、ZnFe2O4的粒径大小分别为6.9、7.2 nm。与TEM观察结果一致。
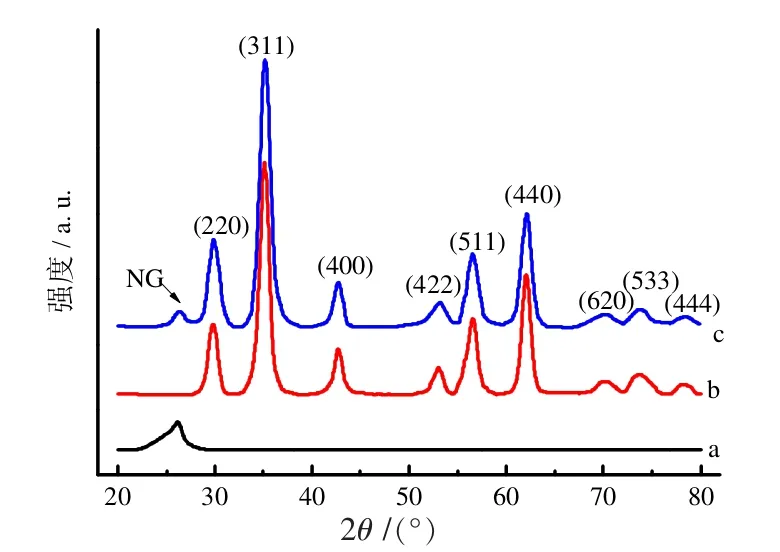
图2 XRD图谱(a:NG;b:ZnFe2O4;c:ZnFe2O4/NG)
2.2 透射电镜
图3为NG、ZnFe2O4、ZnFe2O4/NG不同分辨率下的透射电镜图。通过图3a可看出NG为二维层状结构。图3b中铁酸锌呈颗粒状,尺寸均匀约6-9 nm左右,与XRD分析结果一致,同时ZnFe2O4较好的分布于NG表面。图3c显出了清晰地晶格条纹,其晶格条纹间距为0.25 nm,对应于ZnFe2O4(JCPDS22-1012)(311)面的条纹间距。

图3 透射电镜图(a:NG;b和c:ZnFe2O4/NG)
2.3 拉曼光谱表征
图4为NG、ZnFe2O4和ZnFe2O4/NG的拉曼光谱图。图4a可见NG的D带和G带,图4b可明显观察到三个特征峰:339、474、665 cm-1,分别对应于尖晶石结构的经典振动模式[11-12],进一步证明ZnFe2O4为尖晶石结构。在1 567 cm-1和1 334 cm-1观察到两个特征峰,分别表示石墨烯的G带和D带,1 567 cm-1(G带)为石墨烯E2g振动模式,1 334 cm-1(D带)与缺陷和石墨结构的不规整有关[12-13]。图4c中观察到ZnFe2O4与NG的拉曼峰很好的结合在一起,进一步证实了ZnFe2O4杂化催化剂中NG的存在。

图4 拉曼光谱图(a:NG;b:ZnFe2O4;c:ZnFe2O4/NG)
2.4 紫外可见漫反射光谱表征
图5为ZnFe2O4/NG和ZnFe2O4样品的DRS光谱。图5A为紫外-可见漫反射光谱,通过图5A可以观察到,ZnFe2O4/NG在大于530 nm的波长范围内出现了吸收增强现象,这意味着NG的负载提高了入射光子的吸收效率,拓宽了对可见光的响应范围,有效地抑制光生电子与光生空穴的复合,大大改善了太阳辐照的利用率。
由Tauc公式可计算ZnFe2O4/NG和ZnFe2O4的禁带宽度

其中,A为比例常数;α为吸收系数;ν为光的频率;h为普朗克常数;Eg为半导体禁带宽度。
图5B为对应的(αhν)2与hν关系图,由图5B可得,ZnFe2O4/NG和ZnFe2O4的禁带宽度分别为2.0、2.1 eV。ZnFe2O4催化剂负载氮杂石墨烯后,光谱吸收波长发生了红移且禁带宽度减小,因此,提高了对太阳能的吸收利用率。
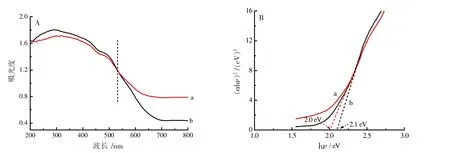
图5 紫外-可见漫反射光谱(A)、对应的(αhν)2与hν关系图(B)(a:ZnFe2O4/NG;b:ZnFe2O4)
2.5 光催化同时脱除亚硝态氮与氨氮
2.5.1 亚硝态氮与氨氮的同时脱除
图6为光照或暗反应或缺少一个组分情况下亚硝态氮与氨氮的脱除曲线,图6 A和6B分别为NN和AN的脱除曲线。以1.5 g·L-1ZnFe2O4/NG(NG 5.0 wt%)为催化剂,溶液体积为250.0 mL,NN和AN的初始浓度分别为50 mg·L-1、100 mg·L-1,pH=9.5。图中曲线对应条件为:(a)NN+AN+ZnFe2O4/NG+光照;(b)NN+AN+光照;(c)NN+ZnFe2O4/NG+光照;(d)NN+AN+ZnFe2O4/NG;(e)AN+ZnFe2O4/NG+光照。图6A(a)、6B(a)显示在催化剂存在下,50 mg·L-1亚硝态氮和100 mg·L-1氨氮混合液光照3 h后,亚硝态氮和氨氮脱除率分别为90.95%和62.84%。而曲线6A(b)、6B(b)表明,无催化剂时,即使有光照,亚硝态氮与氨氮的脱除率仅为20.53%和18.75%。这显示催化剂具有光催化活性,可同时脱除亚硝态氮与氨氮。当反应体系缺少氨氮时,仅有1.03%亚硝态氮被催化剂吸附,如图6A(c)所示。而当反应体系中没有亚硝态氮时,催化剂仅吸附11.96%的氨氮,如图6B(e)所示。在无光照条件下,即使存在光催化剂,也仅有少量的亚硝态氮与氨氮被吸附,如图6A(d)和6B(d)所示。对比可知,ZnFe2O4/NG催化剂在厌氧条件下,可光催化同时脱除亚硝态氮与氨氮。

图6 NN和AN的脱除曲线
2.5.2 pH值的影响
以1.0 mol·L-1NaOH调节溶液的pH值,在50 mg·L-1亚硝态氮和100 mg·L-1氨氮的混合溶液中加入0.375 g ZnFe2O4/NG(NG 5.0 wt%),在不同pH值下白光照射3 h,亚硝态氮和氨氮的脱除效果如图7所示。亚硝态氮和氨氮的脱除率随着溶液pH值的升高而增加。当pH值为9.50时,亚硝态氮和氨氮脱除率达到最佳值,分别为90.95%、62.84%。
2.5.3 催化剂用量的影响
在pH=9.5,亚硝态氮50 mg·L-1,氨氮100 mg·L-1的混合液中,分别加入0.125、0.25、0.375、0.5 g ZnFe2O4/NG杂化催化剂,白光照射3 h,亚硝态氮与氨氮的脱除效率如图8所示。随着催化剂用量的不断增加,亚硝态氮与氨氮的脱除率也随之增加。当催化剂用量为1.5 g·L-1时,亚硝态氮与氨氮的脱除率达到最佳值,分别为90.95%和62.84%。当催化剂用量继续增加时,脱除率反而降低。分析原因,可能由于催化剂用量过多,产生团聚现象,导致脱除率降低。

图7 pH值对亚硝态氮(A)和氨氮(B)脱除效率的影响(50.0 mg·L-1 NN+100.0 mg·L-1 AN+0.375 g·L-1 ZnFe2O4/NG,溶液体积为250.0 mL)

图8 催化剂用量对亚硝态氮(A)和氨氮(B)脱除效率的影响(50.0 mg·L-1 NN+100.0 mg·L-1 AN+ZnFe2O4/NG,溶液体积为250.0 mL,pH=9.50)
2.5.4 NG负载量的影响
以负载不同比例NG(0%~9%)的ZnFe2O4/NG为催化剂,在pH值为9.5,厌氧条件下,白光照射3 h,光催化同时脱除亚硝态氮和氨氮的效率如图9所示。纯的铁酸锌光催化同时脱除亚硝态氮与氨氮的脱除率为81.19%、54.70%。相同实验条件下,亚硝态氮与氨氮的脱除率随着NG配比的增加而提高。NG负载量为5%时,亚硝态氮与氨氮的脱除率达到最佳值,分别为90.95%和62.84%。

图9 NG负载量对亚硝态氮(A)和氨氮(B)脱除效率的影响(50.0 mg·L-1 NN+100.0 mg·L-1 AN+1.5 g·L-1 ZnFe2O4/NG,溶液体积250.0 mL,pH=9.5)
2.5.5 氨氮初始浓度对亚硝态氮脱氮率的影响
通过控制pH值(9.50)、催化剂用量(1.5 g·L-1)、NG负载量(5%)以及催化反应时间(3 h)等实验条件下,探讨氨氮初始浓度对亚硝态氮脱氮率的影响,如图10所示。实验结果表明,亚硝态氮的脱氮率随着氨氮初始浓度的增加而增大。当氨氮初始浓度为100 mg·L-1时,亚硝态氮的脱除率达90.95%。氨氮脱除率也有类似结果,当氨氮初始浓度为100 mg·L-1时,氨氮的脱除率达62.84%。

图10 氨氮初始浓度对亚硝态氮脱氮率(A)的影响及相应氨氮的脱氮率(B)(50.0 mg·L-1 NN+AN+1.5 g·L-1 ZnFe2O4/NG,溶液250.0 mL,pH=9.5)
2.5.6 催化剂稳定性及重复利用
图11为ZnFe2O4/NG杂化催化剂在白光照射下同时脱除亚硝态氮与氨氮的循环实验。经7次循环实验后,亚硝态氮的脱除率为87.28%。这说明ZnFe2O4/NG杂化催化剂稳定性良好,可回收利用。
2.5.7 完全脱氮
图12为光催化同时脱除亚硝态氮与氨氮的脱除率变化图。该实验设计分为两个阶段,第一阶段是在厌氧条件下进行光催化同时脱除亚硝态氮与氨氮的研究,脱除率分别为90.95%、62.84%。溶液中仍剩余37 mg·L-1左右的氨氮未被脱除。第二阶段是将溶液曝气30 min,继续上述反应脱除剩余氨氮。结果如图12所示,在光照第13小时后,亚硝态氮、氨氮和总氮的脱除率分别达到92.04%、89.44%和90.31%。在光催化反应过程中,未检测到硝态氮生成。

图11 催化剂循环利用试验图(50.0 mg·L-1 NN+100.0 mg·L-1 AN+1.5 g·L-1 ZnFe2O4/NG,溶液体积250.0 mL,pH=9.5)
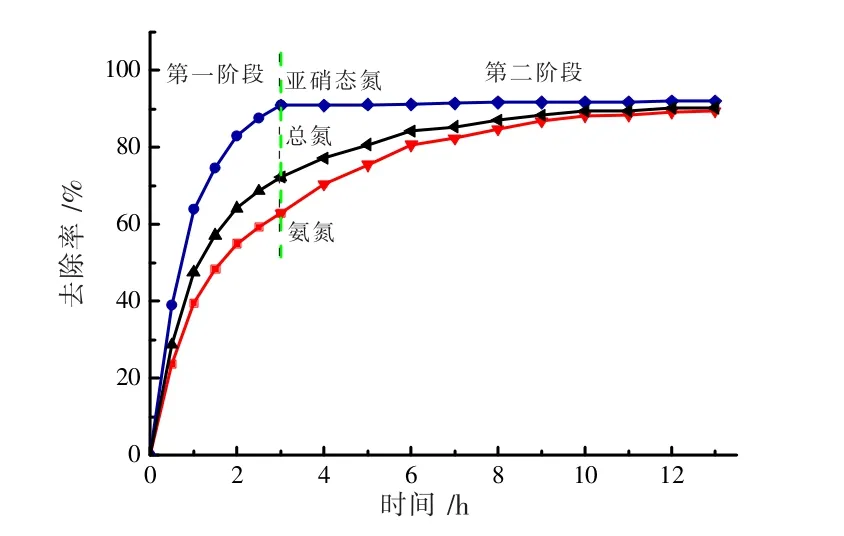
图12 光催化同时脱除亚硝态氮与氨氮的脱氮率变化曲线(50.0 mg·L-1 NN+100.0 mg·L-1 AN+1.5 g·L-1 ZnFe2O4/NG,溶液体积250.0 mL,pH=9.5)
2.5.8 反应机理
由于ZnFe2O4/NG禁带宽度为2.0 eV,其导带电位Ec=-0.9 V vs NHE[4],而亚硝酸根还原的电位1.52 V vs NHE,因此,光生电子可以还原亚硝酸根离子成为氮气;ZnFe2O4/NG的价带电位Ev=1.1 V vs NHE,氨氮的氧化电位为因此,光生空穴可以氧化氨氮为氮气。总反应式为

3 结语
采用水热法合成了ZnFe2O4/NG杂化光催化剂,进行了光催化脱除亚硝态氮与氨氮的实验。实验表明,在厌氧条件下,pH=9.5的亚硝态氮与氨氮混合溶液中,当ZnFe2O4/NG(NG 5.0 wt%)用量1.5 g·L-1,亚硝态氮与氨氮初始浓度分别为50、100 mg·L-1时,白光光照3 h,亚硝态氮与氨氮的脱除率达最大,分别为90.95%、62.84%。随后将溶液曝气30 min,继续光照10 h后,亚硝态氮、氨氮和总氮的脱除率分别达到92.04%、89.44%和90.31%,这说明ZnFe2O4/NG杂化催化剂对光催化脱除亚硝态氮与氨氮有潜在的应用价值。
