利用钢铁酸洗废液芬顿氧化降解溴氨酸水溶液
2019-11-07费学宁曹凌云
赵 倩,费学宁,,曹凌云
(天津城建大学a.材料科学工程学院;b.天津市化工废水源头减排与资源化工程技术中心,天津300384)
酸洗废液是在钢材加工过程中,利用酸的腐蚀性对钢材表面进行清洗的过程中产生的一类污染物.据统计,仅某地一家钢铁厂每年就产生近300 000 t 酸洗废液[1].不同的酸洗工艺以及不同的钢材都会影响酸洗废液的组分和含量[2-3].一般盐酸酸洗废液中主要含有一定浓度的酸和以铁为主的金属离子[4],部分废酸液中还含锌离子[4-5],其pH 约在0.2~3.0 之间[6],具有极强的酸性.
酸洗废液因酸性强,腐蚀性大,含有大量金属离子,直接排放不仅会污染环境,危害人体健康,还造成资源浪费.传统上采取的中和法处理酸洗废液,具有工艺简单、操作容易、成本较低等优点,但处理后产生大量的中和废渣,直接堆积不仅会占用土地资源,还会污染土壤和地下水资源,同时造成酸洗废液中有价值的酸和铁的资源浪费[7].近年来,酸洗废液的合理处理和资源化利用成为备受关注的热点问题,也是符合现代钢铁生产绿色化和可持续发展的客观要求.由于酸性含铁废水种类的多样性和成分的复杂性,使其处理和应用过程具有极高的难度,涉及多学科技术领域.对此,国内外学者在对钢铁酸洗废液中的酸和铁的资源化回收及利用方面,做出了许多卓有成效的成果,探究了直接利用钢铁酸洗废液制备高附加值产品的可行技术,以实现钢铁酸洗废液资源化处理效益的更大化,并进行了一定的推广实践.如利用酸洗废液制备成铁盐混凝剂[8-10]和芬顿试剂[11]用于污水处理;提取出酸洗废液中的铁制备铁系氧化物用于无机颜料[12-13]、磁性材料[14];还可分离出废酸中的游离酸回用于钢铁酸洗工序.本文利用酸洗废液的酸铁资源,辅以双氧水,构成Zn2+/Cl-等杂质离子共同存在条件下的芬顿体系,处理溴氨酸水溶液.采用响应面分析Box-Behnken(BB)设计法,探索最佳反应条件,探究杂质离子对芬顿体系处理溴氨酸水溶液的影响.
1 实验部分
1.1 主要试剂及实验仪器
试剂原料:天津市某钢铁厂酸洗废液(pH=1.99,含有Fe=129.5 mg/L,Zn=135 mg/L);30%过氧化氢,天津市化学试剂三厂;四水合氯化亚铁,分析纯,天津市化学试剂三厂;溴氨酸,分析纯,天津市大茂化学试剂厂;甲基橙,分析纯,北京化工厂;亚甲基蓝,分析纯,天津市基准化学试剂有限公司.
仪器:SP-3801 型原子吸收光谱,上海光谱仪器有限公司;TU-1900 型紫外-可见光分光光度计,北京普析通用仪器有限责任公司;(10~100)μL/(100~1 000)μL移液枪,北京波辉生物科技有限公司.
1.2 实验方法
用酸洗废液/H2O2体系Fenton 氧化降解模拟溴氨酸水溶液:
将一定量H2O2和酸洗废液加入到200 mL 的溴氨酸水溶液中,反应一定时间,测其ρ(吸光度).分别考察pH、H2O2用量和反应时间对溴氨酸脱色率的影响.
用纯Fe2+/H2O2体系Fenton 氧化降解模拟溴氨酸水溶液:
模拟酸洗废液Fe2+含量配制Fe2+溶液,将一定量H2O2和模拟Fe2+溶液加入到200 mL 的溴氨酸溶液中,反应一定时间,测其ρ(吸光度).分别考察pH、H2O2用量和反应时间对溴氨酸脱色率的影响.
1.3 分析方法
利用紫外-可见分光光度计测定溴氨酸最大吸收波长为485 nm.定时取样,在最大吸收波长处测其吸光度并根据下面公式计算脱色率
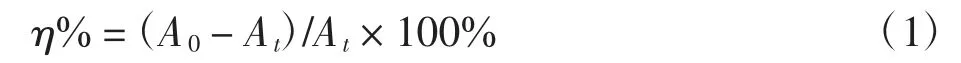
式中:A0表示某一染料废水未处理时的吸光度值;At表示某一染料废水处理进程中t 时刻的吸光度值.
2 结果与讨论
H2O2投加量、Fe2+含量、pH 值及反应时间是影响芬顿氧化效率的重要因素,本文是在废液中Fe2+含量固定条件下,对H2O2投加量、pH 值、反应时间以及Zn2+共存离子等因素进行了考察,并对酸洗废液芬顿体系与纯芬顿体系进行比较,确定出最佳工艺条件.
2.1 废液类Fenton 体系和纯Fenton 试剂体系氧化降解溴氨酸溶液的效率比较
2.1.1 不同pH 值条件下两种Fenton 体系氧化降解效率比较
在H2O2投入量为1.5 mL/L,溴氨酸初始质量浓度为30 mg/L 的条件下,在不同pH 值下将废液类Fenton体系和纯亚铁Fenton 体系氧化降解处理溴氨酸溶液的效率进行了对比,结果如图1 所示.
从图1 可以看出,纯亚铁Fenton 体系与废液类Fenton 体系在不同的pH 条件下存在明显的差异,其脱色率相差5%~10%左右.在pH=3 的条件下,纯亚铁Fenton 体系明显比废液类Fenton 体系的降解处理效果要好,溶液的脱色率高.分析其可能原因在于:废液中存在的阴离子和阳离子对Fenton 反应起到了抑制作用,进而降低了废液脱色率.在pH=4 的条件下,纯亚铁体系下的废液脱色率出现一定程度下降,明显低于废液类Fenton 体系,其原因可能在于:由于废液类Fenton 体系中存在Zn2+离子,由于其溶度积常数较低,会形成沉淀,进而通过絮凝沉淀作用增加废水的脱色率.随着pH 值继续增高,纯亚铁Fenton 体系的脱色率得到明显提高,且大于废液类Fenton 体系.其原因在于:在高pH 值条件下,纯亚铁体系中的Fe2+也会形成沉淀,进而起到絮凝作用,对废水中溴氨酸进行去除,增加废液的脱色率.从而确定纯亚铁芬顿体系的最佳pH=3,而废液类芬顿体系的最佳pH=4.
2.1.2 不同H2O2投入量条件下两种Fenton 体系氧化降解效率比较
在溴氨酸废水溶液初始pH 值为4,初始质量浓度为30 mg/L,相同H2O2投入量条件下,将废水Fenton体系与纯亚铁Fenton 体系对溴氨酸废水溶液氧化降解脱色率进行了比较,如图2 所示.
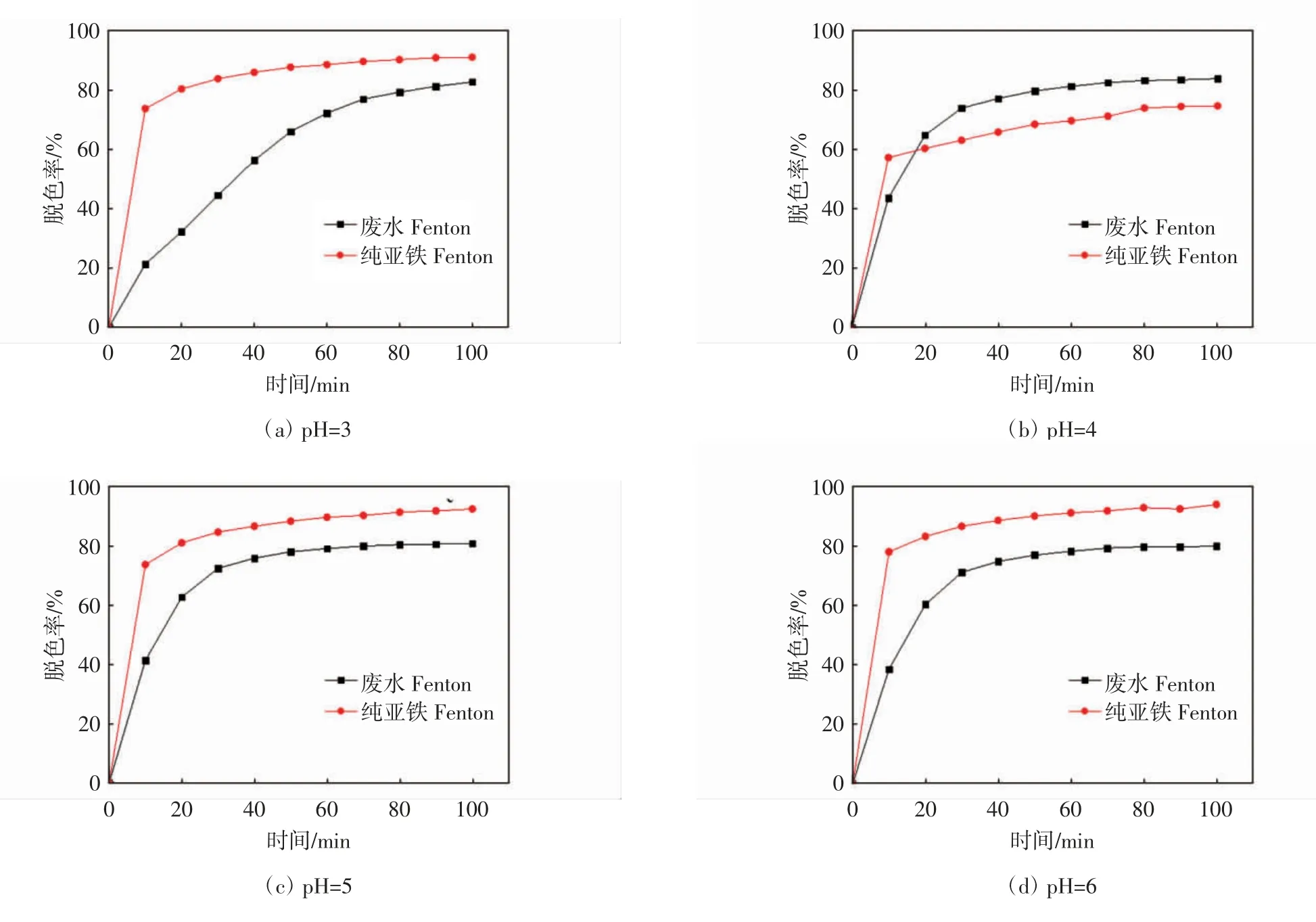
图1 不同pH 值条件下两种Fenton 体系氧化降解处理效率比较
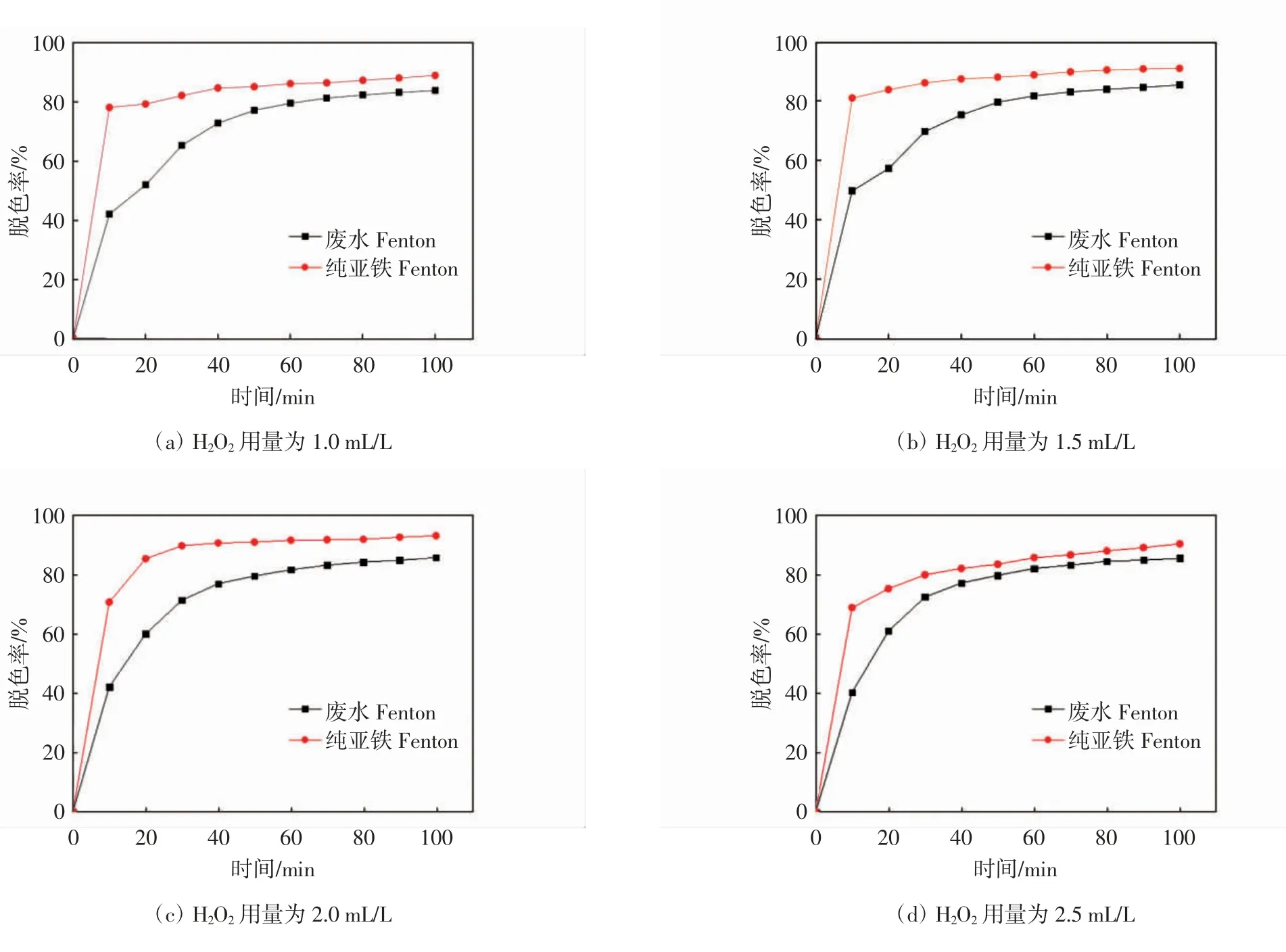
图2 不同H2O2 投入量条件下两种Fenton 体系氧化降解处理效率比较
从图2 可以看出,在不同H2O2投入量条件下,纯亚铁Fenton 体系中溴氨酸水溶液的脱色率比废液类Fenton 体系中的溴氨酸溶液脱色率都要高5%~10%左右.其原因可能在于:废水体系中存在的其他杂质离子(如Cu2+、Zn2+、Cl-等)会对Fenton 体系中由H2O2转化生成·OH 产生抑制,进而影响废液类Fenton 体系对溴氨酸废水的氧化降解效率.从而确定纯亚铁芬顿体系H2O2的最佳用量为2 mL/L(0.4 mL),酸洗废液芬顿体系H2O2的最佳用量为1.5 mL/L(0.3 mL).
2.2 钢铁酸洗废液芬顿氧化溴氨酸溶液响应曲面分析
本实验采用响应面分析Box-Behnken(BB)设计法,对影响溴氨酸水溶液脱色效果的初始pH、H2O2投加量、反应时间3 个因素进行优化,分别用A,B,C 表示,并用响应曲面回归拟合,预测最佳条件;运用SAS对数据做回归、显著性和方差分析.单因素实验结果显示:H2O2投加量为1.5 mL/L,pH=4,反应时间为100 min 时有最大脱色率.
据此确定实验中各量范围如下:pH 为3~5,H2O2投加量为(0.1~0.5)mL,反应时间为(60~100)min.它们都是在高(+1),中(0)和低(-1)3 个水平来研究.各因素水平编码如表1 所示.对三因素的响应面模型进行显著性检查,方差分析见表2.
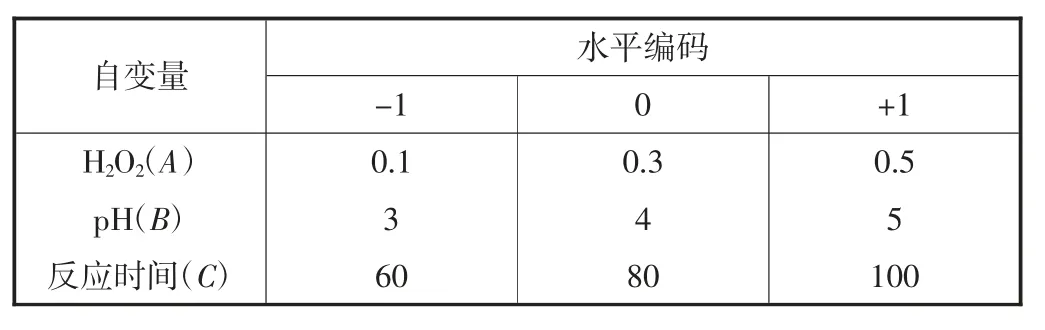
表1 响应面分析因素及水平
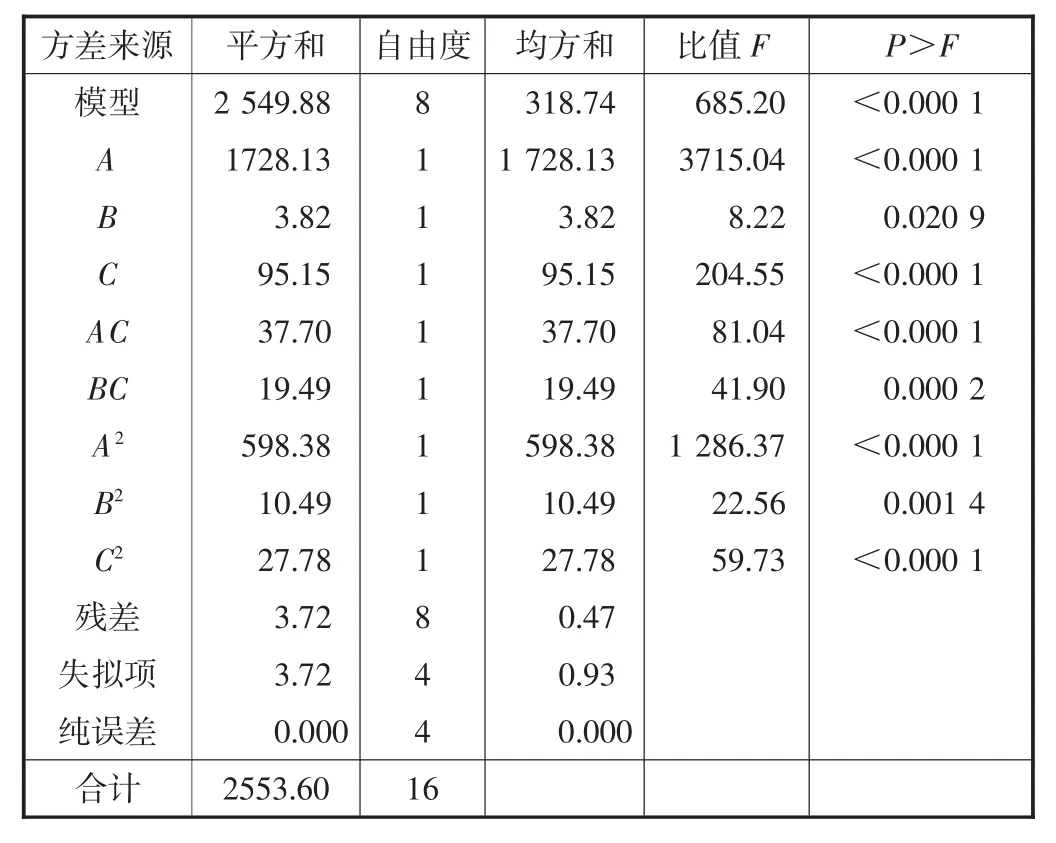
表2 H2O2 投加量、pH、反应时间对脱色率联合影响回归方程方差分析
由表2 可知,模型的F 值为685.20,P>F 的值<0.000 1,这说明此模型对溴氨酸脱色率的模拟是可靠的.P>F 的值<0.050 0 时,说明模型的影响是显著的;P>F 的值>0.100 0 时,说明模型的影响不显著.模型的精密度是14.330(精密度>4),这说明模型的精密度足够[15].模型的校正决定系数RAdj2=0.933 2,说明该模型能解释93.32%响应值的变化,仅有总变异大约7.68%不能用该模型来解释;相关系数R2=0.998 5说明该模型拟合程度良好,预测值与实测值之间有较好的相关性,实验误差小,可以用该模型来分析和预测试样的脱色率.
该模型优化出最佳条件为:H2O2投加量为0.41 mL(2.05 mL/L),pH=3.4,反应时间=80 min 时脱色率达到最大,溴氨酸的脱色率实测值与预测值分别为88.15%和89.71%.实验值接近模型的预测值,表明该模型具有一定的指导意义.
2.3 废水体系中的Zn2+对于不同染料水溶液氧化降解的影响
常温下,量取200 mL pH=3 的质量浓度为30 mg/L溴氨酸溶液、甲基橙溶液、亚甲基蓝溶液置于300 mL的烧杯中,分别加入20 mL 配置好的Fe2+体系、Zn2+体系、Fe2+/Zn2+体系,然后各加入1.5 mL/L H2O2,混合均匀后,磁力搅拌100 min,每10 min 取样并用紫外-可见分光光度计测其染料相应最大吸收波长下的吸光度值,据此计算出脱色结果如图3 所示.
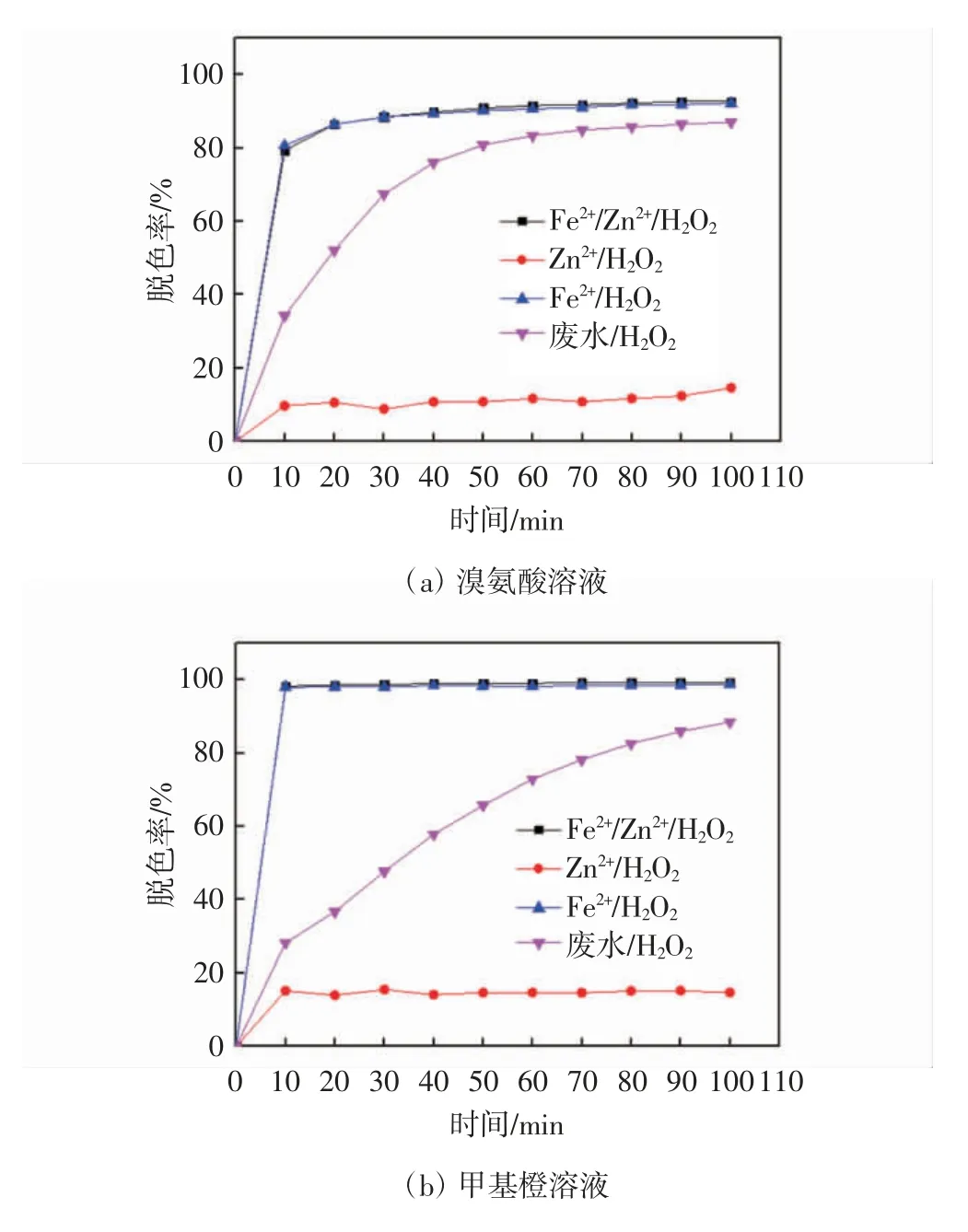
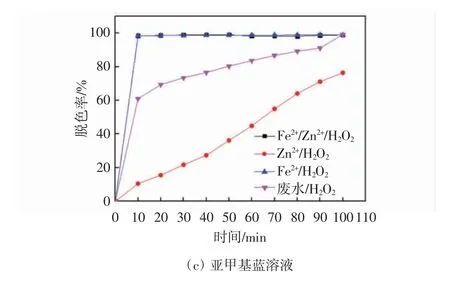
图3 不同催化氧化体系对不同染料溶液脱色效果的影响
从图3 可以看出,所选择的3 种染料水溶液在Fe2+/Zn2+体系与Fe2+体系中的氧化降解效果基本上没有区别,说明废液中Zn2+对于染料水溶液的Fenton 氧化降解效率无明显影响.这与郑第[16]利用Fenton 试剂降解偶氮染料活性艳红X-3B 的实验研究中Zn2+的影响一致.研究人员发现Cu2+、Co2+、Mn2+、Ni2+、Ti3+、Cr2+等金属离子也具有类似芬顿反应的催化作用,即能和H2O2作用产生·OH.进一步研究,原因是同属过渡金属元素,且离子状态含多价态,可与H2O2发生氧化还原反应.而Zn2+虽同属过渡金属元素,但离子状态不存在变价,不能与双氧水发生氧化还原反应.因此,前述废水中对Fenton 氧化降解起到抑制作用的离子不是Zn2+,而是其他阳离子或阴离子,具体种类有待进一步研究.值得注意的是,从Zn2+/H2O2体系降解不同染料关系图中(见图4)可以看出,在亚甲基蓝废水降解体系中,Zn2+对亚甲基蓝的脱色率影响较为明显,其原因在于,Zn2+可与亚甲基蓝形成配合物而增加废水的脱色率.

图4 Zn2+/H2O2 体系对不同染料溶液降解脱色率的影响
3 结 论
钢铁行业是我国国民经济的支柱性产业,但其产生的酸洗废液对我国水环境所造成的严重污染,已成为全国工业污染防治的焦点、热点和难点问题.芬顿氧化技术由于其在污染物降解中具有高效性、普适性和氧化降解的彻底性等优点,已成为国内外水处理研究领域的热点课题.本文利用钢铁酸洗废液中铁离子与双氧水构建了废液类Fenton 体系,并以溴氨酸水溶液为降解对象,与纯亚铁Fenton 体系进行了降解效果对比研究.实验结果表明:废液类Fenton 体系适用于较高的pH 值(pH=4)并降低了H2O2用量(1.5 mL/L).废液类Fenton 体系对不同染料废水的降解效果,其实验结果表明:Zn2+与亚甲基蓝间的配位作用增加了脱色率,而Zn2+对废液Fenton 体系处理溴氨酸和甲基橙水溶液的效果无明显影响.但降解溴氨酸后的废液中的锌离子含量仍然超过国家规定标准(我国污水综合排放标准对Zn2+质量浓度要求在2 mg/L 以下[17]),关于锌离子的回收与利用有待进一步的研究.
