数字减影血管造影引导下植入式静脉输液港在癌症化疗患者中的应用
2019-09-21彭小花
盖 垚 彭小花
化疗是恶性肿瘤最主要的治疗方式,多数化学药物需要经静脉给药,且患者大多需要进行多个疗程的持续治疗。长期大量高浓度、高刺激性的化学药物会对患者外周血管以及周围组织造成损伤,继而出现静脉炎、神经损伤以及肢体关节功能损伤等严重并发症,降低患者治疗耐受性[1-3]。植入式静脉输液港是一种能够长期植入体内的血管通道系统,其特点是减少穿刺血管的次数,降低静脉输液对患者生活及治疗的影响[4]。数字减影血管造影(digital subtraction angiography, DSA)技术是电子计算机图像处理技术和常规血管造影术结合的X线成像系统,在DSA引导下植入静脉输液港(central venous assess port devices, CVAPD),可以准确观察导管头的位置[5-6]。本文则探究癌症化疗患者DSA引导植入CVAPD对治疗安全性的影响。
1 资料与方法
1.1 一般资料
选取2014年2月-2016年2月我科收治的癌症化疗患者152例作为对象,纳入标准:①经病理证实为恶性肿瘤患者;②计划行长期化疗的患者;③拟行输液港植入部位既往无放疗、手术以及外伤史;④患者及家属该研究知情同意且自愿签署临床研究授权书;能配合完成随访调查。排除标准:①有手术禁忌症患者[7];②合并精神疾病患者;③有严重肝、肾等重要脏器疾病者;④治疗依从性较差的患者。采用随机数字表法将其分成对照组和观察组,每组76例。对所有患者进行2年的随访,对照组有16例失访,其中2例电话无应答,3例为手机号空号,2例为手机号错号,7例转至其他医院继续治疗,还有2例拒绝接受随访;观察组有19例失访,其中3例电话无应答,4例为手机号空号,2例为手机号错号,1例停机,8例转至其他医院继续治疗,还有1例拒绝接受随访。剔除脱落病例后,最终对照组60例,男性24例,女性36例,平均年龄(53.2±9.7)岁,病程2~3年,乳腺癌20例,卵巢癌7例,胃肠道恶性肿瘤13例,肺癌患者10例,淋巴瘤患者6例,其他4例;观察组57例,男性19例,女性38例,平均年龄(54.0±10.2)岁,病程2~3年,乳腺癌17例,卵巢癌6例,胃肠道恶性肿瘤14例,肺癌患者10例,淋巴瘤患者6例,其他4例。2组性别、年龄、病程等基本资料比较,差异无统计学意义。
1.2 方法
对照组患者在超声实时引导下植入CVAPD:患者取仰卧位,依据术前超声定位结果,完成局部麻醉后做锁骨下静脉或颈内静脉穿刺,通过导丝指引将导管送入上腔静脉中,钝性分离相应皮下组织,建立皮下隧道和囊袋,连接导管和港体,术后通过胸片检查评估CAVPD导管头的位置和走向是否合适,明确是否有气胸形成。观察组患者在DSA引导下植入静脉输液港,患者仰卧于DSA操作台上,肩部略垫高充分暴露术侧皮肤,将头部偏向穿刺的对侧,行常规消毒,使用浓度为2%的利多卡因做局部麻醉,行锁骨下静脉或颈内静脉穿刺,再引入导丝。在DSA透视下观察导丝情况,及时调整导丝,使其顺利进入上腔静脉,固定后退出穿刺针,再经导丝引入型号为7F的扩张鞘,然后将导丝退出,DAS透视下经扩张鞘将硅胶导管引致上腔静脉距右心房近端,然后撤掉扩张鞘,导管回抽见血表明引入成功,然后使用肝素生理盐水对导管进行冲洗。沿着穿刺点下约2 cm处切一3 cm的切口,钝性分离皮下组织,向上分离至导管并建立皮下隧道,然后拉出导管;向下分离并制作囊袋[8]。导管尖端位于右心房和上腔静脉的交接部位,在透视下准确定位(在第6~8后肋间),剪掉多余导管,分别将导管锁和注射座和硅胶导管相连,把CVAPD置入囊袋中,回抽见血后缝合伤口。使用无菌敷料加压包扎,经DSA胸部摄片,观察是否有导管折叠、脱落以及扭曲现象,是否有气胸产生。术后1周左右依据患者恢复情况拆线。
1.3 观察指标
①比较2组一次性穿刺成功率、总穿刺成功率。②比较2组患者植管后耐受情况。植管耐受评价标准:植管疼痛在患者能够承受的范围内;植管后无明显不适感。③随访2年,比较2组输液港相关并发症发生情况。
1.4 统计学方法

2 结果
2.1 2组一次性穿刺成功率及总穿刺成功率比较
对照组一次性穿刺成功率为100%(60/60),高于观察组91.23%(52/57),2组比较,差异有统计学意义(χ2=5.498,P=0.019),但2组总穿刺成功率无差异,均为100.0%。
2.2 2组患者对输液港耐受情况比较
化疗期间,观察组因局部不适要求取出输液港者1例;对照组因局部不适要求取出输液港者8例,2组比较,差异具有统计学意义(χ2=4.009,P=0.045)。
2.3 2组输液港相关并发症比较
观察组发生输液港相关并发症12例,对照组8例,2组比较,差异无统计学意义(χ2=1.229,P=0.268),具体见表1。
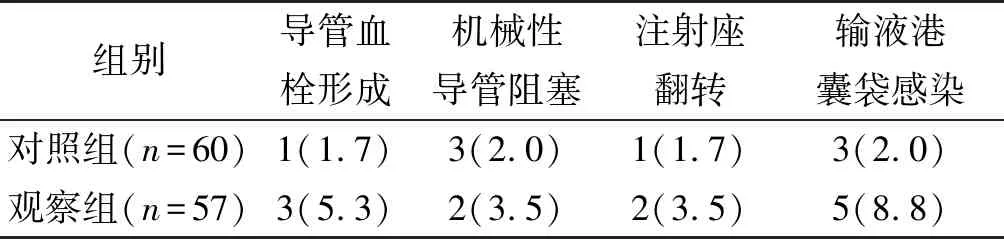
表1 2组输液港相关并发症发生情况 [例(%)]
3 讨论
近年来,植入式静脉输液港在临床上的应用越来越广泛,有研究显示[9-10],CVAPD导管头的准确定位,可降低导管相关血栓以及由于功能不良取出输液港的几率,通常导管头与右心房越近则导管相关血栓的发生率则越低。而DSA技术的应用使输液港的植入精确度显著提升,透视下进行定位能够防止导管进入过深影响心脏;此外,经锁骨下静脉穿刺路径时,导丝、导管尖端可能会进入到同侧/异侧颈内静脉中,透视监视下可以及时进行调整,避免患者出现颈部牵拉、血栓形成等并发症,提升安全性。本研究中对照组患者采用超声实时引导植管,而观察组患者行DSA引导植管,结果显示在一次性穿刺成功率方面超声组优于DSA引导组,主要原因在于超声实时引导下穿刺的针尖部位时刻被监测直至进入到颈内静脉中,因此针尖误入颈内动脉几率大幅降低,一次性穿刺成功率较高。超声实时引导植管的深度是依据穿刺点与同侧胸锁关节距离进行估算的,因此导管末端放置位置准确度较低,因此患者可能会出现不适感。本研究结果显示,观察组患者植管后因不适要求取出输液港者少于对照组。
植入式输液港主要的并发症有导管功能障碍、导管断裂/扭曲、血栓形成、导管相关感染、输液港座翻转、感染等[11-12]。有研究[13]显示,超声实时引导植入静脉输液港的安全性高于PICC,本研究结果显示,2组静脉输液港相关并发症的发生率无统计学差异。植入式CVAPD使用时间长,维护方便,不会对患者的日常生活造成较大影响,但是在植入后依然需要注意其并发症情况。
综上所述,DSA引导下植入CVAPD构建的静脉通路,患者耐受性较好,可以提升癌症患者化疗期间的生活质量,值得推广。
