赋形剂乳液粒径和油脂链长对橘子中β-胡萝卜素的物化特性及生物可给性的影响
2019-09-11刘晓娟
刘 涵,袁 曦,刘晓娟,*,曹 庸
(1.华南农业大学食品学院,广东广州 510642; 2.广东省功能食品活性物重点实验室,广东广州 510642; 3.广东省天然活性物工程技术研究中心,广东广州 510642)
β-胡萝卜素(C40H56)是橘黄色脂溶性类胡萝卜素,是自然界中最普遍存在的天然色素。许多天然食物例如菠菜、胡萝卜、橘子、木瓜、芒果等[1],皆含有丰富的β-胡萝卜素。β-胡萝卜素是维护人体健康不可缺少的营养素,具有抗癌、预防心血管疾病、白内障及抗氧化等多种活性,可防止老化和衰老引起的多种退化性疾病[2]。但人体自身无法合成β-胡萝卜素,主要通过摄入水果和蔬菜来获得。虽然β-胡萝卜素的食物来源广泛,但由于其含有多个共轭双键组成的四萜结构,具有较高的疏水性,在胃肠液中的溶解度较低,并且不易从植物组织中释放,从而导致其生物利用率相对较低[3-5]。目前,已有一些提高人体对某些亲脂性生物活性物质的口服生物利用率的方法,例如以膳食补充剂或营养补充剂的形式来提高活性成分的摄入量,或者对活性成分结构进行修饰,将亲脂性活性成分提取纯化后再进行包埋制成片剂、脂质体、乳液等[6-9]。但是类胡萝卜素这类亲脂性成分从果蔬中分离提取有一定的局限性,有学者认为类胡萝卜素存在于原有食物组分中一同被消化吸收可能具有更好的功效[4,10-13]。许多研究表明,添加油脂或富含油脂的食物可以提高果蔬类胡萝卜素的生物利用率。Nidhi等[14]研究了不同脂肪酸组成及饱和度的植物油对叶黄素生物可给性的影响,叶黄素在橄榄油中的生物可给性最大。Hedrã N等[12]的研究表明,在绿叶蔬菜的烹饪过程中加入红棕榈油后,β-胡萝卜素的生物可给性为无油脂样品的2倍。
McClements等[15]在2014年首次提出运用赋形剂食品(Excipient food)来增加生物活性物质的生物利用率。赋形剂乳液是赋形剂食品中最具发展潜力和应用最广泛的一种形式,能够充分发挥日常膳食中生物活性物质的潜在功效。赋形剂乳液的油脂类型、粒径大小和界面特征等因素对于提升果蔬中类胡萝卜素生物可给性具有很大影响。小粒径赋形剂乳液通常有利于脂溶性活性物质从组织中的释放,从而提高其生物可给性[16],然而有些稳定性较差的脂溶性活性物质(如姜黄素等)过早地暴露在胃肠道容易发生降解,从而导致其活性降低[17]。由于不同链长油脂形成的混合胶束(Mixed micelles)大小不同,并且不同分子量大小和结构(如亲水基团和疏水基团)的亲脂性活性成分会导致混合胶束对其的承载量存在差异,从而影响其生物可给性[18]。此外,存在于不同果蔬中的活性成分由于受到果蔬中其它物质的干扰,其释放程度不同也会影响生物可给性。因此,赋形剂乳液在提高特定食品中特定生物活性物质生物可给性的有效性方面仍然需要进一步阐明。
本实验以β-胡萝卜素的主要膳食来源之一的橘子为原料,利用体外消化模型,探究赋形剂乳液的粒径大小和油脂类型对橘子中β-胡萝卜素的物化特性及生物可给性的影响,旨在为设计高效的赋形剂乳液以提高人体对膳食中的脂溶性物质的生物利用率提供更多理论依据。
1 材料与方法
1.1 材料与仪器
橘子、玉米油 广州当地超市;中链甘油三酯(Medium chain triacylglycerol,MCT) 上海源叶生物科技有限公司;猪胃粘液素II型、胃蛋白酶、脂肪酶 美国Sigma-Aldrich贸易有限公司;糖苷酶、胆盐、L-乳酸钠、柠檬酸钾 上海源叶生物科技有限公司;氢氧化钠、磷酸氢二钠、无水乙醇、丙酮、正己烷、吐温20等 均为国产分析纯;四氢呋喃、二氯甲烷 国产色谱纯,天津市科密欧化学试剂有限公司;乙腈、甲醇 为色谱纯,美国J. T. Baker公司。
AL104万分之一电子天平 梅特勒-托利多仪器(上海)有限公司;DELTA320 pH计 梅特勒-托利多仪器(上海)有限公司;DF-101S数显电热恒温水浴锅 巩义予华仪器有限公司;SHZ-D(Ⅲ)循环水式多用真空泵 巩义市英峪高科仪器厂;RE-52A旋转蒸发仪 上海亚荣生化仪器厂;FD-1冷冻干燥机 北京博医康技术公司;TGL-16G高速台式离心机 上海安亭仪器厂;LC-15C分析高效液相色谱系统 日本岛津公司;Diamonsil C18(2)色谱柱(4.6 mm×250 mm,5 μm) Dikma Technologies;90 Plus动态光散射粒度分析仪 Brookhaven;CX41光学显微镜 Olympus;DL-55全自动电位滴定仪 梅特勒-托利多仪器(上海)有限公司;FJ200-S型高速分散均质机 上海嫩谷机电设备有限公司;AH-BASIC高压均质机 ATS Engineering Incorporated。
1.2 实验方法
1.2.1 不同粒径大小赋形剂乳液的制备 将一定浓度的吐温20(1.0%,w/w)溶解于5 mmol/L pH7.0的PBS中,再将玉米油与水相溶液按照1∶9的重量比混合,用高速分散均质机在10000 r/min下分散2 min(大粒径乳液),然后用高压均质机分别在20 MPa均质1次(中等粒径乳液)、120 MPa下均质5次(小粒径乳液)。
1.2.2 不同链长油脂类型赋形剂乳液及对照组乳液的制备 选用MCT油为代表的中链油脂和玉米油为代表的长链油脂为油相,与水相按照1∶9的重量比混合,用高速分散均质机在10000 r/min下分散2 min,最后用高压均质机在120 MPa下均质5次。对照组乳液即用PBS磷酸缓冲溶液替代油脂,与水相混合,后续制备方法相同。
1.2.3 体外消化模型的构建 标准静态体外模拟消化的过程参考了Minekus等[19]的实验程序并稍作修改,构建了一个模拟消化道[20],主要包括模拟口腔、模拟胃、模拟小肠三个消化阶段。橘子经过剥皮、榨汁、抽滤后得到的橘子汁与稀释乳液混合,使最终样品中含油量为2%,将所得橘子/赋形剂乳液通过模拟体外消化。
模拟口腔消化阶段:通过将粘蛋白(3 mg/mL)和各种盐分散于水中制备模拟唾液(SSF),然后取预热的20 mL橘子/赋形剂乳液样品与20 mL模拟胃液(SSF)混合,并用NaOH溶液调节至pH6.8。所得混合物在连续搅拌(100 r/min)下于37 ℃温育10 min,得口腔消化样品。
模拟胃消化阶段:将2 g NaCl和7 mL HCl溶解在1 L水中,然后将0.064 g胃蛋白酶(酶活力:250 U/mg)分散到20 mL该溶液中,搅拌30 min来制备模拟胃液(SGF)。然后取20 mL模拟口腔消化后的样品与20 mL模拟胃液混合,调节至pH2.5。将胃样品置于37 ℃的恒温摇床中以100 r/min连续旋转2 h,得胃消化样品。
模拟小肠消化阶段:取30 mL模拟胃消化的样品,调节至pH6.8~7.0,加入1.5 mL模拟肠液(CaCl2·2H2O 36.6 g/L和 NaCl 219 g/L溶于蒸馏水中)、3.5 mL胆盐溶液(0.1875 g胆盐溶液溶于3.5 mL PBS(5 mmol/L,pH7.0)中)。再次调节至pH7.0,加入2.5 mL脂肪酶溶液(含脂肪酶30 g/L,脂肪酶酶活力:100~400 U/mg)。然后采用pH-stat法,利用恒电位滴定仪不断向体系中加入0.25 mol/L的NaOH溶液,使体系恒定保持在pH7.0,并记录2 h内消耗的NaOH溶液的量。在整个消化过程中,体系温度维持在37 ℃,搅拌头以50%的速度不断均匀搅拌。
1.2.4 体外模拟消化过程中橘子/赋形剂乳液混合体系粒径和电位的测量 采用90 PLUS动态光散射激光粒度仪,测定初始乳液和经各阶段消化后混合体系的颗粒大小(用表面积加权平均粒径(d32)表示)、颗粒分布和ζ-电位。为避免多重光散射以及橘子组织对测量结果的干扰,对原始乳液及各阶段消化液进行稀释。测量温度:25 ℃,检测角度:90°,波长:658 nm。
1.2.5 模拟消化过程橘子/赋形剂乳液混合体系的微观形态观察 取一滴消化液至载玻片上,然后用盖玻片从左至右轻轻盖上,用滴管取一滴香柏油脂滴在盖玻片观察区域内,利用100倍油镜观察,选择合适区域拍摄获得显微结构图像。
1.2.6 体外模拟小肠消化阶段中橘子/赋形剂乳液混合体系的脂肪酸释放速率测定 在模拟小肠消化阶段中,乳液中的油脂在经脂肪酶的作用分解成游离的脂肪酸。在水解过程中,溶液中不断释放H+,使体系的pH降低。利用pH-stat法[21],向溶液中不断滴入NaOH,使溶液恒定pH为7.0,根据NaOH的消耗体积量,计算小肠消化过程中游离脂肪酸(Free fat acid,FFA)的释放量。
式(1)
式中,VNaOH是消耗的NaOH的体积(L),mNaOH是用于滴定的NaOH的摩尔浓度(M),Wlipid是指小肠消化液中油脂的总质量(g),Mlipid是指油脂的分子质量(g·mol-1)。
1.2.7 体外模拟消化过程中不同阶段的β-胡萝卜素的提取 分别取一定体积的各阶段消化液和胶束,加入正己烷:丙酮(1∶1,V/V)离心(4000 r/min,2 min)后提取上清液。整个提取过程在避光、低温环境中进行。将多次萃取得到的上清液合并,25 ℃下旋蒸,将其浓缩至合适体积,经过氮吹将有机溶剂挥发完毕后置于-20 ℃冷冻过夜,再将提取物经-80 ℃冷冻干燥后于-20 ℃密封保藏直至分析[22]。
1.2.8 体外模拟消化过程中β-胡萝卜素生物可给性的测定 橘子/赋形剂乳液混合体系经体外模拟消化后,取小肠消化液高速离心(15000 r/min,4 ℃)50 min,收集上清液用0.45 μm微孔滤膜过滤得到胶束相,进行HPLC色谱分析。HPLC液相色谱分析条件为:固定相:Diamonsil C18(2)色谱柱(4.6 mm×250 mm,5 μm);流动相A:乙腈∶甲醇(95∶5,V/V);流动相B:乙腈∶甲醇∶四氢呋喃(60∶20∶20,V/V/V),(其中乙腈中含有5%的三乙胺);进样量:20 μL;流速:1 mL/min;检测光波长:450 nm;柱温:30 ℃。梯度洗脱程序:0~20 min:B泵:0%~30%;20~30 min:B泵:30%~100%;30~50 min:B泵:100%。通过HPLC色谱分析得到各个消化阶段的β-胡萝卜素的峰面积,计算出其浓度,再通过下式(2),便可计算得到不同赋形剂乳液经过消化后对β-胡萝卜素的生物可给性的影响。
生物可给性(Bioaccessibility)=胶束中β-胡萝卜素含量/小肠消化液中β-胡萝卜素含量
式(2)
1.3 数据处理
采用SPSS 17.0统计软件进行数据处理。结果以“平均数±标准差”表示,进行单因素方差分析,不同处理间的显著性检验采用Duncan式多重比较,均以p<0.05作为差异显著性判断标准。
2 结果与分析
2.1 不同粒径大小和链长油脂制备的赋形剂乳液表征
2.1.1 粒径大小和分布 将玉米油与水相溶液按照1∶9的质量比混合,用高速分散均质机和高压均质机在不同的条件下分别制得(d32≈ 205 nm)、中等粒径(d32≈ 510 nm)和大粒径(d32≈ 10 μm)的乳液(图1a),三种乳液粒径具有显著差异(p<0.05),从而为后续研究不同粒径大小赋形剂乳液对橘子中β-胡萝卜素生物可给性提供有效材料。由于玉米油具有更高的黏度,高压均质机对玉米油乳液的破碎效率较低[23-24],因此MCT制备的乳液的粒径(d32≈ 128 nm)小于玉米油长链油脂制备的乳液(图1b)。三种不同粒径乳液的多分散指数(PDI)分别为0.099、0.141和0.291,MCT油乳液的PDI为0.139。一般认为,PDI<0.3的乳液具有较好的均一性[25-26]。从图2也可看出,不同粒径和链长油脂制备的赋形剂乳液都呈单峰,均一性好,小粒径分布范围较窄,集中在200 nm左右,大粒径乳液分布在10 μm左右。
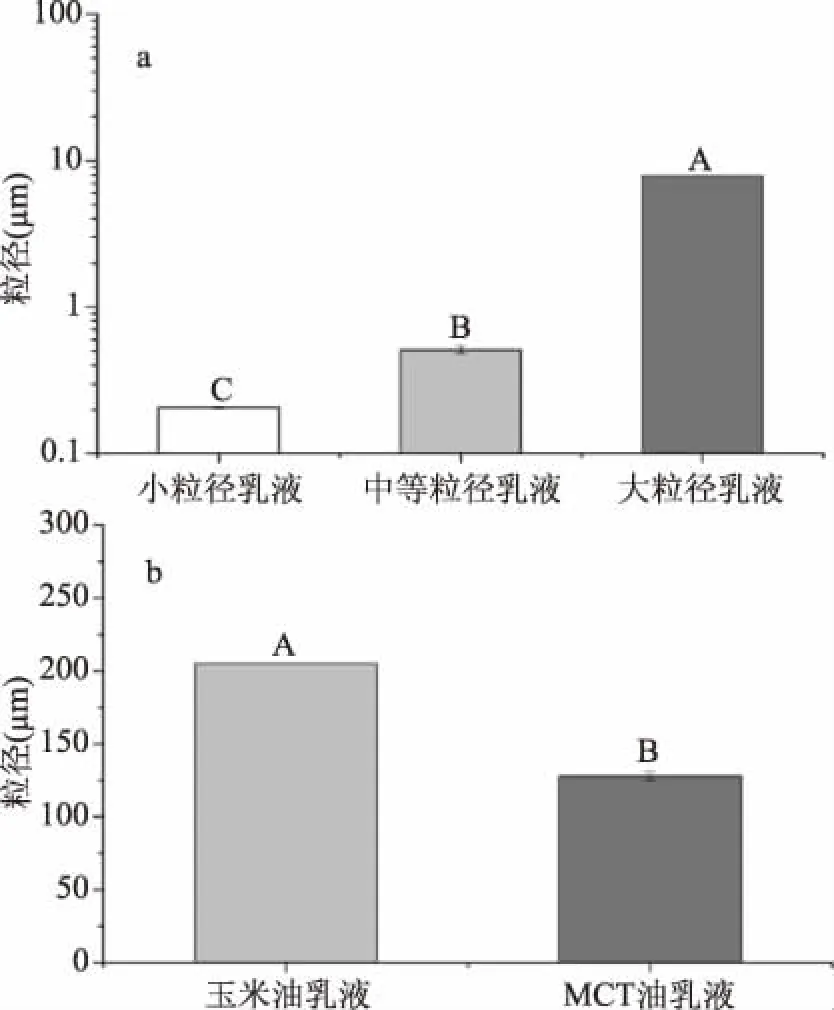
图1 不同粒径(a)和链长油脂(b)赋形剂乳液的平均粒径(d32)Fig.1 The mean particle diameter(d32)of the excipient emulsion with different particle size(a)and different chain length lipids(b)注:不同大写字母表示差异显著(p<0.05),图3、图9、图11同。

图2 不同粒径(a)和链长油脂(b) 赋形剂乳液的粒径分布图Fig.2 The particle size distribution of the excipient emulsion with different particle size(a)and different chain length lipids(b)
2.1.2 ζ-电位 ζ-电位是连续相与附着在分散粒子上的流体稳定层之间的电势差,是对颗粒之间相互排斥或吸引力强度的度量,用于衡量胶体分散体系稳定性的重要指标。ζ-电位的绝对值越大,颗粒间的排斥力越大,体系分散稳定性越好[27-28]。此外,ζ-电位还影响着乳液其它成分之间的相互作用,对乳液功能特性的发挥也具有重要影响[29]。利用电位测量仪测量小、中、大粒径乳液的ζ-电位分别为-29.87、-26.56和-19.62 mV(图3a),三种乳液表面均呈高度的电负性,且电负性随着粒径的增大而减小。这是由于溶液中阴离子杂质的存在,如油脂中的游离脂肪酸、乳液的脂质成分等,非离子表面活性剂(吐温20)包裹的油滴也可能带有较强的电荷[30]。并且由于具有不同液滴尺寸的乳液的界面或水相性质的变化,乳液的ζ-电位绝对值随着平均粒径的增加而降低[31]。MCT乳液的ζ-电位为-24.98 mV,绝对值显著低于玉米油长链油脂乳液的电荷量(-29.87 mV)(图3b),这是由于不同油脂含有的游离脂肪酸和磷脂等组分不同,长链油脂中含有更多的游离脂肪酸[21],这些阴离子或阳离子成分均可吸附到油-水界面,影响整个界面电荷特性[24]。

图3 不同粒径(a)和链长油脂(b)赋形剂乳液的ζ-电位Fig.3 The ζ-potential of the excipient emulsion with different particle size(a)and different chain length lipids(b)
2.2 不同粒径大小和链长油脂制备的橘子/赋形剂乳液混合体系的体外模拟消化特性
在模拟胃肠道消化过程中,赋形剂乳液混合体系中乳液粒径大小、聚集状态和ζ-电位的变化能够反应其消化特性。所有乳液都是用非离子表面活性剂(吐温20)包裹,不易受胃肠道消化过程中pH、盐浓度的变化以及各种消化酶的作用的影响[17],因此乳液在口腔和胃阶段消化过程中性质较为稳定,发生聚集的程度较小。
2.2.1 不同粒径大小和链长油脂橘子/赋形剂乳液混合体系在消化过程中微观结构的变化 从图4显微图像可以观察到,玉米油、MCT油乳液与橘汁混合后液滴均匀分布,而大粒径乳液与橘汁混合后可能导致其状态不稳定,大液滴容易分解成较小的乳滴。经口腔阶段机械作用的剪切力下,橘子碎片进一步被分解,有利于纳米乳液的融入,使橘子植物组织中的色素物质释放,并融入纳米乳液颗粒中[32]。因而可以观察到在口腔阶段小粒径、中等粒径乳液和MCT乳液中的颗粒相互聚集,大小不一。经胃阶段消化后,由于胃消化液的pH和离子强度变化可能改变了乳液脂滴间的吸引力和排斥力大小,乳液也会发生絮凝。但大粒径乳液含有非常大的油滴,能够抵抗粘蛋白分子对其的絮凝作用,并且在消化过程中,这些大油滴易在外力的作用下发生破裂[33],絮凝聚集现象不明显。在模拟小肠阶段,小粒径和中等粒径乳液的油脂几乎被完全消化,而大粒径乳液还有较多油脂未被完全消化。MCT乳液在小肠消化过程中形成了一些较大的囊泡[24]。与PBS对照组相比,橘子与赋形剂乳液共同体外模拟消化时,橘子组织中的色素物质释放更加完全,从图4中可看出,PBS对照组中的橘子组织中残留了较多色素物质。这表明,赋形剂乳液能够促进β-胡萝卜素这一类亲脂性活性成分在植物组织中的释放。

图4 不同橘子/赋形剂乳液混合体系各消化阶段的显微图像(1000×)Fig.4 Microscopy images of orange/excipient emulsion mixtures after exposure to each stage of a simulated GIT(1000×)
2.2.2 不同粒径大小和链长油脂橘子/赋形剂乳液混合体系在消化过程中物化性质的变化 粒径特性:由于pH和离子强度变化可能改变了乳液脂滴间的吸引力和排斥力大小,乳液经模拟胃阶段消化后发生絮凝。从图5中看出,与口腔阶段相比(d32≈234 nm),小粒径乳液在胃、小肠阶段的平均粒径显著增大(d32≈387 nm)(p<0.05),而由于大粒径乳液含有非常大的油滴,能够抵抗粘蛋白分子对其的絮凝作用,MCT乳液对胃酸性环境也有一定抵抗作用,因此其平均粒径与口腔阶段相比也没有明显变化。经模拟小肠阶段消化后,玉米油小粒径乳液和MCT乳液的平均粒径均显著增大(p<0.05),但MCT乳液会形成一些较大的囊泡[24],因此其粒径(d32≈892 nm)显著大于玉米油乳液(d32≈638 nm)(p<0.05)。

图5 不同粒径(a)和链长油脂(b)橘子/赋形剂乳液混合体系各消化阶段的平均粒径(d32)Fig.5 The mean particle diameter(d32)of the orange/excipient emulsion mixtures with different particle size(a)and different chain length lipids(b) after passing through each stage of simulation注:不同大写字母(A,B,C)代表同一样品在不同消化阶段 具有显著性差异(p<0.05),不同小写字母(a,b,c)代表同一消化阶段不同样品间 具有显著性差异(p<0.05)。图6同。
从图6可以看出,在初始阶段,大粒径的电位显著低于小粒径和中等粒径,MCT油乳液的电位也显著低于玉米油乳液(p<0.05)。经过模拟口腔消化后,各类乳液的负电荷均显著减少(ζ-电位为-2.60~-22.55 mV)(p<0.05),该现象在Zhang、Liu等人的研究中也有报道[34-35]。这是由于唾液溶液中存在大量矿物离子和粘蛋白,附着在油脂液滴的表面上,通过静电作用改变了非离子表面活性剂表面的界面状态和张力。在液滴周围的水相中,未吸附表面活性剂的液滴会产生渗透吸引力,从而导致乳液发生聚集和絮凝。在模拟胃消化阶段时,小粒径玉米油乳液的游离脂肪酸在胃酸环境下发生质子化,导致电荷表面静电排斥,降低了油滴的净电荷,从而电位接近于零(ζ-电位为0.100 mV),但中粒径和大粒径乳液油滴仍带有较多的负电荷,这在Liu等人的研究中也有相似结果[35]。模拟小肠阶段,在脂肪酶、胆盐等的作用下,形成不同阴离子胶体颗粒如胆汁盐、磷脂、游离脂肪酸等[21,24]。除大粒径乳液外,其余各类乳液带电量均显著增加(ζ-电位为-16.76~-21.02 mV)(p<0.05)。结合后续油脂消化特性结果(图8a),由于小粒径乳液的油脂消化程度更高,形成不同胶体颗粒的混合物可能更多,ζ-电位呈高度负值,因此更有利于色素物质的溶解。与MCT油脂乳液相比,玉米油乳液释放的长链脂肪酸更容易在油脂表面的积累,抑制了脂肪酸进一步释放和脂肪酶的吸附[21]。

图6 不同粒径(a)和链长油脂(b)橘子/ 赋形剂乳液混合体系各消化阶段的ζ-电位Fig.6 The ζ-potential of the orange/excipient emulsion mixtures with different particle size(a) and different chain length lipids(b)after passing through each stage of a simulated GIT
2.2.3 不同粒径大小和链长油脂赋形剂乳液对油脂消化特性的影响 使用自动滴定法监测不同粒径大小的赋形剂乳液对脂质消化速率程度的影响,在整个模拟小肠消化阶段,脂肪在脂肪酶的作用下不断分解,产生游离的脂肪酸,导致pH降低,用恒电位滴定仪滴定NaOH以维持样品的中性环境,可以根据消耗NaOH的量计算随着消化时间释放的游离脂肪酸(Free fatty acid,FFA)的量。
图7、图8分别为赋形剂乳液粒径大小和油脂键长对橘子/赋形剂乳液混合体系NaOH消耗量及FFA释放量的影响。从图8可以看出,在消化的初期阶段游离脂肪酸释放速率曲线斜率较大,游离脂肪酸含量增加较快,随着消化时间的延长,游离脂肪酸含量逐渐增加,最终趋于稳定。脂肪酸最终释放量从大到小按以下顺序排列:小粒径乳液>中等粒径乳液>大粒径乳液。这是由于,游离脂肪酸的最终释放量和脂滴暴露在消化酶中的比表面积呈正比,和乳液的平均粒径成反比,小粒径乳液脂滴尺寸最小,暴露在消化酶中的比表面积最大,增大了和消化酶的接触面积和反应机会,所以消化速率较快,在一定时间内,游离脂肪酸的释放量较多。这一结果与Ruojie等[36]和Salvia-trujillo等[37]将胡萝卜和番茄等果蔬与设计的不同粒径大小的赋形剂乳液共同摄入的研究结果一致。

图7 赋形剂乳液粒径大小(a)和油脂链长(b)对消化 过程中橘子/赋形剂乳液混合体系NaOH消耗的影响Fig.7 The effects of excipient emulsion particle size(A) and chain length lipids(B)on NaOH consumption in orange/excipient emulsion mixing system during digestion

图8 赋形剂乳液粒径大小(a)和油脂链长(b) 对橘子/赋形剂乳液混合体系中FFA释放的影响Fig.8 The impact of the particle size(A)and chain length lipids(B)of the excipient emulsions on the release of free fatty acids from orange/excipient emulsion mixtures
不同链长油脂的样品的总体消化曲线比较相似:在最初20 min内,FFA生成速度快,之后逐渐增加,逐步趋于平缓。图7(b)中,对比不同油脂制得的赋形剂纳米乳液最终消耗NaOH的量可发现,MCT中链油脂反应结束时消耗NaOH的量为3.77 mL,显著高于玉米油长链油脂(NaOH消耗量为1.76 mL)(p<0.05)。这是由于中链油脂分子量较低,甘油三酯所占的比例高,即每单位脂肪将释放更多的脂肪酸。虽然长链脂肪酸更容易在油脂表面的积累,抑制了脂肪酸的释放和脂肪酶的吸附[21],但最终从脂肪酸FFA释放曲线(图8(b))来看,长链油脂与中链油脂的消化速率的差异不显著(p>0.05)。由此可以得出,游离脂肪酸的释放与乳液粒径大小密切相关,而与油脂链长无明显相关性。
2.2.4 不同粒径大小和链长油脂橘子/赋形剂乳液对β-胡萝卜素生物可给性的影响 通过离心、提取上清液除去了大颗粒的杂质(如未消化的脂滴、囊泡和液晶等)后得到胶束,各类橘子/赋形剂乳液经小肠消化后形成的胶束平均粒径均明显减小,这是因为β-胡萝卜素需要溶解在粒径较小的混合胶束中,穿过未搅动的微绒毛水层被肠粘膜细胞吸收[38]。
利用高效液相色谱法测定了不同赋形剂乳液/橘子中β-胡萝卜素的生物可给性,以小粒径乳液为代表的各消化阶段色谱图呈现的峰面积为样品经提取浓缩得到的各物质峰面积,β-胡萝卜素在37~39 min之间出峰,图10中看到从初始阶段到胶束阶段的消化液样品的峰面积逐渐降低,这是由于样品在消化过程中不断被稀释,并且样品中β-胡萝卜素的含量逐级减少。
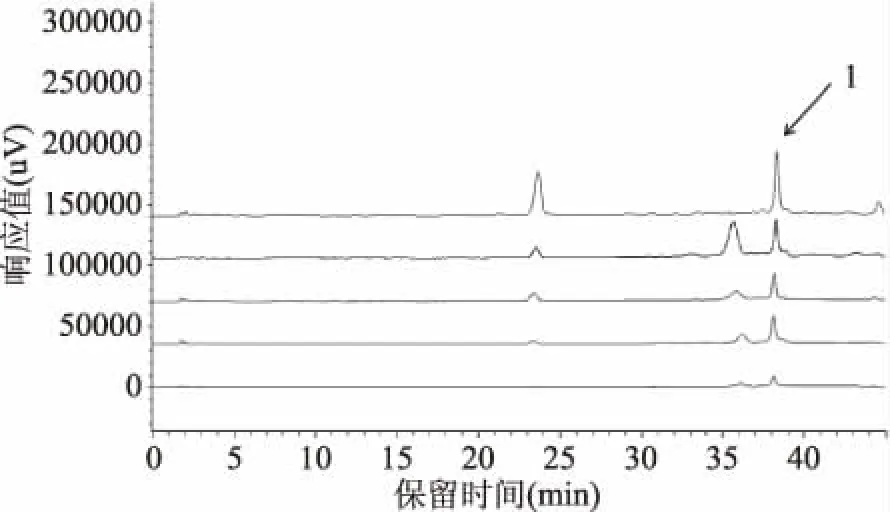
图10 橘子/小粒径乳液混合体系各消化阶段的β-胡萝卜素HPLC谱图Fig.10 The HPLC profile of the orange/small particle size emulsion mixed system following exposure to different GIT regions注:1号色谱峰为β-胡萝卜素。色谱图中 由上至下分别为初始、口腔、胃、小肠及胶束样品的 HPLC谱图;由于在消化过程中样品不断被稀释,色谱图 呈现的峰面积为样品经提取浓缩得到的各物质峰面积。
游离脂肪酸是混合胶束的重要组成成分,影响着混合胶束对脂溶性活性成分的溶解能力,从而影响β-胡萝卜素的生物可给性。β-胡萝卜素存在于油脂的疏水核心之中[39],只有当油脂被脂肪酶消化后β-胡萝卜素才能释放出来,才能从植物组织转移到由游离脂肪酸、胆盐、磷脂等形成的混合胶束中,油脂的消化速率和形成的混合胶束均可能影响其生物可给性。从图9中可以看出,玉米油长链油脂的胶束粒径在250 nm左右,而MCT油脂的胶束粒径为45 nm,MCT赋形剂乳液形成的混合胶束粒径显著小于玉米油赋形剂乳液(p<0.05),这是因为长链油脂更容易与胆盐、磷脂等形成疏水结构大的混合胶束[40]。混合胶束过小的粒径可能阻碍了β-胡萝卜素进入,从而影响其生物可给性。

图9 不同类型橘子/赋形剂乳液的混合胶束平均粒径(d32)Fig.9 The mean particle diameter(d32)of the mixed micelles of orange/excipient emulsion
图11中,PBS对照组与长链油脂制备的小、中、大粒径大小赋形剂乳液的生物可给性分别为6%、38.13%、24.93%和26.23%,这表明与PBS对照组相比,长链油脂的赋形剂乳液对橘子中β-胡萝卜素的生物可给性有显著提高(p<0.05),并且小粒径赋形剂乳液提升效果优于中粒径和大粒径赋形剂乳液。这是由于赋形剂乳液的粒径大小决定了油脂暴露在胃肠消化液中的表面积,在油脂的量一定的情况下,小粒径赋形剂乳液具有更大的比表面积,有利于橘子组织中β-胡萝卜素的释放,油脂的消化速率和消化程度更高,可形成更多的混合胶束来容纳β-胡萝卜素[41-42]。从图11中未得到MCT油脂的生物可给性数据,这是因为MCT油赋形剂乳液在胶束阶段没有检测到β-胡萝卜素的含量,结合图8(b)来看,长链油脂与中链油脂的消化程度无显著差异,因此两种赋形剂乳液形成的不同混合胶束对β-胡萝卜素生物可给性的影响起到主导作用。长链脂肪酸形成的混合胶束具有更大的疏水区域[43],对相对较长的疏水性物质β-胡萝卜素具有更高的溶解能力,因此长链油脂对于提高β-胡萝卜素的生物可给性更加有效。这一研究结果与Liu和Ruojie研究不同类型油脂制备的赋形剂乳液对于提高黄椒[35]、芒果[21]和胡萝卜[44]中的β-胡萝卜素的生物可给性结果一致。

图11 不同赋形剂乳液对橘子中β-胡萝卜素生物可给性的影响Fig.11 The impact of the different excipient emulsions on the bioaccessibility of β-carotene from orange注:N/A表示未得出数据。
3 结论
结果表明,乳液经过模拟消化过程中,静电作用会改变非离子表面活性剂表面的界面状态和张力,从而导致乳液发生聚集和絮凝,小粒径乳液更易发生絮凝,大粒径乳液中的大油滴能够抵抗粘蛋白分子对其的絮凝作用,MCT乳液对胃酸性环境也有一定抵抗作用。在模拟小肠阶段,由于形成不同阴离子胶体颗粒,乳液带电量显著增加(p<0.05),但大粒径乳液的电位没有显著变化。MCT乳液会在小肠消化阶段形成一些较大的囊泡,导致粒径显著增大(p<0.05)。小粒径(200 nm)乳液由于其暴露在消化酶中的比表面积最大,油滴与消化酶之间的接触面积和反应机会更多,因而对于提高β-胡萝卜素的生物可给性的效果优于中粒径和大粒径乳液。长链油脂制备的赋形剂乳液经过体外模拟消化后,产生的长链脂肪酸形成的混合胶束粒径更大,可能具有更大的疏水区域和溶解β-胡萝卜素的能力,因此对提高橘子中β-胡萝卜素的生物可给性具有更显著的影响。
本实验研究结果对于目的性设计赋形剂乳液的粒径大小及油脂链长来提高果蔬中类胡萝卜素的生物可给性具有重要指导意义,并为后续动物细胞实验探究不同赋形剂乳液对果蔬中类胡萝卜素在体内的生物利用率奠定基础。
