大曲酒糟中纤维素提取工艺的优化
2019-05-14杨英柏松
杨英,柏松
(四川化工职业技术学院,四川泸州 646099)
酒糟在我国产量相当大,且酒糟中含有大量的可再利用资源。一般厂家,不是卖作饲料就是丢弃,不仅浪费资源,而且污染环境。本文将酒糟作为提取纤维素的原料,将其资源化,不仅能解决酒糟的污染问题,还能变废为宝,生产出有用的物质,并相应地降低解决生产成本。课题围绕提高大曲酒糟中纤维素的提取率展开,优化已有的研究思路,采用酸水解、碱水解及酶水解相结合的提取方式进行小量提取研究实验。针对水解时碱浓度、料液比及温度对水解的影响不同,设计不同试验加入量,最终筛选出较优的提取工艺。
1 实验材料
实验原料:大曲酒糟(泸州老窖提供)。
2 实验方法
2.1 纤维素的提取工艺流程
水洗→95%乙醇处理→乙醚处理→α-淀粉酶水解→糖化酶水解→碱水解→蛋白酶水解→漂白、去木质素→酸水解→干燥,称量。
2.2 纤维素提取操作要点
(1)水洗
称取大曲酒糟粉末9份,每份 10g于250ml锥形瓶,加入250ml蒸馏水,浸泡2h后,抽滤。
(2)95%乙醇处理
向水洗后的滤渣中,按1:10比例加入100ml95%乙醇,浸泡20min后,抽滤,再加入50ml95%乙醇,浸泡10min后,抽滤。
(3)乙醚处理
向上述滤渣中加入100ml乙醚,浸泡30min后,抽滤,再加入50ml乙醚,浸泡15min后,抽滤。
(4)α-淀粉酶水解
淀粉酶是将淀粉水解为糊精,糖化酶是将糊精水解为葡萄糖,葡萄糖通过过滤可以除去,因此,淀粉水解彻底才能彻底被除去。具体方法为[1],向滤渣中加入100ml蒸馏水后,加热煮沸15min,使淀粉糊化,放冷至60℃以下,调节pH为5.5,先加入40ml浓度为2.0%的α-淀粉酶溶液50℃水解1h,并不时搅拌。取一滴于白色点滴板上,加一滴碘液应不呈蓝色,若呈蓝色,再加热糊化,冷却至60℃以下,再加入40ml淀粉酶溶液,继续水解,直至酶解液加碘不呈蓝色为止。加热煮沸使酶失活,抽滤至中性。
(5)糖化酶水解[2]
调节pH为4.4时,向各样品中加入100ml浓度为0.2%的糖化酶溶液,50℃水解1h后,抽滤至中性。
(6)碱水解
纤维素的提取率因与碱浓度、料液比、以及碱水解温度有很大的关系,应用最佳的碱水解工艺来提取纤维素[3],据资料显示,料液比在1:9至1:11之间效果较好[4],所以设计碱水解因素水平表如表1所示:
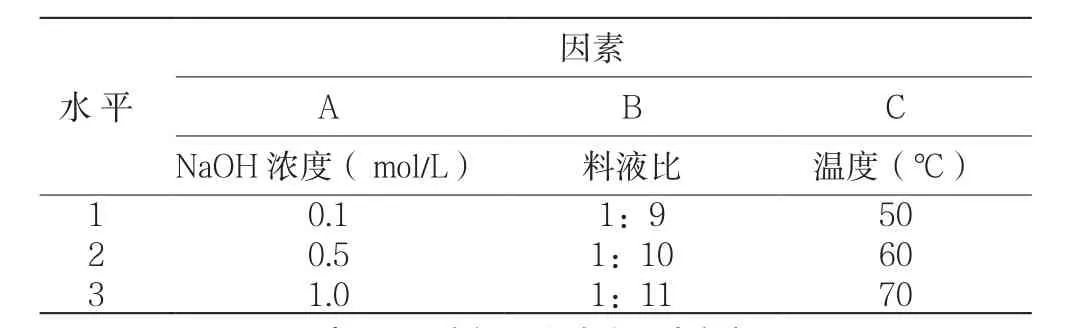
表1 碱水解因素水平表
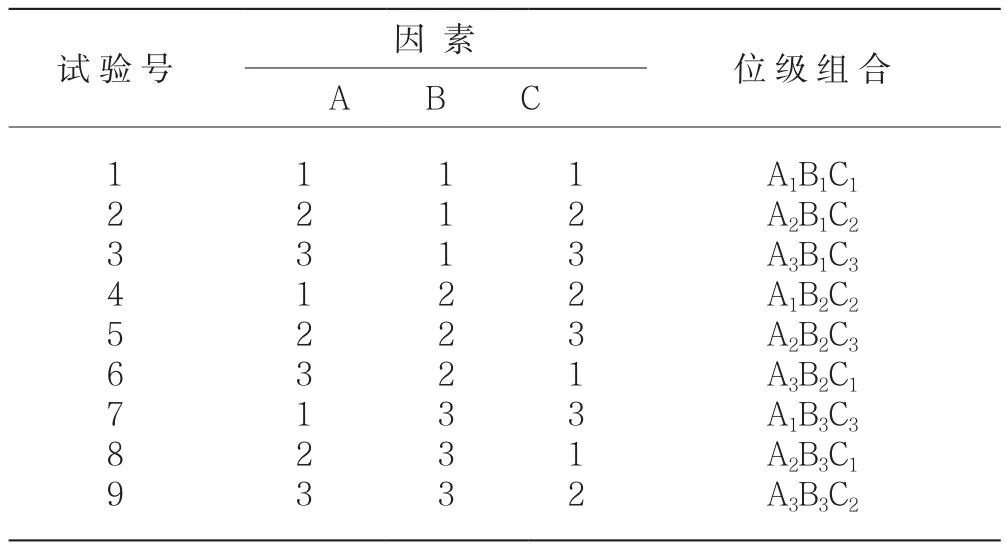
表2 碱水解正交试验设计方案
表2设计方案中[5],A表示NaOH浓度(mol/l),B表示料液比,C表示碱水解温度,位级组合为A、B、C三个因素的组合方式,按设计方案进行实验,碱水解3h后,以4000r/min离心5min后,可观察到沉淀分为两部分,其中上部分为棕色粘稠状物质,因半纤维素等易溶于碱水,故形成粘稠状物质,最后水洗至中性,并将沉淀转移至100ml锥形瓶内。
(7)蛋白酶水解[6]
向上述各沉淀中加入25ml浓度为50μg/ml的蛋白酶K溶液,并调节pH为8.0,于37℃恒温水浴2h后,抽滤,并水洗至中性[5]。
(8)漂白、去木质素[7]
向上述沉淀中加入50ml浓度为5%的次氯酸钠溶液,用36%的乙酸调节pH为5.0,75℃恒温水浴2h后,冷却至室温后,抽滤[6],此时,可观察到滤液为黄色。
(9)酸水解
经1至8步骤处理后,样品中可能还有部分糖类、果胶等物质存在,可向滤渣中加入50ml煮沸的浓度为1.25%的硫酸溶液,加热微沸10min,以使糖类、果胶等水解除去,最后抽滤,并水洗至中性[6]。
(10)将滤渣于恒温干燥箱中干燥至恒重,并称量。
2.3 纤维素含量测定──碘量法测定[8]
2.3.1 原理
试样用乙酸和硝酸混合液加热处理,淀粉、多缩戊糖、木质素、半纤维素、色素、单宁和其他物质发生水解而被除去,纤维被分解成单个的纤维素。用水洗涤除杂质后,纤维素在硫酸下被重铬酸钾氧化成二氧化碳和水,过剩的重铬酸钾用碘量法测定。
2.3.2 操作方法
称取0.05g产品于试管中,加入5ml乙酸和硝酸混合液,置于沸水中煮沸25min,并不时搅拌。
取出、冷却后离心,4000r/min,离心5min,弃去上清液,向沉淀中加入10ml水,混匀,离心,又倒去上清液(如此重复洗涤3次)。
向上述沉淀中准确加入10ml质量分数为10%的硫酸溶液和10ml 0.1mol/L的重铬酸钾溶液,摇匀,浸入沸水中煮沸10min。
冷却后,把溶液部分转移入250ml烧杯中,用20-30ml水冲洗沉淀,洗涤液并入烧杯中,再加入5ml质量分数为20%的KI溶液,放置5min。
向上述溶液中滴加0.2mol/L的硫代硫酸钠溶液,直至溶液由棕红色变为黄色时,加入2ml0.5%淀粉指示剂溶液,继续滴定至溶液由蓝色变为亮绿色为止,并记录所消耗溶液的量。
按同样的操作,以0.2mol/L的硫代硫酸钠溶液单独滴定加入了10ml质量分数为20%的硫酸溶液和10ml浓度为0.1mol/L的重铬酸钾溶液作为空白样,经测定滴定空白样品所消耗的硫代硫酸钠体积为21.4ml。
2.3.3 纤维素含量计算[9]
纤维素含量按下式进行计算:
X=K(a-b)/n×24
式中:X为纤维素百分含量(%)。“24”为1molC6H10O5相当硫代硫酸钠的当量数。K为硫代硫酸钠的浓度(mol/L)。a为空白滴定所消耗硫代硫酸钠体积(ml)。b为溶液所消耗硫代硫酸钠体积(ml)。n为纤维素产品质量(g)。
测定结果及分析如表3:
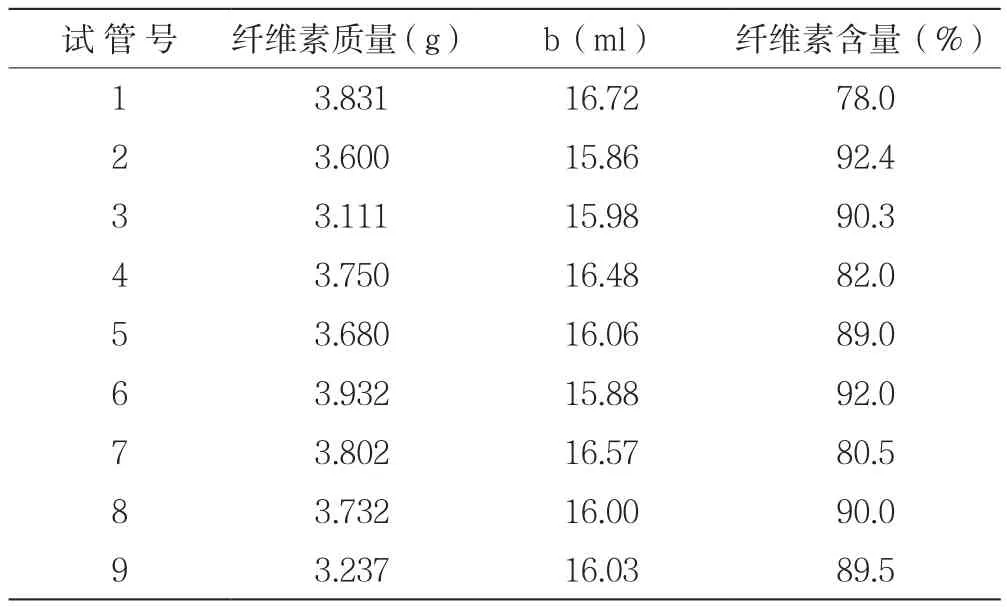
表3 大曲酒糟提得纤维素测定结果
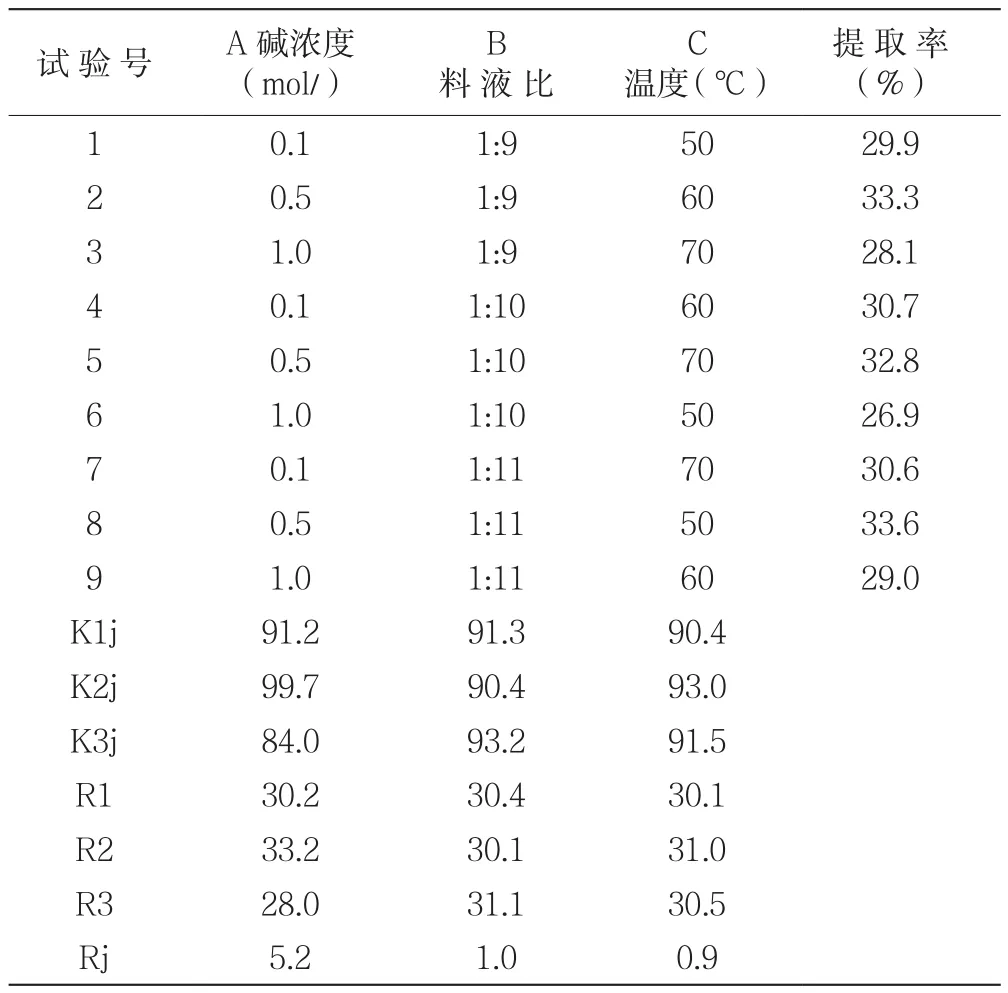
表4 大曲酒糟提取纤维素正交试验及极差分析
极差分析如图1所示:
图中R1为碱浓度对纤维素提取率影响程度的极差分析折线图,R2为料液比对纤维素提取率影响程度的极差分析折线图,R3为温度对纤维素提取率影响程度的极差分析折线图,R越大对提取率的影响越大,从极差R分析可知,RA>RB>RC,在影响大曲酒糟纤维素提取率的诸多因素中,根据影响程度大小的次序为A>B>C,较优的提取条件为A2(0.5mol/L)、B3(1:11)、C2(60℃),即NaOH溶液浓度为0.5mol/L、料液比为1:11,温度为60℃。
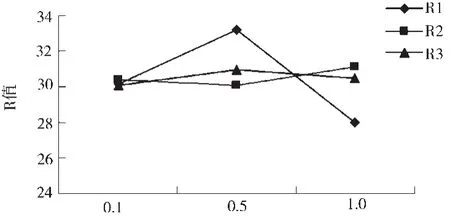
图1 极差分析NaOH浓度(mol/l)
3 结论
从纤维素提取率角度分析,NaOH浓度对其影响最大,浓度确定在0.5mol/L时,提取率最大。纤维素在较高浓度碱溶液中会发生水解,通过极差分析也表明纤维素在碱浓度为1.0mol/L时发生了轻度水解,因此,碱浓度为0.5mol/L时纤维素的提取率较高;因大曲酒糟含稻壳较多,因而料液比应为1:11效果最佳;综合考虑,大曲酒糟纤维素提取较优提取工艺条件为NaOH浓度0.5mol/L,料液比1:11,碱水解温度60℃;
