预包装中药代煎剂微生物限度检查方法研究
2019-03-11沙禕炜张学博郁爱萍陆春胜
沙禕炜 张学博 郁爱萍 陆春胜
中药煎煮剂是中药口服处方的常用种类, 现今大多数中药煎煮剂都采取代加工的方式生产, 即称为预包装中药代煎剂, 目前对于该类产品没有规定进行产品质量检验, 而中药代煎剂的生产环境和关键工艺如控制不严, 极有可能对中药煎煮剂终产品的卫生质量提出挑战[1-3], 尤其是芽孢杆菌、霉菌和酵母菌等耐高渗透压和耐热性微生物[4-6]的残留, 以及预包装中药代煎剂采用“一次制备, 分次服用”的形式,也可能会造成部分微生物的复苏、繁殖, 甚至产生毒素[7],造成对人体不可挽回的伤害。根据中华人民共和国药典(2015年版)四部[8]通则微生物限度检查法(1105、1106、1107)的相关规定, 对预包装中药代煎剂中微生物情况进行研究,从需氧菌总数计数及霉菌和酵母菌总数计数, 控制菌中大肠埃希菌检查法着手, 建立通用性的微生物限度检查方法。
1 材料与方法
1.1 样品及培养基等 预包装中药代煎剂(上海青浦中药饮片厂, 批号:20180626);沙氏葡萄糖琼脂培养基(SDA)、麦康凯液体培养基、TSB、麦康凯琼脂培养基、沙氏葡萄糖液体培养基(SDB)、pH 7.0无菌氯化钠-蛋白胨缓冲液和胰酪大豆胨琼脂培养基(TSA)均由北京陆桥技术股份有限公司提供;0.9 %无菌氯化钠溶液自备。
1.2 仪器设备 SN310C型高压蒸汽灭菌器(重庆雅马拓科技有限公司, 重庆)、MJ-180B型霉菌培养箱(上海跃进医疗器械厂, 上海)、AC2-6S1型生物安全柜(ESCO, 新加坡)、MJX-100B-Z型霉菌培养箱(上海博迅实业有限公司医疗设备厂 , 上海 )。
1.3 标准菌种 黑曲霉(aspergillus niger)[来源:CMCC(F)98003]、金黄色葡萄球菌(staphylococcus aureus)[来源:CMCC(B)26003]、铜绿假单胞菌(pseudomonas aeruginosa)[来源:CMCC(B)10104]、大肠埃希菌(escherichia coli)[来源:CMCC(B)44102]、白色念珠菌(candida albicans)[来源:CMCC(F)98001]和枯草芽孢杆菌(bacillus subtilis)[来源:CMCC(B)63501]均由广东环凯微生物科技有限公司提供。
1.4 菌液的制备 用金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、大肠埃希菌的新鲜培养物接种至胰酪大豆胨液体培养基中, 培养24 h(35℃)后, 用0.9%无菌氯化钠溶液进行10倍稀释上述1 ml的培养物, 分别稀释成菌悬液为1000~10000 CFU/ml(其中大肠埃希菌约为≤100 CFU/ml的菌悬液);用白色念珠菌的新鲜培养物接种至沙氏葡萄糖液体培养基中, 培养2 d(25℃)后, 用0.9%无菌氯化钠溶液进行10倍稀释上述1 ml的培养物, 稀释成菌悬液为1000~10000 CFU/ml;用黑曲霉的新鲜培养物接种至沙氏葡萄糖琼脂培养基中, 培养6 d(25℃)后, 用0.9%无菌氯化钠溶液洗脱并进行10倍稀释上述孢子悬液, 稀释成孢子悬液为1000~10000 CFU/ml。
1.5 供试液和培养基的制备 取预包装中药代煎剂样品1袋, 充分摇匀后, 立即吸取10 ml的样品溶液置于含100 ml pH 7.0氯化钠蛋白胨缓冲液的已灭菌密盖容器中, 充分振摇荡洗≥10 min后, 放置待沉淀下降取上层液即制备成供试液(1∶10)。
1.6 需氧菌总数、霉菌和酵母菌计数方法适用性试验
1.6.1 需氧菌总数测定
1.6.1.1 试验组 取1∶10供试液9.9 ml和铜绿假单胞菌悬液0.1 ml混合, 吸取1 ml上述供试液平均放入5个平皿(0.2 ml/皿)后, 立即倾注胰酪大豆胨琼脂培养基后, 再35℃培养≤3 d, 加和所有平皿后合计铜绿假单胞菌数。另取金黄色葡萄球菌和枯草芽孢杆菌同法操作;黑曲霉和白色念珠菌培养前同法操作, 其后培养时间≤5 d。
1.6.1.2 菌液对照组 分别取上述5种菌悬液(孢子悬液)0.1 ml和9.9 ml pH 7.0无菌氯化钠-蛋白胨缓冲液混匀,分别吸取1 ml上述供试液平均放入5个平皿(0.2 ml/皿)后,立即倾注胰酪大豆胨琼脂培养基后培养, 同法计数。
1.6.1.3 供试品对照组 取1∶10供试液, 用无菌pH 7.0氯化钠蛋白胨缓冲液代替菌液吸取1 ml上述供试液平均放入5个平皿(0.2 ml/皿)后, 立即倾注胰酪大豆胨琼脂培养基后培养, 同法计数。
1.6.1.4 回收试验 5种标准菌种在试验组、菌液对照组中平行操作各2次, 供试品对照组平行制备2份。

1.6.2 霉菌和酵母菌总数测定
1.6.2.1 试验组 取1∶10供试液9.9 ml和白色念珠菌菌悬液0.1 ml混合, 取混合液1 ml分注5个平皿, 0.2 ml/皿,立即倾注SDA, 置规定温度培养, 以5个平皿菌落总和计数。另取黑曲霉孢子悬液同法操作。
1.6.2.2 菌液对照组 分别取上述两种菌悬液(孢子悬液)0.1 ml和9.9 ml pH 7.0无菌氯化钠-蛋白胨缓冲液混匀,吸取1 ml上述供试液平均放入5个平皿(0.2 ml/皿)后, 立即倾注沙氏葡萄糖琼脂培养基后培养, 同法计数。
1.6.2.3 供试品对照组 取1∶10供试液, 用无菌pH 7.0氯化钠蛋白胨缓冲液代替菌液吸取1 ml上述供试液平均放入5个平皿(0.2 ml/皿)后, 立即倾注沙氏葡萄糖琼脂培养基后培养, 同法计数。
1.6.2.4 回收试验 2种标准菌种在试验组、菌液对照组中平行操作各2次, 供试品对照组平行制备2份。

1.7 控制菌大肠埃希菌检查方法适用性试验
1.7.1 试验组 在100 ml胰酪大豆胨液体培养基中同时接种1 ml大肠埃希菌菌液和上述供试液(1∶10)10 ml, 经增菌培养1 d(35℃)后, 在100 ml麦康凯液体培养基中转接上述1 ml增菌液, 继续培养2 d(43℃)后, 直接在麦康凯琼脂培养基平板上划线转接, 最后培养3 d(35℃)即得。
1.7.2 阳性对照组 在100 ml胰酪大豆胨液体培养基中同时接种1 ml大肠埃希菌菌液和pH 7.0无菌氯化钠-蛋白胨缓冲液10 ml, 经增菌培养1 d(35℃)后, 在100 ml麦康凯液体培养基中转接上述1 ml增菌液, 继续培养2 d(43℃)后, 直接在麦康凯琼脂培养基平板上划线转接, 最后培养3 d(35℃)即得。
1.7.3 阴性对照组 在100 ml胰酪大豆胨液体培养基中直接接种pH 7.0无菌氯化钠-蛋白胨缓冲液10 ml, 经增菌培养1 d(35℃)后, 在100 ml麦康凯液体培养基中转接上述1 ml增菌液, 继续培养2 d(43℃)后, 直接在麦康凯琼脂培养基平板上划线转接, 最后培养3 d(35℃)即得。
1.7.4 结果 试验组中生长的大肠埃希菌通过生化和分子生物学鉴定后确证;阳性对照组大肠埃希菌生长良好;阴性对照组无菌落生长。
2 结果
2.1 微生物限度检查法方法适用性试验结果判定 需氧菌总数、霉菌和酵母菌总数试验组各个目标菌的菌数回收比值在0.5~2.0, 控制菌检查试验组检出试验菌大肠埃希菌, 符合中国药典2015年版的要求。见表1, 表2。

表1 需氧菌总数试验结果
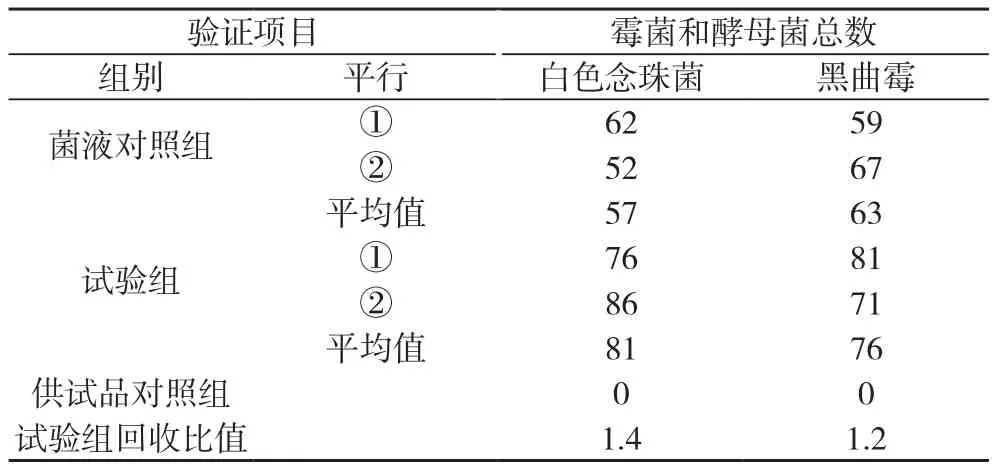
表2 霉菌和酵母菌总数试验结果
2.2 微生物限度检查法的建立 按照本文研究的方法适用性结果, 预包装中药代煎剂的通用性微生物限度检查方法为:取预包装中药代煎剂样品1袋, 充分摇匀后, 立即吸取10 ml的样品溶液置于含100 ml pH 7.0氯化钠蛋白胨缓冲液的已灭菌密盖容器中, 充分振摇荡洗≥10 min后, 放置待沉淀下降取上层液即制备成供试液(1∶10), 用培养基稀释法(0.2 ml/皿)进行需氧菌总数计数及霉菌和酵母菌总数计数;取1∶10的供试液10 ml, 接种至100 ml TSB中, 进行大肠埃希菌检查。
3 讨论
3.1 预包装中药代煎剂样品的选择, 根据国家中医药管理局发布《古代经典名方目录(第一批)》中筛选了4种:“麻黄汤”、“芍药甘草汤”、“小承气汤”和“泽泻汤”分别进行试验, 都满足要求。
3.2 预包装中药代煎剂样品的制备, 从原料中药饮片到成品预包装中药代煎剂, 都处于完全模拟委托代煎的全流程操作过程[9-14]。
3.3 供试品前处理法首先考虑薄膜过滤法, 由于供试品看似溶液状态但是含有较多很细小的不溶性药物残渣无法滤过薄膜;后直接用常规平皿倾注法但试验菌回收试验比值不满足要求。采用液体培养基直接稀释法, 取样品10 ml直接接种到200 ml TSB中培养和取样品20 ml直接接种到500 mlTSB中培养等方法阳性菌均不明显生长。
