理气散结浸膏对小鼠和大鼠急性毒性研究
2018-12-05魏谭军胡凤娇王张肖成宋文杰周殿儒孙位军王毅
魏谭军,胡凤娇,王张,肖成,宋文杰,周殿儒,孙位军,王毅
理气散结浸膏,由柴胡、香附、延胡索、甘草、青皮、蜂房、山慈菇、川芎、当归、白芍等组成,具有理气调血、散结止痛的功效,主治肝郁血瘀,乳腺增生,乳癖结块,乳痈初起,乳房胀痛。此剂型为理气散结丸的改良剂型,原剂型是达州市中西医结合医院临床使用20余年的医疗机构制剂,系药材直接打粉后制成的大蜜丸,存在服用剂量大、口感差、运输携带保存不便、起效缓慢、患者依从性不好、原粉入药微生物易超标等缺点,不仅给患者带来不便,也限制了该药的推广。此次改良剂型,可以更优化的保存药效、稳定质量、减小服用量,便于临床应用,扩大市场规模,受众更广。
根据国家食品药品监督管理局制定的《医疗机构制剂注册管理办法》(试行,局令第20号,2005年[4];征求意见稿, 2015年[5])和四川省食品药品监督管理局制定的《四川省医疗机构制剂研究技术指南(试行版)》(2014年)[6],理气散结颗粒拟申请四川省医疗机构中药制剂批文,因该处方组成含有法定标准中标识有毒性或现代毒理学证明有毒性的药材,如山慈菇和蜂房[7],故需开展急性毒性实验研究,可为长期毒性试验和主要药效学研究中的剂量设置提供依据。
1 材料和方法
1.1 试验药物
理气散结浸膏,生产批号为151125,由达州市中西医结合医院生产。按照理气散结颗粒的最大给药浓度和最大给药体积分别给予小鼠和大鼠后,给药剂量较低,不足以充分暴露其毒性,故改用理气散结浸膏(仅未添加制备成颗粒的辅料糖粉和糊精),尽可能的以实验可操作的最大浓度开展急性毒性实验。
生理盐水:规格为500 mL:4.5 g,批号为C151136,由昆明南疆制药有限公司生产。
1.2 试验动物
SPF级KM种小鼠和SD大鼠各40只,全雌,体重为20±2 g、200±20 g,由成都达硕实验动物有限公司提供,实验动物生产许可证号:SCXK(川)2015-030,《四川省实验动物质量合格证》号:№51203500000542。
动物实验设施、场地由成都中医药大学提供。
1.3 试剂
血常规试剂:溶血剂(批号1608014)、稀释剂(批号1607022)、清洗剂(批号1608018)。
血液生化学试剂:谷丙转氨酶(批号1612118)、谷草转氨酶(批号1611104)、碱性磷酸酶(批号1603110)、谷氨酰转移酶(批号1605132)、总胆红素(批号1603111)、总蛋白(批号1611109)、白蛋白(批号1604101)、尿素氮(批号1604212)、肌酐(批号1609114)、胆固醇(批号1610110)、甘油三脂(批号1612101)、葡萄糖(批号1603114)、肌酸激酶(批号1605135)。
血常规试剂和血液生化学试剂均购自上海特康科技有限公司。
1.4 仪器
全自动生化分析仪,型号TC6010L,产自上海特康科技有限公司;全自动三分群血液分析仪,型号TEK-Ⅱ MINI,产自上海特康科技有限公司。
1.5 实验方法
1.5.1 预实验 小鼠和大鼠分别按最大给药容积40和20 mL﹒kg-1给予最大浓度2.4365 g原生药材/mL的理气散结浸膏溶液后,动物仍未出现死亡,故给予理气散结浸膏原液无法测出LD50。因此,按《中药、天然药物急性毒性研究技术指导原则》的要求,依据“动物能耐受的最大给药容积、最大给药浓度的药量单次或24 h内多次(2~3次)给药”的规定,采用最大给药量法评价理气散结浸膏的急性毒性[3]。
1.5.2 动物分组 将实验小鼠和大鼠按体重分层,随机分为空白对照组和理气散结浸膏组,每组20只,试验前禁食16小时,但不禁水。
1.5.3 给药方法 经预试结果可知,理气散结浸膏组小鼠可按照最大容积(40 mL﹒kg-1)、最大给药浓度2.4365 g生药/mL一次性灌胃给药,即给药剂量为97.46 g生药/(kg.d);理气散结浸膏组大鼠可按照最大容积(20 mL﹒kg-1)、最大给药浓度2.4365 g生药/mL分两次灌胃给药,每次间隔4 h,即给药剂量为48.73 g生药/(kg﹒d)。空白对照组均给予最大容积的生理盐水。给药后1 h内,观察并记录动物是否出现中毒反应以及中毒反应的出现时间、维持时间、是否可逆及严重程度,分析可能的靶器官、组织或系统。后每天观察1次,连续观察14天。
1.5.4 观察指标
1.5.4.1 一般状况观察 观察并记录各组每只动物有无异常,注意有无颤抖、震颤、抽搐、流涎、腹泻、少动、精神萎靡不振、昏迷等毒性反应症状。同时观察中毒反应的出现时间、维持时间、是否可逆及严重程度,分析可能的靶器官、组织或系统。
1.5.4.2 体重和饲料消耗量 在给药前1天、给药当天、给药后第7天和第14天时,观察和记录各组动物的体重(g)变化及进食(饲料消耗量,g/(kg﹒d))情况。
1.5.4.3 血常规和血液生化学检测 在给药后第14天时,观察未死亡动物的一般情况、天然孔道情况,然后小鼠摘眼球取血,其中每组的10只小鼠取0.5~1 mL抗凝处理,另10只小鼠取0.5~1 mL凝固后分离血清0.3~0.5 mL;大鼠以3 mL﹒kg-1腹腔注射10%的水合氯醛麻醉后,经腹主动脉取血,其中取0.5~1 mL抗凝处理,另取0.5~1 mL凝固后分离血清0.3~0.5 mL,检测相应血常规和血液生化学指标。
1.6 统计学应用
运用SPSS 19.0计学软件进行数据分析,计量资料数据用均数±标准差(±S)表示,两组间比较采用t检验;以P<0.05为差异有统计学意义。
2 结果
2.1 一般状况和尸检结果
灌胃30 min~1 h内,小鼠和大鼠均出现精神萎靡、行动迟缓、鼻尖微微发红的症状,但很快恢复正常,观察期内,无动物死亡。尸检,脏器均未出现肉眼可见病变。
2.2 体重及饲料消耗量
2.2.1 小鼠 与给药前一天比较,给药后第1、7、14天,各组小鼠的体重及饲料消耗量均存在显著性差异(P<0.05,P<0.01);与空白对照组比较,无统计学意义(P>0.05),详见表1、表2。
表1 小鼠体重的变化情况(g, ±S)

表1 小鼠体重的变化情况(g, ±S)
注:与给药前1天比较,# P<0.05,## P<0.01;与空白对照组比较,* P<0.05,** P<0.01
组别 剂量g生药﹒kg-1﹒d-1 给药前1天 给药后第1天 给药后第7天 给药后第14天空白对照组(n=20) —— 23.06±1.10 23.84±1.20# 26.20±1.53## 27.88±1.55##理气散结浸膏组(n=20) 97.46 23.40±0.86 24.37±0.90## 25.55±2.83## 27.56±1.78##
表2 小鼠饲料消耗量的变化情况(g﹒kg-1﹒d-1, ±S)

表2 小鼠饲料消耗量的变化情况(g﹒kg-1﹒d-1, ±S)
注:同上
组别 剂量g生药﹒kg-1﹒d-1 给药前1天 给药后第1天 给药后第7天 给药后第14天空白对照组 —— 216.06±7.64 169.54±36.97 157.78±10.14## 157.93±8.53##理气散结浸膏组 97.46 222.10±11.83 145.82±21.99## 177.16±23.44# 152.74±8.12##
2.2.2 大鼠 与给药前一天比较,给药后第1天,大鼠的饲料消耗量显著降低(P<0.05),给药后第7、14天,各组大鼠体重有十分显著地差异(P<0.01);与空白对照组比较,给药后第1天,大鼠的饲料消耗量显著降低(P<0.05),详见表3、表4。
表3 大鼠体重的变化情况(g, ±S)

表3 大鼠体重的变化情况(g, ±S)
注:同上
组别 剂量g生药﹒kg-1﹒d-1 给药前1天 给药后第1天 给药后第7天 给药后第14天空白对照组(n=20) —— 215.77±6.41 216.07±5.12 233.16±8.74## 246.96±8.67##理气散结浸膏组(n=20) 48.73 212.44±5.02 213.91±5.17 228.54±9.18## 242.70±12.89##
表4 大鼠饲料消耗量的变化情况(g﹒kg-1﹒d-1, ±S)
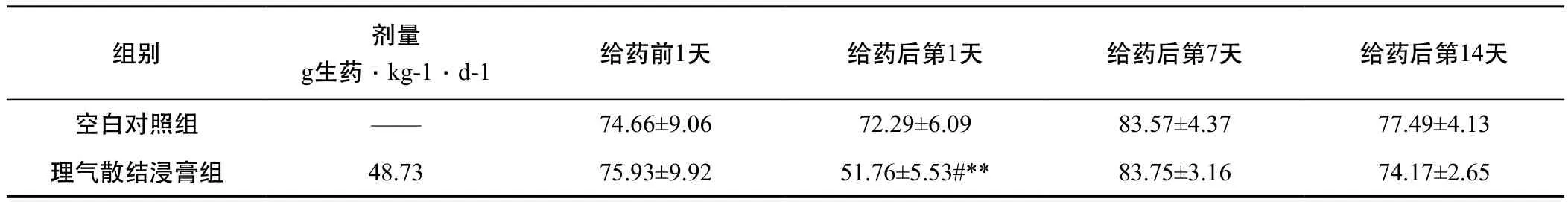
表4 大鼠饲料消耗量的变化情况(g﹒kg-1﹒d-1, ±S)
注:同上
组别 剂量g生药﹒kg-1﹒d-1 给药前1天 给药后第1天 给药后第7天 给药后第14天空白对照组 —— 74.66±9.06 72.29±6.09 83.57±4.37 77.49±4.13理气散结浸膏组 48.73 75.93±9.92 51.76±5.53#** 83.75±3.16 74.17±2.65
2.3 血常规
2.3.1 小鼠 与空白对照组比较,理气散结浸膏经口一次性灌胃给予小鼠后14天,动物血红蛋白(HGB)、红细胞比积(HCT)、平均红细胞体积(MCV)和平均血小板体积(MPV)差异显著(P<0.05),但其变化均在正常范围内;其余各项血常规指标均无显著性差异(P>0.05),详见表5、表6。
表5 小鼠的血常规测定结果(±S)
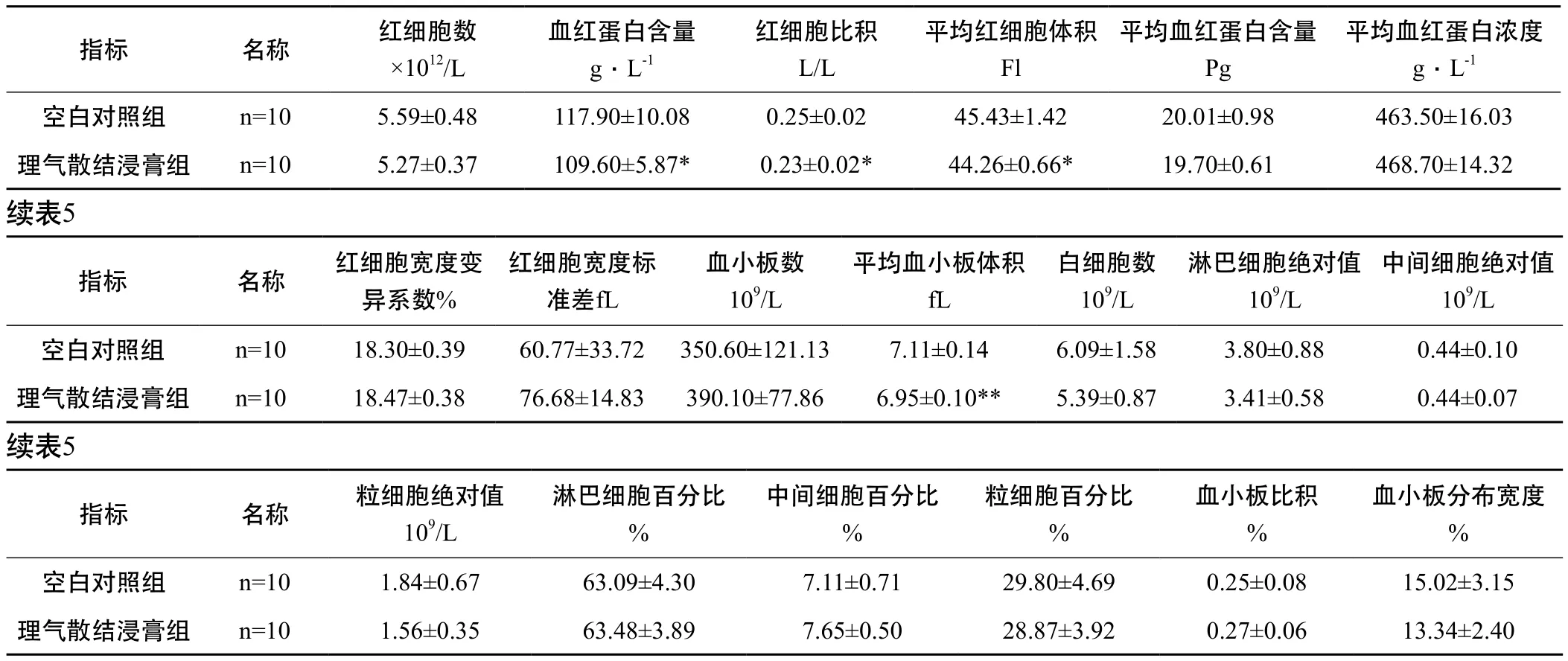
表5 小鼠的血常规测定结果(±S)
注:与空白对照组比较,* P<0.05,** P<0.01
血红蛋白含量g﹒L-1指标 名称 红细胞数×1012/L红细胞比积L/L平均红细胞体积Fl平均血红蛋白含量Pg平均血红蛋白浓度g﹒L-1空白对照组 n=10 5.59±0.48 117.90±10.08 0.25±0.02 45.43±1.42 20.01±0.98 463.50±16.03理气散结浸膏组 n=10 5.27±0.37 109.60±5.87* 0.23±0.02* 44.26±0.66* 19.70±0.61 468.70±14.32续表5中间细胞绝对值109/L空白对照组 n=10 18.30±0.39 60.77±33.72 350.60±121.13 7.11±0.14 6.09±1.58 3.80±0.88 0.44±0.10理气散结浸膏组 n=10 18.47±0.38 76.68±14.83 390.10±77.86 6.95±0.10** 5.39±0.87 3.41±0.58 0.44±0.07指标 名称 红细胞宽度变异系数%红细胞宽度标准差fL血小板数109/L平均血小板体积fL白细胞数109/L淋巴细胞绝对值109/L续表5血小板分布宽度%空白对照组 n=10 1.84±0.67 63.09±4.30 7.11±0.71 29.80±4.69 0.25±0.08 15.02±3.15理气散结浸膏组 n=10 1.56±0.35 63.48±3.89 7.65±0.50 28.87±3.92 0.27±0.06 13.34±2.40指标 名称 粒细胞绝对值109/L淋巴细胞百分比%中间细胞百分比%粒细胞百分比%血小板比积%
2.3.2 大鼠 与空白对照组比较,理气散结浸膏经口分两次灌胃给予大鼠后14天,各项血常规指标均无显著性差异(P>0.05),详见表6。
表6 大鼠的血常规测定结果(±S)
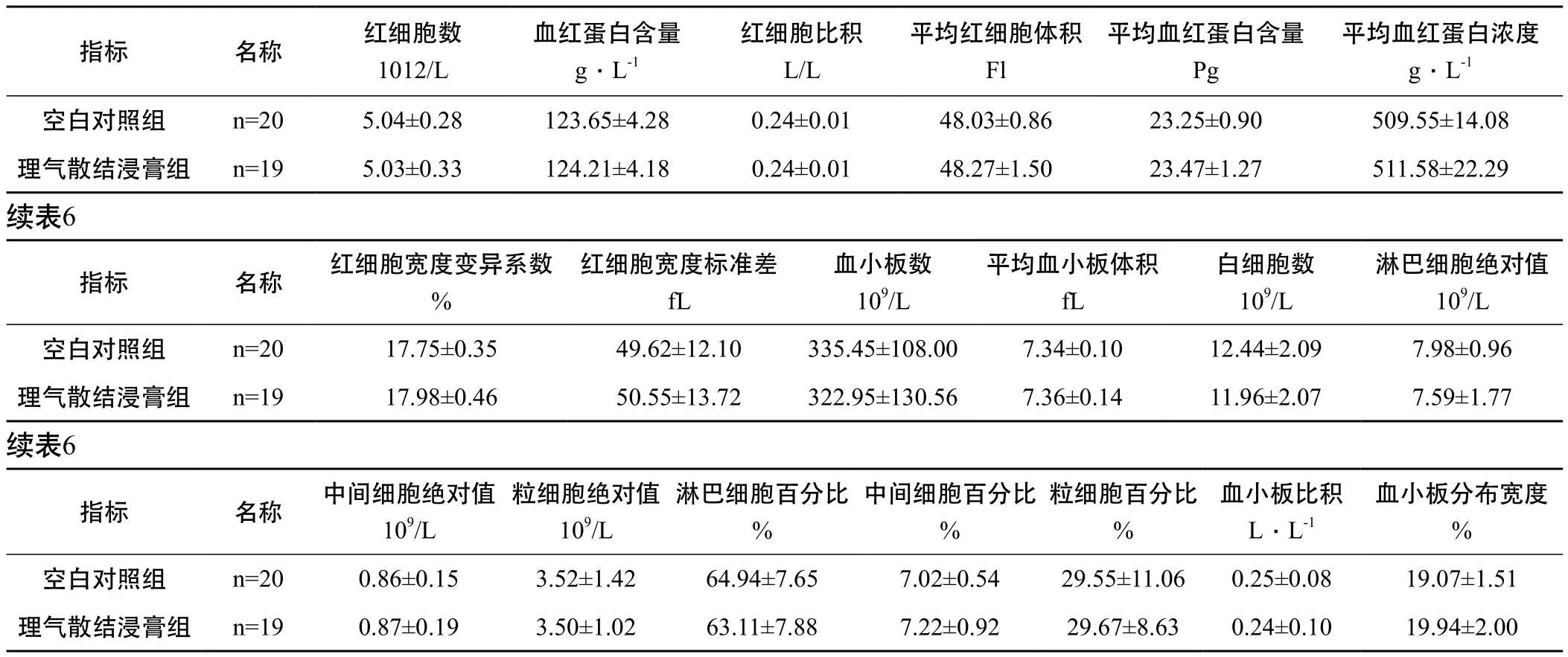
表6 大鼠的血常规测定结果(±S)
注:与空白对照组比较,* P<0.05,** P<0.01
血红蛋白含量g﹒L-1指标 名称 红细胞数1012/L红细胞比积L/L平均红细胞体积Fl平均血红蛋白含量Pg平均血红蛋白浓度g﹒L-1空白对照组 n=20 5.04±0.28 123.65±4.28 0.24±0.01 48.03±0.86 23.25±0.90 509.55±14.08理气散结浸膏组 n=19 5.03±0.33 124.21±4.18 0.24±0.01 48.27±1.50 23.47±1.27 511.58±22.29续表6淋巴细胞绝对值109/L空白对照组 n=20 17.75±0.35 49.62±12.10 335.45±108.00 7.34±0.10 12.44±2.09 7.98±0.96理气散结浸膏组 n=19 17.98±0.46 50.55±13.72 322.95±130.56 7.36±0.14 11.96±2.07 7.59±1.77指标 名称 红细胞宽度变异系数%红细胞宽度标准差fL血小板数109/L平均血小板体积fL白细胞数109/L续表6血小板分布宽度%空白对照组 n=20 0.86±0.15 3.52±1.42 64.94±7.65 7.02±0.54 29.55±11.06 0.25±0.08 19.07±1.51理气散结浸膏组 n=19 0.87±0.19 3.50±1.02 63.11±7.88 7.22±0.92 29.67±8.63 0.24±0.10 19.94±2.00指标 名称 中间细胞绝对值109/L粒细胞绝对值109/L淋巴细胞百分比%中间细胞百分比%粒细胞百分比%血小板比积L﹒L-1
2.4 血液生化学
2.4.1 小鼠 与空白对照组比较,理气散结浸膏经口一次性灌胃给予小鼠后14天,动物血清中胆固醇(TC)含量显著降低(P<0.05),但其变化值在正常范围内;其余各项血液生化学指标均无显著性差异(P>0.05),详见表7。
表7 小鼠的血液生化学指标测定结果(±S)
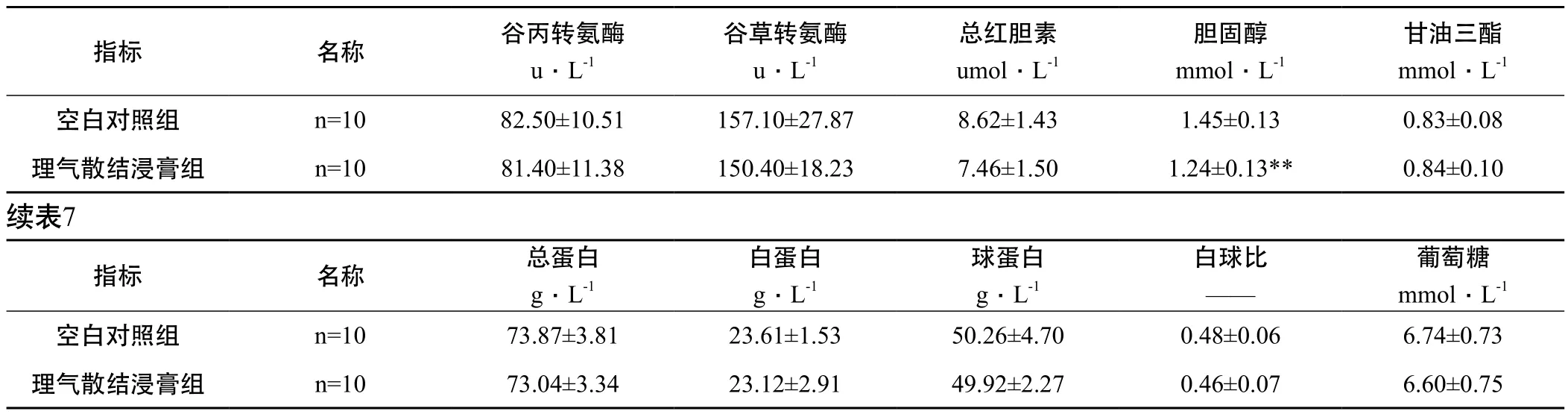
表7 小鼠的血液生化学指标测定结果(±S)
注:与空白对照组比较,* P<0.05,** P<0.01
甘油三酯mmol﹒L-1空白对照组 n=10 82.50±10.51 157.10±27.87 8.62±1.43 1.45±0.13 0.83±0.08理气散结浸膏组 n=10 81.40±11.38 150.40±18.23 7.46±1.50 1.24±0.13** 0.84±0.10指标 名称 谷丙转氨酶u﹒L-1谷草转氨酶u﹒L-1总红胆素umol﹒L-1胆固醇mmol﹒L-1续表7葡萄糖mmol﹒L-1空白对照组 n=10 73.87±3.81 23.61±1.53 50.26±4.70 0.48±0.06 6.74±0.73理气散结浸膏组 n=10 73.04±3.34 23.12±2.91 49.92±2.27 0.46±0.07 6.60±0.75指标 名称 总蛋白g﹒L-1白蛋白g﹒L-1球蛋白g﹒L-1白球比——
2.4.2 大鼠 与空白对照组比较,理气散结浸膏经口分两次灌胃给予大鼠后14天,动物血清中谷丙转氨酶(ALT)、谷草转氨酶(AST)和葡萄糖(GLU)差异显著(P<0.05),但变化均在正常范围内;其余各项血液生化学指标均无显著性差异(P>0.05),详见表8。
表8 大鼠的血液生化学指标测定结果(±S)
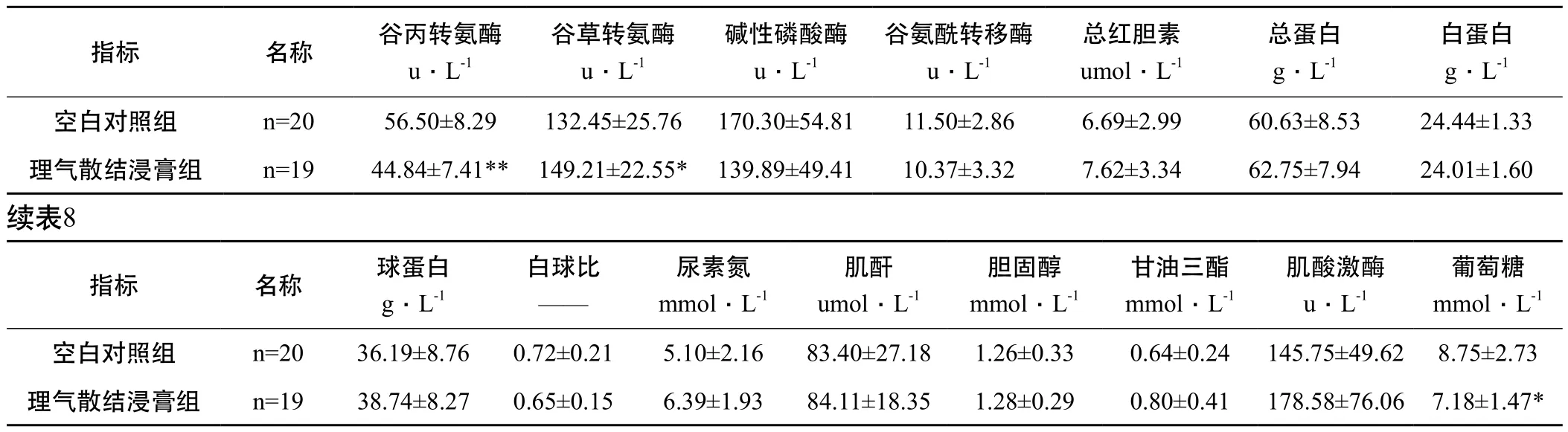
表8 大鼠的血液生化学指标测定结果(±S)
注:与空白对照组比较,* P<0.05,** P<0.01
谷草转氨酶u﹒L-1指标 名称 谷丙转氨酶u﹒L-1碱性磷酸酶u﹒L-1谷氨酰转移酶u﹒L-1总红胆素umol﹒L-1总蛋白g﹒L-1白蛋白g﹒L-1空白对照组 n=20 56.50±8.29 132.45±25.76 170.30±54.81 11.50±2.86 6.69±2.99 60.63±8.53 24.44±1.33理气散结浸膏组 n=19 44.84±7.41** 149.21±22.55* 139.89±49.41 10.37±3.32 7.62±3.34 62.75±7.94 24.01±1.60续表8白球比——指标 名称 球蛋白g﹒L-1尿素氮mmol﹒L-1肌酐umol﹒L-1胆固醇mmol﹒L-1甘油三酯mmol﹒L-1肌酸激酶u﹒L-1葡萄糖mmol﹒L-1空白对照组 n=20 36.19±8.76 0.72±0.21 5.10±2.16 83.40±27.18 1.26±0.33 0.64±0.24 145.75±49.62 8.75±2.73理气散结浸膏组 n=19 38.74±8.27 0.65±0.15 6.39±1.93 84.11±18.35 1.28±0.29 0.80±0.41 178.58±76.06 7.18±1.47*
3 讨论
本次急性毒性实验小鼠和大鼠经口灌胃给予理气散结浸膏的最大剂量分别为97.46 g生药/(kg﹒d)和48.73 g生药/(kg﹒d),相当于成人临床日用剂量0.3914 g生药/(kg﹒d)的249倍和124倍,根据《中药、天然药物急性毒性研究技术指导原则》进行MTD法的测定,采用小鼠最大耐受药量倍数计算,以耐受人临床用量的100倍以上为安全[2]。且实验结果表明,在此剂量下给药后,均未见动物死亡、中毒症状、脏器、体重和饲料消耗量等异常变化,血常规和血液生化学指标的变化也都在正常范围内,说明组方中山慈菇和蜂房在经过炮制加工之后,其毒性降低到了较为安全的范围。综上可得,理气散结浸膏整体毒性较低,无明显急性毒性。本结果可为长期毒性试验和主要药效学研究中的剂量设置提供依据。
