慢性阻塞性肺疾病患者合并周围神经病变情况及临床意义研究
2018-09-03刘贤兵李芳陈晓萍
刘贤兵,李芳,陈晓萍
本研究背景:
慢性阻塞性肺疾病(COPD)是一种全身性疾病,早在20世纪80年代就有学者提出COPD容易并发周围神经病变,但是并未引起重视。随着对COPD认识的深入、肌电图检查的普及,临床上发现更多COPD患者合并周围神经病变,特别是重度COPD患者。COPD合并周围神经病变对患者的危害巨大,且早期常无症状,当症状明显并出现肌无力或肌肉萎缩时,患者已经到达疾病终末期(呼吸肌疲劳、呼吸衰竭)。本研究重点探讨COPD合并周围神经病变的发病情况,同时观察营养神经干预治疗是否可改善患者的预后。
慢性阻塞性肺疾病(COPD)是一种破坏性的慢性气道炎症性疾病,其特点为不可逆性的气流受限和病情进行性加重,具有高患病率、致残率及病死率的特点,严重影响人类身体健康,到2030年其将成为全世界第3大致死性疾病,死亡人数将接近全球死亡总数的8.5%,世界经济负担位居第5位[1]。COPD也是全身性疾病,能引起代谢异常、心血管疾病、肌萎缩、营养不良、贫血、骨质疏松、肿瘤及焦虑抑郁等[2-3]。由此可见COPD对机体的损害是巨大的。随着对疾病的认识,越来越多的COPD患者被发现合并周围神经病变,特别是重度COPD患者[4]。本研究立足于该理论依据,探讨COPD患者周围神经病变发病情况,营养神经干预是否可改善预后,为下一步研究提供理论依据。
1 资料与方法
1.1 临床资料 选取2015年6月—2016年6月衢州市人民医院就诊的COPD患者120例为研究对象,其中男60例,女60例;年龄55~80岁,平均年龄(65.6±6.7)岁;病程8~22年,平均病程(15.4±4.0)年;吸烟80例。纳入标准:(1)符合2007年中华医学会呼吸病学分会COPD学组修订的COPD诊治指南的诊断标准[5];(2)排除支气管哮喘、肺结核、支气管扩张、肺癌等其他慢性肺部疾病及严重并发症;(3)既往体健,无急慢性肝病、高血压、尿毒症、甲状腺功能减退症、糖尿病、中枢及周围神经病变、胃肠道疾病及心脏病等病史,无长期使用引起多发性神经病变的相关药物;(4)年龄≥55岁且≤80岁;(5)患者同意入组,并签署知情同意书,能配合进行5次随访(为期12个月)。患者均来自衢州地区,无明显地域差异。为排除气候对研究的影响,随访时间为12个月。
1.2 方法 记录患者性别、年龄、病程、吸烟情况。1.2.1 肌电图检查 采用肌电图仪(广州维迪医疗器械有限公司,KP-W.NET型)测定双侧正中神经、尺神经、腓总神经、胫神经感觉神经传导速度(SNCV)、运动神经传导速度(MNCV),肌电图检查由本院肌电图室完成。根据检查结果分为周围神经病变组(72例)及无周围神经病变组(48例)。
1.2.2 COPD周围神经病变诊断标准 因COPD周围神经病变在发病机制上与糖尿病周围神经病变(DPN)有一定的相似之处,故本研究诊断标准参考DPN[6]。必备条件为必要符合以下两条:(1)确诊为COPD;(2)排除其他病变或药物对周围神经的损伤。诊断标准为符合以下3条中的两条:(1)存在因COPD引起的临床症状(如双侧、趾尖或足底及肢体麻木、疼痛、感觉异常或感觉减退,并且排除症状仅表现在上肢或仅因周围血管病变引起冷感症状);(2)双侧内踝震动觉减弱;(3)双侧踝反射减弱或消失。参考诊断为满足下述两条中任何一条,即使不符合上述条件,也可诊断:(1)电生理检测发现2条或2条以上神经有异常(神经传导速度、波幅或潜伏期);(2)有明显的自主神经功能障碍(排除其他原因)。如果临床上无神经受损的临床表现,但肌电图提示周围神经病变时,称为亚临床型周围神经病变。
1.2.3 有无症状 周围神经病变组需要询问患者是否有周围神经病变的症状(如肢体是否有感觉异常、是否有疼痛、是否有肌无力等)。
1.2.4 症状分级 采用COPD“田”字格式(ABCD)分级法进行症状分级,分为低风险少症状(A级)、低风险多症状(B级)、高风险少症状(C级)、高风险多症状(D级)[5]。
1.3 治疗 两组患者均规律使用噻托溴铵粉吸入剂(江苏正大天晴药业股份有限公司,药品批号:150916202)(1吸,1次/d)单独或联合沙美特罗替卡松粉吸入剂(GlaxoSmithKline,药品批号:R719886)(50 μg:500 μg,1吸,2次/d)维持治疗。周围神经病变组采用随机数字表法分为干预亚组36例和未干预亚组36例。干预亚组给予甲钴胺〔卫材(中国)药业有限公司,药品批号:1501081〕(500μg,肌肉注射,1次/d)联合硫辛酸(烟台只楚药业有限公司,药品批号:1508122)(450 mg,1次/d,30 min内静脉滴注完)治疗3周。
1.4 观察指标 所有患者入组后随访12个月(第1、3、6、9、12个月各随访1次),每次随访时统计发病次数、完成肺功能检测、慢性阻塞性肺疾病评估测试(COPD assessment test,CAT)、改良英国医学研究学会呼吸困 难 指 数(modified British medical research council,mMRC)、医院焦虑抑郁量表(HAD)。
1.4.1 肺功能检测 采用肺功能仪(德国耶格公司)检测第1秒用力呼气末容积(FEV1),由本院肺功能室完成。
1.4.2 CAT[5]CAT共包括8个问题:咳嗽、咳痰、胸闷、睡眠、精力、情绪、运动耐力、日常运动影响。患者根据自身情况,对每个问题做出相应评分(0~5分),CAT分值范围为0~40分。0~10分为“轻微影响”,11~20分为“中等影响”,21~30分为“严重影响”,31~40分为“非常严重影响”。患者CAT评分≥2分的差异或改变量即可提示具有临床意义。要求患者独立完成CAT,如患者有疑问,可以做适当解释,但不能做任何有暗示性的提醒,调查结束后立即统计分值,并由患者签字。CAT评分>10分时,提示患者的症状评分高。
1.4.3 mMRC[5]根据患者活动能力分为5级(0~4级),mMRC级别为2级或2级以上,提示患者的症状评分高。
1.4.4 HAD HAD共由14个条目组成,其中7个条目评定焦虑,7个条目评定抑郁。共有6条反向提问条目,1条在焦虑分量表,5条在抑郁分量表。采用HAD的主要目的是进行焦虑、抑郁的筛选检查。焦虑与抑郁两个分量表的分值划分:0~7分属无症状,8~10分属症状可疑,11~21分属肯定存在症状。但对于HAD筛查的临界数值,目前仍不统一,本研究采用叶维菲等[7]的研究结果,以9分作为焦虑或抑郁的临界值。
1.5 统计学方法 采用SPSS 17.0软件进行统计学分析,符合正态分布的计量资料以()表示,重复测量数据采用重复测量方差分析,两组间比较采用t检验,同组间不同时间比较采用单因素方差分析;计数资料比较采用χ2检验;等级资料比较采用秩和检验。以p<0.05为差异有统计学意义。
2 结果
2.1 无周围神经病变组与周围神经病变组患者临床资料比较 无周围神经病变组与周围神经病变组患者年龄、病程、症状分级比较,差异均无统计学意义(P>0.05);周围神经病变组患者男性、吸烟率、年发病次数、CAT评分、mMRC级别、合并焦虑/抑郁比例较无周围神经病变组高,FEV1较无周围神经病变组低,差异均有统计学意义(p<0.05,见表1)。
2.2 周围神经病变组有症状者与无症状者临床资料比较 周围神经病变组有症状者与无症状者性别、年龄、病程、吸烟率比较,差异均无统计学意义(P>0.05);有症状者年发病次数、CAT评分、mMRC级别、合并焦虑/抑郁比例、症状分级较无症状者高,FEV1较无症状者低,差异均有统计学意义(p<0.05,见表2)。
2.3 COPD合并周围神经病变患者干预亚组与未干预亚组临床资料比较 COPD合并周围神经病变患者干预亚组与未干预亚组性别、年龄、病程、吸烟率、年发病次数、症状分级比较,差异均无统计学意义(P>0.05,见表3)。COPD合并周围神经病变患者干预亚组与未干预亚组FEV1、CAT评分、mMRC级别、HAD评分治疗方法与时间存在交互作用(p<0.05),治疗方法及时间主效应显著(p<0.05)。干预前两组FEV1、CAT评分、mMRC级别、HAD评分比较,差异均无统计学意义(P>0.05);随访第1、3、6、9、12个月干预亚组FEV1较未干预亚组高,CAT评分、mMRC级别、HAD评分较未干预亚组低,差异均有统计学意义(p<0.05,见表4)。
COPD合并周围神经病变患者干预亚组与未干预亚组不同时间点合并焦虑/抑郁比例比较,差异有统计学意义(χ2=14.280,p<0.001),其中干预前、随访第1个月两组合并焦虑/抑郁比例比较,差异无统计学意义(P>0.05);随访第3、6、9、12个月干预亚组合并焦虑/抑郁比例低于未干预亚组,差异均有统计学意义(p<0.05)。干预亚组随访第6个月合并焦虑/抑郁比例低于干预前和随访第1、3个月,差异均有统计学意义(p<0.003);随访第9、12个月合并焦虑/抑郁比例高于随访第6个月,差异均有统计学意义(p<0.003,见表5)。
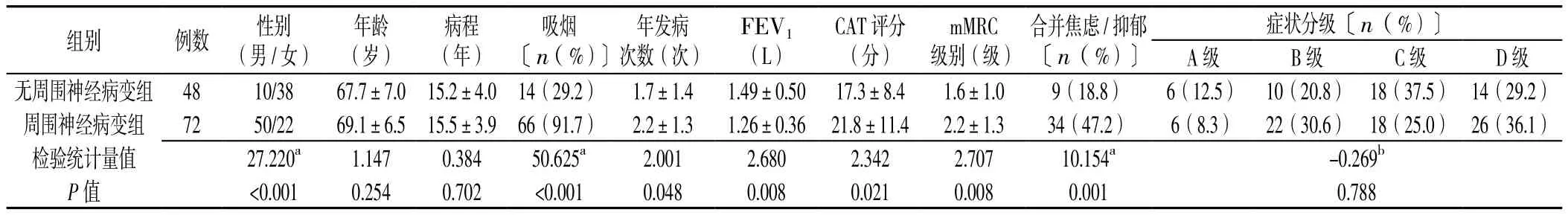
表1 无周围神经病变组与周围神经病变组患者临床资料比较Table 1 Comparison of clinical data between the non-peripheral neuropathy group and the peripheral neuropathy group
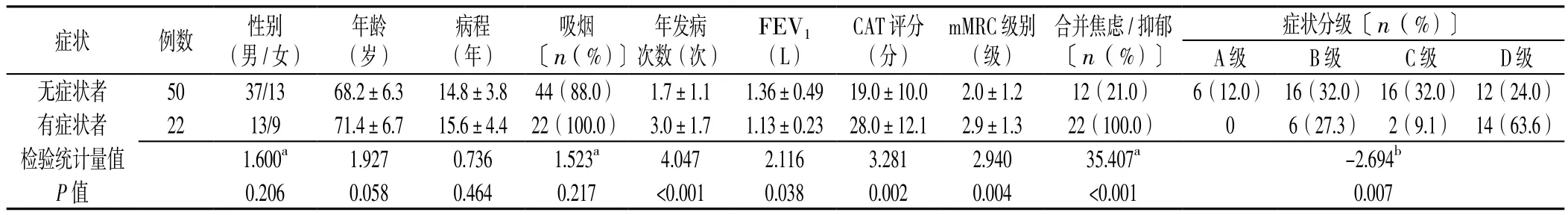
表2 周围神经病变组有症状者与无症状者临床资料比较Table 2 Comparison of clinical data between symptomatic and asymptomatic patients in the peripheral neuropathy group
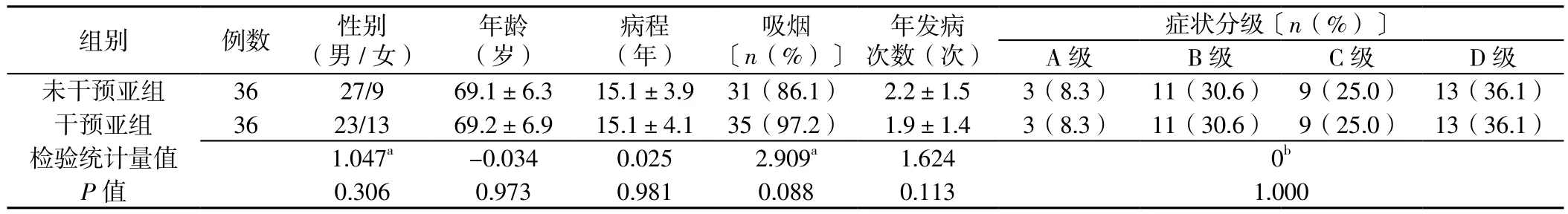
表3 COPD合并周围神经病变患者干预亚组与未干预亚组临床资料比较Table 3 Comparison of clinical data between the intervention and non-intervention subgroups of patients with COPD complicated with peripheral neuropathy
表4 COPD合并周围神经病变患者干预亚组与未干预亚组不同时间点观察指标比较Table 4 Comparison of the observational indices between the intervention and non-intervention subgroups at different time points
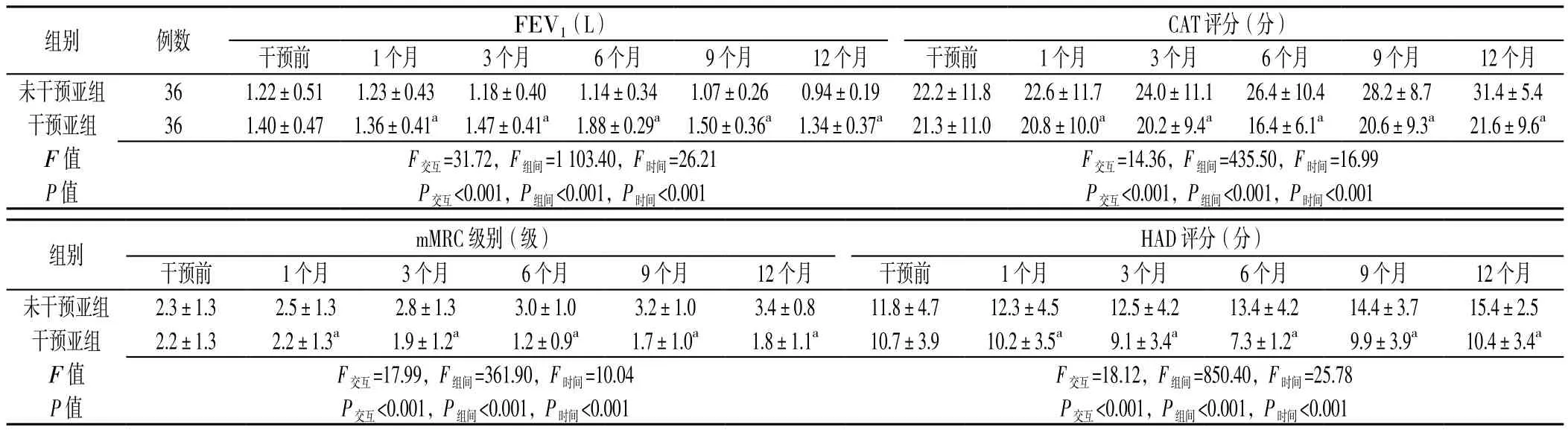
表4 COPD合并周围神经病变患者干预亚组与未干预亚组不同时间点观察指标比较Table 4 Comparison of the observational indices between the intervention and non-intervention subgroups at different time points
注:HAD=医院焦虑抑郁量表;与未干预亚组比较,ap<0.05
CAT评分(分)干预前 1个月 3个月 6个月 9个月 12个月 干预前 1个月 3个月 6个月 9个月 12个月未干预亚组 36 1.22±0.51 1.23±0.43 1.18±0.40 1.14±0.34 1.07±0.26 0.94±0.19 22.2±11.8 22.6±11.7 24.0±11.1 26.4±10.4 28.2±8.7 31.4±5.4干预亚组 36 1.40±0.47 1.36±0.41a 1.47±0.41a 1.88±0.29a 1.50±0.36a 1.34±0.37a 21.3±11.0 20.8±10.0a 20.2±9.4a 16.4±6.1a 20.6±9.3a 21.6±9.6a F值 F交互=31.72,F组间=1 103.40,F时间=26.21 F交互=14.36,F组间=435.50,F时间=16.99 P 值 P交互<0.001,P组间<0.001,P时间<0.001 P交互<0.001,P组间<0.001,P时间<0.001组别 例数 FEV1(L)组别 mMRC级别(级)HAD评分(分)干预前 1个月 3个月 6个月 9个月 12个月 干预前 1个月 3个月 6个月 9个月 12个月未干预亚组 2.3±1.3 2.5±1.3 2.8±1.3 3.0±1.0 3.2±1.0 3.4±0.8 11.8±4.7 12.3±4.5 12.5±4.2 13.4±4.2 14.4±3.7 15.4±2.5干预亚组 2.2±1.3 2.2±1.3a 1.9±1.2a 1.2±0.9a 1.7±1.0a 1.8±1.1a 10.7±3.9 10.2±3.5a 9.1±3.4a 7.3±1.2a 9.9±3.9a 10.4±3.4a F值 F交互=17.99,F组间=361.90,F时间=10.04 F交互=18.12,F组间=850.40,F时间=25.78 P值 P交互<0.001,P组间<0.001,P时间<0.001 P交互<0.001,P组间<0.001,P时间<0.001

表5 COPD合并周围神经病变患者干预亚组与未干预亚组不同时间点合并焦虑/抑郁比例比较〔n(%)〕Table 5 Comparison of the proportion of patients complicated with anxiety/depression in the intervention and non-intervention subgroups at different time points
3 讨论
COPD不仅是慢性呼吸道疾病,也是一种全身性疾病,与气道炎性递质〔如细胞因子、白介素(IL)-1、IL-6、肿瘤坏死因子α(TNF-α)及皮质醇等〕进入全身血液系统有关,引起全身炎性反应,造成多系统脏器功能损伤[8]。目前研究较多的是其对机体心肺功能、免疫功能、营养、机体代谢、消化道及社会心理的影响,而对机体周围神经损伤的研究相对较少。虽然,早在20世纪80年代就有学者提出COPD容易并发周围神经病变[9],吸烟及病情重者发生的概率更大,但是此类研究均是小样本研究。随着对COPD认识的深入、肌电图检查的普及,临床上发现更多COPD患者合并周围神经病变,但目前文献对其发病率的报道并不统一,为28%~94%[10]。本研究发现入选患者中有60.0%(72/120)合并周围神经病变,且周围神经病变组患者男性、吸烟率、年发病次数、CAT评分、mMRC级别、合并焦虑/抑郁比例高于无周围神经病变组,FEV1低于无周围神经病变组。同时也发现无论患者是否合并周围神经病变,症状分级无明显差异,说明COPD合并周围神经病变对患者病情是有影响的,但是并不是唯一的因素,也进一步说明了COPD发病机制的复杂性。为此,在诊治COPD时需要扩大思路,治疗上不能仅满足于改善呼吸道症状,而且需要兼顾到全身各系统。
COPD合并周围神经病变发病机制至今不明,相关文献报道也较少,可能由于其隐匿起病,早期症状不明显,临床上早期不被重视,故相关的研究也就较少。分析发病机制可能与机体炎性反应、缺氧、缺血、营养不良、慢性病消耗、氧化应激、反复肾上腺皮质激素使用及内分泌代谢异常等因素有关[11-12]。研究发现COPD合并周围神经病变常隐匿性起病[13],在行肌电图检查前常无明显不适,即亚临床周围神经病变。当患者症状明显并出现肌无力或肌肉萎缩时,说明患者已经处于疾病终末期(呼吸肌疲劳、呼吸衰竭),临床上也将这类表现归类为“COPD合并肌肉萎缩”。肌肉萎缩最易累及骨骼肌和呼吸肌,导致患者运动不耐受及呼吸肌疲劳,并呈进行性加重,严重影响疾病预后[14-15]。由此可见,加强对COPD合并周围神经病变的认识刻不容缓,肌电图在COPD的诊治过程中应列为常规检查。在临床表现上,COPD合并周围神经病变和其他周围神经病变相似,表现为感觉障碍、肌肉无力与萎缩、腱反射减退以及血管运动症状(缺血性改变),上述症状可单独也可组合存在。早期症状以感觉障碍为主,临床上多表现为对称性疼痛和感觉异常,下肢症状较上肢多见[16]。
COPD合并周围神经病变除了对患者生活质量有影响外,对社会心理也是有不同程度的影响。患者持续出现周围神经病变的各种不适症状,如肢体远端疼痛、灼痛和痛觉过敏,肢体麻木感或感觉缺失,甚至出现不宁腿综合征、肌无力等,可导致患者发生焦虑/抑郁,导致社会心理障碍[17]。本研究也发现COPD合并周围神经病变患者容易合并焦虑/抑郁(47.2%),有周围神经病变症状者均有不同程度焦虑/抑郁(100.0%),可能与患者持续的躯体不适感有关。但因本研究样本量、课题设计及经费等问题,未能进一步深入阐述两者的关系,有待后续研究进一步论证。
由此可见,COPD合并周围神经病变对患者的影响巨大,需要早期发现及干预性治疗。但目前对于该合并症的治疗方案还没有确切标准,也未见具体的文献报道。搜索文献发现很多周围神经病变的治疗方案均是针对DPN,也许与DPN较早被发现和重视,故对其研究也较早和全面有关。考虑到两者在周围神经病变的发病机制上有一定的相似之处,如均存在炎性反应、缺氧、营养不良、慢性病消耗、氧化应激、内分泌代谢异常等因素[4,11],故本研究借鉴DPN的治疗方案,选择了甲钴胺联合硫辛酸治疗COPD合并周围神经病变,疗程为3周。甲钴胺作为维生素B12衍生物,通过甲基化反应促进卵磷脂合成及神经元髓鞘形成,修复受损神经组织,发挥营养神经、保护神经元的作用,而改善疼痛、麻木等临床症状。硫辛酸具有独特双硫键的抗氧化分子结构,可转化还原型二氢硫辛酸,有效清除过多氧自由基,减少脂质过氧化反应;还能还原人体抗氧化系统,延长普通抗氧化剂的寿命或促进其再生;同时增加周围神经血管的血流量,从而缓解神经性疼痛症状。甲钴胺联合硫辛酸可从不同途径发挥治疗周围神经病变的临床作用,具有协同作用。本研究通过观察COPD合并周围神经病变患者不同时间点各指标情况,发现与未干预亚组比较,干预亚组在随访第1、3、6、9、12个月时CAT评分、mMRC级别、HAD评分下降,FEV1升高,说明对于合并周围神经病变的COPD患者,给予营养神经治疗可以改善其生活质量,也进一步说明了干预性治疗的必要性。但考虑到本研究样本量较小及治疗方案尚处于摸索阶段,故对于COPD合并周围神经病变干预性治疗方案的选择、疗程及周期,还需要进一步临床研究去佐证。本研究还发现随着疾病的进展,患者焦虑/抑郁的发病情况逐渐加重。对于COPD合并周围神经病变患者干预性治疗后,随着患者生活质量的改善,焦虑/抑郁的发生情况有所减少,而且与同期未干预亚组相比,其发生率较少,但随着随访时间的延长焦虑/抑郁的发生率有所升高,在今后的研究中应注重治疗的长期效果。
综上所述,COPD患者存在不同程度的周围神经病变,严重者可发展为肌肉萎缩、肌无力,而肌肉萎缩将直接影响患者的运动耐力和生活质量。同时持续的神经肌肉不适感也导致或加重患者社会心理问题,两者相互影响,加速病情恶化,影响患者预后。目前对COPD治疗多局限于延缓肺功能下降进程,合并症的治疗常被忽视。虽然肺功能的损伤是不可逆的,但从某种意义上讲,COPD患者生活质量低下、运动耐力减退至少部分是可逆的。也许可以通过早期发现和治疗COPD合并周围神经病变,从而避免或延缓肌肉萎缩、呼吸肌疲劳的发生,最终达到提高患者生活质量和改善患者预后的目的。由此可见,加强对COPD合并周围神经病变的认识刻不容缓,肌电图在COPD诊治过程中应该列为常规检查,从而做到早期发现,早期干预。
作者贡献:刘贤兵、陈晓萍进行文章的构思与设计,研究的实施与可行性分析;刘贤兵、李芳进行数据收集,统计学处理,结果的分析与解释,撰写论文;刘贤兵、李芳、陈晓萍进行数据整理;刘贤兵进行论文的修订,负责文章的质量控制及审校,对文章整体负责,监督管理。
本文无利益冲突。
