胶质瘤疫苗的研究进展
2018-08-13张鹏幸任东妮涂艳阳空军军医大学唐都医院实验外科陕西西安710038
祁 婧,张鹏幸,任东妮,涂艳阳 (空军军医大学唐都医院实验外科,陕西西安710038)
0 引言
多形性胶质细胞瘤(glioblastoma multiforme,GBM)是成年人中最常见且最具侵袭性的原发性脑肿瘤,对常规治疗方法具有抗性。虽然临床中常用手术后辅助放疗和化疗的治疗策略,但是每年15 000例患者的中位生存时间仅为14.6个月[1]。治疗难度集中于肿瘤本身的遗传异质性、患者异质性、肿瘤诱导的免疫抑制、血脑屏障的有限性和不可避免的肿瘤复发等方面。尽管面临诸多挑战,然而研究人员在GBM治疗方面仍然取得了可观的进展,特别是在免疫治疗领域,多项药物已经进入不同程度临床试验。
肿瘤疫苗是将肿瘤抗原以多种形式如肿瘤细胞、肿瘤相关蛋白或多肽以及表达肿瘤抗原的基因等导入患者体内,以克服肿瘤引起的免疫抑制状态[2],增强免疫原性,激活患者自身的免疫系统,诱导机体细胞免疫和体液免疫,从而控制或清除肿瘤[3-4]。
根据抗原呈递给免疫系统的方式将疫苗分为非细胞疫苗与细胞疫苗两大类。其中非细胞疫苗是指患者直接接种特异性肿瘤抗原,其又被呈递给宿主抗原呈递细胞(antigen presenting cell,APC)以引发免疫应答。而细胞疫苗由APC组成,APC在体内被启动并通过疫苗重新引入宿主,导致抗原的出现和肿瘤特异性T细胞反应的扩增(图1)。
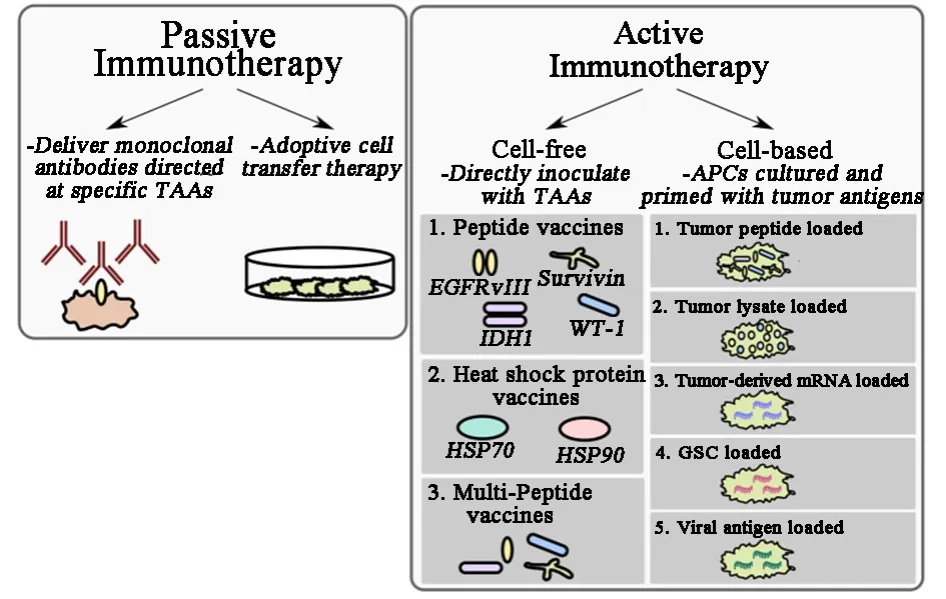
图1 被动和主动免疫治疗策略示意图[4]
1 非细胞疫苗
1.1 肽疫苗肽疫苗由一个或多个短的或长的氨基酸序列作为肿瘤抗原,也能结合某些疫苗佐剂[5]。这些肽通常与载体蛋白连接以增强免疫原性[例如破伤风类毒素或钥孔血蓝蛋白(KLH)][6-7]。 另外,它们经常与免疫刺激剂如Toll样受体(toll-like receptor,TLR)激活剂(例如脂多糖)或细胞因子[例如,粒细胞巨噬细胞集落刺激因子(granulocyte/macrophage-colony stimulating factor, GM-CSF),白细胞介素(IL)-2]一起使用以增强免疫反应[8-9]。胶质瘤发生与几种TAA的异常产生相关,可能有潜质用于肽疫苗的开发。然而,挑战难度在于鉴定肿瘤特异性,均匀表达的抗原,并具有足够的免疫原性[10]。在许多潜在的GBM抗原靶标中,只有少数符合这些标准。
1.1.1 EGFRvIII 在肽疫苗中,关于表皮生长因子受体Ⅲ型突变体(epidermal growth factor receptor variantⅢ,EGFRvⅢ)的研究最广泛。通常,表皮生长因子或转化生长因子α诱导的EGFR激活促进受体二聚化,导致细胞内酪氨酸激酶结构域的自磷酸化和促进增殖的Ras/丝裂原活化激酶信号传导[11-12]。蛋白质的其他部分的融合也产生与新的甘氨酸残基的独特连接,其侧翼是野生型蛋白质中不存在的氨基酸序列[13-14]。 重要的是,EGFRvIII在 GBM 患者(25%~30%)中表达,与长期存活者的不良预后有关。此外,这种突变的存在可以通过免疫组织化学分析来确定,作为标准病理学处理的一部分[15-18]。研究报道EGFRvIII在胶质瘤干细胞也表达,即使其表达在肿瘤内是异质的,EGFR vIII阳性细胞也可以影响相邻细胞,随后提供增殖信号[19-20]。鉴于这些因素,EGFRvIII已经成为免疫治疗的靶点。
在临床前模型中评估了EGFRvIII疫苗的有效性。Heimberger等[11]报道相对于对照组接种导致颅内肿瘤小鼠的存活率增加了26%。此外,还证明在肿瘤植入之前接受疫苗接种的小鼠体内肿瘤不再继续发展。为了临床评估皮内给药的EGFRvIII疫苗(CDX-110/rindopepimut)在 EGFRvIII阳性患者中的安全性和有效性,启动了 3个Ⅱ期试验:ACTIVATE[5],ACT Ⅱ[22]和 ACT Ⅲ[18]。 3 项试验均给予患者连环磷霉素和GM-CSF作为佐剂。无论如何,与接受标准治疗的匹配对照组相比,中位生存时间和无进展生存期(PFS)时间均显着增加。ACTⅡ报告在疫苗治疗的患者(n=22)中,历史对照组(n=17)的中位生存时间为6.3个月,中位PFS时间(组织学诊断)为15.2个月。接种疫苗的患者和历史对照的总生存时间分别为 23.6和 15个月。调整患者年龄和Karnofsky表现量表评分后,差异有统计学意义(P<0.05)。值得注意的是,复发时,肿瘤被认为是EGFR-vIII阴性,表明抗原性丧失[5]。这是源于天然疾病过程还是免疫消除是未知的,但表明靶向异质表达的抗原可能不满足临床要求。对于使用靶向EGFRvIII的嵌合抗原受体方法的结果较为理想启动了第Ⅳ期Ⅲ期试验。在安慰剂对照的双盲研究中,患者接受了rindopepimut/GM-CSF或 KLH,以及 TMZ维持治疗。不幸的是,2016年3月7日,Celldex宣布停止 ACT IV。该决定是基于临时数据分析的结果,显示接受疫苗接种的患者与对照组患者相比,总体生存率并未有明显改善。尽管结果不理想,ReACTⅡ期试验目前正在进行,并将CDX-110与贝伐珠单抗联合使用,结果仍在分析中。
靶向EGFRvIII(ADU-623)的另一种药物目前正在Ⅰ期临床试验中进行评估。ADU-623是靶向EGFRvIII和NYESO的活减毒李斯特菌疫苗,其是另一种已知的肿瘤抗原,据报道具有高免疫原性[19-25]。这项试验正在招募患有复发性高级胶质瘤的患者,结果仍在分析中。
1.1.2 存活素 尽管EGFRvIII是研究最多的,但还有用于GBM肽疫苗的其他抗原候选物正在研究中。存活素是属于凋亡蛋白家族抑制剂的分子。尽管其作用机制尚未得到充分描述,但研究表明,存活素既是有丝分裂的调节剂,又是细胞死亡抑制剂[25]。它在几种癌症中被上调,成为免疫治疗的潜在靶标。重要的是,生存素在GBM中比在正常组织中表达水平更高,且预后较差[26]。 在使用 SVN53-67/M57(一种源自存活蛋白的肽疫苗)的研究中评估了存活蛋白作为免疫治疗靶标的有效性,其可以激活对存活蛋白表达细胞的免疫应答。该疫苗与KLH结合,单个半胱氨酸取代蛋氨酸,增强免疫原性,增加肿瘤反应[30]。SVN53-67/M57在体外产生细胞毒性T细胞介导的人神经胶质瘤细胞的杀伤作用。此外,注射SVN53-67/M57(与GM-CSF组合)显著增加存活时间,并减少GL261胶质瘤小鼠的肿瘤负荷。基于这些结果和完成的Ⅰ期试验,SVN53-67/M57-KLH和TMZ的Ⅱ期试验目前正在招募恶性胶质瘤患者。
1.1.3 异柠檬酸脱氢酶1 异柠檬酸脱氢酶1(isoci-trate dehydrogenase 1,IDH1)是可在胶质瘤中突变的酶。在精氨酸132残基中最常发生突变,产生2-羟基戊二酸代谢产物,基因组超甲基化和恶性转化。IDH1 R132H突变,特别是在≥90%的次级GBM中表达[27]。IDH1 R132H是癌症免疫治疗的重要靶标,因为它是肿瘤特异性抗原,在肿瘤细胞中具有统一的表达[27]。EGFRvIII的临床经验突出了GBM抗原异质性在免疫治疗发展中的挑战。建议靶向驱动突变,如IDH,可以避免异质性诱导的免疫逃逸[28-29]。最近的研究表明,用突变型IDH1肽接种的小鼠诱导特异性T细胞应答。此外,疫苗接种抑制了携带 IDH1 R132H表达肉瘤的小鼠的肿瘤生长。这种效应在表达野生型IDH的肉瘤中未见,证实该反应是突变特异性的[30]。需要进一步的数据来确定IDH疫苗是否适用于胶质瘤。目前有一项Ⅰ期临床试验,用于评估IDH1 R132H突变胶质瘤患者IDH1肽疫苗的安全性,计划入组39例,结果仍在分析中。
1.1.4 WT1 Wilms肿瘤基因 WT1 在多种实体瘤中过表达,被认为是致癌基因[31-32]。WT1编码锌指转录因子,其参与细胞增殖和凋亡[33-36]。多项研究[37-39]已经确定了WT1在胶质瘤中的表达。Hashiba等[40]报道,73 例胶质瘤患者中有 70 例(95.9%)检测到WT1蛋白,该表达与WHO等级相关。在另外评估829例胶质瘤样品中,Rauscher等[41]报道,弥漫性星形细胞瘤中的WT1表达与WHO分级相关。由于WT1蛋白已经被鉴定为TAA,因此假设WT1产物可能适合开发基于肽的免疫治疗。最近公布的Ⅰ期临床试验测试了7例新诊断为GBM的患者中基于WT1的肽疫苗联合TMZ施用的安全性,并报告了PFS时间为 5.2 至 49.1 个月[42]。 在小型非随机Ⅱ期试验中,21例患有WT1/人白细胞抗原(HLA)-A∗ 2402阳性复发性GBM的患者用HLAA∗2402限制性WT1肽的真皮内接种治疗。研究[43]报道6个月PFS为33.3%,治疗副作用最小。然而,没有一个患者具有完整的放射成像反应。
1.2 多肽疫苗在实用性方面,肽疫苗具有多种益处,包括易于批量生产,直接给药(例如皮内)[44]。几种肽疫苗(不包括EGFRvIII肽)的一个局限性是,它们仅限于hla-02单倍体,然而,GBM患者存在多种单倍型,限制了该疗法的通用性[45]。第二个局限性是,只有一小部分患有GBM的患者才能最终从靶向单个肿瘤抗原中获益。最后,肽疫苗,特别是单一肽的主要缺点是GBM中抗原表达的异质性[20]。在CDX-110接种后肿瘤复发的EGFRvIII疫苗试验中证实了这种现象,82%的病例表现出靶抗原(EGFRvIII)的丧失[46]。这表明复发后接种需要替代治疗或联合治疗。
为了规避这些问题,已经开发了靶向各种肿瘤抗原的多肽疫苗。为了鉴定潜在的免疫原性肿瘤抗原,从GBM细胞的HLA复合物中洗脱肽。使用液相色谱-质谱法,鉴定出3000个肽。45例新诊断的GBM患者接受了手术切除,然后进行标准治疗,完成了IMA950(加 GM-CSF)第一期Ⅰ/Ⅱ试验[47]。 IMA-950与国立癌症研究所环磷酰胺,GM-CSF和咪喹莫特组合的第二阶段研究由于入组速度过慢被提前终止。值得注意的是,使用这些类型的肽和辅助方法的克隆型T细胞扩增的程度是否足以消除肿瘤也是未知的[48]。SL701是目前在临床试验中进行评估的另一种最近开发的多肽疫苗。SL-701由对应于在胶质瘤中过表达的靶标的3种肽组成:靶向存活蛋白、IL-13受体α-2和ephrin A2的高免疫原性突变体,结果仍在分析中。
另一种方法是根据单个肿瘤的抗原特征生成个性化的肽疫苗。一种策略是从患者的手术切除肿瘤组织中制备疫苗,以及从其他切除肿瘤中收集到的同种异体抗原。ERC-1671(Gliovac)是GBM肿瘤裂解物,来自患者的自体肿瘤细胞(从切除的肿瘤生成)和来自3种不同GBM供体的肿瘤细胞组成的多肽疫苗。该疫苗构建的目的是最大限度地使患者暴露于异种的GBM肿瘤抗原。暴露于更多的同种异体和自体肿瘤相关抗原,可减少肿瘤免疫逃逸的机会。ERC-1671在临床评估中显示出较为理想的结果[49-50]。9例复发性GBM患者,接受标准放化疗和贝伐单抗治疗ERC 1671导致生存期增加。具体来说,Gliovac患者6个月生存率为100%,而历史对照组为33%[50]。基于这些结果,正在进行Ⅱ期试验,以评估ERC1671(与GM-CSF和环磷酰胺联合使用)加贝伐单抗在复发性GBM患者中的安全性和临床疗效。
当然,肽疫苗可以与免疫检查点抑制剂联合使用。虽然这具有明显的理论吸引力,但实施可能是有挑战性的。例如,虽然 30%的 GBM具有针对rindopepimut/CDX-110 的 EGFRvIII 靶标表达[16],但只有6%的患者在肿瘤内存在程序性死亡受体1(PD-1)+T 细胞,1%具有 PD 配体 1(PD-L1)共表达[55]。授予PD-1+T细胞和/或PD-L1表达可能只是用于响应免疫检查点抑制剂的富集生物标志物,并且患者可在没有这些生物标志物的情况下作出反应[52-54]。尽管如此,这些数据表明,这种类型的组合只能使少数患者受益。已经发现高肿瘤突变载量与其他癌症中免疫检查点抑制剂的反应相关[55-59],但是这些水平(每兆塔变化12个突变)仅在<10%的胶质母细胞瘤患者中发现[60]。
1.3 热休克蛋白(heat shock protein, HSP)疫苗HSP是分子伴侣蛋白,通过防止蛋白质聚集和指导错误折叠的蛋白质的降解,在细胞应激反应中起重要作用[61]。包括HSP70和HSP90在内的某些HSP亚型已显示与GBM中的肿瘤抗原结合并模拟先天性和适应性反应[62]。HSP-抗原复合物通过在APC上表达的CD91进行受体介导的摄取。在内化后,通过蛋白酶体处理复合物以加载到MHC I类分子上并呈递至CD8细胞毒性T细胞。此外,HSP-抗原复合物还通过各种受体(即 CD36、CD91、CD40、CD14、TLR2 和TLR4)结合巨噬细胞,并刺激促炎细胞因子的产生[63]。HSP接种需要从患者切除的肿瘤中纯化HSP,随后重新接种于患者,以使HSP与宿主APC和主要效应细胞与抗原肽相互作用[63]。HSPs有助于抗原肽呈递循环的APC,随着APCs与HSP结合,吞噬其伴侣蛋白,并提出这些抗原多肽靶向T细胞介导的细胞毒性破坏,随后引发免疫应答[63-64]。
大多数HSP疫苗试验使用HSP-肽复合物96(HSPPC-96),其包含由HSP糖蛋白-96伴随的抗原肽[65-66]。在12例复发性GBM患者的Ⅰ期试验中,HSP疫苗治疗显示无显著毒性,其中有11例发现肿瘤特异性免疫反应(在肿瘤微环境和外周血中都观察到)[67]。在随后的单次非随机Ⅱ期试验中,手术切除后,41例复发性GBM患者每周接受一剂HSPPC-96,持续4周。中位PFS和总生存期分别为19.1和42.6周[68]。在新近诊断的GBM且正在接受放化疗标准治疗的患者中,HSPPC-96的Ⅱ期临床试验已经完成并正在出版(NCT00905060)。另外,一项随机Ⅱ期试验结合HSPPC-96和贝伐珠单抗复发性GBM患者也正在积极招募,估计入组222例。
通过在疫苗接种期间检测各种类型的潜在抗原蛋白的能力来鉴定这种治疗策略。HSP疫苗也可能通过多种机制刺激先天和适应性免疫系统的反应。除细胞毒性T细胞外,HSP还诱导巨噬细胞分泌促炎细胞因子,如肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)、GM-CSF 和 IL-12等。 IL-12随后激活淋巴细胞和天然杀伤细胞的细胞毒活性。HSP复合物还能够增加DC和巨噬细胞中一氧化氮的产生和分泌。最后,HSP诱导不成熟的DCs成熟[69],这可能有助于更强大的免疫反应。应该注意的是,HSP疫苗的局限性在于需要大量的组织来产生疫苗[63]。
2 细胞疫苗
2.1 DC疫苗DC是专业的APC,并且是细胞介导的免疫应答中最强大的激活剂。在MHC的背景中,DC吞噬、加工和呈递后,将抗原呈递给初始T细胞,引发抗原特异性CD8+和CD4+淋巴细胞反应。除此之外,T细胞功能通过促炎细胞因子活化的DC分泌增强。由于这些功能,DC是疫苗开发的理想选择。在疫苗制备中,从患者中提取DC,离体培养并加载TAA。随后将这些引发的DC再次引入患者以促进抗原特异性T细胞活化。
DC疫苗已在GBM中进行了研究。成功的临床前研究和小型临床研究已经引起人们的兴趣,以确定最佳分子加载到DC以产生最强大和肿瘤特异性的反应[70]。尽管构建直流疫苗的过程比肽疫苗的费用要高得多,但其最大的优点在于其灵活性能够为DC提供广泛的刺激物,包括肽、肿瘤裂解物和癌症干细胞,所有这些都是针对肿瘤的个体而定制。
2.1.1 肿瘤肽负载的DC疫苗 在最基本的水平上,可以用与肽疫苗相同类型的肽表位来刺激DC。在临床试验中,EGFRvIII是加载到DC中的最早的肽之一。在Ⅰ期研究中,12例新诊断的GBM患者接受了EGFRvIII特异性肽(PEPvIII)-KLH脉冲的DC手术切除和放射治疗。进展时间和总生存时间(从疫苗接种)的中位数分别为6.8和18.7个月。没有观察到严重的不良反应或毒性。Phuphanich等[71]进行了ICT-107的Ⅰ期临床试验,一种由患者DC与6种相关GBM肽抗原组成的自体疫苗。在21例患者的初步资料中,接种疫苗后产生良好的生存期,中位PFS和总生存时间分别为16.9个月和38.4个月。目前正在招募患者进行Ⅲ期临床试验评估。
2.1.2 肿瘤裂解物负载DC疫苗 在这种技术中,肿瘤裂解物由外科手术切除后获得的自体肿瘤细胞制备。裂解患者肿瘤细胞以产生细胞碎片,随后脉冲进DC。DC暴露于这些肿瘤片段允许吞噬和随后的肽抗原呈递到MHC I类和II类[72]。使用肿瘤溶菌素的优点是无偏性地刺激DC以充分补充患者特有的TAAs,包括未被认识的肿瘤抗原[73]。或者,这可能产生非肿瘤特异性免疫应答或可将T细胞的克隆型扩增稀释为弱免疫原性抗原。在Ⅰ期研究中,确定了自体肿瘤裂解物基DC疫苗的安全性和生物活性。此外,复发性GBM(n=8)患者的中位生存时间是133周[4]。在这种疫苗亚型中更加强效的治疗方法是DC-VaxL。DCVaxL目前正在进行Ⅲ期临床试验,其结果非常符合预期[74].
2.1.3 mRNA负载DC疫苗 DC也可以加载肿瘤衍生的mRNA。与肿瘤蛋白质相比,mRNA可以在体外扩增,使这种技术具有实际的优势。扩增可用相对较小的细胞来源用于生产大量抗原负载的DC。此外,有报道[74]称,RNA在 DC诱导 T细胞中优于 DNA。目前有几项实施这项技术的临床试验。
2.1.4 胶质瘤干细胞负载DC疫苗 神经胶质瘤干细胞(glioma stem cells,GSCs)是与其余肿瘤细胞相比独特的细胞亚型,表现出自我更新能力[75]。已知GSCs具有耐化疗作用并且导致复发[76-77]。GSCs也具有抑制T细胞增殖和活化,诱导调节性T细胞和触发 T 细胞凋亡的能力[78]。 已有研究[8]称 GSCs作为DC免疫治疗的靶标,因为有效地破坏了肿瘤介导的免疫抑制的驱动因素,可能会有更大的疗效。Pellegatta等[79]报道,加载GL261神经球(富含干细胞)的DC治疗了80%的GL261荷瘤小鼠,而用含有GL261裂解物的DC治疗的小鼠仅为50%。Vik-Mo等[80]报道了在I/Ⅱ期用干细胞的DC疫苗治疗的7名患者。分离GBM标本,在体外分离并扩增患者干细胞。之后,将干细胞mRNA扩增并加载到DC中。在接种疫苗的患者中,没有观察到严重的毒性。此外,治疗患者的PFS间期是匹配对照的2.9倍(分别为694 d vs 236 d,P=0.0018)。 目前的第一阶段试验正在测试ICT-121的安全性,ICT-121是一种基于DC的疫苗,靶向CD133+(干细胞标记)细胞。应该注意的是,使用GSC生成/收获的技术是昂贵且困难的,这可能限制了该手段的广泛性。
2.1.5 病毒抗原负载DC疫苗 2002年初确定了巨细胞病毒(CMV)及其基因产物的存在,CMV被认为在致癌途径中具有相关的作用[81]。考虑到这一点,广泛的研究致力于开发GBM免疫治疗的这一功能。人CMV病毒粒子被一种天然壳包围着。最丰富的蛋白质是pp65,这种CMV抗原可用于靶向免疫治疗。临床试验正在评估基于CMV的治疗GBM的策略。在本研究中,自体DC装载有CMV pp65-溶酶体相关膜蛋白 mRNA,并与抗 CD25单克隆抗体(basiliximab)组合施用。抗CD25的作用是抑制T调节细胞并增强CMV特异性T细胞活性。最近的研究[81]发现,使用召回抗原破伤风/白喉(Td)类毒素预处理疫苗部位可以促进DC归巢到淋巴结和DC疫苗接种的功效。研究[82]报道,用Td类毒素预处理的患者具有增强DC迁移并显著改善生存的作用,ELEVATE是一项Ⅱ期随机临床试验。
2.1.6 综合治疗中DC疫苗 由于DC疫苗接种的临床前和临床前景,该免疫治疗策略已经与其他形式的免疫治疗相结合,以增强所需的免疫应答。免疫系统抑制途径可能特异性地破坏DC疫苗接种的效果。免疫检查点是参与这些途径的受体。最近的一项临床前研究[83]评估了肿瘤裂解物脉冲DC与免疫检查点封锁相结合的功效,特别是抑制PD-1/PD-L1轴。该信号轴已涉及几种癌症,已被证明可以减少效应T细胞的活化并促进肿瘤免疫反应。在胶质瘤小鼠中,DC接种和PD-1抗体的联合治疗导致肿瘤浸润淋巴细胞中免疫记忆和归巢(即L-选择蛋白、整联蛋白α-4链)的标志物的上调。此外,用联合治疗治疗的动物比用单一疗法治疗的动物存活时间显著更长。具体来说,单药治疗未见效果,但联合治疗组长期存活率为40%[83]。Ⅰ期试验(AVERT)正在测试CMV特异性DC疫苗与尼莫单抗(抗PD-1抗体)的联合治疗方案,目前正在招募复发性高级胶质瘤患者.
3 结论
肿瘤疫苗允许免疫系统被引导到肿瘤靶标,并且在适当的背景中可以诱导长期的免疫应答。目前有多项临床试验探索该治疗平台。基于迄今为止关于肿瘤疫苗的研究结果,未来的研究应该重点关注将疫苗接种治疗与常规治疗相结合,结合靶向不同抗原的疫苗和潜在的其他形式的免疫治疗(例如检查点抑制,过继转移治疗)。联合治疗可能降低肿瘤免疫耐受和逃逸的潜力。此外,需要更准确地了解免疫治疗的时间,以及疫苗接种方案的标准化,佐剂和监测患者免疫应答的方法。此外,还需要解决这一患者群体频繁并发使用类固醇的问题,因为经常需要减少颅内压和症状的类固醇治疗可能会破坏所需的免疫反应[83]。肿瘤因子对疫苗疗效的影响也没有完全阐明,特别是对于低级胶质瘤。具体来说,这包括诸如肿瘤部位、切除程度、原发性与继发性GBM以及复发性疾病与初始治疗相关的因素[75]。总体来说,疫苗治疗是一种具有潜力但仍需进一步优化的治疗策略。
