乙型肝炎表面抗原阴性的非霍奇金淋巴瘤患者化疗后乙型肝炎病毒再激活的影响因素分析
2018-07-26张丛丛索晓慧孙国锋陈莉赵燕莉侯娟娟
张丛丛,索晓慧,孙国锋,陈莉,赵燕莉,侯娟娟
邯郸市中心医院血液内科,河北 邯郸056001
非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)是临床上常见的血液系统恶性肿瘤,并且NHL患者乙型肝炎病毒(hepatitis B virus,HBV)的感染率明显高于普通人群及其他恶性肿瘤患者[1]。目前,化疗是NHL治疗的首选方法,但是免疫抑制药的应用及化疗引起的骨髓抑制等均可导致患者的免疫功能下降,化疗后患者出现HBV再激活[2]。研究发现,预防性抗病毒治疗可以明显降低NHL患者HBV的再激活率及肝功能不全的发生率[3],但研究主要集中于乙型肝炎表面抗原(hepatitis B surface antigen,HBsAg)阳性的患者,HBsAg阴性患者的研究较少[4]。本研究对112例HBsAg阴性NHL患者的HBV再激活影响因素进行分析,为临床诊治提供依据。
1 对象与方法
1.1 研究对象
选取2013年6月至2017年9月邯郸市中心医院收治的112例NHL患者作为研究对象,按照随机数字表法分为观察组和对照组,每组56例。所有患者均给予环磷酰胺+多柔比星+长春新碱+醋酸泼尼松(CHOP)化疗方案或利妥昔单抗+CHOP(rituximab-CHOP,R-CHOP)化疗方案,观察组患者于化疗前1周开始口服恩替卡韦。纳入标准:①经病理学及免疫组织化学检查确诊为NHL;②患者HBsAg阴性,血清HBV DNA定量检测<500 IU/ml,乙型肝炎E抗原/抗体阳性,乙型肝炎核心抗体阳性;③既往未接受抗HBV治疗;④肝功能无明显异常;⑤自愿参与本研究并签署知情同意协议。排除标准:①不愿意配合研究的患者;②既往有抗HBV治疗、化疗及放疗史的患者;③合并有酒精性肝炎、脂肪肝、胆汁性肝硬化、自身免疫性肝病、甲型肝炎、丙型肝炎及丁型肝炎的患者;④合并有免疫缺陷疾病的患者。本研究经邯郸市中心医院伦理委员会审核批准。观察组56例患者中,男40例,女16例;年龄为41~69岁,平均为(53.1±14.5)岁。对照组56例患者中,男38例,女18例;年龄为40~69岁,平均为(52.2±14.6)岁。两组患者的性别、年龄、病理类型、病理分期及化疗方案比较,差异均无统计学意义(P>0.05),具有可比性,详见表1。
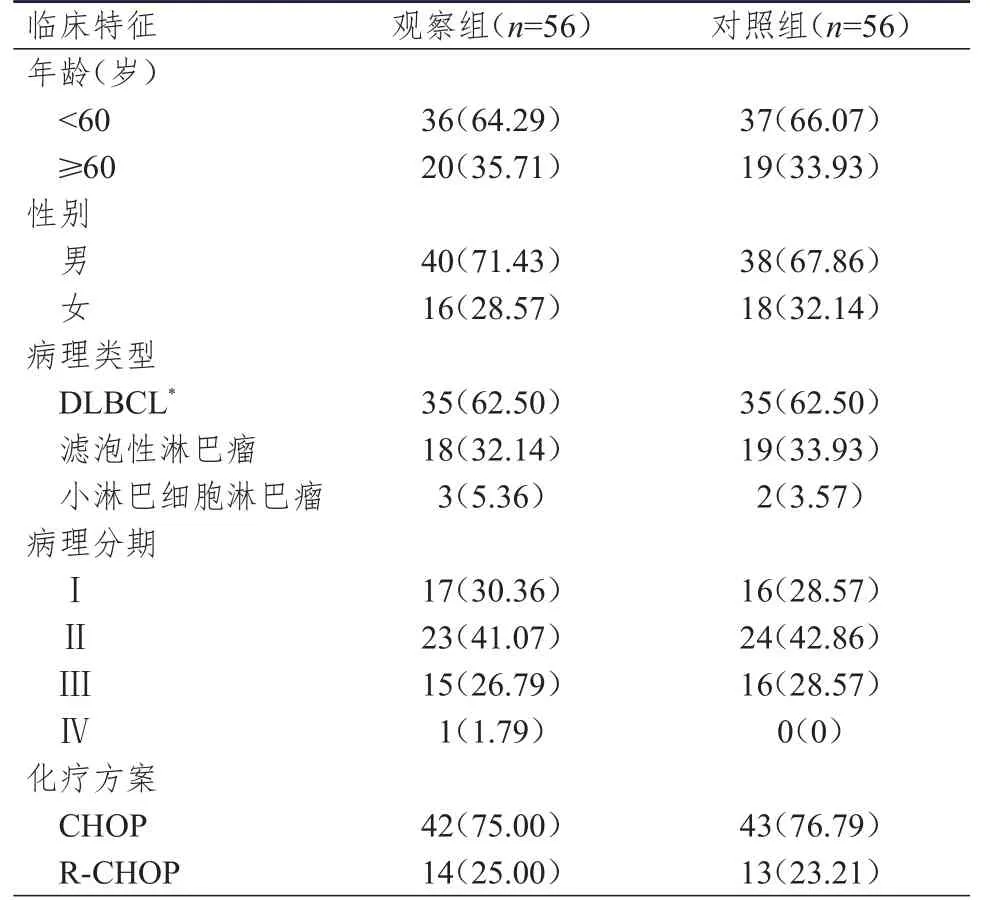
表1 两组患者的基线资料[ n(%)]
1.2 治疗方法
所有患者均给予CHOP或R-CHOP化疗方案。CHOP化疗方案:化疗第1天,环磷酰胺750 mg/m2、多柔比星 50 mg/m2、长春新碱 1.4~2.0 mg/m2,静脉滴注;化疗第1~5天,醋酸泼尼松60 mg/m2口服,21天为1个疗程。R-CHOP化疗方案是在CHOP方案的基础上于化疗前1天联合利妥昔单抗375 mg/m2静脉注射,21天为1个疗程,持续3~4个疗程。
观察组56例患者于化疗前1周开始口服恩替卡韦0.5 mg,每天1次,持续至化疗结束后4~6周。对照组56例患者不给予预防性抗HBV治疗,在丙氨酸转氨酶(alanine aminotransferase,ALT)超过正常值上限1.5倍时暂停化疗,接受抗HBV治疗,口服恩替卡韦0.5 mg,每天1次。
1.3 观察指标
比较两组患者的HBV再激活率和肝功能不全发生率,分析HBV再激活的影响因素。
HBV再激活的判断标准为患者治疗后HBV DNA水平比化疗前高10倍及以上,或HBV DNA绝对值≥105拷贝数/毫升。
肝功能不全分级按照世界卫生组织(WHO)制定的不良反应分级标准[5]划分:0级,ALT、天冬氨酸转氨酶(aspartate aminotransferase,AST)及总胆红素(total bilirubin,TBIL)水平低于正常参考范围上限的1.25倍;Ⅰ级,ALT、AST、TBIL水平为正常参考范围上限的 1.25~2.50倍;Ⅱ级,ALT、AST、TBIL水平为正常参考范围上限的2.51~5.00倍;Ⅲ级,ALT、AST、TBIL水平为正常参考范围上限的5.01~10.00倍;Ⅳ级,ALT、AST、TBIL水平高于正常参考范围上限10.00倍。肝功能不全的总发生率=不同级别的肝功能不全患者的总例数/总病例数×100%。
1.4 统计学方法
采用SPSS 21.0统计软件分析数据,计量资料以均数±标准差(±s)表示,采用t检验;计数资料以率(%)表示,采用χ2检验;HBV再激活的相关因素分析采用Logistic回归分析,P<0.05为差异有统计学意义。
2 结果
2.1 HBV再激活率与肝功能不全发生率比较
观察组患者HBV再激活率为10.71%(6/56),低于对照组的28.57%(16/56),差异有统计学意义(χ2=10.431,P<0.05)。观察组患者肝功能不全0级8例,Ⅰ级3例,总发生率为19.64%,对照组患者肝功能不全0级2例,Ⅰ级15例,Ⅱ级3例,总发生率为35.71%,观察组患者肝功能不全的总发生率低于对照组,差异有统计学意义(χ2=9.335,P<0.05)。
2.2 HBV再激活的影响因素分析
112例患者中,22例(19.64%)出现HBV再激活,其中观察组6例(10.71%)、对照组16例(28.57%)。Logistic回归分析显示:病理分期为Ⅲ~Ⅳ期及R-CHOP化疗方案是HBV再激活的危险因素(P<0.05),应用恩替卡韦是HBV再激活的保护因素(P<0.05),详见表2。
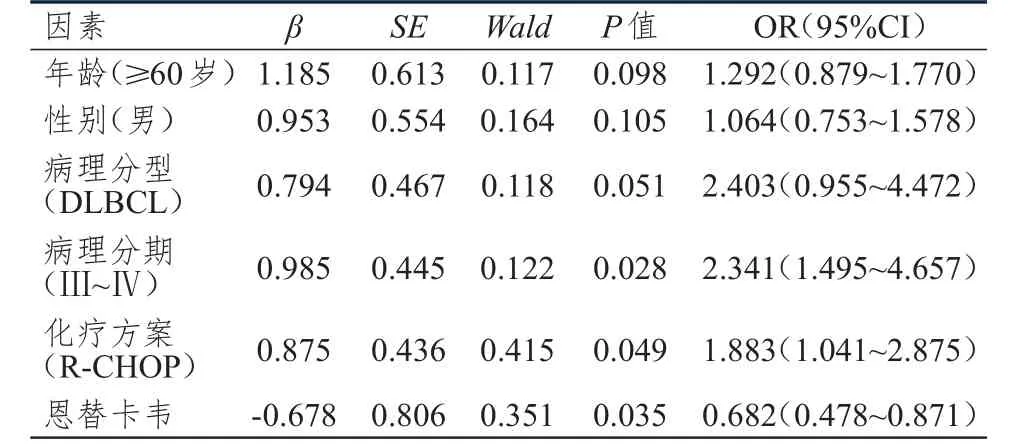
表2 HBV再激活的影响因素分析
3 讨论
中国是HBV感染的高发区域,流行病学研究发现,中国慢性HBV携带者数量超过1亿[6]。有研究发现,NHL患者的HBsAg阳性率为28.02%,高于其他类型肿瘤患者的14.79%[7],NHL患者HBV感染高发,与多种机制相关,主要是淋巴瘤患者的免疫功能减退,病毒感染与再激活的风险升高;HBV感染可能导致NHL发病率增加[8-9]。NHL患者化疗方案主要包括CHOP和R-CHOP等。近年来,含有利妥昔单抗的化疗方案成为B细胞淋巴瘤的一线治疗方案,该方案中应用的细胞毒性药物和免疫抑制药等可以导致患者机体免疫功能减退,患者HBV再激活并发生肝功能不全,严重者需要中断化疗,严重影响患者的治疗效果和预后。
目前,临床上HBsAg阳性NHL患者HBV再激活的研究较多,而HBsAg阴性NHL患者HBV再激活的研究较少。HBsAg阴性患者占HBV感染者的10%~25%,与HBsAg阳性患者比较,HBsAg阴性患者起病更加隐匿且症状较轻,容易被忽略[10]。既往研究发现,预防性应用抗HBV药物可以明显降低合并有HBV感染的乳腺癌患者化疗后HBV再激活率和肝功能不全的发生率[11],但是HBsAg阴性是否应该接受预防性抗HBV治疗仍存在争议。
有研究表明,合并HBV感染的肿瘤(NHL[12]及肺癌、乳腺癌、消化系统肿瘤、妇科肿瘤[13])患者化疗后HBV再激活率增加。本研究发现,HBsAg阴性而乙型肝炎E抗原/抗体阳性、乙型肝炎核心抗体阳性患者化疗后也存在一定的HBV再激活和肝功能不全的情况,观察组患者肝功能不全的发生率及病毒再激活率均低于对照组,多因素分析显示恩替卡韦与HBV再激活的发生呈负相关。这提示此类患者也需要进行预防性抗HBV治疗,从而保证化疗顺利进行。
有研究发现,B细胞NHL患者化疗后HBV再激活率增加,B细胞NHL主要累及B细胞亚群,而B淋巴细胞是免疫系统的主要细胞,可介导体液免疫,在抗HBV感染中发挥着重要的作用[14],但本研究中病理分型DLBCL与HBV再激活无相关性。本研究显示,R-CHOP化疗方案的应用是HBV再激活的危险因素。这是因为,利妥昔单抗属于CD20单抗,是DLBCL的一线治疗药物,与前B细胞及成熟B细胞表面CD20抗原结合后,通过补体依赖及抗体依赖的细胞毒性作用,诱导B淋巴细胞凋亡,在减少肿瘤细胞数量的同时导致浆细胞数量减少,继而抗体减少,为病毒再激活创造条件[15]。本研究显示,病理分期为Ⅲ~Ⅳ期是HBV再激活的危险因素。这是因为Ⅲ~Ⅳ期NHL患者的一般状态较差,化疗后免疫功能减退,HBV再激活的发生率增加。
综上所述,HBsAg阴性NHL患者的HBV再激活与多种因素相关,恩替卡韦可以减少NHL患者的HBV再激活率及肝功能不全总发生率。此类患者化疗前需要进行预防性抗HBV治疗,以保证化疗顺利进行。
