VITEK-MS质谱仪直接检测BacT/ALER T3D仪阳性血培养瓶微生物的实验研究*
2017-10-12李聪丁守甫黄颖王中新沈继录徐元宏
李聪,丁守甫,黄颖,王中新,沈继录,徐元宏
(安徽医科大学第一附属医院 检验科,安徽 合肥 230022)
VITEK-MS质谱仪直接检测BacT/ALER T3D仪阳性血培养瓶微生物的实验研究*
李聪,丁守甫,黄颖,王中新,沈继录,徐元宏
(安徽医科大学第一附属医院 检验科,安徽 合肥 230022)
目的 评估基质辅助激光解析电离飞行时间质谱(VITEK-MS)仪直接检测BacT/ALERT 3D仪阳性培养瓶微生物方法的可行性与准确性。方法 选取2016年9月-2016年11月安徽医科大学第一附属医院微生物室BacT/ALERT 3D全自动培养仪当天报告阳性的血培养瓶,差速离心法处理后直接用VITEK-MS进行检测,并与常规鉴定法进行比较。结果 150例阳性培养瓶中,除13例培养瓶中无细菌生长外,VITEK-MS直接鉴定法正确检测出97例(70.8%)菌株,错误检测出10例(7.3%)菌株,30例(21.9%)鉴定无结果。其中,革兰阴性杆菌正确鉴定出61例(88.4%)菌株,鉴定无结果8例(11.6%);革兰阳性球菌正确鉴定出36例(52.9%)菌株,鉴定错误10例(14.7%),鉴定无结果22例(32.4%)。结论 利用VITEK-MS直接鉴定阳性血培养瓶的方法准确性高、特异性强,革兰阴性杆菌鉴定准确率远高于革兰阳性球菌,且鉴定时间短(只需2 h)。该方法可以作为快速诊断阳性血培养瓶的新方法。
基质辅助激光解析电离飞行时间质谱;血培养;直接鉴定法
Abstract:Objective To evaluate the performance of matrix-assisted laser desorption/ionization time-offlight mass spectrometry system (VITEK-MS)for direct detection of bacteria in the positive bottles by BacT/ALERT 3D blood culture system and its identification rate.Methods All positive blood culture botlles reported by BacT/ALERT 3D blood culture system that had been obtained from the patients in the First Affiliated Hospital of Anhui Medical University from September to November 2016 were selected.The bacteria were directly detected by VITEK-MS after differential centrifugation,and compared with the results by traditional biochemical identification.Results Among 150 positive blood culture bottles,there was no bacteria growth in 13 bottles;in the rest 137 bottles,VITEK-MS correctly identified 97 (70.8%),wrongly detected 10(7.3%),and could not identify 30 (21.9%).For Gram-negative bacilli,the correct identification rate was 88.4% (61 cases)and 8 cases (11.6%)were not identified.In Gram-positive cocci,the correct and wrong identification rate were 52.9% (36 cases)and 14.7% (10 cases),and 22 cases (32.4%)could not be identified.Conclusions The method of using VITEK-MS to identify the positive blood culture bottles is accurate and specific.The accurate identification rate of Gram-negative bacilli is much higher than that of Gram-positive cocci.The time for identification is reduced to 2 h.Thus,this method can provide rapid andreliable identification of microorganisms in blood culture bottles.
Keywords:matrix-assisted laser desorption/ionization time-of-flight mass spectrometry;blood culture;direct identification
血流感染在临床有很高的发病率和病死率,快速诊断出致病菌并进行对应的抗生素治疗至关重要,不仅可以减少血流感染的死亡率,而且可以降低患者的费用[1]。基质辅助激光解析电离飞行时间质谱(matrix-assisted laser desorption ionization-time of flight mass spectrometry system,VITEK-MS)的原理是采用激光照射微生物与基质形成的结晶,使其发生电离形成特异的质量图谱,然后与数据库中的图谱进行比较,鉴定出微生物的种属[2]。VITEK-MS对纯菌落菌种快速鉴定具有很高的稳定性和准确性,鉴定时间从常规生化鉴定的48~72 h缩短为24 h,对常见细菌和酵母菌种属的鉴定率能达85%~99%,已常规应用于临床微生物室[3]。目前,国内外学者均有尝试用VITEK-MS直接法检测阳性血培养瓶中的微生物,如细胞裂解法和分离胶促凝管辅助法等[4-5]。本实验将采用VITEK-MS直接法鉴定阳性培养瓶中的微生物,同时进行常规培养程序,培养的单个菌落用VITEK 2 Compact全自动细菌鉴定仪系统(以下简称VITEK-2 Compact)进行检测,并以其结果为标准。将差速离心法结果与常规法比较,确定该方法的可行性与准确率。
1 材料与方法
1.1 细菌来源
选取2016年9月1日-2016年11月30日安徽医科大学第一附属医院微生物室BacT/ALERT 3D全自动培养仪报告阳性的需氧血培养瓶(同一患者只选取1瓶阳性瓶纳入研究),并于当天完成处理后进行直接鉴定,共收集150例报告阳性的需氧血培养瓶。
1.2 仪器和试剂
无水乙醇、甲酸及乙腈购于合肥飒英斯生物科技有限公司(所用70%甲酸均使用当天配制),VITEKMS质谱仪及配套的靶板、α-氰基-4-羟基肉桂酸(a-Cyano-4-hydroxy-cinnamic acid,CHCA)基质液、BacT/ALERT 3D仪、VITEK-2 Compact仪,以及相应配套的革兰阴性杆菌鉴定卡(gram-negative,GN)购于法国生物梅里埃有限公司,质控菌株为ATCC8739菌株(北京中原公司)。
1.3 VITEK-MS直接法
抽取阳性血培养瓶中2.0 ml样本,700 r/min离心10 min,上清液吸入新的离心管中,6 000 r/min离心15 min,弃去上清液。沉淀物加1 ml去离子水,6 000 r/min离心15 min,弃去上清液。再加300 μl去离子水和900 ul无水乙醇,涡旋至均匀,13 000 r/min离心2 min,弃去上清液,沉淀干燥。加入25 μl 70%甲酸和25 μl乙腈,涡旋至均匀,13 000 r/min离心1 min。取1 μl上清液液涂于VITEK-MS的靶板上,待完全干燥后加1 μl CHCA完全覆盖点种的菌膜,待完全干燥后用VITEK-MS进行检测[6-7]。
1.4 常规鉴定方法
收集当天报告阳性的需氧血培养瓶,取1或2滴分别接种于血平板和巧克力平板上,在37℃、5%二氧化碳CO2培养18~24 h后,挑取纯菌落,调取0.5麦氏浊度插入GN卡,放入VITEK-2 Compact进行鉴定,以其结果为标准结果。
1.5 统计学方法
数据分析采用SPSS 20.0统计软件,将常规细菌鉴定方法所得出的结果作为标准,差速离心提取法所测的结果与其比较,根据VITEK-MS检测结果,将置信度>85%的数据作为其鉴定结果,其余均视为鉴定无结果,如鉴定无结果、频谱采集错误、波峰不足、鉴定出≥2种菌种且置信度低[7]。
2 结果
2.1 革兰菌检测结果
150例阳性血培养瓶,用VITEK-2 Compact常规法鉴定出69例革兰阴性杆菌,68例革兰阳性球菌(13例无细菌生长)。VITEK-MS直接法正确鉴定97例(70.8%),错误鉴定 10例(7.3%),鉴定无结果30例(21.9%)。见附表。
2.2 肠杆菌科细菌检测结果
56株肠杆菌科中,经VITEK-MS直接法检测后,有48株(85.7%)与 VITEK-2 Compact检测相同,7株(12.5%)鉴定无结果。见附表。
2.3 非发酵革兰阴性杆菌检测结果
11株非发酵菌中,经VITEK-MS直接法检测后,有10株(90.1%)与 VITEK-2 Compact检测相同,1株(9.1%)鉴定无结果。其中鲍曼不动杆菌与铜绿假单胞菌鉴定准确率均达100%。见附表。
2.4 其他革兰阴性杆菌检测结果
经VITEK-MS直接法鉴定出2株(100%)嗜水/豚鼠气单胞菌,1株(100%)副溶血嗜血杆菌,其与VITEK-2 Compact鉴定结果一致。见附表。
2.5 革兰阳性球菌检测结果
68株革兰阳性球菌经VITEK-MS直接法检测后,正确鉴定36株(52.9%),错误鉴定10株(14.7%),鉴定无结果22株(32.5%)。用VITEK-2 Compact鉴定主要分为葡萄球菌属、链球菌属、肠球菌属,其经VITEK-MS直接法鉴定正确的分别为31株(54.4%)、2株(40.0%)和 2株(50.0%);错误鉴定分别为 7株(22.6%)、3株(60.0%)和0株(0.00%);鉴定无结果分别为 19株(33.3%)、0株(0.00)和 2株(50.0%)。对于2株藤黄微球菌,1株鉴定正确,1株鉴定无结果。见附表。
2.6 鉴定错误的结果
与常规方法比较,VITEK-MS直接法共有10株菌株鉴定错误,且全为革兰阳性球菌。其中,葡萄球菌属鉴定错误7株,3株表皮葡萄球菌分别错误鉴定为金黄色葡萄球菌、人型葡萄球菌及溶血葡萄球菌;3株人型葡萄球菌分别错误鉴定为2株表皮葡萄球菌和1株溶血葡萄球菌;1株耳葡萄球菌错误鉴定为人型葡萄球菌。链球菌属错误鉴定3株,将唾液链球菌、格氏链球菌及草绿色链球菌分别错误鉴定为前庭链球菌、毗邻颗粒链球菌及溶血葡萄球菌。
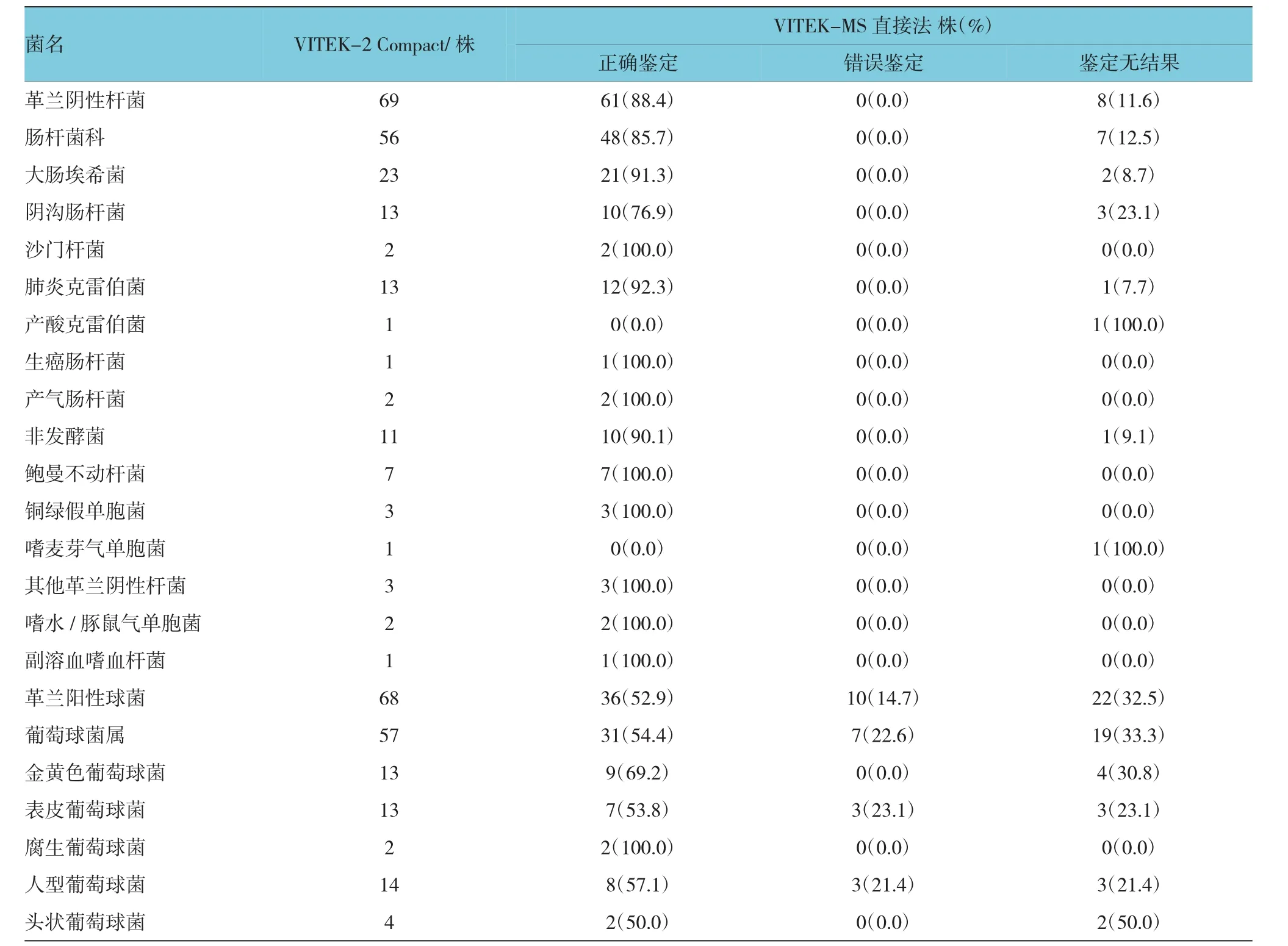
附表 150例阳性培养瓶VITEK-MS直接检测与VITEK-2 C om pact检测结果比较
2.7 VITEK-MS直接鉴定法的方法学特点
本实验以VITEK-2 Compact常规鉴定法结果为标准结果,将VITEK-MS直接鉴定法结果与其比较。VITEK-MS直接法鉴定阳性97例,且全部常规鉴定结果阳性;VITEK-MS直接法鉴定阴性53例,其中常规鉴定结果阳性40例。该实验方法的准确性为 73.3%(110/150),敏感性为 70.8%(97/137),特异性为100.0%(13/13)。其准确性、敏感性及特异性的95%CI分别为(66.3,80.4)、(63.2,78.4)和(100.0,100.0)。
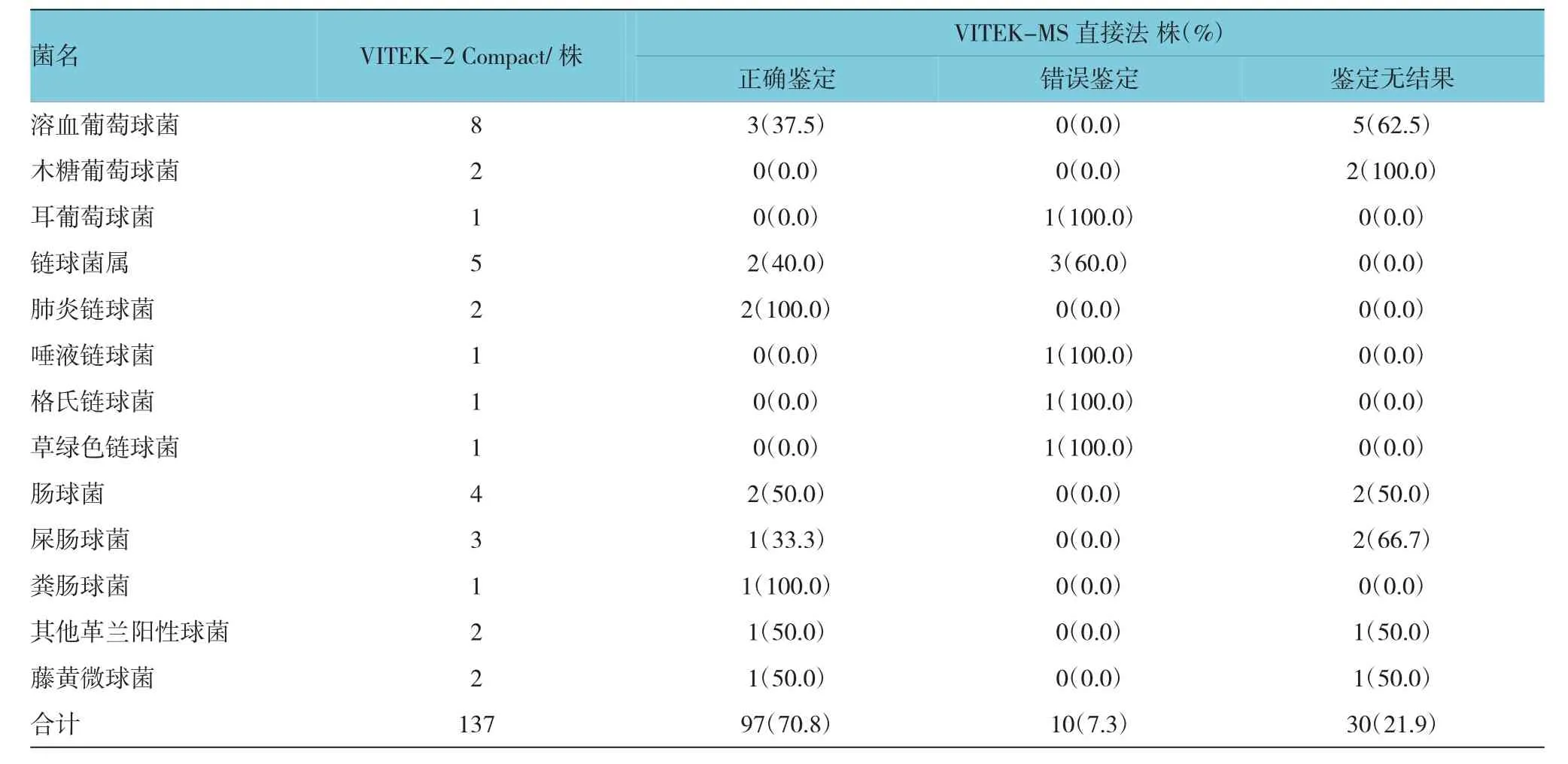
续附表
3 讨论
基质辅助激光解吸电离飞行时间质谱系统是近年才发展起来的新型软电离技术,采用该技术的VITEK-MS因其高通量的微生物鉴定系统和强大、可靠的数据库,已成为一种快速、准确、操作简单的鉴定微生物的新方法[8]。本院目前对报告阳性血培养瓶中微生物的鉴定方法为取阳性培养瓶中标本接种于血平板和巧克力平板中,置于35℃、CO2培养箱需氧或厌氧培养24~48 h,取培养出的单个菌落经过VITEK-MS鉴定得出结果。VITEK-MS不仅可以鉴定单个纯菌落,而且可以鉴定细菌的蛋白提取物。本实验采用差速离心法来提取细菌蛋白,因培养瓶中的血细胞、蛋白、活性炭等均会影响鉴定结果,所以笔者采用低速离心去除细胞和大颗粒,高速离心获取细菌沉淀物,经过洗涤和离心后进行蛋白提取(常用甲酸和乙腈)。
本实验收集的培养瓶均在2 h内完成检验,保证细菌的活性,真菌和≥2种细菌的感染均不在研究范围内。VITEK-MS直接法正确鉴定率为70.8%(97/137),其中革兰阴性杆菌的正确鉴定率为88.4%(61/69),革兰阳性球菌的正确鉴定率为52.9%(36/68),表明该方法革兰阴性杆菌的鉴定结果优于革兰阳性球菌,与国外研究基本相符[9]。本方法的准确性为 73.3%(110/150),敏感性为 70.8%(97/137),特异性为100.0%(13/13)。对于13例用传统方法培养无细菌生长且VITEK-MS直接法也未检测出的原因可能是:①血培养瓶为假阳性,所以2种方法均未测出;②培养瓶中为一些苛养菌、厌氧菌、结核杆菌、真菌等一些难培养的微生物,常规方法培养时间短,未生长出菌落;③VITEK-MS直接法鉴定无结果,可能是数据库中缺少谱图;④对真菌及一些少见菌和难培养菌用菌蛋白检测鉴定率低;⑤培养瓶中菌浓度低等原因[10-11]。
针对用常规方法检测出菌种,而本实验的21.9%(30/137)鉴定无结果和7.3%(10/137)鉴定错误可能是因为培养瓶中碳粒的存在[12]。预处理提取细菌蛋白的不同,导致仍有细胞碎片的存在,干扰图谱过多,影响分析[13];也可能洗涤过程中的蛋白质丢失或蛋白提取不足等原因的存在,导致分析图谱收集的不足。而实验中革兰阳性球菌鉴定正确率较低的具体原因还不确切,可能是由于以下几个方面[14-15]:①革兰阳性球菌的细胞壁较厚,抗溶菌作用强,导致提取的蛋白量过少;②革兰阳性球菌的蛋白结构相似,形成的蛋白图谱相似,导致VITEK-MS难以鉴别;③污染菌的存在,VITEK-MS是分析细菌大量的核糖蛋白来进行鉴定的,最适宜的检测是细菌处于生长对数期,大量活菌存在并大量表达核糖蛋白,当是污染菌造成的培养瓶报告阳性时,通常其生长缓慢,需要长时间的孵育时间,这将导致VITEK-MS的错误鉴定或检测不出,如常见污染菌表皮葡萄球菌。无论是何种原因造成的革兰阳性球菌检测率低下,笔者对革兰阳性球菌的检测都要重视并探索解决方法。
本实验方法的优点是较常规方法检测迅速(只需2 h)、操作简单、不需要特殊设备、价格低廉、准确性高等。总之,该方法实用性强,可以临床推广使用,但仍然不能完全替代传统的鉴定方法。未来应该进一步探索其实验室的操作标准及对革兰阳性球菌的鉴定和用VITEK-MS进行耐药性的分析,帮助临床更快、更准确地得到结果。
[1] FEBBRARO F,RODIO D M,PUGGIONI G,et al.MALDI-TOF MS versus VITEK 2:comparison of systems for the identification of microorganisms responsible for bacteremia[J].Curr Microbiol,2016,73(6):843-850.
[2] CROXATTO A,PROD'HOM G.Applications of MALDI-TOF mass spectrometry in clinical diagnostic microbiology[J].FEMS Microbiology Reviews,2012,36(2):380-407.
[3] 陈飞,胡玢婕,赵虎.MALDI-TOF MS在临床微生物样本直接检测中的应用[J].检验医学,2015,30(7):750-756.
[4] TANNER H,EVANS J T,GOSSAIN S.Evaluation of three sample preparation methods for the direct identification of bacteria in positive blood cultures by MALDI-TOF[J].BMC Research Notes,2017,10(1):48.
[5] 陈峰,李媛睿,皇甫昱婵,等.分离胶促凝管联合MALDI-TOF MS直接检测血培养阳性细菌[J].检验医学,2015(2):113-121.
[6] MARCH-ROSSELLÓ G A,MUÑOZ-MORENO M F,GARCÍALOYGORRI-JORDÁN de URRIÉS M C.A differential centrifugation protocol and validation criterion for enhancing mass spectrometry (MALDI-TOF)results in microbial identification using blood culture growth bottles[J].European Journal of Clinical Microbiology Infectious Diseases,2013,32(5):699-704.
[7] MESTAS J,FELSENSTEIN S.Direct identification of bacteria from positive BacT/ALERT blood culture bottles using matrixassisted laser desorption ionization-time-of-flight mass spectrometry[J].Diagnostic Microbiology and Infectious Disease,2014,80(3):193-196.
[8] CROXATTO A,PROD'HOM G.Applications of MALDI-TOF mass spectrometry inclinical diagnostic microbiology[J].FEMS Microbiol Rev,2012,36(2):380-407.
[9] RODRÍGUEZ-SÁNCHEZ B,SÁNCHEZ-CARRILLO C,RUIZ A,et al.Direct identification of pathogens from positive blood cultures using matrix-assisted laser desorption-ionization time-of-flight mass spectrometry[J].Clinical Microbiology and Infection,2014,20(7):421-427.
[10] IDELEVICH E A,GRÜNASTEL B.Rapid detection and identification of candidemia by direct blood culturing on solid medium by use of lysis-centrifugation method combined with matrixassisted laser desorption ionization-time of flight mass spectrometry (MALDI-TOF MS)[J].Journal of Clinical Microbiology,2017,55(1):97-100.
[11] CHIEN J Y,LEE T F,DU S H,et al.Applicability of an inhouse saponin-based extraction method in bruker biotyper matrixassisted laser desorption/ionization time-of-flight mass spectrometry system for identification of bacterial and fungal species in positively flagged blood cultures[J].Frontiers in Microbiology,2016,7:1432.
[12] ROMERO-GÓMEZ M P.The effect of the blood culture bottle type in the rate of direct identification from positive cultures by matrix-assisted laser desorption/ionisation time-of-flight(MALDITOF)mass spectrometry[J].The Journal of Infection,2011,62(3):251-253.
[13] THOMIN J,AUBIN G G,FOUBERT F.Assessment of four protocols for rapid bacterial identification from positive blood culture pellets by matrix-assisted laser desorption ionization-time of flight mass spectrometry (VitekMS)[J].Journal of Microbiological Methods,2015,115:54-56.
[14] YONETANI S,OHNISHI H,OHKUSU K,et al.Direct identification of microorganisms from positive blood cultures by MALDITOF MS using an in-house saponin method[J].Int J Infect Dis,2016,52:37-42.
[15] RANDAZZO A,SIMON M,GOFFINETP,etal.Optimal turnaround time for direct identification of microorganisms by mass spectrometry in blood culture[J].Journal of Microbiological Methods,2016,130:1-5.
(童颖丹 编辑)
VITEK-MS direct identification of bacteria from positive BacT/ALERT 3D blood culture bottles*
Cong Li,Shou-fu Ding,Ying Huang,Zhong-xin Wang,Ji-lu Shen,Yuan-hong Xu
(Clinical Laboratory,the First Affiliated Hospital of Anhui Medical University,Hefei,Anhui 230022,China)
R446.5
A
10.3969/j.issn.1005-8982.2017.23.003
1005-8982(2017)23-0013-05
2017-02-13
国家自然科学基金(No:81171606)
徐元宏,E-mail:xyhong1964@163.com
