泽兰中迷迭香酸含量测定方法学研究△
2017-09-21相婷吴丽真王绍青郑璐
相婷,吴丽真,王绍青,郑璐
(扬子江药业集团有限公司 国家中医药管理局 中药质量控制实验室,江苏 泰州 225321)
·基础研究·
泽兰中迷迭香酸含量测定方法学研究△
相婷,吴丽真,王绍青,郑璐*
(扬子江药业集团有限公司 国家中医药管理局 中药质量控制实验室,江苏 泰州 225321)
目的:建立泽兰中迷迭香酸的含量测定方法,为《欧洲药典》泽兰专论的质量标准提供研究数据。方法:采用高效液相色谱法。基于样品提取和色谱条件的优化结果建立迷迭香酸的分析方法,同时对该方法进行系统的方法学验证,包括采用单变量分析(OVAT)进行方法的耐用性研究及按照《欧洲药典》的方法测定该色谱系统的滞留体积。结果:迷迭香酸检测质量浓度线性范围为5.02~60.30 μg·mL-1(r=0.999 9);加样回收率为95.5%~101.6%,RSD=2.1%(n=9);重复性、中间精密度、稳定性及耐用性试验的RSD均小于3.0%;该色谱系统滞留体积为 2.4 mL。结论:该方法操作简单,重复性、准确度及耐用性良好,可作为泽兰中迷迭香酸的含量测定方法列入《欧洲药典》泽兰专论的质量标准草案。
高效液相色谱法;泽兰;迷迭香酸;方法学;欧洲药典
泽兰为唇形科植物毛叶地瓜儿苗LycopuslucidusTurcz.var.hirtusRegel.的干燥地上部分,临床上主要用于治疗月经不调、闭经、痛经、产后出血腹痛及水肿。文献表明,泽兰的主要化学成分包括黄酮类、酚酸类、萜类和甾体类等[1]。迷迭香酸是泽兰中的主要活性成分之一,表现出多种生物活性,如抗氧化[2]、抗炎[3]、抑制疼痛[4]、抗血栓和抗血小板凝集[5]、心肌保护[6]、抗抑郁[7]、神经保护[8]及抗肿瘤[9]等。因此,本研究选取迷迭香酸作为特征性成分,建立其在泽兰中的含量测定方法,用于泽兰药材的质量控制;同时为欧洲药典泽兰专论的质量标准提供研究数据。
1 材料
1.1 仪器
Agilent1260型高效液相色谱仪,包括四元泵(G1311C)、柱温箱(G1316A)、自动进样器(G1329B)、DAD紫外检测器(G1315D)和Openlab色谱工作站(美国安捷伦公司);XS-205DU型十万分之一天平(瑞士梅特勒公司)。
1.2 药材与试剂
泽兰药材共8批次,产地分虽为河南、山东、天津、江苏,经中国药科大学天然药物活性组分与药效国家重点实验室李会军教授鉴定为正品;迷迭香酸对照品(中国食品药品检定研究院,批号:111871-201404,纯度:98.6%);甲醇、乙腈为色谱纯,磷酸为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:月旭Ultimate XB-C18(250 mm×4.0 mm,5 μm);流动相A:磷酸-乙腈-水(1∶19∶80,V/V/V),流动相B:磷酸-甲醇-乙腈(1∶40∶59,V/V/V);梯度洗脱,洗脱程序为:0~20 min,100%A→70%A,20~25 min,70%A→0%A,25~30 min,0%A→100%A;流速为1.0 mL·min-1;检测波长为330 nm;进样量为20 μL。
2.2 溶液的制备
2.2.1 空白溶液 70%甲醇水溶液。
2.2.2 对照品溶液 取迷迭香酸对照品10.0 mg,精密称定,置于20 mL容量瓶中,用70%甲醇水溶液溶解并定容至刻度,摇匀,精密吸取上述溶液1 mL,70%甲醇水溶液稀释定容至25 mL,即得。
2.2.3 供试品溶液 取泽兰药材粉末(过50目筛)约1.00 g,精密称定,置于具塞容量瓶中,精密加入25 mL 70%甲醇水溶液后称重,然后在92 ℃条件下加热回流30 min,冷却后补足损失的重量,摇匀,过滤,收集续滤液,精密量取上述续滤液2 mL,70%甲醇水溶液稀释定容至10 mL,进样前用0.45 μm微孔滤膜过滤。
2.2.4 空白供试品溶液 不加入泽兰药材,按照2.2.3方法制备,即得。
2.2.5 混合溶液 分别量取适量的2.2.2和2.2.3项下溶液,以1∶1体积等量混合,即得。
2.3 系统适用性试验
按照2.2方法分别制备得到空白溶液、对照品溶液和供试品溶液,按2.1项下色谱条件进行测定,记录色谱,见图1。结果显示对照品连续进样5针,峰面积的RSD=0.27%,对照品和供试品溶液中迷迭香酸色谱峰的对称因子在0.95~1.05,理论塔板数均不小于50 000,迷迭香酸色谱峰与前后杂质峰分离度均大于1.50,提示该色谱系统系统适用性良好。
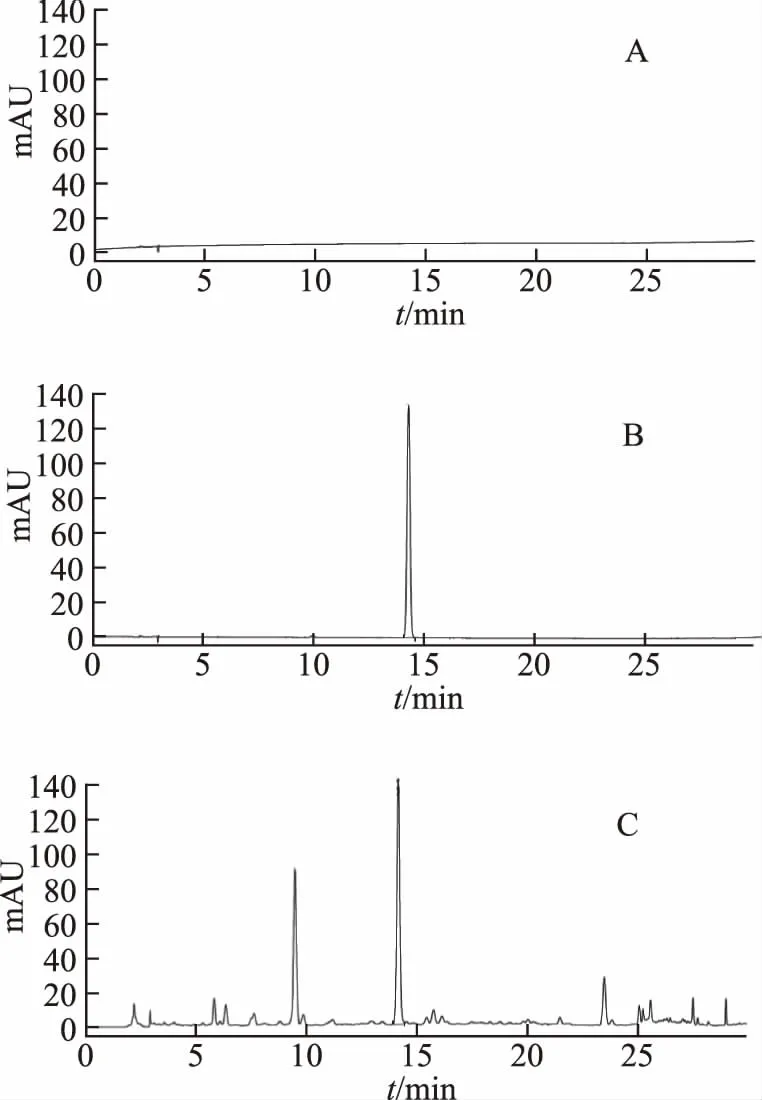
注:A.空白溶液;B.迷迭香酸对照品;C.供试品溶液。图1 泽兰及其对照品高效液相色谱图
2.4 专属性试验
按照2.2方法分别制备得到空白溶液、对照品溶液、供试品溶液、空白供试品溶液和对照品供试品混合溶液,按2.1项下色谱条件进行测定,记录色谱。结果显示空白溶液和空白供试品溶液对主色谱峰无干扰,对照品供试品混合溶液中主色谱峰无裂分现象,提示该方法专属性良好。
2.5 线性关系考察
2.5.1对照品线性关系考察 取迷迭香酸对照品适量,精密称定,置于25 mL容量瓶中,加入70%甲醇水溶解并定容,作为母液。分别精密量取适量上述母液,稀释配制成浓度为5.02、10.05、20.10、25.12、50.25、60.30 μg·mL-1的系列对照品溶液。按2.1项下色谱条件进行测定,记录色谱。以质量浓度(X,μg·mL-1)为横坐标、峰面积(Y)为纵坐标进行线性拟合,得回归方程Y=62.678 8X-3.463 9(r=0.999 9)。结果表明,迷迭香酸在5.02~60.30 μg·mL-1线性关系良好。
2.5.2供试品线性关系考察 分别取泽兰药材粉末(过50目筛)约0.20 g、0.40 g、0.80 g、1.00 g、1.50 g和2.00 g,精密称定,按照2.2.3方法制备得到一系列不同质量分数的供试品溶液。按2.1项下色谱条件分别对以上供试品溶液进行测定,记录色谱。以质量分数(X,%)为横坐标、峰面积(Y)为纵坐标进行线性拟合,得回归方程Y=12.456 1X+29.790 1(r=0.999 8)。结果表明,供试品质量分数在20.47%~200.96%线性关系良好。
2.6 重复性试验
分别取泽兰药材粉末(过50目筛)约0.50、1.00、1.50 g(相当于50%、100%和150%3个质量分数水平)各3份样品,精密称定。按照2.2.3方法制备得到9份供试品溶液。按2.1项下色谱条件进行测定,记录色谱。结果迷迭香酸含量在低、中、高3个质量百分比浓度水平下RSD值分别为0.76%、0.31%和0.70%,提示该方法重复性良好。
2.7 中间精密度试验
另外一名操作者取泽兰药材粉末(过50目筛)约1.00 g,平行6份样品,精密称定。按照2.2.3方法制备得到6份供试品溶液。按2.1项下色谱条件用另外一台高效液相色谱仪Agilent 1200进行测定,记录色谱。结果两名操作者在不同仪器上测得迷迭香酸含量的RSD=2.2%,提示该方法中间精密度良好。
2.8 加样回收试验
取已知含量的泽兰药材粉末(过50目筛)约0.50 g,平行9份样品,分为3组,分别加入3个质量分数水平(50%、100%和150%)的迷迭香酸对照品。按照2.2.3项下溶液制备方法制备得到9份供试品溶液。按2.1项下色谱条件进行测定,记录色谱并计算加样回收率,结果见表1。
2.9 稳定性试验
分别取2.2.2和2.2.3项下对照品和供试品溶液适量,分别于室温下放置0、2、4、6、8、10、12、18、24 h时按2.1项下色谱条件进行测定,记录色谱。结果对照品和供试品峰面积的RSD值分别为0.12%和0.27%,提示对照品和供试品在70%甲醇溶液中24 h内稳定性良好。
2.10 耐用性试验
本研究中耐用性试验是通过单变量分析法(OVAT)微调测试条件中的单个变量观察结果的不受影响程度,改变的测试变量包括提取条件变量(提取溶剂比例)和色谱条件变量(流速、波长和色谱柱),结果表明该方法耐用性良好,具体数据见表2和表3。
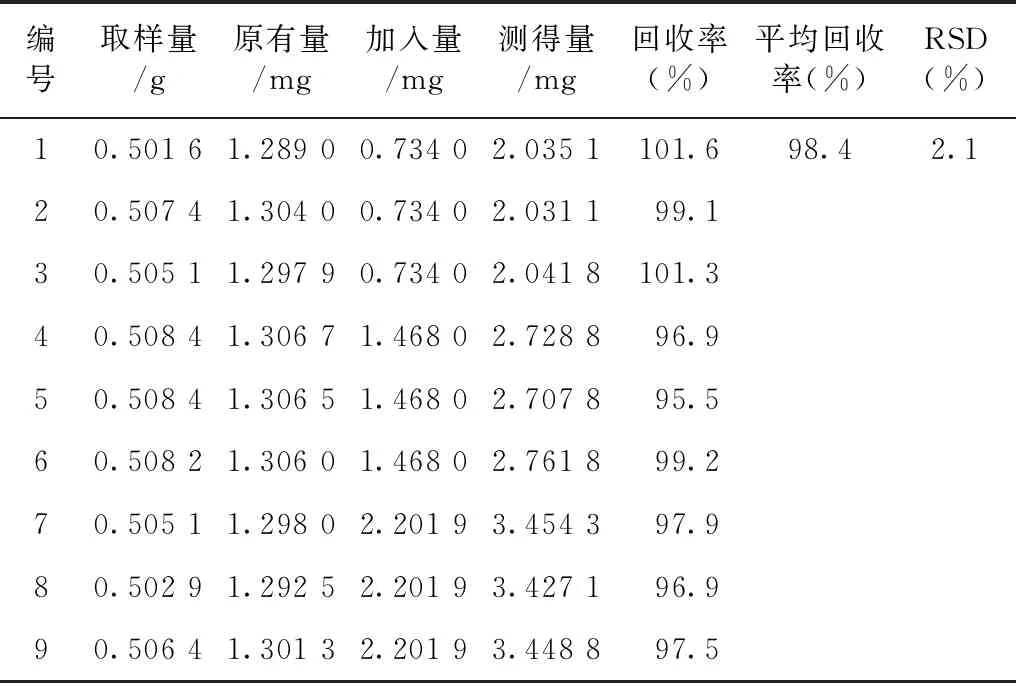
表1 泽兰中迷迭香酸加样回收率试验结果(n=9)
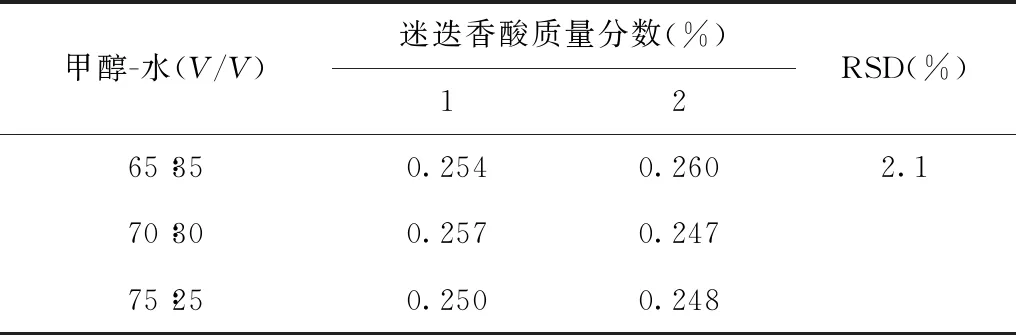
表2 提取条件耐用性结果

表3 色谱条件耐用性结果
2.11 滞留体积的测定
按照《欧洲药典》EP8.0“2.2.46”项下规定方法进行测定[10]。
2.11.1 测定条件 peek管:1.35 m×0.18 mm;流动相:水(A)-0.1%丙酮(B);洗脱程序:0~20 min,100% A→0% A;20~30 min,0%A;流速:2.0 mL·min-1;检测波长:265 nm。
2.11.2 计算结果 滞留体积VD=tD×F(tD=t0.5-0.5tG,tG=20 min,F=2 mL·min-1,t0.5=11.2 min)=2.4 mL。
2.12 样品含量测定
取8批次泽兰样品适量,按照2.2.3方法制备供试品溶液,再按2.1项下色谱条件进行测定,双样双针,记录色谱并计算样品含量,结果见表4。
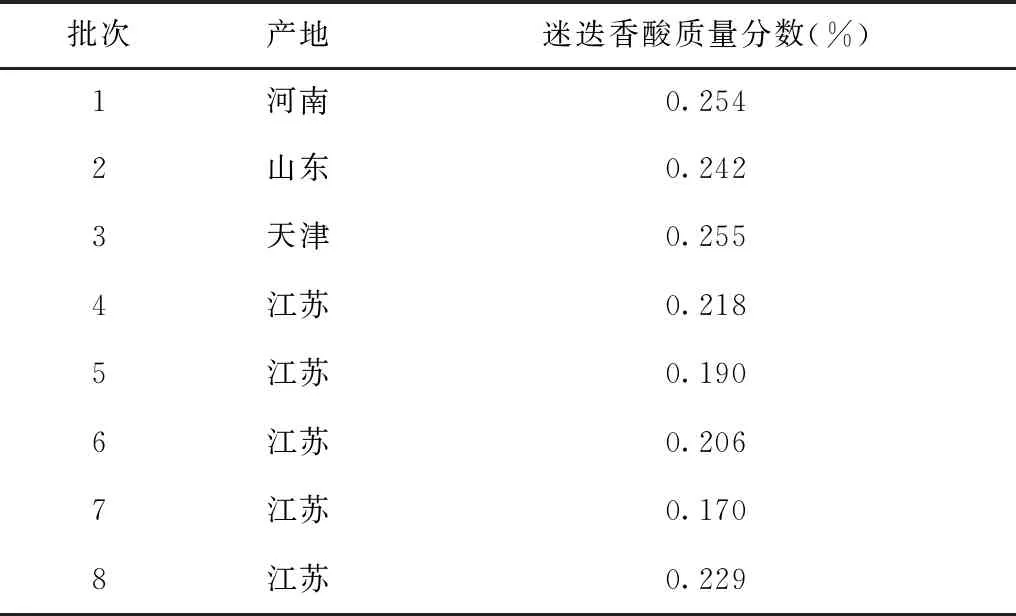
表4 泽兰样品中迷迭香酸含量测定结果(n=2)
3 讨论
3.1 提取条件的优化
本研究考察了4种不同比例的提取溶剂(30%、50%、70%甲醇水溶液和100%甲醇)进行提取,同时考察了不同提取方式(超声、回流和振摇)、不同溶剂量(15、25、50 mL)和不同提取时间(15、30、45 min)对迷迭香酸含量的影响,结果发现提取溶剂和提取方式对结果有较显著的影响,而溶剂量和提取时间对含量结果影响较小,因此最终确定最佳提取条件为25 mL 70%甲醇水溶液、回流提取30 min。
3.2 色谱条件的优化
本研究考察了甲醇-水、乙腈-水、甲醇-磷酸水、乙腈-磷酸水为流动相时对色谱峰分离的效果,结果峰形均未达到要求,后又筛选出甲醇-乙腈-柠檬酸水作为流动相,峰形能到得到较好改善,然而又出现保留时间过长的问题。最终本文参考《欧洲药典》香蜂草专论中迷迭香酸的色谱条件[10],并在其基础上进一步优化得到最佳色谱条件。
综上所述,该方法操作简单,重复性、准确度及耐用性良好,可作为泽兰中迷迭香酸的含量测定方法列入欧洲药典泽兰专论的质量标准草案。
[1] 任强,王红玲,周学刚,等.泽兰的化学成分、质量分析及药理作用研究进展[J].中国药房,2015,26(18):2588-2592.
[2] Slusarczyk S,Hajnos M,Skalicka-Wozniak K,et al.Antioxidant activity of polyphenols fromLycopusLucidusTurcz[J].Food Chem,2009,113(1):134.
[3] Ramalho L N Z,Pasta A A C,Terra V A,et al.Rosmarinic acid attenuates hepatic ischemia and reperfusion injury in rats[J].Food Chem Toxicol,2014,74:270.
[4] Boonyarikpunchai W,Sukrong S,Towiwat P.Anti-nociceptive activity and anti-inflammatory effects of rosmarinic acid isolated fromThunbergialaurifoliaLindl[J].Pharmacol Biochem Behav,2014,124:67-73.
[5] 邹正午,徐理纳,田金英.迷迭香酸抗血栓和抗血小板聚集作用[J].药学学报,1993,28(4):241-245.
[6] 李雪丽,刘建勋,李澎,等.迷迭香酸对心肌细胞缺氧复氧损伤的保护作用研究[J].中国中药杂志,2014,39(10):1897-1901.
[7] 晋翔,刘鹏,张雅红.迷迭香酸对大鼠抑郁样行为的作用及其机制研究[J].解放军医药杂志,2014,26(5):14-18.
[8] Ghaffari H,Venkataramana M,Ghassam B,et al.Rosmarinic acid mediated neuroprotective effects against H2O2-induced neuronal cell damage in N2A cells[J].Life Sci,2014,113(1/2):7-13.
[9] Ahamed M B,Aisha A F,Nassar Z D,et al.Cat’s whiskers tea(Orthosiphon stamineus)extract inhibits growth of colon tumor in nude mice and angiogenesis in endothelial cells via suppressing VEGFR phosphorylation.Nutr Cancer,2012,64(1):89-99.
[10]Council of Europe.European Pharmacopoeia[S].8th Edition.Strasbourg:Directorate for the Quality of Medicines & HealthCare(EDQM),2013:1318-1319.
ValidationofHPLCMethodforDeterminationofRosmarinicAcidinLycopiHerba
XIANGTing,WULizhen,WANGShaoqing,ZHENGLu*
[YangtzeRiverPharmaceutical(Group)Co.,Ltd.,TheNationalKeyInstituteofTCMQualityControl,
StateAdministrationofTraditionalChineseMedicineoftheP.R.China(NKI-TCM),Taizhou,225321,China]
Objective:To establish a method for determination of rosmarinic acid in Lycopi Herba and provide research data for Lycopi Herba monograph recommended to European Pharmacopeia(EP).Methods:An HPLC method was established by optimizing different extraction and chromatographic conditions and totally validated.Meanwhile,One-variable-at-a-time(OVAT)method was applied in the robustness test,and dwell volume of the HPLC system was determined following the described method in EP.Results:It was shown that the method kept good linearity(r=0.999 9)in the concentration range of 5.02-60.30 μg·mL-1for rosmarinic acid.The recovery was in the range of 95.5%-101.6% with RSD value of 2.1%.RSDs of repeatability,intermediate precision,stability and robustness test were less than 3.0%,and the dwell volume was determined as 2.4 mL for the HPLC system.Conclusion:The method is simple,accurate and reliable with good repeatability and robustness,which could be selected as determination method of rosmarinic acid for the draft of Lycopi Herba monograph recommended to EP.
HPLC;Lycopi Herba;rosmarinic acid;methodology;European Pharmacopeia
国家中医药管理局中医药行业科研专项(201307002)
] 郑璐,高级工程师,研究方向:中药欧盟质量标准研究;Tel:(021)68128999,E-mail:zhenglu@yangzijiang.com
10.13313/j.issn.1673-4890.2017.2.009
2016-06-23)
*[
