子洲黄芩中黄酮成分的含量测定及指纹图谱研究△
2017-09-21党珍张艳萍王西芳
党珍,张艳萍,王西芳*
(1.陕西中医药大学,陕西 咸阳 712046;2.安康市中医院,陕西 安康 725000)
·基础研究·
子洲黄芩中黄酮成分的含量测定及指纹图谱研究△
党珍1,张艳萍2,王西芳1*
(1.陕西中医药大学,陕西 咸阳 712046;2.安康市中医院,陕西 安康 725000)
目的:比较分析陕西子洲与其他产区黄芩中黄酮成分的含量并建立其HPLC指纹图谱,为子洲黄芩的质量评价及道地药材品牌建设提供资料。方法:采用HPLC测定样本中不同产区的黄芩所含黄芩苷、黄芩素和汉黄芩素3个主要黄酮成分的含量。色谱条件:Eclipse-YDB-C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-0.2%磷酸水溶液系统,梯度洗脱;体积流量为1.0 mL·min-1;检测波长为277 nm;柱温为30 ℃。结果:子洲黄芩中黄芩苷的平均质量分数为19.3%,明显高于样本包含的其他产地的黄芩;以黄芩苷峰为参照物峰,确定11个共有峰,建立了子洲黄芩HPLC指纹图谱共有模式方法。结论:陕西子洲黄芩有效成分含量高,品质优;建立的HPLC指纹图谱可以作为分析和控制子洲黄芩质量的基础资料。子洲作为黄芩道地药材产区发展潜力巨大。
子洲黄芩;HPLC指纹图谱;黄芩苷;品质质量
黄芩为唇形科植物黄芩ScutellariabaicalensisGeorgi的干燥根,具有清热燥湿、泻火解毒、止血、安胎的功效[1-2]。研究显示,黄芩苷、黄芩素和汉黄芩素等黄酮类化合物为黄芩的主要有效成分[3-6],具有解热抗炎、抗肿瘤、解毒、保肝及调节免疫等药理作用[7-9]。黄芩为我国传统常用中药,主产于陕西、甘肃、山西、河北、山东、河南等地;陕西子洲县位于陕西北部黄土高原丘陵沟壑区的腹地,是古代陕西黄芩的道地产区之一[2],子洲黄芩有40余年的栽培历史,药材以其条长、质实、色黄的优良性状享誉省内外,现已成为该县中药材产业的主要经济支柱。有关子洲黄芩品质质量分析与研究,目前尚未见有报道,本文以黄芩中黄酮类为质量指标性成分,比较分析子洲与其他不同产区黄芩中黄酮成分的含量,建立HPLC指纹图谱,为子洲黄芩的品质质量评价及道地药材品牌建设提供基础资料。
1 仪器与试药
1.1 仪器
Agilent 1260系列高效液相色谱仪及其工作站;GB204型十万分之一电子天平(梅特勒电子天平);KQ-200KDE型超声波清洗机(昆山市超声仪器有限公司);优普系列超纯水机UPT-Ⅱ(成都超纯水科技有限公司)。
1.2 试药
黄芩素对照品(批号:111595-201306)、黄芩苷对照品(批号:110715-201117)和汉黄芩素对照品(批号:111514-200403),均购自中国食品药品检定研究院。
1.3 黄芩药材
收集黄芩样品24批,经陕西中医药大学药学院生药教研室王西芳教授鉴定,均符合《中华人民共和国药典》2015版黄芩药材标准,样品来源的详细情况见表1。甲醇、乙醇、乙腈、甲酸、磷酸均为色谱纯,水为超纯水。其他试剂均为分析纯。
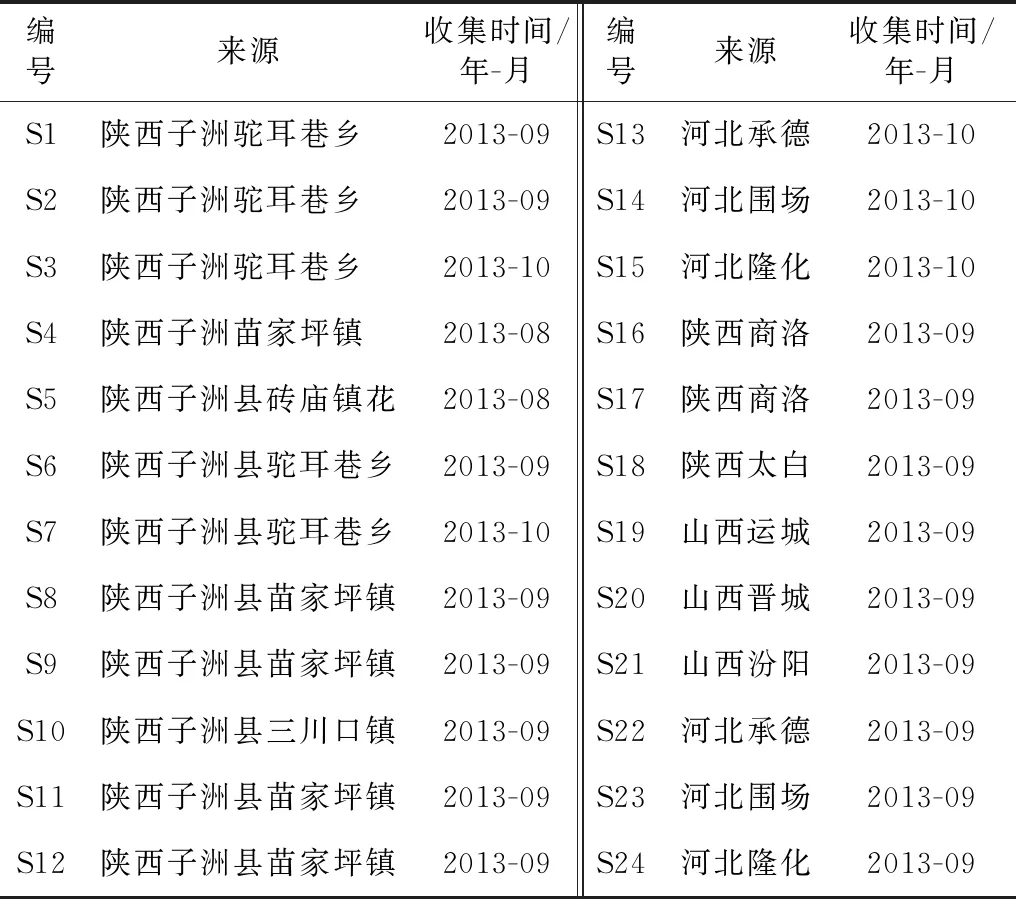
表1 黄芩样品来源
2 方法与结果
2.1 色谱条件
Eclipse-YDB-C18柱(250 mm×4.6 mm,5m);流动相为甲醇(A)-0.2%磷酸(B),梯度洗脱;程序:0~10 min,30%~40%A;10~20 min,40%~50%A;20~30min,50%~50%A;30~40 min,50%~60%A;40~50 min,60%~70%A;50~60 min,70%~30%A;检测波长:277 nm;体积流量:1.0 mL·min-1;柱温:30 ℃;进样量:10L。
2.2 对照品溶液的制备
分别取黄芩苷、黄芩素、汉黄芩素对照品6.20、3.00、3.00 mg,精密称定,加入10 mL容量瓶内,甲醇超声使溶解,并用甲醇稀释至刻度,然后分别移取定容好的溶液5、2、1 mL,置50 mL量瓶中,加甲醇稀释至刻度,制成含黄芩苷、黄芩素、汉黄芩素分别为 62、12、6 μg·mL-1的溶液,作为对照品溶液。HPLC图见图1。
2.3 供试品溶液制备
取0.2 g黄芩药材粉末,精密称定,置 50 mL量瓶中,加70%乙醇水溶液40 mL超声提取40 min,放置至室温,加甲醇至刻度,摇匀,滤过,精密量取2 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,用0.45m微孔滤膜过滤后作为供试品溶液。HPLC图见图1。
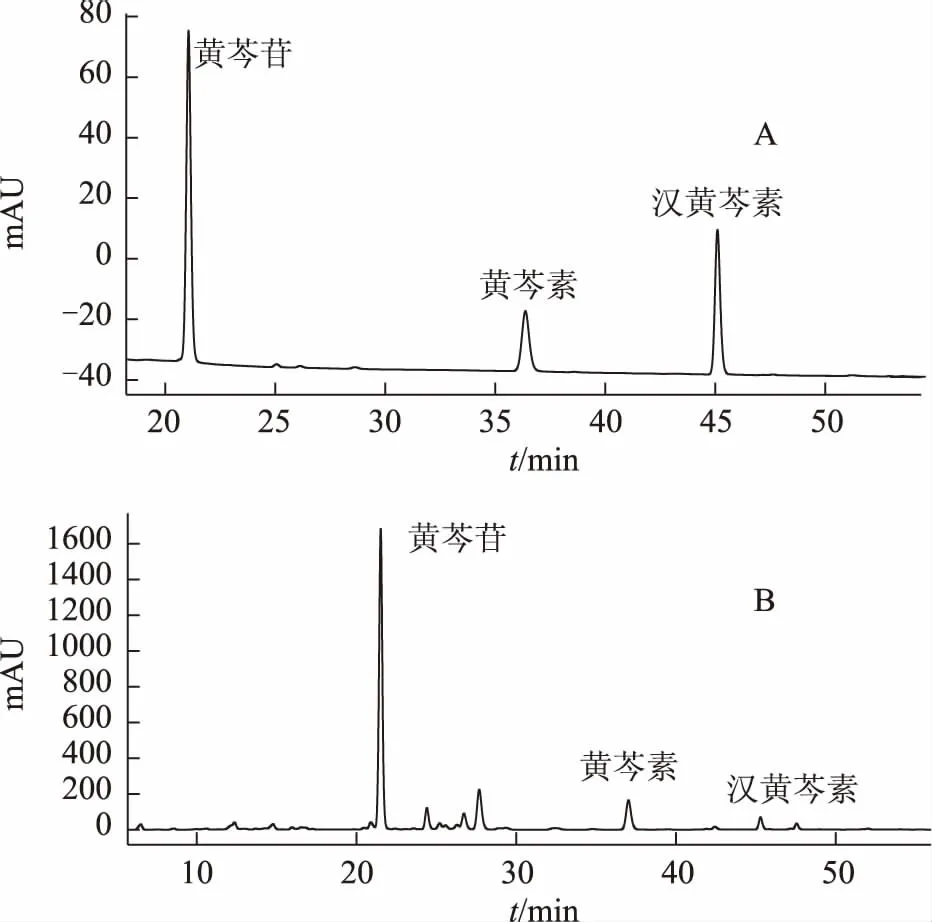
注:A.混合对照品;B.供试品。图 1 混合对照溶液和黄芩供试溶液HPLC图
2.4 方法学考察
2.4.1 线性关系考察 取上述黄芩苷、黄芩素、汉黄芩素混合对照品溶液,按2.1色谱条件分别进样3、5、10、15、20、25、30L测定峰面积值。以进样量为横坐标(X),峰面积值为纵坐标(Y),得黄芩苷、黄芩素、汉黄芩素回归方程,分别为:Y=2 614.3X+14.318,r=1;Y=4 031.4X+4.746 8,r=1;Y=4 980.7X+4.927 9,r=0.999 8;黄芩苷、黄芩素、汉黄芩素线性范围分别为:0.186~1.860g、0.036~0.360g、0.0186~0.186g。
2.4.3 稳定性试验 取S1号供试品溶液,按2.1方法分别在0、2、4、6、8、12、24 h测定黄芩苷、黄芩素、汉黄芩素的峰面积。在24 h内其RSD 值分别为1.5%、1.9%、1.8%,说明样品溶液在24 h 内稳定。
2.4.4 重复性试验 取S1号样品粉末6份,根据2.3方法制备供试品溶液,按2.1项下方法,测定黄芩苷、黄芩素和汉黄芩素的峰面积,RSD值分别为1.5%、1.5%、2.0%(n=6),表明方法重复性良好。
2.4.5 加样回收率试验 取已知含量的S1号黄芩样品6份,每份0.1 g,精密称定,按2.3方法制备溶液,精密吸取2 mL于10 mL量瓶中,分别精密加入对照品溶液(黄芩苷730 g·mL-1、黄芩素48 g·mL-1、汉黄芩素12 g·mL-1)各1 mL,用甲醇定容。按2.1方法测定,计算加样回收率,结果见表2。
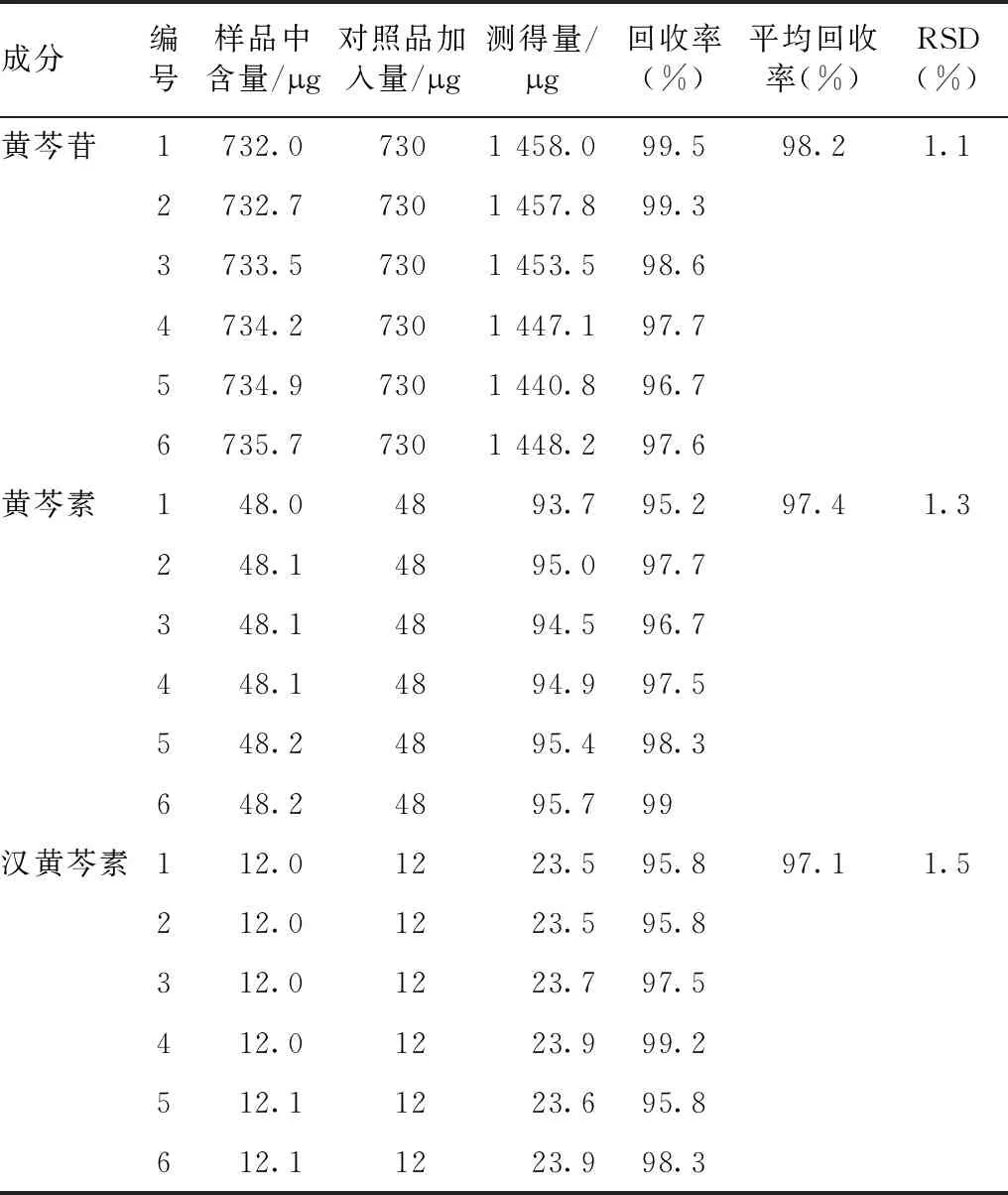
表2 黄芩中黄芩苷、黄芩素、汉黄芩素加样回收试验结果(n=6)
2.4.6 样品含量测定 每个批次的药材样品按2.3方法平行制备3份,按2.1方法测定黄芩苷、黄芩素、汉黄芩素的峰面积,用外标法以峰面积计算样品中3个成分的含量,结果见表3。
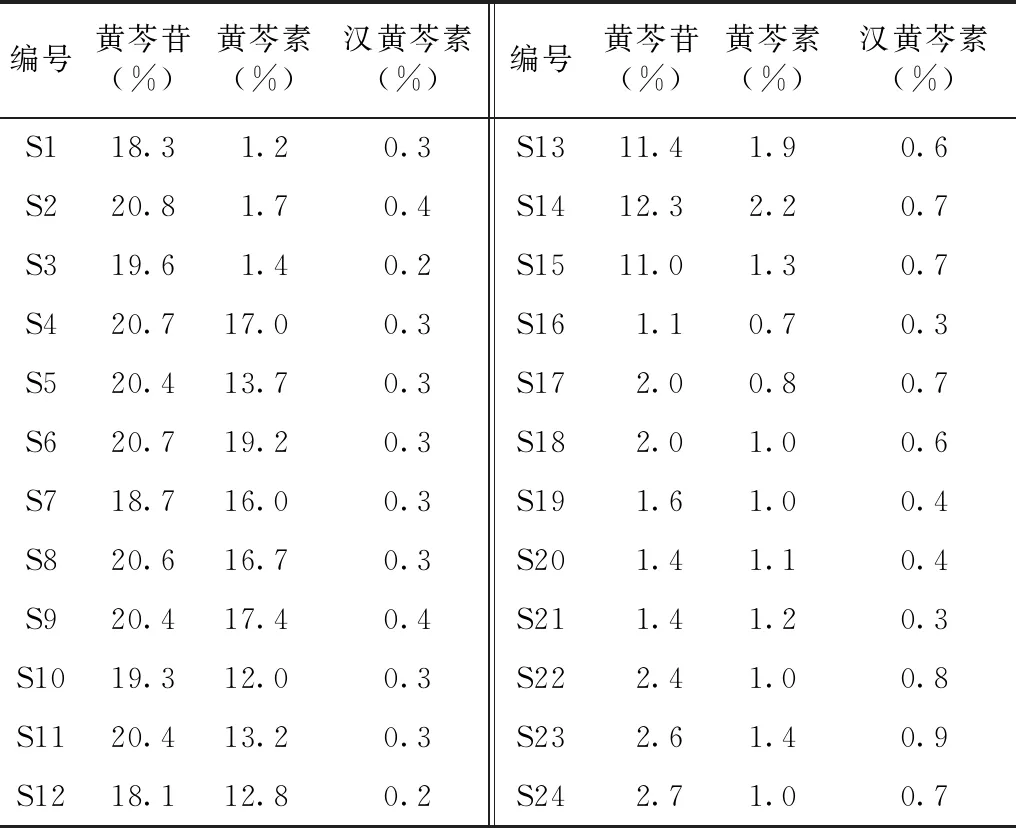
表3 黄芩中3种黄酮类成分的含量测定结果
2.5 指纹图谱研究
2.5.1方法学考察
2.5.1.1 内参照峰的选择 按2.1色谱条件,分别注入黄芩苷、黄芩素、汉黄芩素对照品10L,测定,结果发现黄芩苷出峰时间适中、峰明显高,而且分离度比较好,故选择黄芩苷作为内参照峰。
2.5.1.2 精密度试验 按2.4.2所记录的色谱图上黄芩苷的色谱峰为内参照峰,比较各主要色谱峰的相对保留时间和峰面积在5%以上峰的相对峰面积,RSD分别在0.2%~1.45%和1.02%~1.80%,符合指纹图谱研究技术的要求。
2.5.1.3 重复性试验 按2.4.3所记录的色谱图上黄芩苷的色谱峰为内参照峰,比较各主要色谱峰的相对保留时间和峰面积在5%以上峰的相对峰面积,RSD值分别在0.1%~0.9%和0.75%~1.78%,该方法重复性良好,符合指纹图谱研究技术的要求。
2.5.1.4稳定性试验 按2.4.4所记录的色谱图上黄芩苷的色谱峰为内参照峰,比较各主要色谱峰的相对保留时间和峰面积在5%以上峰的相对峰面积,RSD值分别在0.1%~1.0%和0.83%~1.91%,表明该方法稳定性良好,符合指纹图谱研究技术的要求。
2.6 子洲黄芩指纹图谱的建立
将子洲的10个批次的黄芩样品,按2.3方法进行制备,按2.1条件测定并记录60 min色谱图,按照指纹图谱研究技术的要求,建立子洲产黄芩的指纹图谱。将黄芩苷的峰作为内参比峰,对各色谱峰的相对保留时间进行分析,从共有峰中选取稳定性好、峰面积大、特征明显的色谱峰作为特征峰。选取了其中11个色谱峰为特征峰,并计算各个共有峰相当于内参比峰的峰面积比值,通过和对照品的保留时间进行比较,并结合文献资料,指认了其中的6个峰,其中3为野黄芩苷、4为黄芩苷、7为汉黄芩苷、8为黄芩素、10为汉黄芩素、11为千层纸素,结果见图2、表4、表5,各样品的非共有峰面积与总峰面积的比值均小于10%,符合指纹图谱研究技术的要求。
2.7 相似度分析
运用中药色谱指纹图谱相似度评价系统2004A版,进行相似度评价[10-11]。将实验数据导入该软件,
选定参照谱图,设定成中位数匹配模式,进行多点校正后自动匹配,然后软件会自动生成对照谱峰R,见图3,相似度计算结果见表6,相似度在0.994以上,相似度较高。
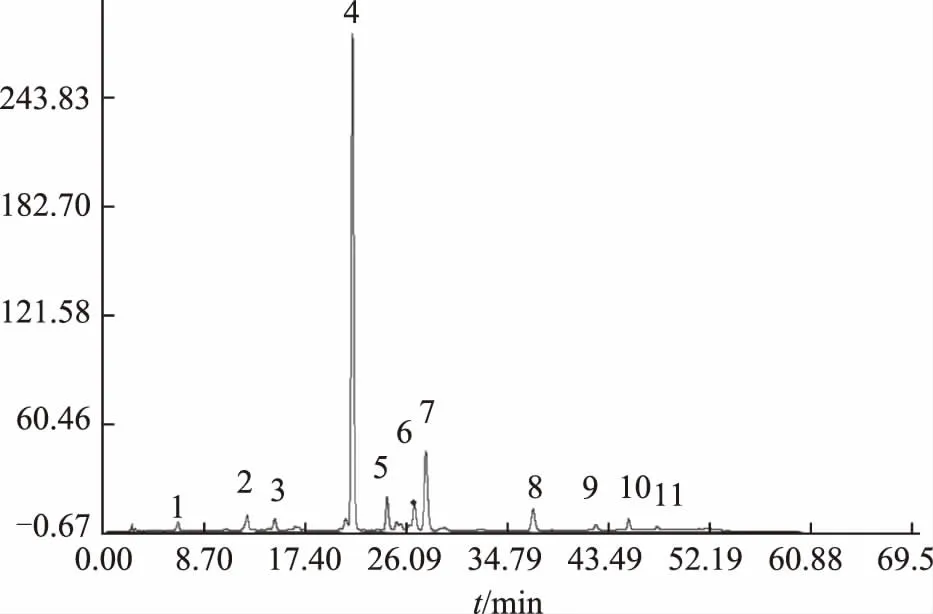
图2 子洲黄芩指纹图谱共有峰
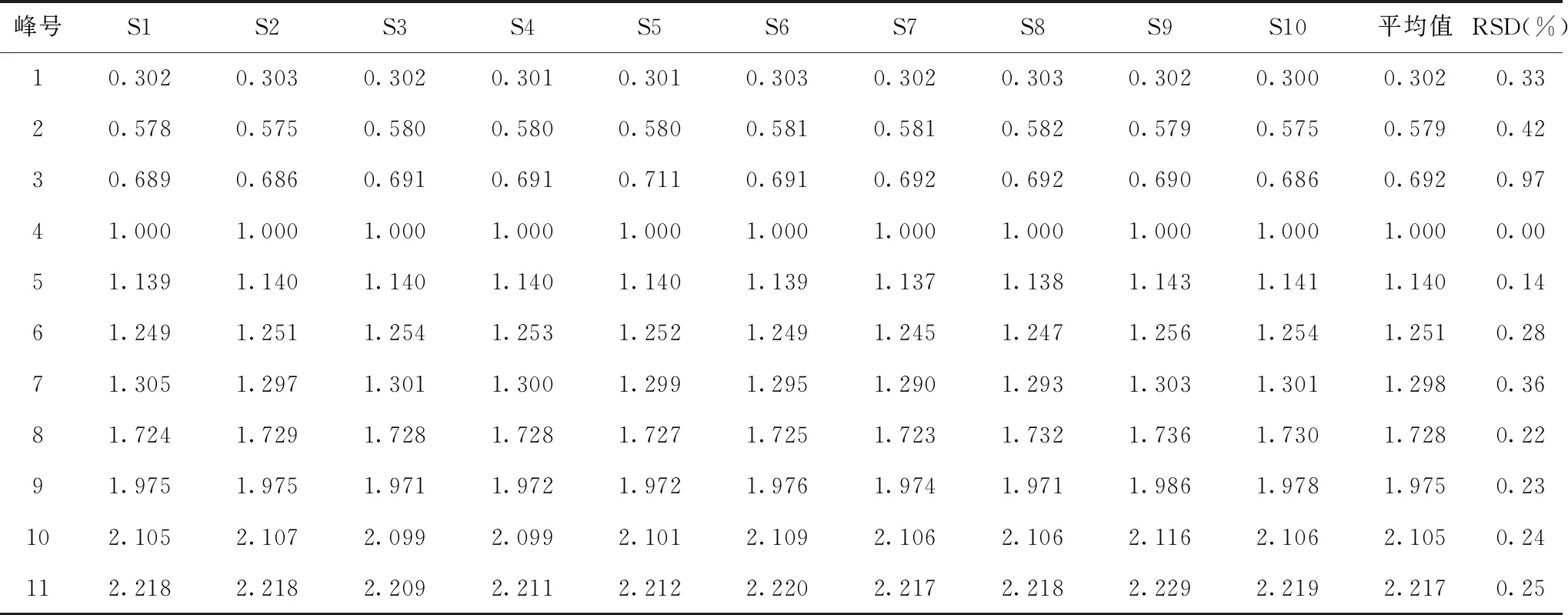
峰号S1S2S3S4S5S6S7S8S9S10平均值RSD(%)10.3020.3030.3020.3010.3010.3030.3020.3030.3020.3000.3020.3320.5780.5750.5800.5800.5800.5810.5810.5820.5790.5750.5790.4230.6890.6860.6910.6910.7110.6910.6920.6920.6900.6860.6920.9741.0001.0001.0001.0001.0001.0001.0001.0001.0001.0001.0000.0051.1391.1401.1401.1401.1401.1391.1371.1381.1431.1411.1400.1461.2491.2511.2541.2531.2521.2491.2451.2471.2561.2541.2510.2871.3051.2971.3011.3001.2991.2951.2901.2931.3031.3011.2980.3681.7241.7291.7281.7281.7271.7251.7231.7321.7361.7301.7280.2291.9751.9751.9711.9721.9721.9761.9741.9711.9861.9781.9750.23102.1052.1072.0992.0992.1012.1092.1062.1062.1162.1062.1050.24112.2182.2182.2092.2112.2122.2202.2172.2182.2292.2192.2170.25
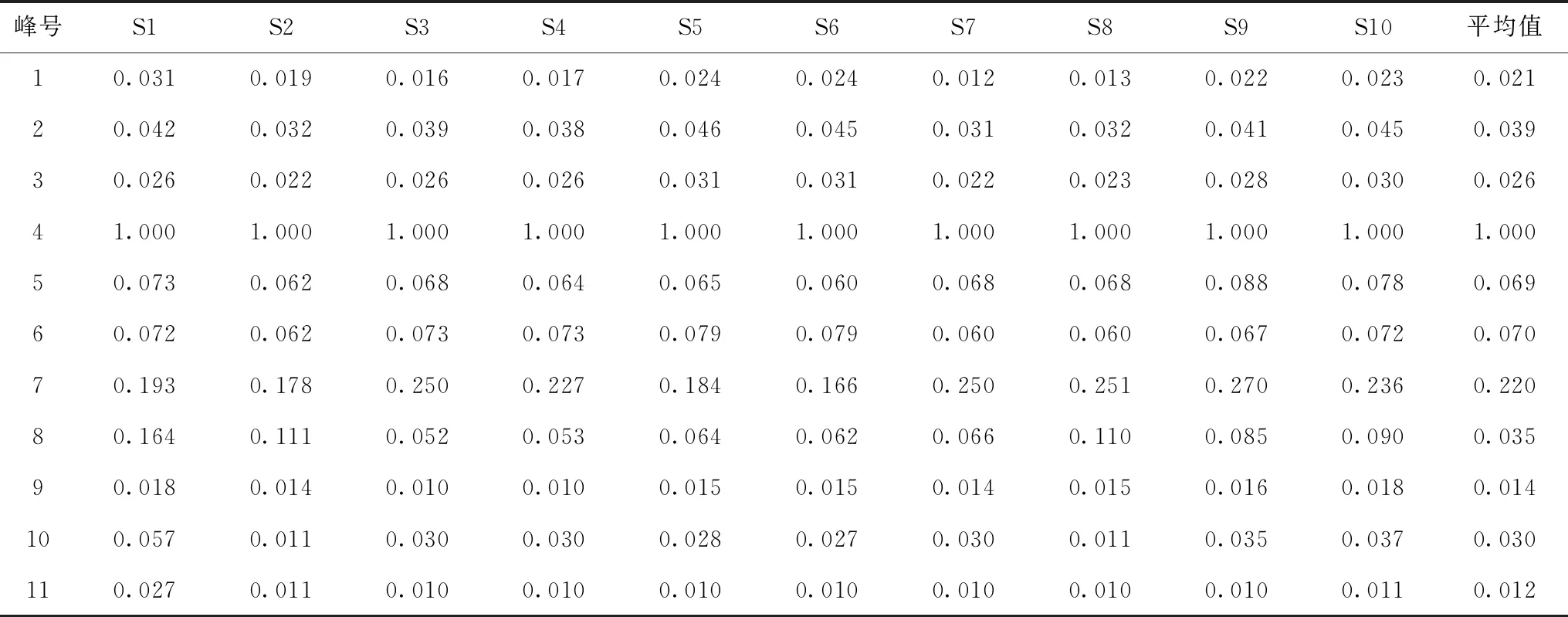
表5 子洲黄芩指纹图谱共有峰相对峰面积
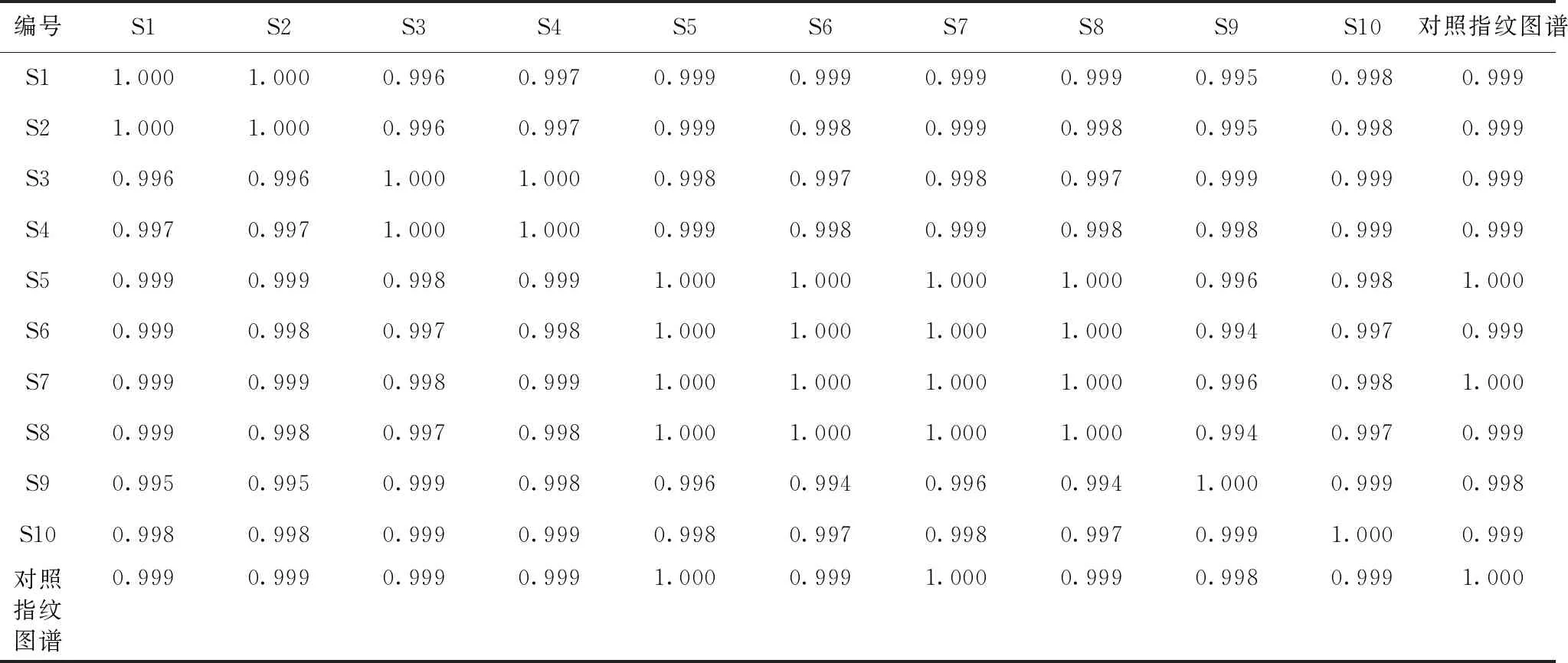
表6 黄芩药材相似度计算结果
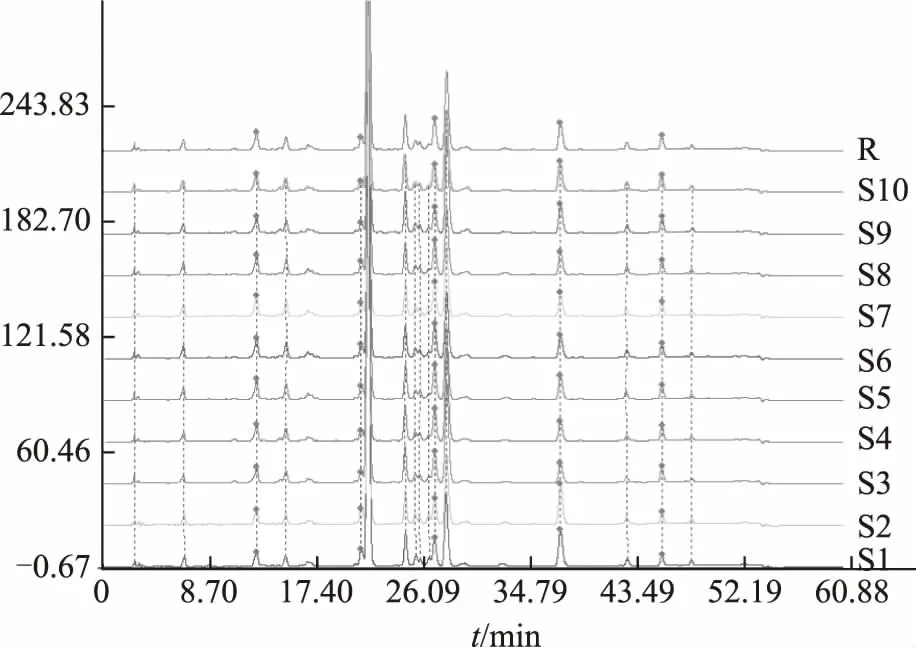
注:R.对照指纹图谱。图3 10批子洲产黄芩药材的指纹图谱
3 结论与讨论
子洲黄芩的黄芩苷含量范围为:18.1%~20.8%,黄芩苷含量明显较高(《中华人民共和国药典》规定黄芩苷含量不得低于8%);其中黄芩素、汉黄芩素的含量范围为:0.7%~1.7%,0.2%~0.4%,与其他产地样品比较没有明显差异。以黄芩苷含量为评价指标,子洲产黄芩的质量明显优于其他产地,子洲产黄芩具有很大的发展潜力。但单一成分并不能全面评价黄芩的品质,HPLC指纹图谱比较全面地反映了药材所含化学成分的数与量关系,可以更加有效地评价药材的内在质量。用子洲产10个批次的黄芩药材的HPLC色谱图建立了子洲产黄芩的指纹图谱共有模式,分析各指纹图谱发现存在一定差异,但均有相同的特征峰,而且分离效果都比较好,保留时间也相对稳定,该方法建立的指纹图谱可用于子洲产黄芩的质量评价,对子洲黄芩的品牌建设与产业发展有一定的指导意义。
[1] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2015:301-302.
[2] 李欣,黄璐琦,邵爱娟,等.黄芩种质资源的研究概况[J].世界科学技术—中医药现代化,2003,5(6):54-58.
[3] 金敏.黄芩中黄酮类化学成分研究进展[J].中国民族医药杂志,2009,9(9):55-56.
[4] 杨立新,刘岱,冯学峰,等.高效液相色谱法测定不同产地黄芩中黄酮化合物的含量[J].中国中药杂志,2008,27(3):166.
[5] 田建红.不同产地黄芩中的有效成份含量分析[J].海峡药学,2009,21(3):57-59.
[6] 常小平,王影.不同产地黄芩中主要有效成分含量比较[J].河南中医,2010,30(12):1176.
[7] 张瑜,武斌,许建卫.黄芩药理作用的研究进展[J].医学综述,2013,19(6):1091-1093.
[8] 郑勇凤,王佳婧,傅超美,等.黄芩的化学成分与药理作用研究进展[J].中成药,2016,38(1):141-147.
[9] 辛文妤,宋俊科,何国荣,等.黄芩素和黄芩苷的药理作用及机制研究进展[J].中国新药杂志,2013,22(6):647-653.
[10] 肖蓉, 张志斐, 袁志芳,等. 河北道地药材黄芩指纹图谱的研究[J]. 药物分析杂志, 2007,27(7):1018-1023.
[11] 薛黎明,秦雪梅,张丽增.不同产地黄芩药材的黄芩苷含量测定及指纹图谱研究[J].中成药,2008,30(1):11.
DeterminationofFlavonoidsandFingerprintsofScutellariabaicalensisfromZizhou
DANGZhen1,ZHANGYanping2,WANGXifang1*
(1.ShaanxiUniversityofChinesemedicine,Xianyang712046,China;2.AnkangHospitalofTraditionalChineseMedicine,Ankang725000,China)
Objective:To compare the contents of flavonoids inScutellariabaicalensisfrom Zizhou and other areas,and establish the HPLC fingerprint of ZizhouS.baicalensisaimed at providing references for the quality evaluation and pharmaceutical raw materials.Methods:Baicalin,baicalein and wogonin were determined by HPLC,and Eclipse-YDB-C18column(250 mm×4.6 mm,5 μm)were used with methanol(B)and 0.2% phosphoric acid solution(A)in gradient elution mode at a flow rate of 1.0 mL·min-1.The detection wavelength was set at 277 nm and the column was 30 ℃.Results:The average content of baicalin in ZizhouS.baicalensiwas 19.3%,significantly higher than those of the other samples.11 common peaks were identified by using the baicalin peak as the reference,established the HPLC fingerprints of ZizhouS.baicalensitotal pattern method was establsied.Conclusion:ZizhouS.baicalensihas a high content of effective ingredients,good quality.HPLC fingerprint can be applied for analyzing and controlling the quality of ZizhouS.baicalensi.As the typicalScutellariaproducing region,Zizhou has a great potential for further development.
Scutellariabaicalensisfrom Zizhou;HPLC fingerprint;biaealin;quality
陕西省教育厅基金项目(Z54)
] 王西芳,教授,硕士生导师,研究方向:中药资源的开发利用;E-mail:wangxifang@vip.sina.com
10.13313/j.issn.1673-4890.2017.2.008
2016-07-28)
*[
