土贝母乙酸乙酯部位化学成分研究
2017-06-28向梅先
向梅先,吴 丽,范 亚,尹 娴,张 浪
(中南民族大学 药学院,武汉430074)
土贝母乙酸乙酯部位化学成分研究
向梅先,吴 丽,范 亚,尹 娴,张 浪
(中南民族大学 药学院,武汉430074)
通过现代分离技术并经波普分析研究,分离得到了土贝母乙酸乙酯部位8个化合物,并鉴定为:7-羟基-6-甲氧基香豆素(1)、表儿茶素(2)、儿茶素(3)、(E)-N-(4-羟基苯乙基)-3-(4-羟基-3-甲氧基苯基)丙烯酰胺(4)、邻苯二甲酸二丁酯(5)、(Z)-3-O-咖啡酰基-4-O-甲基奎宁酸甲酯(6)、绿原酸(7)、3-O-[β-D-吡喃鼠李糖-(1-6)- β-D-吡喃葡萄糖]-5,7,4′-三羟基黄酮(8). 此8个化合物均为首次从该植物中分离得到.
土贝母;乙酸乙酯部位;化学成分
土贝母为葫芦科植物土贝母Bolbstemmapaniculatum(Maxim .)Franquet的干燥块茎,也称藤贝母,以鳞茎入药. 土贝母原载于清代赵氏编纂的《本草纲目拾遗》,在《中药大辞典》和《中华人民共和国药典》中记载:其性味苦、微寒,有清热解毒、消肿散结等功效[1,2], 用于乳痈、瘰疬、乳腺炎等治疗.土贝母主要含有皂苷类、甾醇及其苷类和酯类、生物碱类及其他化学成分.研究表明土贝母分离的多种化学成分具有良好的抗肿瘤和杀精等作用[3],但对于该物质的抗肿瘤机理并不清楚[4].本研究通过对其乙酸乙酯部位抗肿瘤活性筛选,发现乙酸乙酯部位对肝癌细胞具有较好的抑制作用,为进一步了解其作用原理,本文通过正反向硅胶柱、凝胶色谱、高效液相等多种方法,对其乙酸乙酯部位进行结构解析并鉴定,分离鉴定出8个化合物(图1),此8个化合物均是首次从该植物中分离得到.
1 材料和方法
1.1 材料与仪器
土贝母药材采自湖北省恩施州,经中南民族大学药学院鉴定教研室万定荣教授鉴定为葫芦科土贝母属植物土贝母Bolbostemmapaniculatum(Maxim.)Franquet.
AM-400型核磁共振仪(Bruker公司); LCQ-Deca 型质谱仪(Finnigan公司);高效液相色谱仪(戴安3000,美国Dionex公司);色谱柱(5C18-MS-∏型,Agela公司);旋转蒸发仪(RE-52AA,上海亚荣生化仪器厂);超声波清洗仪(KQ-500E,上海嘉鹏科技有限公司);傅立叶红外光谱仪(MEXUS-670,Nicolet公司);ZF-6型三用紫外光谱仪(宁波新芝公司);电子天平(AR2140型,上海奥豪斯公司).
1.2 试剂
石油醚、乙酸乙酯、正丁醇、甲醇(分析纯,天津博迪),95%乙醇为工业试剂,液相甲醇(色谱纯,天地公司).柱层析用硅胶(100~300目),硅胶G高效预制板(青岛海洋化工).
1.3 提取与分离
取土贝母10 kg 淋洗后晒干,粉碎成粗粉. 将藤贝母粗粉置95% 的乙醇中浸泡,室温提取3 次,每次24 h. 将3次提取液过滤后合并,旋转蒸发仪减压浓缩得到土贝母总浸膏2.1 kg,总浸膏用适量的90%甲醇溶液溶解后分别用石油醚、乙酸乙酯、正丁醇萃取,各萃取液减压浓缩得浸膏200、600和900 g. 乙酸乙酯部位用200~300目硅胶柱分离,以氯仿-甲醇梯度洗脱(100∶1,80∶1,50∶1,40∶1,30∶1,20∶1,10∶1,9∶1,8∶2,7∶3,6∶4,4∶6,0∶1),收集各洗脱液,TLC检测合并相同流分,再经凝胶柱、正反硅胶柱色谱、葡聚糖凝胶柱、高效液相色谱法(HPLC)等反复分离纯化,得单体化合物.
2 结构鉴定
化合物1 白色针状结晶. C10H8O4,1H-NMR(400 MHz,CDCl3),δppm: 6.30(1H,d,J=9.2 Hz,H-3),7.63(1H,d,J=9.2 Hz,H-4),6.94(1H,s,H-5),3.98(3H,s,-OCH3,H-6),8.50(1H,s,-OH,H-7),6.87(1H,s,H-8);13C-NMR(100 MHz,CDCl3)δppm: 161.42(C-2),113.40(C-3),143.30(C-4),111.49(C-5),144.01(C-6),150.26(C-7),107.48(C-8),103.19(C-9),150.26(C-10),56.41(7-OCH3).以上数据与文献[5]报道基本一致,故鉴定化合物1为7-羟基-6-甲氧基香豆素 .
化合物2 白色粉末. C15H14O6,1H-NMR(400 MHz,CD3OD)δppm: 4.83(1H,d,H-2),4.19(1H,m,H-3),2.89(1H,dd,J=16.8,4.8 Hz,H-4),2.75(1H,d,J=16.2 Hz,H-5),5.92(1H,s,H-6),5.95(1H,s,H-8),6.99(1H,s,H-1′),6.78(1H,d,J=8.0 Hz,H-5′),6.83(1H,d,J=8.0 Hz,H-6′).13C-NMR(100 MHz,CD3OD)δppm: 78.50(C-2),66.10(C-3),27.83(C-4),156.29(C-5),95.08(C-6),155.97(C-7),94.55(C-8),98.73(C-4a),156.59(C-8a),130.91(C-1′),114.54(C-2′),144.39(C-3′),144.56(C-4′),113.97(C-5′),118.04(C-6′). 以上数据与文献[6]报道基本一致,故鉴定化合物2为表儿茶素.
化合物3 白色粉末. C15H14O6,1H-NMR( 400 MHz,CD3OD )δppm: 4.73(1H,s,H-2),4.01(1H,d,H-3),2.67(2H,dd,J=16.8,4.8 Hz,H-4),5.89(1H,s,H-6),5.72(1H,s,H-8),6.89(1H,s,H-2′),6.69(1H,d,J=8.0 Hz,H -5′),6.66(1H,d,J=8.0 Hz,H-6′).13C-NMR( 100 MHz,CD3OD )δppm: 82.7(C-2),68.5(C-3),28.4(C-4),100.5(C-4a),157.3(C-5),96.3(C-6),156.9(C-7),94.7(C-8),157.5(C-8a),131.7(C-1′),115.1(C-2′),145.3(C-3′),145.5(C-4′),115.5(C-5′),120.2(C-6′). 以上数据与文献[6]报道基本一致,故鉴定化合物3为儿茶素.
化合物4 黄褐色粉末. C18H19O4N,1H-NMR(400 MHz,DMSO-d6)δppm: 7.12(1H,s,J=1.6 Hz,H-2),3.80(3H,s,-OCH3-3),6.79(1H,d,J=8.4 Hz,5-H),6.99(1H,d,J=8.4,1.6 Hz,H-6),7.32(1H,d,J=15.6 Hz,H-7),6.44(1H,d,J=15.6 Hz,H-8),3.33(2H,m,H-8′),2.65(2H,m,H- 7′),7.01(2H,d,J=8.4 Hz,H-2′,6′),6.68(2H,d,J=8.4 Hz,H-3′-5′),8.39(1H,s,H-4′).13C-NMR(100 MHz,DMSO-d6)δppm: 127.06(C-1),116.09(C-2),148.88(C-3),148.86(C-4),119.46(C-5),121.96(C-6),139.33(C-7),111.17(C-8),165.97(C-9),41.11(C-8′),34.87(C-7′),130.17(C-1′),129.92(C-2′,6′),115.56(C-3′-5′),156.27(C-4′),55.96(-OCH3-3). 以上数据与文献[7]报道基本一致,故鉴定化合物4为(E)-N-(4-羟基苯乙基)-3-(4-羟基-3-甲氧基苯基)丙烯酰胺.
化合物5 墨绿色油状. C16H22O4,1H-NMR(400 MHz,CDCl3)δppm: 4.32(4H,t,H-1-1′),1.73(4H,m,H-2-2′),1.47(4H,m,H-3-3′),1.17(6H,td,H-4-4′),7.56(2H,m,H -3″-6″),7.76(2H,m,H-4″-5″).13C-NMR(100 MHz,CDCl3)δppm: 65.53(C-1-1′),30.58(C-2-2′),19.12(C-3-3′),13.66(C-4-4′),130.89(C- 1″-2″),128.84(C-3″-6″),132.40(C-4″-5″),167.67(C-7″,8″). 以上数据与文献[8]报道基本一致,故鉴定化合物5为邻苯二甲酸二丁酯.
化合物6 灰绿色粉末. C17H20O9,1H-NMR(400 MHz,CD3OD)δppm: 2.18(2H,m,H-2′),5.26(1H,m,J=3.6 Hz,H-3′),3.67(1H,m,H-4′),4.07(1H,m,H-5′),2.01(2H,m,H-6′),7.40(1H,s,J=1.6 Hz,H-2),6.72(1H,d,J=8.4 Hz,H-5),7.04(1H,dd,J=1.6,8.0 Hz,H-6),6.80(1H,d,J=12.8 Hz,H-7),5.71(1H,d,J=12.8 Hz,H-8),3.68(3H,s,-OCH3-7′).13C-NMR(100 MHz,CD3OD)δppm: 76.28(C-1′),71.87(C-2′),72.14(C-3′),38.12(C-4′),70.54(C-5′),38.12(C-6′),175.78(C-7′),128.48(C-1),118.61(C-2),145.38(C-3),148.47(C-4),115.66(C-5),125.17(C-6),145.75(C-7),116.54(C-8),167.42(C-9),53.33(-OCH3- 7′).以上数据与文献[9]报道基本一致,故鉴定化合物6为(Z)-3-O-咖啡酰基-4-O-甲基奎宁酸甲酯.
化合物7 灰绿色粉末. C16H18O9,1H-NMR(600 MHz,CD3OD)δppm: 6.94(1H,d,J=1.8 Hz,H-2),6.68(1H,d,J=7.8 Hz,H-5),6.85(1H,dd,J=1.8,7.8 Hz,H-6),7.43(1H,d,J=16.2 Hz,H-7),6.12(1H,d,J=16.2 Hz,H-8),5.16(1H,m,J=4.8 Hz,H-3′),2.09(2H,m,H-2′),2.09(1H,m,H-6′),1.92(1H,m,H-6′),3.67(1H,m,H-4′),4.15(2H,m,H-5′).13C-NMR(150 MHz,CD3OD)δppm: 127.58(C-1),115.06(C-2),149.71(C-3),146.87(C-4),116.58(C-5),122.98(C-6),147.21(C-7),114.98(C-8),168.25(C-9),75.16(C-1′),37.65(C-2′),72.16(C-3′),72.31(C-4′),70.32(C-5′),37.65(C-6′),175.35(C -7′). 以上数据与文献[10]报道基本一致,故鉴定化合物7为绿原酸.
化合物8 黄绿色粉末. C27H29O15,1H-NMR(600 MHz,CD3OD)δppm: 8.18(1H,d,J=8.7 Hz,H-2′,6′),6.58(1H,d,J=8.6 Hz,H-3′,5′),6.58(1H,brs,H-8),6.19(1H,brs,H-6),5.13(1H,d,J=7.8 Hz,H-1″of Gal),4.62(1H,s,H-1‴of Rha),1.28(3H,d,J=6.2 Hz,H-6‴of Rha).13C-NMR(150 MHz,CD3OD)δppm: 179.4(C=O),166.8(C-7),162.8(C-5),161.7(C-4′),158.6(C-4),159.3(C-2),135.6(C-3),132.4(C-2′,6′),122.5(C-1′),116.3(C-3′,5′),105.7(C-1″ of Gal),105.4(C-10),101.7(C-1‴ of Rha),100.3(C-6),95.0(C-8),75.5(C-3″of Gal),75.2(C-5″of Gal),73.7(C-4‴of Rha),73.1(C-2″of Gal),72.4(C-3‴of Rha),72.2(C-2‴of Rha),70.1(C-5‴of Rha),69.8(C-4″of Gal),67.4(C-6″of Gal),18.1(C-6‴of Rha). 以上数据与参考文献[11]一致 ,故鉴定化合物8为3-O-[β-D-吡喃鼠李糖-(1-6)-β-D-吡喃半乳糖]-5,7,4′-三羟基黄酮.
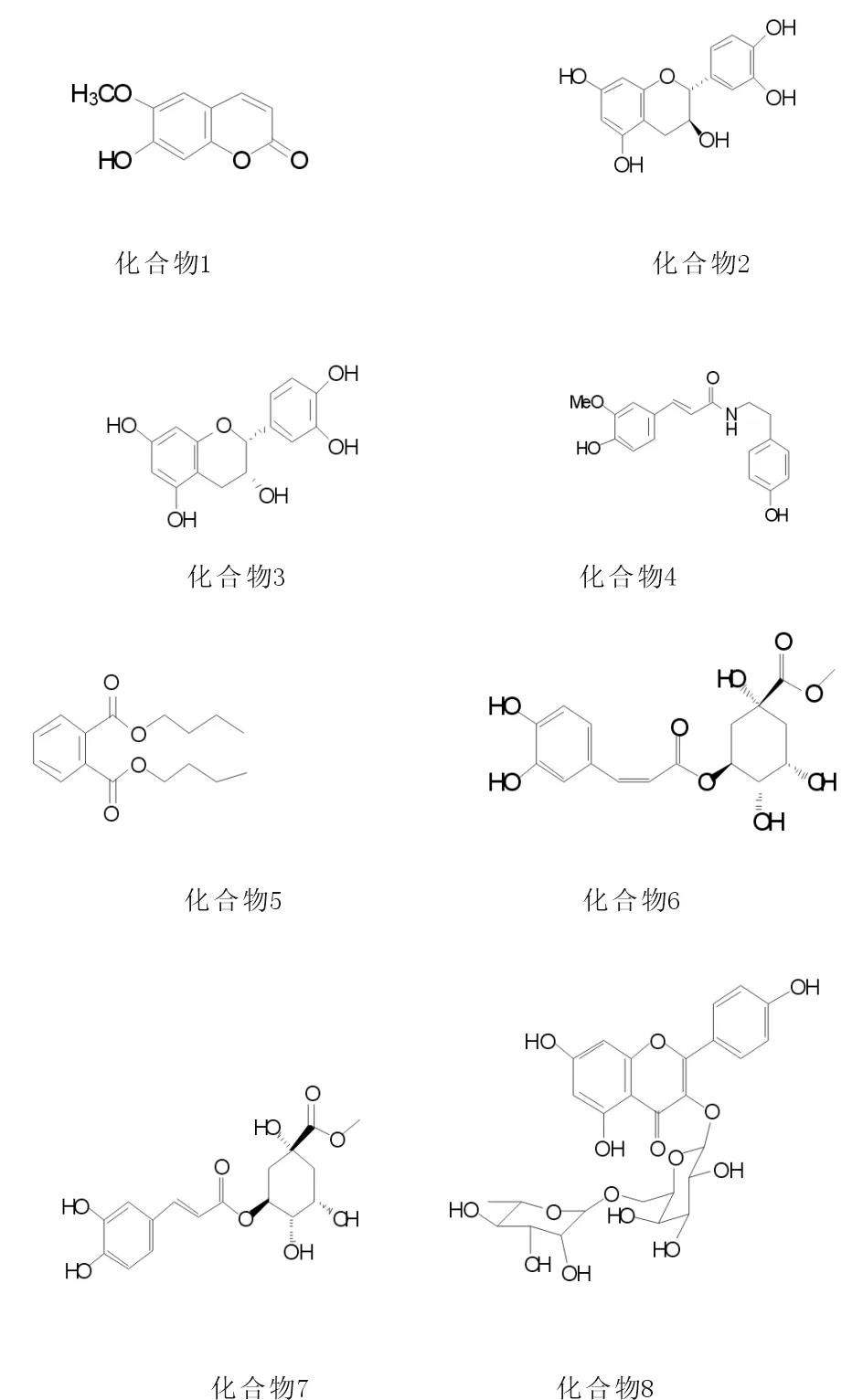
图1 化合物1~8的结构Fig.1 Structure of the compound 1-8
3 结语
通过对土贝母乙酸乙酯部位的分离,结构解析,得到了8个化合物:7-羟基-6-甲氧基香豆素、表儿茶素、儿茶素、丙烯酰胺、邻苯二甲酸二丁酯、奎宁酸甲酯、绿原酸、三羟基黄酮苷,此8个化合物均为初次从该植物中提取得到,为进一步研究该药奠定了一定的基础.
[1] 陈启亮,唐东昕,龙奉玺. 中医药对肝癌治疗的研究进展[J]. 贵阳中医学院学报,2016,38(2):99-100.
[2] 尹 艳. 土贝母苷甲诱导人肝癌HepG2细胞凋亡机制的研究[D]. 武汉:武汉大学,2011.
[3] 孙毅毅,李彤晖,汤臣康,等. 土贝母抗癌有效成分肝靶向给药系统的研究[J]. 中国中药杂志,2005,30(11):817-821.
[4] 刘 凯. 中药在癌症治疗中的应用[J]. 内蒙古中医药,2009,28(2):106.
[5] 向梅先,胡亚京,闫云君.血三七乙酸乙酯部位化学成分研究[J].中药材,2012,35(10): 1610-1614.
[6] Wang K J,Zhang Y J,Yang C R,et al. Antioxidant phenolic compounds from rhizomes ofPolygonumpaleaceum[J]. Journal of Ethnopharmacology,2005,96: 483-487.
[7] Foo L Y,Lu Y,Mcnabb W C,et al. Proanthocyanidins fromLotuspedunculatus[J]. Phytochemistry,1997,45(8): 1689-1696.
[8] 张丽玲,肖英龙,李向高,等. 中国红参麦芽酚的分离与鉴定[J]. 中成药,1989,11(6):32-33.
[9] Cardoso C L,Bolzani Vda S,Silva D H,et al. The absolute configuration of 1-(3′,4′-dihydroxycinnamoyl)cyclopentane-2,3-diol from the amazonian treeChimarrhisturbinate[J]. Journal of Natural Products,2006,69(7):1046-1050.
[10] 翁裕馨,陈湘宏,刘占厚,等. 细毡毛忍冬叶绿原酸类化学成分研究[J]. 安徽农业科学,2011,39(27):16566-16568.
[11] 易 衍,巫 鑫,王 英,等. 霸王花黄酮类成分研究[J]. 中药材,2011,34(5):712-716.
Study on Chemical Compound of Ethyl Acetate Fraction fromBolbostemmapaniculatum(Maxim.)Franquet
XiangMeiXian,WuLi,FanYa,YinXian,ZhangLang
(College of Pharmacy,South-Central University for Nationalities,Wuhan 430074,China)
The modern extraction techniques and spectral analysis were used to isolate and analyze the chemical compositions of ethyl acetate fraction fromBolbostemmapaniculatum(Maxim.)Franquet . Eight compounds were obtained and identified as : 7-6-hydroxy-6-methoxy coumarin (1),epicatechin (2),catechin (3),(E)-N-hydroxy phenyl ethyl -3-4-hydroxy-3-methoxy phenyl Acrylamide (4),Di Butyl Phthalate (5),(Z)-3-O-Coffee acyl-4-O-Methyl quinic acid methyl ester (6),chlorogenic acid (7),3-O-[beta-D-pyran rhamnose-(1-6)-beta-D-Pyran glucose]-5,7,4′-three hydroxyl flavone (8) .All of the eight compounds were isolated from this plant for the first time.
Bolbostemmapaniculatum(Maxim.)Franquet ; ethyl acetate fraction; chemical constituents
2017-02-20
向梅先(1975-),女,副教授,博士,研究方向:中药、民族药活性及制剂研究,E-mail:xiangmeixian99@163.com
湖北省自然科学基金科技支撑项目(2015BCA268);武汉市科技计划项目(创新团队,2016070204020162)
O629;R931.7
A
1672-4321(2017)02-0056-04
