基于化学共沉淀的两步法合成LiMnPO4正极材料研究进展
2017-05-10秦显忠杨改高剑蔡飞鹏王波蒋波谭春晖
秦显忠,杨改,高剑,蔡飞鹏,王波,蒋波,谭春晖
(山东省科学院能源研究所,山东省生物质气化技术重点实验室,山东 济南 250014)
【新材料】
基于化学共沉淀的两步法合成LiMnPO4正极材料研究进展
秦显忠,杨改*,高剑,蔡飞鹏,王波,蒋波,谭春晖
(山东省科学院能源研究所,山东省生物质气化技术重点实验室,山东 济南 250014)
磷酸锰锂(LiMnPO4)是一种非常有应用前景的锂离子电池正极材料,化学共沉淀法是制备这种材料的理想方法。针对LiMnPO4正极材料目前研究过程中存在的电子电导率低和锂离子扩散慢等问题,本文从Mn3(PO4)2、MnPO4、NH4MnPO4等不同Mn-P前驱体合成LiMnPO4出发,综述了近年来基于化学共沉淀工艺的两步法合成LiMnPO4正极材料并采用碳包覆和离子掺杂两种手段改性的国内外研究进展。对当前研究过程中存在的不同Mn-P前驱体获得LiMnPO4产品性能差异的问题,认为应该通过进一步地探讨化学共沉淀过程的反应机理并进行相关反应动力学及热力学研究解决。本文为LiMnPO4正极材料的研究及产业化提供了参考。
化学共沉淀法;锂离子电池;磷酸锰锂;正极材料
正交橄榄石型结构的磷酸盐LiMPO4(M为Fe、Mn、Co、Ni、V等)正极材料因具有成本低、无污染、循环寿命长和安全性能好等优点得到了研究者的认可[1-2],目前已商品化生产及应用的磷酸铁锂(LiFePO4)就是其中的典型代表,但Fe3+/Fe2+相对于Li+/Li的电极电势仅为3.4 V,较低的能量密度限制了LiFePO4材料的发展。与LiFePO4同属橄榄石结构的LiMnPO4材料,Mn3+/Mn2+相对于Li+/Li的电极电势为4.1 V,且位于现有电解液体系的稳定电化学窗口内,因此成为潜在高能量密度正极材料的首选。然而,LiMnPO4材料固有的电子电导率低和锂离子扩散慢的缺陷影响了其电化学活性的发挥。借助改善LiFePO4电化学性能的成功经验,目前多采用颗粒纳米化[3-4]、表面碳包覆[5-6]和掺杂[7-8]等手段提高LiMnPO4材料的电化学活性。
合成方法是制备正极材料的关键,对材料的颗粒形貌、粒径分布及电化学性能有着重要影响,一般来说,LiMnPO4正极材料的合成方法有高温固相法[9-10]、溶胶凝胶法[11-12]、水热合成法[13-14]及化学共沉淀法[15-16]等。其中,化学共沉淀法具有环境友好、能耗低、成本低和适合于规模化制备等优点,可制备形貌较好、颗粒细小均匀的纳米及微米级LiMnPO4材料,且材料的包覆及掺杂改性均可在液相合成中进行,进而提高其电化学性能。化学共沉淀法制备LiMnPO4正极材料可分为直接共沉淀合成LiMnPO4的一步法和先利用共沉淀反应得到Mn-P前驱体,再经过后续处理得到LiMnPO4的两步法。Delacourt等[17]以Mn(NO3)2·4H2O、H3PO4、LiNO3和LiOH为原料采用一步化学共沉淀法制备了粒径约为100 nm的LiMnPO4材料,该材料在C/20及C/5倍率下的可逆比容量分别约为70、50 mAh·g-1。虽然整个合成工艺操作较为简单,但由于Li、Mn、P难以按理想比例沉淀析出,因此所得LiMnPO4样品的电化学性能仍需改进。Maja等[18]以Mn(NO3)2·4H2O和H3PO4为原料先采用化学共沉淀法制备MnPO4前驱体,然后与锂源、碳源按一定的化学计量比球磨混合制备LiMnPO4材料。研究结果表明,制备的LiMnPO4颗粒粒径为15~20 nm,C/20及C/5倍率下的可逆比容量分别约为130、100 mAh·g-1。由此可见,先通过化学沉淀法制备Mn-P前驱体材料,可以获得电化学性能良好的LiMnPO4正极材料。
本文基于不同Mn-P前驱体合成路线,综述了化学共沉淀的两步法合成及改性LiMnPO4正极材料的国内外研究进展,对当前研究过程中存在的问题和未来的研究方向进行了总结和展望,为LiMnPO4正极材料的研究及产业化提供参考。
1 研究进展
近年来,LiMnPO4因资源丰富、价格低廉且对环境无污染等优点,成为锂离子电池中最有前途的正极材料,但其电子电导率低和锂离子扩散慢等问题导致高倍率放电性能差。目前国内外采用不同的Mn-P前驱体合成LiMnPO4,并采用碳包覆和离子掺杂两种手段进行改性研究,使制备的LiMnPO4具有较高的倍率性能。
1.1 Mn3(PO4)2前驱体
Mn3(PO4)2是目前采用化学共沉淀法制备LiMnPO4正极材料最多的前驱体,这主要是因为采用其制备的材料颗粒形貌呈球形,粒度较小、分布均匀、组分均匀、表面能比较大且活性更高。
纯相LiMnPO4的电子电导率低和锂离子扩散慢的问题导致其电化学活性非常低。王俊红等[19]以MnSO4、H3PO4为原料并用碱液调节溶液的pH,在表面活性剂的辅助下制备了粒径约为815 nm的Mn3(PO4)2前驱体,将其和碳酸锂混合锻烧制得LiMnPO4,该材料在0.1 C、0.5 C和1.0 C三个倍率下的首次放电比容量分别为102、97、88 mAh·g-1。在 0.1 C、0.5 C和1.0 C三个倍率下循环80次后放电比容量的保持率分别为93.21%、88.75%和83.02%。Kim等[20]以MnSO4、H3PO4和CTAB为原料在pH=1的条件下制备了Mn3(PO4)2前驱体,然后将Mn3(PO4)2和LiOH混合热处理制备LiMnPO4材料。结果表明,LiMnPO4材料颗粒平均粒径小于100 nm,该材料在0.1 C、1 C和5 C三个倍率下的首次放电比容量分别为135、102 、62 mAh·g-1。
碳包覆一直以来是改善电极材料颗粒尺寸与导电性的有效办法,从而被广泛用于各种锂电材料的改性。将碳包覆应用到LiMnPO4材料中是提高其电子电导性的重要途径,碳源的种类、碳含量、加入方式及包覆的均匀性是制备高电化学活性的 LiMnPO4的关键。Wu等[21]以MnSO4·H2O和NH4H2PO4为原料并以乙醇为引发剂,采用化学共沉淀法制备Mn3(PO4)2·3H2O前驱体,再将Mn3(PO4)2·3H2O、NH4H2PO4、Li2CO3与蔗糖球磨混料热处理制备LiMnPO4/C正极材料。研究表明,LiMnPO4/C具有约100 nm的颗粒尺寸和2 nm的碳包覆层;经650 ℃热处理的LiMnPO4/C复合材料在在0.05 C、1 C和5 C倍率下,放电比容量分别为141.7、119.9 和88.7 mAh·g-1,0.5 C倍率下循环100次后容量保持率仍可达95.2%。Su等[22]以Mn(CH3COO)2·4H2O、H3PO4和HCl为原料,采用化学沉淀法制备Mn3(PO4)2·H2O前驱体,然后以葡萄糖为碳源、 CH3COOLi·2H2O为锂源,制备的LiMnPO4/C材料颗粒粒径为60 nm,在0.05 C、0.2 C、1 C、5 C和 10 C倍率下首次放电比容量分别为154、134、120、 90和61 mAh·g-1且在大倍率(5 C和10 C)下放电具有良好的循环稳定性。Zhu等[23]以Mn(CH3COO)2、NH4H2PO4为原料,用LiOH·H2O调节溶液pH,通过化学共沉淀法制备了Mn3(PO4)2·H2O前驱体。将LiOH·H2O、Mn3(PO4)2·H2O、NH4H2PO4和C6H12O6·H2O按化学计量比3∶1∶1∶0.67 混合均匀,经干燥、热处理后制备LiMnPO4/C正极材料。通过比较有无包覆碳的LiMnPO4电化学性能,发现碳包覆LiMnPO4放电比容量明显高于无碳包覆的,循环性能也比无包覆碳的要好的多,包覆质量分数4.54%碳的LiMnPO4/C在0.05 C 的放电比容量为137 mAh·g-1。
除表面碳包覆制备LiMnPO4/C复合材料提高其电子电导率外,多数研究者还利用金属离子掺杂对LiMnPO4材料进行改性,采用化学共沉淀工艺可以在液相反应过程中将异相离子掺杂进入Mn-P前驱体晶格中,这对LiMnPO4离子导电性的提高起到了关键作用。Oh等[24]以MnSO4·7H2O、FeSO4·7H2O和H3PO4为原料,用NH3·H2O调节溶液pH,采用化学共沉淀法制备了(Mn1-xFex)3(PO4)2·xH2O (x=0,0.5)前驱体,然后与Li3PO4按一定的化学计量比混合高温处理制备LiMn0.5Fe0.5PO4/C。结果表明,LiMn0.5Fe0.5PO4/C的振实密度为1.27 g·cm-3,C/20和C/5 倍率下放电比容量分别为145和101 mAh·g-1。Hu等[25]采用掺杂铁离子取代锰离子制备了(Mn0.9Fe0.1)3(PO4)2前驱体,然后和LiOH、蔗糖混合制备了LiMn0.9Fe0.1PO4/C正极材料。结果表明,在10 C高倍率下放电比能量能达到60 mAh·g-1,掺杂铁离子具有更高的放电比容量。
1.2 MnPO4前驱体
MnPO4是文献中报道较多的制备LiMnPO4的另一种前驱体,与Mn3(PO4)2前驱体相比,该前驱体制备的材料形貌呈花状分布,电化学性能稍差。
Boonchom等[26]以Mn(NO3)2·4H2O、H3PO4和CH3CH2OH为原料制备MnPO4·H2O前驱体,经抽滤、洗涤和干燥后,置于600 ℃管式炉中焙烧制备了Mn2P2O7,将Mn2P2O7与Li2CO3经高温焙烧制备LiMnPO4。研究表明制备的MnPO4·H2O、Mn2P2O7和LiMnPO4均具有纯净的晶形结构,颗粒尺寸分别为100~200 nm、50~100 nm和30~50 nm,该材料在0.01 C首次放电比容量为132 mAh·g-1。
Xiao等[27]以Mn(NO3)2·4H2O和H3PO4为原料合成MnPO4·H2O纳米前驱体,然后将MnPO4·H2O与锂源混合制备LiMnPO4/C材料。研究发现LiMnPO4/C的结晶反应发生在438 ℃,完全成核反应发生在550 ℃,制备的样品在1/20 C首次放电比容量为115 mAh·g-1,几个循环后库仑效率约保持在100%。Wang等[28]以Mn(NO3)2和H3PO4为原料,用尿素调节溶液pH制备纳米MnPO4·H2O 前驱体,按一定的化学计量比将前驱体、CH3COOLi和过量质量分数10%的蔗糖球磨混料,干燥、热处理制备LiMnPO4/C正极材料。研究表明,制备的MnPO4·H2O颗粒粒径为40~50 nm,LiMnPO4/C颗粒粒径为40~100 nm,在1 C倍率下的可逆放电容量为114 mAh·g-1。 Cao等[29]以MnSO4·H2O、H3PO4、NH4NO3和NaOH为原料,采用化学共沉淀法制备了纳米MnPO4·H2O 前驱体,以PVA作为碳源,采用碳热还原法制备了碳包覆的LiMnPO4/ C纳米复合材料。研究发现,原位包覆质量分数6.8%碳的LiMnPO4/C正极材料在0.05 C的首次放电比容量为124 mAh·g-1,1 C的放电比容量为108 mAh·g-1,并且循环20次后,容量保持率仍接近100%。
Liu等[30]以Mn(NO3)2·4H2O和H3PO4为原料,采用化学共沉淀法制备MnPO4·H2O前驱体,再按一定的化学计量比将该前驱体与LiOH、FeC2O4、NH4H2PO4、PEG6000球墨混料煅烧制备LiMn0.7Fe0.3PO4/C材料。研究发现,制备的LiMn0.7Fe0.3PO4/C颗粒粒径在5~50 nm,在55 °C下0.5 C、1 C和0.1 C倍率的放电容量分别为114、102和145 mAh·g-1,0.5 C循环100次后放电容量仍可达113 mAh·g-1,表现出良好的倍率性能和循环性能。Sun等[31]采用化学共沉淀方法制备纳米Mn0.85Fe0.15PO4前驱体材料,然后与Li2CO3、沥青混合处理制备了颗粒粒径分布为100~200 nm的纳米花状LiMn0.85Fe0.15PO4/C材料。该材料具有优异的电化学性能,0.05 C 倍率的放电容量超过148 mAh·g-1,2 C 倍率的放电容量约 110 mAh·g-1。
1.3 NH4MnPO4前驱体
NH4MnPO4·H2O前驱体制备的材料形貌呈片状分布,具有晶粒小与低团聚的结构特性,有利于其与锂盐高温反应时得到相更纯、晶面生长更优、结晶度更高、与电解液接触面积更大、锂离子扩散更容易、电性能更优的 LiMnPO4/C复合材料。该材料具有循环稳定性强、能量密度高、循环性能好、倍率性能优异等特点,适合锂离子动力电池应用领域。
Sronsri等[32]将MnCl2·4H2O和(NH4)2HPO4在85 ℃混合搅拌1 h制备了NH4MnPO4·H2O前驱体,然后将该前驱体与Li2CO3混热处理10 h制备了粒径约为48 nm的纯相LiMnPO4材料。该材料0.1 C倍率下首次放电比容量为120 mAh·g-1,循环100次后,容量保持率仍可达95%以上,表现出良好的循环性能。Bramnik等[33]采用化学共沉淀法制备NH4MnPO4·H2O前驱体,该前驱体和LiOH通过高温固相反应,可以得到LiMnPO4,在0.05 C和1 C倍率下放电比容量为136.4 、118 mAh·g-1。
Liu等[34]采用新型化学共沉淀法以Mn(CH3COO)2·4H2O、柠檬酸、NH4H2PO4为原料,用NH3·H2O调节溶液pH,制备了NH4MnPO4·H2O前驱体,以葡萄糖为碳源、 CH3COOLi·2H2O为锂源,制备得到的LiMnPO4/C材料形貌呈花状,在0.05 C下的放电比容量仅为85 mAh·g-1,在倍率性能方面还需改善,但该方法能有效调节颗粒形貌和尺寸,为其他材料的制备提供了参考和借鉴。
Sronsri等[35]采用改进的化学共沉淀法制备Co及Mg掺杂的NH4M(II)PO4·H2O(M(II)为 Mn0.9Co0.1和 Mn0.8Co0.1Mg0.1)前驱体材料,然后采用高温固相法制备LiMn0.9Co0.1PO4和LiMn0.8Co0.1Mg0.1PO4材料。该材料在0.1C和0.05倍率下的放电容量分别为130、140 mAh·g-1,性能明显优于未掺杂的LiMnPO4材料。
1.4 其他Mn-P前驱体
除了采用Mn3(PO4)2、MnPO4和NH4MnPO4作为前驱体制备LiMnPO4,最近还有研究者采用MnHPO4和(C2N2H10)Mn2(PO4)2为前驱体制备LiMnPO4正极材料,也获得了一些不错的研究成果。
Sronsri等[36]以MnCl2·3H2O和H3PO4为原料,用NaOH调节溶液pH=7,采用化学共沉淀法制备了MnHPO4·3H2O前驱体。然后与Li2CO3按一定的化学计量比混合高温处理获得的LiMnPO4正极材料,平均粒径为150~200 nm,该材料在0.1 C放电倍率下比容量达到156 mAh·g-1,表现出良好的电化学性能。Xia等[37]以MnSO4·H2O和H3PO4为原料,用已烯二胺调节溶液pH=9,先采用化学共沉淀法制备了(C2N2H10)Mn2(PO4)2·2H2O前驱体,然后按一定的化学计量与LiCOOCH3、(C2N2H10)Mn2(PO4)2·2H2O高温处理获得LiMnPO4/C正极材料。结果表明,制备的LiMnPO4/C材料具有良好的晶形结构,颗粒平均粒径为30~50 nm,在 0.01 C、0.1 C、 0.5 C、1 C和2 C倍率下的首次放电比容量分别为151、142、135、130和128 mAh·g-1。
1.5 利用不同碳源包覆和离子掺杂改性的研究结果
将上述利用不同碳源包覆和离子掺杂改性LiMnPO4正极材料的研究结果分别列于表1和表2。
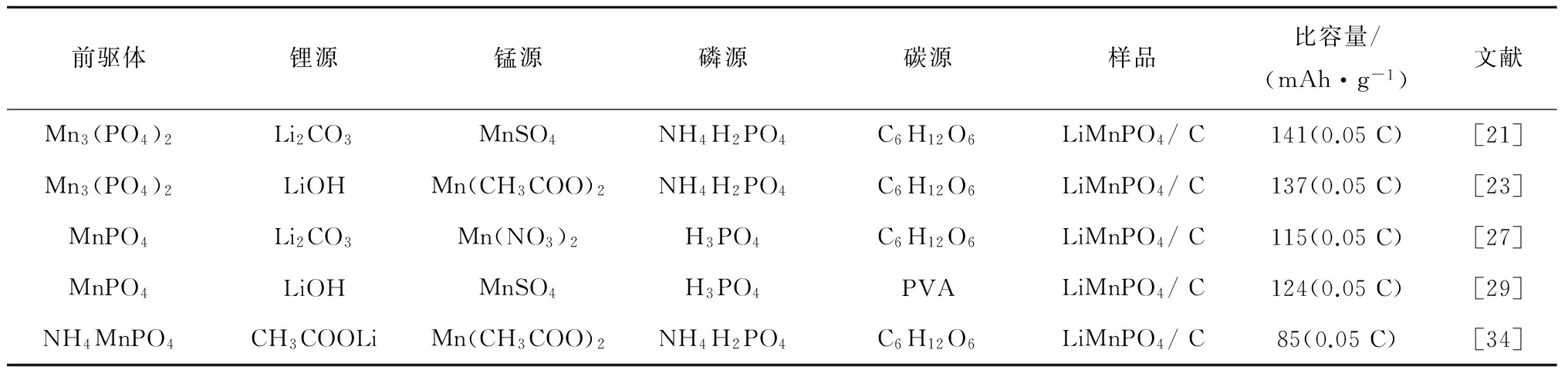
表1 表面碳包覆改性LiMnPO4正极材料电化学性能
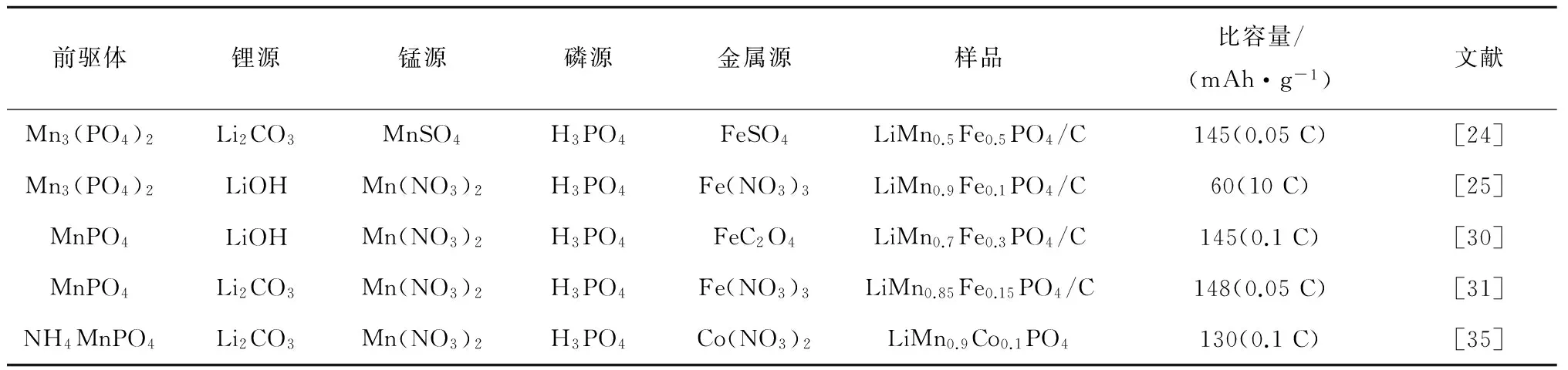
表2 离子掺杂改性磷酸锰锂正极材料粒径及电化学性能
由表1可以看出,以不同Mn-P前驱体为原料,采用碳热还原工艺制备LiMnPO4正极材料时主要采用葡萄糖作为碳源,其中以Mn3(PO4)2为前驱体制备的LiMnPO4正极材料具有更高的放电比容量。由表2可知,Fe2+的掺杂是目前改性LiMnPO4正极材料的主要手段,以MnPO4为前驱体,掺杂摩尔分数15%Fe2+的LiMnFePO4/C材料具有更高的放电比容量。
2 存在问题
LiMnPO4存在的主要问题是电子电导率低和锂离子扩散慢,针对这个问题,本文从不同Mn-P前驱体合成LiMnPO4出发,综述了近年来基于化学共沉淀的两步法合成及改性LiMnPO4的国内外研究现状。从已有的研究可以看出,采用Mn3(PO4)2、MnPO4和NH4MnPO4作为前驱体合成LiMnPO4具有操作简便的优点,但还存在以下问题:
(1)目前合成LiMnPO4材料的方法很多,即使采用化学共沉淀法制备,也存在不同的前驱体材料制备的材料颗粒尺寸、形貌及电化学性能有较大差异的问题,但是这方面的机理研究目前还不太完善;
(2)缩小颗粒尺寸可提高电子传导以及离子传输性能,但材料纳米化的制造成本通常很高,同时纳米材料需要更多其他材料如导电碳、粘接剂、聚流体的匹配,还会对环境和人体健康产生影响;
(3)采用碳包覆是提高 LiMnPO4材料导电性最为普遍的研究方法,但是从研究结果来看,碳包覆可以在一定程度上改善LiMnPO4的电化学性质,但是还远不能满足实际锂离子电池制备的需要;
(4)掺杂或替换是另一种能有效改善LiMnPO4材料性能的方法,但在这方面的研究还不够深入,相关研究有待于今后进一步加强;
(5)经过改性后,多数研究者制备的LiMnPO4正极材料在0.05 C放电倍率下的比容量在130~160 mAh·g-1之间,但是缺乏高放电倍率下的数据,这不利于促进LiMnPO4材料在动力电池领域的应用与推广。
3 展望
目前锂离子电池仍以小容量、低功率电池为主,这使其很难在高容量UPS、储能电池、电动工具、电动汽车等中得到广泛应用。对高容量、大功率的锂离子电池来说,正极材料的成本、高温性能、安全性十分重要,因此,研究开发能用于高容量、大功率的锂离子电池的新型正极材料成为当前的热点。为推动LiMnPO4用于实际生产,今后应在以下方面展开深入研究:
(1)合成工艺会对LiMnPO4的粒径大小与分布、颗粒的形貌及电化学性能产生重要影响,因此开发优化出成本低廉、工艺简单、适合工业推广的新合成工艺是关键;
(2)制备形貌和尺寸可控的前驱体材料有利于后续的材料性能改性,化学共沉淀法作为一种新型的合成方法,可以有效地控制各工艺参数。探讨化学共沉淀过程的反应机理和电化学活性改进的机理,进行相关动力学、热力学研究,分析其中的导电机理和晶体结构是以后研究的重点;
(3)缩小颗粒尺寸、碳包覆和掺杂是提高材料电子传导以及离子传输性能的主要改性方法,这些方法通常相互关联,还受合成方法和工艺的影响,因此需要深入研究碳包覆及掺杂机理;
(4)安全性能、低温性能良好以及与LiMnPO4材料相匹配的电解液均是评价材料电化学性能的关键,也是以后研究的重点;
(5)LiMnPO4材料的研究目前还停留在实验室阶段,可以借鉴LiFePO4材料产业化过程,对LiMnPO4材料在合成材料粒径、结构上进行更深入细致的研究,以开发出更有效的改性技术,这将是提高材料性能的关键。
[1]DOAN T N, BAKENOV Z, TANIGUCHI I T. Preparation of carbon coated LiMnPO4powders by a combination of spray pyrolysis with dry ball-milling followed by heat treatment [J]. Advanced Powder Technology, 2010, 21(2): 187-196.
[2]HERRERA J O, CAMACHO-MONTES H, FUENTES L E, et al. LiMnPO4: Review on synthesis and electrochemical properties[J]. Journal of Materials Science and Chemical Engineering,2015, 3:54-64.
[3]李丽娥. 磷酸锰锂纳米材料的制备及其锂离子电池正极材料性能研究[D].济南:山东大学,2013.
[4]DOKKO K, HACHIDA T, WATANABE M. LiMnPO4nanoparticles prepared through the reaction between Li3PO4and molten aqua-complex of MnSO4[J]. J Electrochem Soc, 2011,158(12): A1275-A1281.
[5]ZHONG S K, XU YB, LI Y H, et al. Synthesis and electrochemical performance of LiMnPO4/C composites cathode materials[J]. Rare Metals, 2012, 31(5): 474-478.
[6]DUAN J G, CAO Y B, JIANG J B, et al. Novel efficient synthesis of nanosized carbon coated LiMnPO4composite for lithium ion batteries and its electrochemical performance [J]. Journal of Power Sources, 2014, 268:146-152.
[7]SU L L, LI X W, MING H, et al. Effect of vanadium doping on electrochemical performance of LiMnPO4for lithium-ion batteries [J]. Journal of Solid State Electrochemistry, 2014, 18(3): 755-762.
[8]WANG D Y, OUYANG C Y, DRÉZEN T, et al. Improving the electrochemical activity of LiMnPO4via Mn-site substitution [J]. Journal of The Electrochemical Society, 2010, 157(2):A225-A229.
[9]李志军, 王红英, 汤伟杰,等. 锂离子电池正极材料LiMnPO4/C的固相法制备及性能研究[J]. 人工晶体学报, 2015, 44 (3): 773-778.
[10]ZHENG J G, NI L, LU Y W, et al. High-performance, nanostructure LiMnPO4/C composites synthesized via one-step solid state reaction [J]. Journal of Power Sources, 2015,282: 444-451.
[11]汪燕鸣, 王飞, 王广健. 溶胶-凝胶法制备LiMnPO4/C正极材料及其电化学性能[J]. 无机材料学报, 2013, 28(4): 415-419.
[12]KODERA T, ISOBE F, OGIHARA T. Preparation and electrochemical properties of LiMnPO4nanoparticles by polyol method [J]. Key Engineering Materials, 2013, 566:95-98.
[13]PAN X L, XU C Y, ZHEN L. Synthesis of LiMnPO4microspheres assembled by plates, wedges and prisms with different crystallographic orientations and their electrochemical performance [J]. Cryst Eng Comm, 2012, 14(20): 6412-6418.
[14]LIU A F, LIU Y F, HU Z H, et al. High performance of LiMnPO4/C prepared by hydrothermal reaction [J]. Energy Materials, 2009,4(1):44-48.
[15]蒋波, 杨改, 蔡飞鹏,等. 化学沉淀法制备磷酸铁锂正极材料的研究进展[J]. 稀有金属材料与工程, 2014,43(8):2043- 2048.
[16]DELACOURT C, POIZOT P, MORCRETTE M, et al. One-step low-temperature route for the preparation of electrochemically active LiMnPO4powders[J]. Chem Mater, 2004, 16(1):93-99.
[17]DELACOURT C, WURM C, REALE P, et al. Low temperature preparation of optimized phosphates or Li-battery applications [J]. Solid State Ionics, 2004, 173(1/2/3/4):113-118.
[18]MAJA P, MARJAN B, ELENA T, et al. Synthesis of nanometric LiMnPO4via a two-Step technique [J]. Chemistry of Materials, 2012, 24(6): 1041-1047.
[19]王俊红. 亚微米级碳酸锰和磷酸锰的制备研究[D]. 南昌:南昌大学, 2013.
[20]KIM T H, PARK H S, LEE M H, et al. Restricted growth of LiMnPO4nanoparticles evolved from a precursor seed [J]. J Power Sources, 2012, 210:1-6.
[21]WU K P, HU G R, PENG Z D, et al. Novel synthesis of Mn3(PO4)2·3H2O nano plate as a precursor to fabricate high performanceLiMnPO4/C composite for lithium-ion batteries[J].RSC Advances, 2015, 5:95020-95027.
[22]SU K, LIU F, CHEN J T. Preparation of high performance carbon-coated LiMnPO4nanocomposite by an acetate-assisted antisolvent precipitation method[J]. Journal of Power Sources, 2013,232: 234-239.
[23]ZHU H J, ZHAI W, YANG M, et al. Synthesis and characterization of LiMnPO4/C nano-composites from manganese(II) phosphate trihydrate precipitated from a micro-channel reactor approach [J]. RSC Advances, 2014, 4(49): 25625-25632.
[24]OH S M, MYUNG S T, CHOI Y S, et al. Co-precipitation synthesis of micro-sized spherical LiMn0.5Fe0.5PO4cathode material for lithium batteries [J]. Journal of Materials Chemistry, 2011, 21(48):19368-19374.
[25]HU C L, YI HH, FANG H S, et al. Improving the electrochemical activity of LiMnPO4via Mn-site co-substitutionwith Fe and Mg [J]. Electrochem Commun, 2010,12(12):1784-1787.
[26]BOONCHOM B, YOUNGME S, MAENSIRI S, et al. Nanocrystalline serrabrancaite (MnPO4·H2O) prepared by a simple precipitation route at low temperature [J]. Journal of Alloys and Compounds, 2008, 454 (1/2):78-82.
[27]XIAO J, XU W, CHOI D, et al. Synthesis and characterization of Lithium manganese phosphate by a precipitation method[J]. Journal of the Electrochemical Society, 2010, 157(2): A142-A147.
[28]WANG L, SUN W T, HE X M, et al. Synthesis of nano-LiMnPO4from MnPO4·H2O prepared by methanol chemistry [J]. International Journal of electrochemical science, 2011, 6: 2022-2030.
[29]CAO Y B, DUAN J G, HU G R, et al. Synthesis and electrochemical performance of nanostructured LiMnPO4/C composites as lithium-ion battery cathode by a precipitation technique[J]. Electrochimica Acta, 2013, 98: 183-189.
[30]LIU T, XU J J, WU B B, et al. Porous LiMn0.7Fe0.3PO4/C prepared by a thermal decomposition method as high performance cathode materials for Li-ion batteries [J]. RSC Advances, 2013, 3(32): 13337-13341.
[31]SUN Y K, OH S M, PARK H K, et al. Micrometer-sized nanoporous high-volumetric-capacity LiMn0.85Fe0.15PO4cathode material for rechargeable lithium-ion batteries[J]. Adv Mater,2011, 23(43): 5050-5054.
[32]SRONSRI C C, NOISONG P, DANVIRUTAI C. Solid state reaction mechanisms of the LiMnPO4formation using special function and thermodynamic studies[J]. Industrial & Engineering Chemistry Research, 2015, 54(28): 7083-7093.
[33]BRAMNIKA N N, EHRENBERGA H. Precursor-based synthesis and electrochemical performance of LiMnPO4[J]. Journal of Alloys and Compounds, 2008,464(1/2):259-264.
[34]LIU J L, HU D G, HUANG T, et al. Synthesis of flower-like LiMnPO4/C with precipitated NH4MnPO4·H2O as precursor [J]. Journal of Alloys and Compounds, 2012, 518: 58-62.
[35]SRONSRI C C, NOISONG P, DANVIRUTAI C. Synthesis characterization and vibrational spectroscopic study of Co, Mg co-doped LiMnPO4[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2016,153 (3):436-444.
[36]SRONSRI C C, NOISONG P, DANVIRUTAI C. Synthesis non-isothermal kinetic and thermodynamic studies of the formation of LiMnPO4from NH4MnPO4·H2O precursor [J]. Solid State Sciences, 2014, 32: 67-75.
[37]XIA Q B, LIU T, XU J J, et al. High performance porous LiMnPO4nanoflakes: synthesis from a novel nanosheet precursor[J]. Journal of Materials Chemistry A, 2015, 3(12): 6301-6305.
Research progress in chemical co-precipitation based synthesis of LiMnPO4cathode material by two steps
QIN Xian-zhong,YANG Gai*,GAO Jian,CAI Fei-peng, WANG Bo,JIANG Bo,TAN Chun-hui
( Shandong Provincial Key Laboratory of Biomass Gasification Technology , Energy Research Institute ,Shandong Academy of Sciences,Jinan 250014,China)
∶LiMnPO4has the potential applications as a cathode material for lithium-ion batteries, and chemical co-precipitation is an ideal method to prepare LiMnPO4. There have been problems, such as the low conductivity and low Li+diffusion, lying in the recent studies of LiMnPO4cathode materials. According to these problems,this paper, starting from the synthesis of LiMnPO4using Mn3(PO4)2、MnPO4、NH4MnPO4and other different kinds of Mn-P precursors, summarized the recent research progresses at home and abroad in LiMnPO4prepared by chemical co-precipitation of two-step method, in which carbon coating and metal ion doping were usual modification methods. Aiming at the existing problems in recent researches that LiMnPO4with different properties can be obtained from different kinds of Mn-P precursors, it was considered that the mechanism of chemical co-precipitation should be further discussed and the related kinetics and thermodynamics study should be carried on. This paper provides references for the further study of LiMnPO4cathode materials and its industrialization.
∶chemical co-precipitation method; lithium ion battery; lithium manganese phosphate; cathode material
10.3976/j.issn.1002-4026.2017.02.007
2016-10-26
山东省自主创新重大专项(2014ZZCX05501);山东省自然科学基金(ZR2016BQ44);济南市高校院所自主创新计划(201402023);纯电动汽车关键技术研究及产业化应用(鲁科院字2015,67号)
秦显忠(1988—),女,硕士,研究方向为电池材料。
*通信作者。E-maill:yangg@sderi.cn
TQ152
A
1002-4026(2017)02-0043-07
