胍基乙酸的致突变性研究
2017-03-06代重山王泽明田耀耀张德福杨立彬汤树生
代重山, 马 佳, 王泽明, 田耀耀, 张德福, 杨立彬, 汤树生*
(1.中国农业大学 农业部兽药安全监督检验测试中心(北京),北京海淀 100193;2.固安君德同创生物工程有限公司,河北固安 065500;3.北京君德同创农牧科技股份有限公司,北京海淀 100085)
胍基乙酸的致突变性研究
代重山1, 马 佳2, 王泽明3, 田耀耀3, 张德福3, 杨立彬3, 汤树生1*
(1.中国农业大学 农业部兽药安全监督检验测试中心(北京),北京海淀 100193;2.固安君德同创生物工程有限公司,河北固安 065500;3.北京君德同创农牧科技股份有限公司,北京海淀 100085)
本文选用Ames试验、小鼠骨髓细胞微核试验和精子畸形试验三种短期测试组合探究胍基乙酸是否具有致突变作用。结果发现:Ames试验结果显示,胍基乙酸在8~5000 μg/皿,有或无代谢活化系统(S9)时,对鼠伤寒沙门氏菌TA97、TA98、TA100、TA102四种试验株均没有诱变性;骨髓细胞微核试验结果显示,胍基乙酸在1250~5000 mg/kg体重剂量内经口染毒后,各剂量组小鼠骨髓细胞中嗜多染红细胞(PCE)微核率与阴性对照组比较均无显著性差异(P>0.05);小鼠精子畸形试验结果显示,胍基乙酸在1250~5000 mg/kg体重剂量内经口染毒后,各剂量组小鼠精子畸形率与阴性对照组比较均无显著性差异(P>0.05)。结果表明,三个致突变试验结果均为阴性,胍基乙酸为非致突变物质。
胍基乙酸;饲料添加剂;致突变
胍基乙酸又称胍乙酸、N-咪基甘氨酸,是动物体内合成肌酸(Cr)的主要内源性前体物质,而Cr是动物机体能量代谢中的重要物质,是能量的贮存场所(张俊玲等,2016)。已有研究表明,在日粮中补充胍基乙酸能够提高畜禽生长性能和胴体品质,从而提高生产效益(张德福等,2016;Michiels等,2012;张堂田等,2011;江涛等,2011)。也有研究发现,外源性补充胍基乙酸可增加人和动物血液及肌肉组织内Cr水平,且更加优越于直接补充Cr(Ostojic等,2016;McBreairty等,2015)。近期研究证实,日粮中添加0.04%~0.08%胍基乙酸可改善肉种鸡种蛋孵化性能 (张俊玲等,2016);日粮中添加0.05%胍基乙酸可改善樱桃谷肉鸭的屠宰性能和抗氧化能力(王亚琼等,2016)。另一方面,高剂量补充胍基乙酸可诱导大鼠产生高同型半胱氨酸血症(Liu等,2014),且存在雌雄差异,如亚急性毒性研究中发现,雌性大鼠连续90 d饲喂胍基乙酸 (1000 mg/kg饲料)可导致血浆高半胱氨酸水平明显升高,远远高于雄性大鼠 (10000 mg/kg饲料)(Feedap,2009);另外,用添加3000 mg/kg胍基乙酸的饲料饲喂肉鸡35 d,鸡血液中红细胞平均体积及红细胞血红蛋白浓度显著增加,表明高剂量胍基乙酸可能存在一定的毒性(Feedap,2016)。然而,关于胍基乙酸安全性及其毒理学方面的风险评估报道较少。本研究参照国内外致突变性试验方法研究了胍基乙酸的致突变作用,以期为胍基乙酸的安全使用提供理论依据。
1 材料与方法
1.1 样品 胍基乙酸(商品名为肌源®)由北京君德同创农牧科技股份有限公司提供,纯度≥98%;二甲基亚砜(DMSO)、敌克松、2-氨基芴(2-AF)、叠氮钠(NaN3),购自西格玛公司;环磷酰胺(CP),购自江苏恒瑞医药股份有限公司;羧甲基纤维素钠(CMC-Na),购自天津科密欧化学试剂有限公司;其他试剂均为分析纯。
1.2 试验动物 ICR小鼠购自于北京维通利华动物科技有限公司 (试验动物生产许可证号SCXK(京)2007-0001),饲养于农业部兽药安全监督检验测试中心(北京)实验动物房,采用独立通风笼盒饲养,自由采食,维持12 h光照/黑暗的节律,正式试验前均适应喂养5 d。
1.3 Ames试验 试验严格按GB15193.4-2003标准(中华人民共和国卫生部,2004)鼠伤寒沙门氏菌回复突变试验(Ames试验)方法进行操作,试验在同条件下重复2次。所用试验菌株为鼠伤寒沙门氏菌突变型菌株TA97、TA98、TA100、TA102(试验前已鉴定合格),其中,TA97和TA98可检测移码型诱变剂;TA100可检测碱基置换型诱变剂;TA102检测移码型和碱基置换型诱变剂。试验时先用预备试验(点试验)确定正式试验(平皿掺入法)的剂量 (5000、1000、200、40 μg/皿和8 μg/皿),同时设灭菌蒸馏水和0.2%DMSO为阴性对照组及其不同的阳性对照组。上述8个试验组均分为加代谢活化系统S9组和不加 S9组,点试验加 S9时,TA97、TA98、TA100、TA102四种菌株均用2-AF作为阳性对照物,浓度为20.0 μg/10 μL;点试验不加S9时,四种菌株均用敌克松作为阳性对照物,浓度为50.0 μg/皿。掺入试验加S9时,四种菌株均用2-AF作为阳性对照物,浓度为10.0 μg/皿;掺入试验不加S9时,菌株TA97、TA98、TA102用敌克松为阳性对照物,浓度为50.0 μg/皿,菌株TA100用NaN3为阳性对照物,浓度为1.5 μg/皿。
1.4 小鼠骨髓细胞微核试验 选用体重25~30 g ICR小鼠100只,随机分为5组,每组20只(雌雄各半)进行试验,参照GB15193.5-2003标准(中华人民共和国卫生部,2004)进行。胍基乙酸分为1250、2500、5000 mg/kg三个剂量组,用1%CMCNa配成混悬液,采用经口灌胃法对试验动物进行染毒,小鼠灌胃体积为0.2 mL/10 g体重,每天染毒1次,连续染毒2 d。在第二次染毒后6 h颈椎脱臼处死小鼠,取股骨制片。以双盲法镜下检查计数嗜多染红细胞数(PCE)、含微核多染红细胞数及成熟红细胞数(RBC)。试验另设阴性对照组(1%CMCNa)和阳性对照组(CP 40 mg/kg,用生理盐水溶解为2 mg/mL溶液)。阴性对照组染毒方法亦采用灌胃染毒方式,阳性对照组采用腹腔注射法进行染毒。阴性对照组和阳性对照组的染毒方案及随后操作均与受试物各剂量组相同。
1.5 小鼠精子畸形试验 选用体重25~35 g雄性ICR小鼠50只,随机分为5组。胍基乙酸分为1250、2500、5000 mg/kg三个剂量组,用1%羧甲基纤维素钠配成混悬液。采用经口灌胃法对试验动物进行染毒,小鼠灌胃体积为0.2 mL/10 g体重,每天染毒1次,连续染毒5 d,在第1次给药后第35 d颈椎脱臼法处死小鼠,摘取两侧附睾按GB15193.7-2003标准 (中华人民共和国卫生部,2004)操作方法制片。在显微镜下检查精子形态,对同一视野下正常精子、各型畸形精子进行计数。试验另设阴性对照组(1%CMC-Na)和阳性对照组(CP 40 mg/kg,用生理盐水溶解为2 mg/mL溶液)。阴性对照组染毒方法亦采用灌胃染毒方式,阳性对照组采用腹腔注射法进行染毒。阴性对照组和阳性对照组的染毒方案及随后操作均与受试物各剂量组相同。
2 结果
2.1 胍基乙酸对Ames试验结果的影响 胍基乙酸2次Ames试验的结果见表1和表2,与阴性对照组相比,加减S9活化系统,胍基乙酸浓度为8~5000 μg/皿时,4种鼠伤寒氏沙门氏菌试验株的每皿平均回变菌落数2次重复性试验结果无显著差异(P>0.05),且未见剂量反应关系。
2.2 胍基乙酸对小鼠骨髓细胞微核试验的影响胍基乙酸小鼠骨髓细胞微核试验结果见表3和表4,与阴性对照组(1%CMC-Na)相比,阳性对照物CP处理可显著提高小鼠PCE微核率(P<0.01),胍基乙酸各剂量组PCE/RBC在正常范围内,无显著差异(P>0.05)。
2.3 胍基乙酸对小鼠精子畸形试验的影响 胍基乙酸小鼠精子畸形试验试验结果见表5和表6,胍基乙酸各剂量组精子畸形率与阴性对照组差异不显著(P>0.05),精子畸形主要表现为无钩、颈扭转和无定形等;与阴性对照组(1% CMC-Na)相比,阳性对照组(CP)显著提高精子畸形率(P<0.01)。

表1 胍基乙酸对鼠伤寒沙门氏菌回复突变试验结果的影响(第1次)
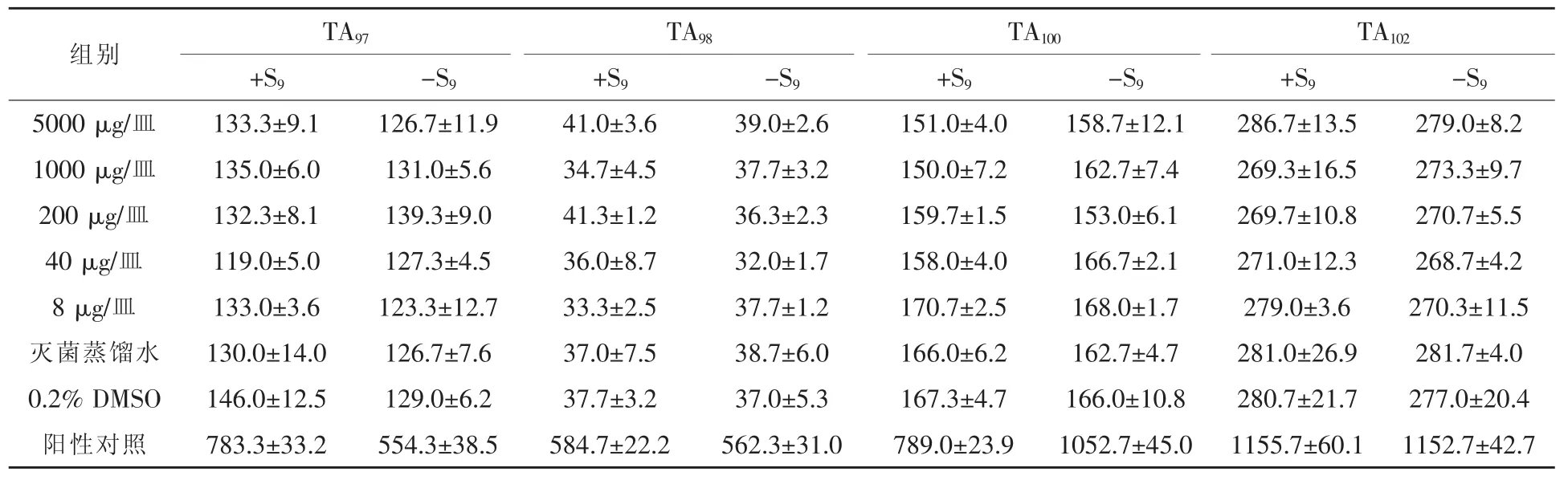
表2 胍基乙酸对鼠伤寒沙门氏菌回复突变试验结果的影响(第2次)

表3 胍基乙酸对小鼠骨髓细胞微核试验结果的影响(雌性小鼠)

表4 胍基乙酸对小鼠骨髓细胞微核试验结果的影响(雄性小鼠)
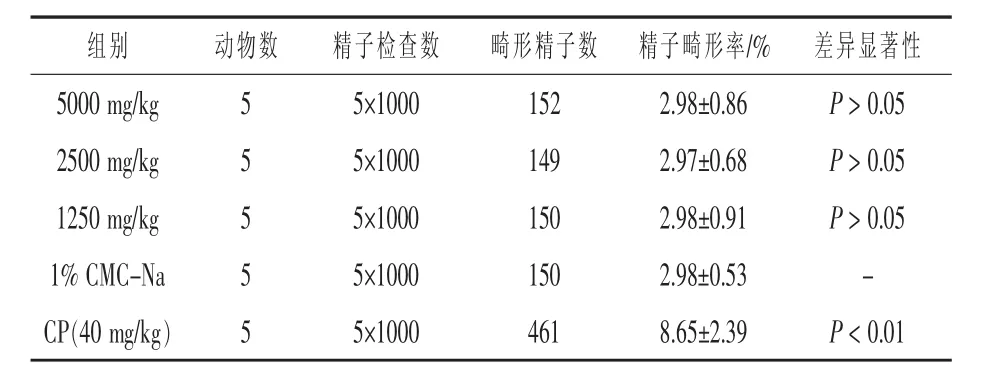
表5 胍基乙酸对小鼠精子畸形率的影响

表6 各类畸形精子百分率%
3 分析与讨论
胍基乙酸是甘氨酸的衍生物,作为肌酸的前体物,可在动物或人体内自然生成,在机体的能量循环中发挥着重要作用 (Ostojic等,2016;McBreairty等,2015)。本研究选择了Ames试验、小鼠骨髓细胞微核试验和精子畸形试验三种短期测试组合检测胍基乙酸的致突变作用,符合《食品安全性毒理学评价程序和方法》(2003)中致突变性测定要求。欧洲食品安全局报告(2009),使用平皿法检测胍基乙酸在62~5000 μg/皿时对鼠伤寒沙门氏菌 TA102、TA100、TA98、TA97a、TA1535的致突变作用,结果均为阴性,本研究结果与其一致。在使用人周围淋巴细胞的测试中,0.01 M胍基乙酸处理20 h不会造成染色体异常(Feddap,2009)。此外,本研究进一步采用了小鼠体内试验方法,检测了胍基乙酸的致突变性及遗传毒性,发现小鼠骨髓细胞微核试验和小鼠睾丸精子畸形试验结果均为阴性,进一步证实胍基乙酸为非致突变物质。胍基乙酸的非致突变性结果一方面可能与胍基乙酸是机体内源性物质有关,因为胍基乙酸可在动物或人体内自然生成,具有较好的安全性;另一方面可能与其高稳定性结构有关(韦长梅,2004)。
4 小结
体外及动物试验证实,动物饲料添加剂胍基乙酸是一种非致突变物质。
[1]江涛.胍基乙酸的合成及其对肉鸡生长性能和血液理化指标的影响[D].合肥:安徽农业大学,2012.
[2]王亚琼,刘强,姜发彬,等.胍基乙酸对樱桃谷肉鸭生产性能和抗氧化能力的影响[J].2016,39(2):269~274
[3]韦长梅.胍基化合物的合成与晶体结构研究:[硕士学位论文][D].南京:南京工业大学,2004.
[4]张德福,田耀耀,马佳,等.胍基乙酸对AA肉仔鸡生长性能和经济效益的影响[J].饲料研究,2016,17:32~36
[5]张俊玲,张德福,崔军,等.胍基乙酸对AA+肉种鸡繁殖性能的影响[J].饲料研究,2016,14:25~28
[6]张俊玲,张德福,石凤云,等.胍基乙酸在动物生产上的研究进展[J].中国畜牧兽医,2016,52(4):63~66.
[7]张堂田,孟秀丽,江涛,等.胍基乙酸和N-甲基-D-天冬氨酸对育肥猪生长和肉品质的影响[J].湖南农业科学,2011,23:121~123
[8]中华人民共和国卫生部,中国国家标准化管理委员会.GB15193.7-2003.食品安全性毒理学评价程序和方法[S].北京:中国标准出版社,2004.
[9]中华人民共和国卫生部,中国国家标准化管理委员会.GB15193.4-2003.食品安全性毒理学评价程序和方法[S].北京:中国标准出版社,2004.
[10]中华人民共和国卫生部,中国国家标准化管理委员会.GB15193.5-2003.食品安全性毒理学评价程序和方法[S].北京:中国标准出版社,2004.
[11]中华人民共和国卫生部,中国国家标准化管理委员会.GB15193.1-21-2003.食品安全性毒理学评价程序和方法[S].北京:中国标准出版社,2004.
[12]Feedap.Safety and efficacy of guanidinoacetic acid as feed additive for chickens for fattening[J].EFSA Journal,2009,998:1~30.
[13]Feedap.Safety and efficacy of guanidinoacetic acid for chickens for fattening,breeder hens and roosters,and pigs[J].EFSA Journal 2016,14(2):4394.
[14]Liu Y Q,Jia Z,Han F,et al.Suppression effects of betaine-enriched spinach on hyperhomocysteinemia induced by guanidinoacetic acid and choline deficiency in rats[J].Scientific World Journal,2014,2014:904501.
[15]McBreairty L E,Robinson J L,Furlong K R,et al.Guanidinoacetate is more effective than creatine at enhancing tissue creatine stores while consequently limiting methionine availability in Yucatan miniature pigs[J].PLoS One.2015,10(6):e0131563.
[16]Michiels J,Maertens L,Buyse J.Supplementation of guanidinoacetic acid to broiler diets:Effects on performance,carcass characteristics,meat quality,and energy metabolism[J].Poultry Sci,2012,91(2):402~412.
[17]Ostojic S M,Ostojic J,Drid P,et al.Guanidinoacetic acid versus creatine for improved brain and muscle creatine levels:a superiority pilot trial in healthy men[J].Appl Physiol Nutr Metab,2016,41(9):1005~1007.■
The present study was aimed to investigate the mutagenicity of guanidinoacetic acid(GA)by using Ames test,mouse bone marrow micronucleus test and mouse sperm shape abnormality test.The results showed that,compared to the negative control group,the treatment of GA at the range of 8~5000 μg/dish did not induced the marked mutation for Salmonella typhimurium strains TA97,TA98,TA100and TA102with or without metabolic activation system (S9).In the mouse bone marrow micronucleus test and mouse sperm shape abnormality test,there are both no significant difference observed in all the GA treatment(1250~5000 mg/kg)groups,compared to the negative control group(P>0.05).These results revealed that GA is a non-mutagenic substance.
guanidinoacetic acid;feed additive;mutagenicity
S811
A
1004-3314(2017)03-0016-04
10.15906/j.cnki.cn11-2975/s.20170305
北京市科技计划项目(Z151100001215001)
*通讯作者
