在体单向肠灌流模型研究三七人参皂苷Rb3大鼠肠吸收特性
2016-10-17沈佳伟曹秀琴
沈佳伟 曹秀琴
上海中医药大学附属岳阳中西医结合医院闵行分院,上海 200241
在体单向肠灌流模型研究三七人参皂苷Rb3大鼠肠吸收特性
沈佳伟曹秀琴*
上海中医药大学附属岳阳中西医结合医院闵行分院,上海200241
目的:研究人参皂苷Rb3在大鼠肠道的吸收动力学,并考察不同的药物浓度和常用的吸收促进剂对其吸收速率的影响。方法:进行大鼠在体肠灌流实验,研究人参皂苷Rb3在肠道不同肠段的吸收情况。结果:人参皂苷Rb3在十二指肠、空肠、回肠、结肠的吸收速率为十二指肠 > 空肠 ≈ 回肠 > 结肠,人参皂苷Rb3在低、中、高3个浓度下的吸收速率分别为低浓度 > 中浓度 ≈ 高浓度。结论:小肠整个肠段是人参皂苷Rb3的主要吸收部位,十二指肠、空肠、回肠、结肠都有不同程度的吸收,其中十二指肠段吸收速率最快。人参皂苷Rb3在小肠中吸收速率随着浓度的增加而逐渐减小,推测被动扩散、易化扩散和主动转运为影响人参皂苷Rb3吸收的主要转适机制。
人参皂苷Rb3;在体肠吸收;吸收速率常数
三七又名田七,为五加科植物三七[Panaxnotoginseng(Burk.)F.H.Chen]的干燥根,主要分布于云南、广西等省份,是我国传统珍贵药材[1]。三七具有散瘀止血、消肿定痛之功效,提高机体免疫力等多种药理活性[2],其药效的物质基础主要是三萜皂苷类成分,此外还含有一些氨基酸、多糖类等成分。三七的主要药用部位是其根和根茎。现在随着研究的深入,发现在三七叶中也存在着许多种皂苷成分,其中以人参皂苷Rb3、Fc和Rb1含量较高,具有镇静安神、清热消肿、活血止血之功效,能用于治疗神经衰弱,失眠,抑郁等疾病[3]。本实验根据大鼠肠道的生理状况与人相似这一特点,采用大鼠在体肠吸收模型,研究Rb3在大鼠肠道的吸收动力学特征,并考察吸收促进剂对吸收速率的影响,为三七口服给药制剂的研制提供生物药剂学依据。
1 仪器与材料
1.1实验动物Wistar大鼠,雄性,体重( 230±20)g[上海斯莱克实验动物有限责任公司,动物许可证:scxk(泸)2008-2016]。
1.2仪器HL-2型恒流泵(上海精科实业有限公司);FA-2004型电子天平(上海精密仪器厂);Agilent1260高效液相色谱仪(美国Agilent公司);Thermo Syncronis C18(4.6mm×250mm,5μm)色谱柱,0.45μm微孔滤膜。
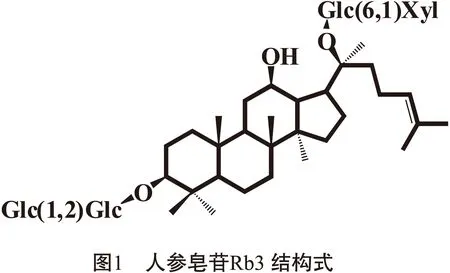
1.3药品及试剂人参皂苷Rb3对照品(批号:201012,纯度大于98%,结构式如图1),氯化钙、葡萄糖、氯化钠、氯化钾、碳酸氢钠、磷酸二氢钠、氯化镁(购自国药集团化学试剂有限公司),戊巴比妥钠(上海行知化工厂),Krebs-Ringer’s营养液(pH=7.4),乙腈(Fisher),其他试剂均为分析纯。
2 实验方法
2.1HPLC分析方法
2.1.1色谱条件的建立Thermo Syncronis C18(4.6mm×250mm,5μm)色谱柱,流动相为乙腈-水(60∶40),流速为1mL·min-1,检测波长为203nm,进样量10μL。
2.1.2空白Kreb-Ringer’s 缓冲液的配置[4](下文简称K试液)精密称取氯化钙0.37g、葡萄糖1.4g,分别加入少量蒸馏水溶解;称取氯化钠7.8g、氯化钾0.35g、碳酸氢钠1.37g、磷酸二氢钠0.32g,氯化镁0.02g,加蒸馏水溶解后与溶解的氯化钠及葡糖糖液混匀,蒸馏水定容至1L,1mol·L-1盐酸调pH至7.4即得,备用。
2.1.3空白干扰试验用空白K试液按2.5项下方法进行大鼠不同肠段单向灌流,收集流出液,即得空白肠灌流液,采用9倍甲醇稀释上述空白肠灌流液,过0.45 μm微孔滤膜,取滤液按2.1.1项下色谱条件测定,考察空白肠灌流液对人参皂苷Rb3的测定是否有干扰。2.1.4标准曲线制备精密称取人参皂苷Rb3对照品5mg,置10mL量瓶中,用K试液溶解并稀释至刻度,摇匀,得500mg·L-1的储备液。用K试液为溶剂,逐步稀释配制质量浓度分别为250.0、100.0、50.0、20.0、10.0、5.0mg·L-1的人参皂苷Rb3溶液,照2.1.1项下色谱条件测定,记录峰面积。以峰面积(A)对质量浓度(C,mg·L-1)进行线性回归分析,得标准曲线,回归方程为C=5.6933×A+0.9093,R2=0.9996,人参皂苷Rb3在5~500mg·L-1线性良好,符合定量分析要求。
2.1.5精密度和回收率试验精密称取适量药物,用K试液配制20.0、50.0、100.0mg·L-1低、中、高3种质量浓度的人参皂苷Rb3溶液,照2.1.1项下色谱条件测定,记录峰面积。以上述低、中、高3个质量浓度做日内和日间变异(n=6),结果见表1,表明低、中、高3个质量浓度的日内和日间RSD均<2.0%。低、中、高3个质量浓度的相对回收率见表2,分别为(99.18±0.99)%、(98.96±0.83)%、(95.97±1.91)%。

表1 精密度实验测定结果

表2 回收率测定结果
2.2人参皂苷Rb3溶液的配置用少量生理盐水溶解人参皂苷Rb3,用一定量的K试液(pH=7.4)稀释定容即得。
2.3人参皂苷Rb3在灌流液中稳定性研究取K试液对大鼠小肠段灌流,收集流出液,为空白肠液。用此液配制60mg·L-1的人参皂苷Rb3溶液3份,置37℃水浴恒温。分别于0、1、2、3、4、5、6 h各取1mL置1.5mL离心管中,过0.45μm微孔滤膜,取滤液按2.1.1项下色谱条件测定峰面积响应值,根据峰面积的变化研究人参皂苷Rb3在灌流液中稳定性。
2.4恒流泵管道对人参皂苷Rb3的物理吸附情况考察根据2.3项方法,配制人参皂苷Rb3浓度为60mg·L-1的灌流液3份,用恒流泵将此灌流液以0.2mL·min-1的速度泵入硅胶管道内,体外空循环2 h,分别于0.25、0.5、0.75、1、1.5、2 h收集流出的灌流液1mL,置1.5mL离心管中,过0.45μm微孔滤膜,取滤液按2.1.1项下色谱条件测定峰面积响应值,计算灌流液中人参皂苷Rb3浓度。
2.5单向肠灌流将Wistar大鼠随机分为4个组,每组5只。取Wistar大鼠,实验前禁食12h,自由饮水,称重,腹腔注射1%戊巴比妥钠(剂量40mg·kg-1),麻醉并固定。沿大鼠的腹中线打开约3cm,在待考察的大鼠小肠部分的两端插管(十二指肠是从幽门以下2cm处开始约10cm长的肠段,回肠是从盲肠上10~20cm处开始的肠段,空肠是十二指肠和回肠之间的肠段[5]),用线扎紧,与恒流泵连成回路。用预热至37℃的生理盐水轻缓地将肠内容物冲洗干净,再用空气将生理盐水排净,然后先用空白K试液以2mL/min的流速循环15min,排除肠内气泡,再取含一定浓度人参皂苷Rb3的K试液(预热至37℃)以2 mL/min的流速平衡30min,再以0.2mL/min的流速循环,调节流速时即为0时,以后分别于0.25、0.5、0.75、1、1.5、2 h取样3.0mL,所收集的循环液,经0.45μm微孔滤膜过滤,取续滤液,高速离心(10000 r·min-1)10min,取上清液。按照2.1.1项下色谱条件进行测定。最后将大鼠处死,剪下被灌流肠段,准确测量其长度和内径[6]。根据恒流泵管道对人参皂苷Rb3的物理吸附情况考察结果,将实验中所使用的硅胶管道用供试液饱和1h,为排除实验过程中所使用的硅胶管道对人参皂苷Rb3可能存在的物理吸附作用。 2.6灌流液体积的校正及数据处理在研究药物的肠吸收机制时,由于小肠不仅吸收药物也吸收水分,因此会使得灌流液体产生积变化。目前,国内常用的校正水分的方法主要有重量法和酚红法。本实验采用何承华等[7]使用的重量法,精密量取供试液1.00mL放入已称重的玻璃瓶中,称量液体的质量,算出其密度ρin。从接收液样品中精密量取1.00mL,放入已经称重玻璃瓶中,称量液体的质量,计算出流出液的平均密度ρout。Min和Mout分别为一定时间内进出肠道灌流液的质量,则Vin=Min/ρin,Vout= Mout/ρout。按下式[5]计算药物吸收速率常数(Ka)以和药物表观渗透系数(Papp)。
Ka=(1-Cout/Cin×Vout/Vin)×Qin/πr2L
Papp=-QinLn(Cout/Cin×Vout/Vin)/2πrL
式中Vin和Vout分别为灌入和收集的供试液体积(mL);Cin和Cout分别为进口和出口处缓冲液中的药物质量浓度(g·L-1);L和r分别为被考察肠段长度(cm)和半径(cm);Qin为灌流速度(0.2mL·min-1);Ka和Papp为6个时间点(0.25~2h)样品的平均值。肠吸收数据处理后用统计分析软件SPSS 21.0进行方差分析。
3 实验结果
3.1空白干扰实验通过比较空白肠灌流液,含人参皂苷Rb3的肠灌流液和人参皂苷Rb3标准品溶液的色谱图,结果表明,在上述色谱条件下,样品与人参皂苷Rb3对照品在相应位置有相似的吸收峰,而空白对照在药物出峰处基线平稳,对药物测定无任何干扰(图2)。

3.2人参皂苷Rb3在灌流液中稳定性3份溶液中人参皂苷Rb3的峰面积在6h内RSD分别为1.6%、1.3%、1.7%,表明6 h内在37 ℃的供试液中人参皂苷Rb3稳定性良好。
3.3恒流泵管道对人参皂苷Rb3吸附情况恒流泵的管道是硅胶管道,有一定物理吸附作用。根据恒流泵管道对人参皂苷Rb3的物理吸附情况考察结果,各时间点人参皂苷Rb3的峰面积RSD均<2.0%。通过计算人参皂苷Rb3浓度,发现前0.75h收集到的灌流液,测得药物浓度略低于所配溶液的浓度,而在后0.45h收集的灌流液,所测得药物浓度逐渐达到平衡,计算出的平衡浓度为配制的溶液浓度的(99.5±0.8)%。说明硅胶管道对人参皂苷Rb3有一定的物理吸附作用,且在0.75h时硅胶管道对人参皂苷Rb3的吸附作用可能达到饱和。3.4人参皂苷Rb3肠吸收用K试液分别配制高、中、低(分别为90、60、30 mg·L-1)3种不同质量浓度的人参皂苷Rb3溶液,按照2.5项下的方法对4个小肠分段灌流,研究在不同小肠分段吸收速率常数(Ka)和表观渗透系数(Papp)。实验结果如表3所示,表明人参皂苷Rb3可在全肠道被吸收,但在十二指肠的吸收速率最高,而在结肠中的吸收速率最低,其中在不同肠段中的吸收速率常数Ka大小顺序是十二指肠>空肠≈回肠>结肠,表观渗透系数Papp大小顺序是十二指肠>空肠>回肠≈结肠。对各肠段参数进行方差分析,十二指肠的吸收速率和渗透性显著高于其他3个肠道(P<0.05),回肠、结肠之间无统计学差异。在30~90mg·L-1,在不同浓度时, 吸收速率常数也有显著性差异。对不同浓度下的吸收速率常数进行单侧t检验,结果:低浓度>中浓度≈高浓度(P<0.05),实验证明, 药物浓度对Rb3在全肠道的吸收速率是有一定的影响的,说明Rb3大鼠肠道吸收存在饱和现象,提示其在机体内的转运机制不仅仅是简单的被动扩散过程,可能还有主动转运或促进扩散也参与其中。

表3 不同浓度人参皂苷Rb3在不同肠段的吸收参数 ±s,n=5)
4 讨论
研究药物在肠道吸收的方法很多,在体法能较真实地反映肠道的生理环境,实验操作简单易行,技术成熟可靠。对药物的小肠吸收研究常常采用在体肠循环灌流法及单向灌流法[8]。本研究采用大鼠在体单向肠灌流法,其实验条件与口服给药后药物接触的肠道正常生理环境较接近。由于动物个体间的差异性,在体单向肠灌流实验对受试动物的数目有要求,即必须具有一定数量的实验动物以保证足够小的变异。本实验每个肠段都采用了5只大鼠的实验数据,保证了数据的真实可靠[9]。
在体单向肠灌流法对要考察的某一肠段,以较低的灌流速度(0.2~0.3mL·min-1)进行单向灌流,其吸收速率稳定[10],本实验选择大鼠肠灌流速度为0.2mL·min-1。
单向灌流模型中,肠道对水分的吸收往往会导致灌流液体积随时间的变化而改变,有报道[11]采用吸收差的物质如酚红作为灌流液体积标记的标示物。但是长时间灌流酚红也存在一定程度的吸收,且酚红可能干扰某些化合物的肠道转运和分析测定,14C标记的PEG存在放射性和安全性问题[12],检测方法的复杂性限制了其在普通实验室的应用。Sutton等[13-14]采用单向灌流模型,对重量法、酚红法和14C-PEG-3350法进行了比较,结果表明重量法能显著减少实验误差,可作为大鼠单向灌流实验在体肠循环吸收实验中矫正灌流液体积的有效方法。故本实验采用具有较高准确度的重量法来标定灌流液体积的变化。
药物分子的物理性质对其体内过程的行为起着重要作用[7],药物分子结构与其物理性质与其体内生物利用度之间有一个“五规则”的联系[15],即大多数药物分子的lgP≤5,相对分子质量≤500,氢键受体(氧原子和氮原子总数)≤10,氢键供体≤5,如果违背了1条以上规则,则该药物分子存在体内生物利用度问题。人参皂苷Rb3相对分子质量为1078,违背“五规则”,理论推测人参皂苷Rb3生物利用度较低,此结论也与文献[16]报道的药动实验结果(0.54%)一致。
综上研究人参皂苷Rb3为低渗透性,高溶解度的药物,即吸收的限速过程是药物的渗透过程,在制备其口服制剂时可采用改善药物脂溶性的方法以提高其生物利用度,因此本实验对人参皂苷Rb3的口服剂型的设计具有一定的指导意义。由于本实验在药物灌流之前先用生理盐水冲洗了肠道使得多数菌群可能在循环前已随肠内容物一起被清除,因此小肠菌群代谢对人参皂苷Rb3肠吸收的影响情况还需进行进一步的研究。
[1]国家药典委员会. 中华人民共和国药典一部[M].北京:中国医药科技出版社, 2015: 11.
[2]宋建平,曾江,崔秀明,等. 三七根茎的化学成分研究(Ⅱ)[J]. 云南大学学报,2007,29 (3) : 287.
[3]朱洁,杨蓉,张洪彬. HPLC-ELSD法测定三七叶中人参皂苷Rb3、Rc、Rb1的含量[J]. 中草药,2004,35 (12) : 1365-1366.
[4]周伟,狄留庆,毕肖林,等. 双黄连口服液中有效成分的大鼠在体肠吸收研究[J]. 中国中药杂志,2011,36 (13) : 1733-1738.
[5]王小潘,吕慧侠,Ayman Y Waddad,等. 藤黄酸大鼠在体肠吸收动力学的研究[J]. 中国中药杂志,2012,37 (14) : 2081.
[6]刘馨,张建军,周建平. 马洛替酯单向灌流法大鼠在体肠吸收机制研究[J]. 抗感染药学,2011,8 (2) : 100-103.
[7]何承华,张振海,王舒,等. 芹菜素大鼠在体肠吸收动力学的研究[J]. 中国中药杂志,2013,38 (9) : 1416-1420.
[8]张艳,王平,王进荣,等. 在体单向肠灌流模型研究大黄素的大鼠肠吸收特性[J]. 中药新药与临床药理,2012,23 (3) : 286-290.
[9]陈新民,李俊松,李文,等. 五味子有效成分的大鼠在体单向灌流肠吸收[J]. 药学学报,2010,45 (5) : 652-658.
[10]王进荣,王平. 单向灌流法评价芦荟大黄素大鼠体内肠吸收的研究[J]. 中国中药杂志,2011,36 (17) : 2396.
[11]冯亮,蒋学华,周静,等. 三七皂苷R1和人参皂苷Rg1的大鼠在体肠吸收动力学研究[J]. 中国药学杂志,2006,41 (14) : 1097-1102.
[12]李凌军,李季,娄华伟. 天钩降压胶囊中黄芩苷大鼠在体肠吸收研究[J]. 中国中药杂志,2013,38 (6) : 894-898.
[13]Sutton S C,Rinaldi M T,Vukovinsky K E. Comparison of the gravimetric, phenol red and 14C-PEG-3350 methods to determine water absorption in the rat single-pass intestinal perfusion model[J]. AAPS Pharm Sci Tech,2001,3 (3) : E25.
[14]Issa C,Piyush Gupta P,Bansal A K,et al. Implications of densitycorrection in gravimetric method for water flux determinationusing rat single-pass intestinal perfusion technique: a technicalote[J]. AAPS Pharm Sci Tech,2003,4 (2) : E16.
[15]Lipinski C A,Lombardo F,Dominy B W,et al. Experimental and computational approaches to estimate solubility and permeabilityin drug discovery and development settings[J]. Adv Drug Deliv Rev,1997,23 (1/3) : 3.
[16]Jie Z,Chang S,Yang C,et al. Determination of ginsenosides Rb 1, Rb 2, and Rb3, in rat plasma by a rapid and sensitive liquid chromatography tandem mass spectrometry method: Application in a pharmacokinetic study[J]. Planta Medica,2012,64-65(3):94-97.
(编辑:梁志庆)
Studies on absorption of Ginsenoside Rb3 in Rat Intestine by in situ single pass intestine perfusion model
SHEN JiaweiCAO Xiuqin*
Minhang branch, Shanghai university of traditional Chinese medicine affiliated yueyang hospital, Shanghai 200241,China
Objective To investigate the absorption kinetics of ginsenoside Rb3 at different intestinal segments of rats and the influence of concentration on the absorptive kinetics. Methods An in situ intestinal perfusion model was applied to investigate systemically the absorptive kinetics of ginsenoside Rb3.Results The absorptive rate constants (Ka) of ginsenoside Rb3 at different intestinal segments was duodenum > jejunum ≈ ileum > colon. The Ka of ginsenoside Rb3 at the concentrations of low, medium, high levels was low > medium ≈ high level.Concluslon Ginsenoside Rb3 was well absorbed at the whole segment of intestine in rats, among which duodenum was the fastest. The absorption rate decreased with the increasing concentration of ginsenoside Rb3, implied that the absorption mechanism was mainly the passive diffusion, facilitated diffusion and active transport mechanism.
Ginsenoside Rb3; In Situ Intestinal Absorptive Model;Absorptive Promoter
2016-06-24
沈佳伟(1986-),男,汉族,在读硕士,主管中药师,研究方向为中药化学成分分析。E-mail:redfenix@126.com
曹秀琴(1972-),女,汉族,本科,副主任药师,研究方向为分析化学。E-mail:caoxqin@163.com
R965.1
A
1007-8517(2016)17-0037-05
