H PLC测定盐酸帕洛诺司琼原料药中光学异构体
2016-08-03曹天海昆明积大制药股份有限公司国际GMP认证部云南昆明650106
曹天海(昆明积大制药股份有限公司国际GMP认证部,云南 昆明 650106)
H PLC测定盐酸帕洛诺司琼原料药中光学异构体
曹天海
(昆明积大制药股份有限公司国际GMP认证部,云南 昆明 650106)
目的:建立高效液相色谱法测定盐酸帕洛诺司琼中光学异构体含量的方法。方法:对于非对映异构体,采用C18色谱柱,以乙腈-25 mmol/L磷酸二氢钠溶液(含0.1%三乙胺,用磷酸调pH值至4.0)(25∶75)为流动相;对于对映异构体,采用Chiralcel,OD-RH色谱柱,以100 mmol六氟磷酸钾水溶液-乙腈(70∶30)为流动相;非对映异构体和对映异构体检测波长分别为217 nm和240 nm。结果:盐酸帕洛诺司琼4个异构体线性关系良好,定量限和检测限、方法回收率满足要求。结论:本法灵敏、可靠,可用于盐酸帕洛诺司琼中光学异构体的质量控制。
盐酸帕洛诺司琼;高效液相色谱;光学异构体;测定
盐酸帕洛诺司琼(palonosetron hydrochloride),化学名(3aS)-2-[(3S)-1-氮杂双环[2.2.2]辛烷-3-基]-2,3,3a,4,5,6-六氢-1-氧代-1H-苯并[de]异喹啉盐酸盐(图1)。盐酸帕洛诺司琼注射液是5-HT3受体拮抗剂,用于预防在实施中度或高度致呕吐性化疗方案时所引起的急性和迟发性呕吐,2003年由美国食品药品监督管理局(FDA)批准在美国上市。盐酸帕洛诺司琼分子中含有2个手性中心,应存在一个对映体(RR-异构体)和一对非对映体(SR-异构体和RS-异构体)。本文建立了高效液相色谱法(HPLC)测定盐酸帕洛诺司琼中光学异构体的方法,采用普通反相色谱法测定非对映异构体,采用手性固定性拆分了对映异构体,结果表明本方法准确、灵敏、可靠。
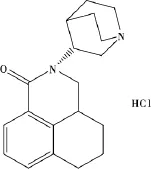
图1 盐酸帕洛诺司琼结构式
1仪器与试药
岛津 LC-2010CHT高效液相色谱仪,包括CLASS-VP色谱工作站(日本岛津公司);戴安Summit P680高效液相色谱仪,包括Chameleon色谱工作站。
盐酸帕洛诺司琼(批号:130901,130902,131001)、盐酸帕洛诺司琼SS、RR、SR、RS对照品(均由昆明积大制药股份有限公司提供);乙腈为色谱纯、水为重蒸馏水、其余试剂均为分析纯。
2方法与结果
2.1溶液配制
取本品适量,精密称定,加水制成每1 mL中含0.06 mg的溶液,作为供试品溶液。
取供试品溶液1 mL,加水溶解并稀释制成100 mL,作为对照溶液。
2.2色谱条件
色谱柱:Kromasil C18(4.6 mm ×250 mm,5 μm)(Akzo Nobel公司),用于测定非对映异构体,Chiralcel,OD-RH(4.6 mm ×150 mm,5 μm)(大赛璐公司),用于测定对映异构体;流动相:乙腈-25 mmol/L磷酸二氢钠溶液(含0.1%三乙胺,用磷酸调pH值至4.0)(25∶75),用于测定非对映异构体,100 mmol六氟磷酸钾水溶液-乙腈(70∶30)用于测定对映异构体;流速:1.0 mL/min用于测定非对映异构体,0.6 mL/min用于测定对映异构体;柱温:30℃;检测波长:217 nm用于测定非对映异构体,240 nm用于测定对映异构体;进样量:50 μL用于测定非对映异构体,50 μL用于测定对映异构体。理论塔板数按盐酸帕洛诺司琼计算应不低于1 500。测定非对映异构体时,本品与盐酸帕洛诺司琼SR-异构体的分离度不得低于1.0;测定对映异构体时,本品及盐酸帕洛诺司琼RR-异构体的分离度不得低于1.5。

图2 非对映异构体HPLC图
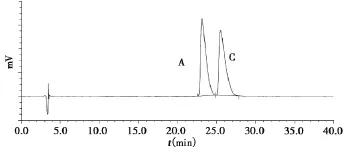
图3对映异构体HPLC图
2.3波长选择
取盐酸帕洛诺司琼对照品、盐酸帕洛诺司琼SR-异构体、盐酸帕洛诺司琼 RS-异构体及盐酸帕洛诺司琼RR-异构体对照品分别加水制备成每1 mL中约含20 μg的溶液,测定各对照品的紫外吸收光谱,结果表明各对照品在240 nm附近处均有较强吸收,考虑到本品非对映异构体测定色谱条件与有关物质测定的色谱条件一致,因此选用有关物质的测定波长217 nm测定非对映异构体,选定240 nm作为对映异构体的检测波长。
2.4专属性
2.4.1非对映异构体取盐酸帕洛诺司琼对照品、盐酸帕洛诺司琼SR-异构体、盐酸帕洛诺司琼RS-异构体对照品各适量,加水分别制成0.06 mg/mL的溶液;分别取上述溶液各50 μL,记录色谱图,盐酸帕洛诺司琼保留时间为9.942 min,盐酸帕洛诺司琼SR-异构体保留时间为9.453 min,盐酸帕洛诺司琼RS-异构体保留时间为9.391 min。取盐酸帕洛诺司琼对照品和盐酸帕洛诺司琼SR-异构体对照品各适量,加水制成每 1 mL含盐酸帕洛诺司琼对照品0.06 mg和盐酸帕洛诺司琼SR-异构体对照品0.000 3 mg的溶液,作为非对映异构体测定系统适用性试验溶液,取上述溶液50 μL,记录色谱图,本品及盐酸帕洛诺司琼分离度为1.26,达到基线分离,符合要求。取盐酸帕洛诺司琼RS-异构体及SR-异构体溶液各0.5 mL,混匀,取上述溶液各50 μL,记录色谱图,得到一个色谱峰,说明盐酸帕洛诺司琼RS-异构体及SR-异构体出峰位置相同,可以合并计算。
2.4.2对映异构体取盐酸帕洛诺司琼对照品、盐酸帕洛诺司琼RR-异构体各适量,加水分别制成0.06 mg/mL的溶液;分别取上述溶液各50 μL,记录色谱图,盐酸帕洛诺司琼保留时间为23.479 min,盐酸帕洛诺司琼RR-异构体保留时间为25.521 min。取盐酸帕洛诺司琼及盐酸帕洛诺司琼RR-异构体溶液各0.5 mL,混匀,作为系统适用性溶液,取上述溶液50 μL,记录色谱图,本品及盐酸帕洛诺司琼RR-异构体分离度为 1.68,达到基线分离,符合要求。
2.5精密度
2.5.1非对映异构体取“2.4.1”中系统适用性溶液,连续进样6次,计算盐酸帕洛诺司琼对照品与非对映异构体(SR)主峰的RSD值,分别为2.9% 和2.0%,均小于3.0%。
2.5.2对映异构体取“2.4.2”中系统适用性溶液,连续进样6次,计算盐酸帕洛诺司琼对照品与对映异构体(RR)主峰的RSD值,分别为0.3%和0.4%,均小于2.0%。
2.6检测限与定量限
按信噪比为3∶1得出检测限,信噪比为10∶1得出定量限。
2.6.1非对映异构体盐酸帕洛诺司琼和SR-异构体检测限分别为0.005 6 μg/mL和0.006 1 μg/mL;定量限分别为0.016 8 μg/mL和0.018 3 μg/mL;盐酸帕洛诺司琼RS-异构体检测限为0.005 5 μg/mL,定量限为0.016 5 μg/mL。
2.6.2对映异构体盐酸帕洛诺司琼和盐酸帕洛诺司琼RR-异构体定量限分别为0.036 μg/mL和0.036 μg/mL,检测限为0.012 μg/mL及0.012 μg/mL。
2.7线性和范围及相对响应因子
2.7.1非对映异构体分别取“2.4”专属性中盐酸帕洛诺司琼对照品及盐酸帕洛诺司琼SR-异构体溶液各 0.2,0.4,0.6,0.8,1.0,1.2 mL,分别置于100 mL量瓶中,以水稀释至刻度。分别取50 μL进样,记录色谱图,计算各种物质的相关系数。得出盐酸帕洛诺司琼线性范围为 0.000 122~0.000 732 mg/mL,回归方程为:
y=1 464.87x+0.006 1,
相关系数为0.999 0;盐酸帕洛诺司琼SR-异构体线性范围为0.000 112~ 0.000 672 mg/mL,回归方程为:
y=1 302.09x-0.017,
相关系数为0.999 9。同法得出盐酸帕洛诺司琼RS-异构体线性范围为0.000 22~0.000 66 mg/mL,回归方程为:
y=1 489.73x-0.004,
相关系数为0.998 7。分别以盐酸帕洛诺司琼SR-异构体和盐酸帕洛诺司琼RS-异构体回归方程的斜率除以盐酸帕洛诺司琼回归方程的斜率,得到盐酸帕洛诺司琼SR-异构体和盐酸帕洛诺司琼RS-异构体对盐酸帕洛诺司琼相对响应因子分别为0.9和1.0,均为0.9~ 1.1,说明可以用盐酸帕洛诺司琼自身对照溶液代替盐酸帕洛诺司琼SR-异构体和盐酸帕洛诺司琼RS-异构体作为对照溶液。
2.7.2对映异构体分别精密移取“2.4.2”中盐酸帕洛诺司琼对照品溶液、盐酸帕洛诺司琼RR-异构体对照品溶液各0.2,0.4,0.6,0.8,1.0,1.2 mL,分别置于100 mL容量瓶中,加水稀释至刻度。分别取50 μL进样,得出盐酸帕洛诺司琼线性范围为0.000 125~ 0.000 752 mg/mL,回归方程为:
A=108 906 199C-1 979.17,
相关系数为0.999 6;盐酸帕洛诺司琼RR-异构体线性范围为0.000 124~ 0.000 743 mg/mL,回归方程为:
A=109 708 146C-2 394.363,
相关系数为0.999 8。分别以盐酸帕洛诺司琼RR-异构体回归方程的斜率除以盐酸帕洛诺司琼回归方程的斜率,得到盐酸帕洛诺司琼RR-异构体对盐酸帕洛诺司琼相对响应因子为 1.0,处于0.9~ 1.1之间,说明可以用盐酸帕洛诺司琼自身对照溶液代替盐酸帕洛诺司琼RR-异构体为对照溶液。
2.8准确度
2.8.1非对映异构体取本品已测定非对映异构体的原料药 1批(130901),加水制成每1 mL中含有0.6 mg盐酸帕洛诺司琼的溶液,分别精密移取 10 mL,置 100 mL量瓶中,共制备 9份,分别加入浓度为0.055 mg/mL的盐酸帕洛诺司琼SR-异构体溶液各0.40,0.50,0.60 mL各3份,依法测定,平均回收率为96.3%,RSD为3.0%。
2.8.2对映异构体取本品已测定对映异构体的原料药 1批(130901),加水制成每1 mL中含有0.6 mg盐酸帕洛诺司琼的溶液,分别精密移取10 mL,置100 mL量瓶中,共制备9份,分别加入浓度为0.048 5 mg/mL的盐酸帕洛诺司琼RR-异构体溶液0.40,0.50,0.60 mL各3份;依法测定,平均回收率为95.7%,RSD为3.2%。
2.9样品测定
本品 3批样品(130901,130902,131001)非对映异构体测定结果分别为0.05%,0.05%,0.04%;对映异构体测定结果均未检出。
3讨论
据文献报道[1],盐酸帕洛诺司琼的合成路线有4条,无论采用哪条路线,均需测定本品光学异构体的含量。
文献[2]已经报道了本文中非对映异构体测定方法的色谱条件,但是仅用于本品中有关物质的测定,没有发现此色谱条件也可用于非对映异构体的测定。
目前,文献[3-6]报道的测定盐酸帕洛诺司琼光学异构体的方法主要为正相色谱法,方法的检测灵敏度与本法相比较差。
本方法快速、简便,所用的色谱条件均为反相色谱条件,也可直接用于本品注射液中光学异构体的测定,无需因注射液辅料中含有大量无机盐而进行前处理。
[1]杨新华,欧阳强.盐酸帕洛诺司琼合成路线图解[J].中国医药工业杂志,2009,40(3):231-233.
[2]沈曦,周慧,王万青,等.反相高效液相色谱法检测盐酸帕洛诺司琼及其有关物质[J].中国现代应用药学,2007,24(4):307-308.
[3]于晓蓉,宋敏,杭太俊.盐酸帕洛诺司琼光学异构体的手性HPLC检查[J].中国新药杂志,2008,17(10):870-872.
[4]李霞,高媛,胥娜,等.手性拆分法同时测定盐酸帕洛诺司琼光学异构体[J].中南药学,2015,13(4):406-409.
[5]赵慧英,李桂萍,吴敬飞,等.盐酸帕洛诺司琼3个光学异构体的分离与测定[J].药物分析杂志,2012,32(6):978-980.
[6]潘红娟,杨哲峰,时惠麟,等.盐酸帕洛诺司琼注射液中异构体含量的 NP-HPLC测定[J].中国医药工业杂志,2009,40(8):610-612.
Determination of Isomers and Enantiomer in Palonosetron Hydrochloride by HPLC
Cao Tianhai(International GMP Certification Department,Kunming Jida Pharmaceutical Co.,Ltd.,Yunnan Kunming 650106,China)
Objective:To develop a HPLC method for determination of isomers and enantiomer in palonosetron hydrochloride.Methods:Isomers were determined by a C18column with the mobile phase of 25 mmol/L sodium dihydrogen phosphate buffer(containing 0.1%triethylamine,of which pH value was adjusted to 4.0 by phosphoric acid)-acetonitrile(75∶25).However,enantiomers were determined by a Chiralcel,OD-RH column with the mobile phase of 100 mmol potassium hexafluorophosphate solution-acetonitrile(70∶30).The wavelengths for detection of isomers and enantiomers were 217 and 240 nm respectively.Results:The calibration curve of isomers and enantiomers of palonosetron hydrochloride showed good linearity,while the LOQ,LOD and accuracy met the relevant requirements.Conclusion:The developed methods was sensitive and reliable,which might be used for the quality control of isomers and enantiomer in palonosetron hydrochloride.
Palonosetron Hydrochloride;HPLC;Optical Isomer;Determination
10.3969/j.issn.1672-5433.2016.05.007
曹天海,男,硕士,工程师。主要从事药物研发工作。E-mail:skyrin_jida@126.com
2016-02-14)
