紫外-可见吸收光谱法研究阴离子对刚果红/β-葡聚糖络合物的影响
2016-07-12吴小燕李琳琳王汉源
吴小燕,赵 兰,李琳琳,李 健,王汉源,吴 佳
福州大学生物科学与工程学院,福建 福州 350116
紫外-可见吸收光谱法研究阴离子对刚果红/β-葡聚糖络合物的影响
吴小燕,赵 兰,李琳琳,李 健,王汉源,吴 佳*
福州大学生物科学与工程学院,福建 福州 350116
利用紫外-可见吸收光谱法探究了阴离子的浓度及种类对刚果红在溶液中形成聚集体的影响,在此基础之上,进一步研究了阴离子浓度和种类对刚果红与燕麦β-葡聚糖所形成络合物的影响规律。结果表明: 随着阴离子浓度的增大,刚果红溶液的峰值吸光度呈逐渐下降趋势,且最大吸收波长发生蓝移。刚果红最大吸收波长、峰值吸光度和499 nm处吸光度与阴离子浓度的对数值之间具有明显的线性相关性。阴离子对刚果红聚集的影响符合Hofmeister序列的顺序,说明疏水相互作用是刚果红分子聚集成胶束的重要驱动力。对于刚果红/β-葡聚糖络合物体系来说,当阴离子浓度超过第一临界浓度时,刚果红胶束开始形成并结合在β-葡聚糖上形成络合物,差谱图在556 nm处产生了络合物的吸收峰;当阴离子浓度超过第二临界浓度时,刚果红/β-葡聚糖络合物进一步通过刚果红胶束之间的聚集形成超分子结构,导致差谱图吸收峰红移至583 nm处,并因为更大尺寸超分子结构的形成而在光谱图长波方向出现明显的米氏散射效应。阴离子对上述超分子结构的影响也符合Hofmeister序列的顺序,说明刚果红/β-葡聚糖络合物主要通过刚果红胶束之间的疏水相互作用聚集成超分子结构。本研究提示,离子对刚果红分子本身在溶液中的聚集状态及其与生物大分子的相互作用具有重要的影响。
紫外可见吸收光谱法;阴离子;刚果红;燕麦β-葡聚糖;聚集
引 言
偶氮染料刚果红可与纤维素类物质紧密结合,早期曾广泛应用于织物的染色[1-2]。刚果红也被广泛用于生物染色,国内外已有大量学者通过刚果红染色法研究淀粉样蛋白的结构和特性[3-5]。某些小分子物质可以与刚果红发生络合反应,已应用于测定铜、硝酸根及贵金属的分离富集[6-8]。刚果红与某些分子结合导致复合物的形成和散射光强度的增大,据此也可以应用于特定分子的浓度测定[9]。
刚果红分子结构如图1所示。有文献报道刚果红水溶液在较低浓度即可聚集形成胶束[10]。刚果红胶束的结构不仅与其分子排列有关,还受到温度、离子强度的影响[11]。
燕麦β-葡聚糖是一种水溶性线型多糖,具有调节血糖、降低胆固醇、提高免疫力等生理功能。Wood等[12]最早提出利用刚果红与燕麦β-葡聚糖结合后溶液吸光度增大的现象可以定量测定燕麦β-葡聚糖,该方法简便易行,得到了较为广泛的应用[13]。本研究在应用刚果红法测定燕麦β-葡聚糖时发现,缓冲液的浓度对两者的结合有显著影响。在此发现的基础之上,重点研究了阴离子种类及浓度对刚果红溶液本身以及刚果红/燕麦β-葡聚糖络合物紫外-可见吸收光谱的影响规律。
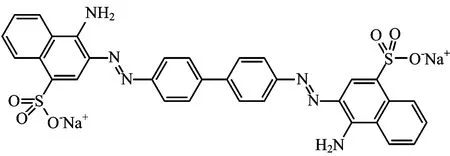
图1 刚果红的分子结构示意图
1 实验部分
1.1 仪器与试剂
紫外-可见吸收光谱用Cary 50 Bio光谱仪测定,使用光径为1 cm的石英比色皿。燕麦β-葡聚糖为本实验室从燕麦中提取,纯度>90%;刚果红购于日本TCI公司,纯度>98%;其他试剂均为分析纯。
1.2 方法
1.2.1 阴离子对刚果红的影响
分别移取2 mL不同浓度的各盐溶液于试管中,加入22.5 μg·mL-1的刚果红水溶液4 mL。立即涡旋振荡10 s,反应30 min后进行紫外-可见光扫描。以不加盐的刚果红溶液为空白对照,每个试验均做3个平行。
1.2.2 阴离子对刚果红/β-葡聚糖络合物的影响
分别在试管中加入0.48 mL的β-葡聚糖溶液和1.52 mL的不同浓度的盐溶液,再加入4 mL刚果红溶液,立即振荡10 s,静置30 min后进行紫外-可见光扫描。以不加β-葡聚糖和盐的刚果红溶液为空白组,每个试验均做3个平行。
2 结果与讨论
选取了Na2SO4,NaCl和NaSCN三种钠盐,其中的阴离子分别处于Hofmeister序列的前、中和后位置。在序列中靠前的离子会增加溶剂的表面张力,降低非极性基团的溶解度,实质上是增强了疏水相互作用。相反的,在序列中靠后的离子减弱了疏水相互作用。Hofmeister序列的影响不仅仅限于蛋白质,还表现在对其他分子,例如多糖等大分子和染料等小分子的影响,且影响规律通常符合Hofmeister序列的顺序。
2.1 阴离子对刚果红溶液的影响
2.1.1 阴离子对刚果红紫外-可见吸收光谱的影响


图2 刚果红在不同浓度Cl-溶液中的吸收光谱

图3 阴离子浓度和类型对刚果红溶液的λmax (a), A499 (b)和Amax (c)的影响
2.1.2 阴离子对刚果红光谱参数的影响
随着盐浓度的增大,刚果红溶液的最大吸收峰波长λmax发生了蓝移,为探究波长的变化程度与阴离子浓度间的关系,将刚果红的λmax与阴离子浓度对数值作图得图3(a),结果表明两者之间存在线性关系,说明增加盐离子浓度促进了刚果红分子形成聚集体,导致吸收峰向短波方向移动。刚果红水溶液的最大吸收波长位于499 nm,对应着刚果红单体的吸收。随着阴离子浓度的增大刚果红在499 nm处的吸光度A499逐渐下降[图3(b)],两者之间呈负的线性相关,说明刚果红单体浓度随盐离子浓度的增加而下降,部分刚果红分子在盐离子的作用下聚集成为胶束结构。随着阴离子浓度的增大,刚果红溶液的峰值吸光度Amax不断下降[图3(c)],且Amax与阴离子浓度的对数值之间存在线性关系,反映出盐浓度增加促进了刚果红聚集体的形成。

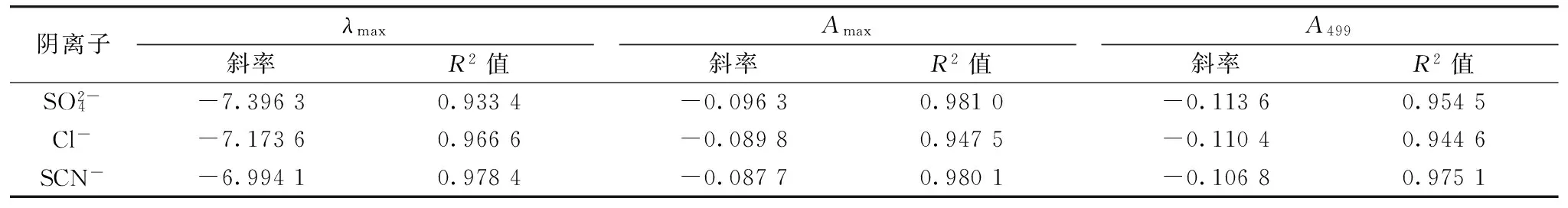
表1 光谱参数与阴离子浓度对数值间回归直线的斜率和R2
2.2 阴离子对络合物紫外-可见吸收光谱的影响
刚果红/β-葡聚糖络合物在NaCl溶液中的紫外-可见吸收光谱如图4(a)所示,可以看出,Cl-对刚果红/β-葡聚糖络合物的影响规律比较复杂。需要指出的是,图中纵坐标为络合物与单独刚果红溶液之间的吸光度之差ΔA,即两者的差谱。为了方便说明,对499,556和583 nm处光谱的变化分别进行讨论。刚果红单体对应的499 nm处ΔA随着Cl-浓度的增加而不断下降,说明盐离子的加入促进了刚果红胶束的形成,导致刚果红单体浓度的降低。556 nm处的吸收峰对应结合于β-葡聚糖上的刚果红胶束,其吸光度的变化如图4b所示,当Cl-浓度低于0.005 mol·L-1时,ΔA556接近于0;当Cl-浓度介于0.01~0.1 mol·L-1时,ΔA556上升至0.1以上;当Cl-浓度为0.2 mol·L-1时,ΔA556急剧下降至小于0;随着Cl-浓度增加至0.4 mol·L-1以上,ΔA556呈上升趋势,在较高离子浓度时ΔA556又回到0以上。当Cl-浓度小于0.2 mol·L-1时ΔA的峰值位于556 nm处,当Cl-浓度增加至0.4 mol·L-1时ΔA的峰值移动至583 nm处。
从图4(b)容易看出,存在两个Cl-临界浓度,第一个临界浓度在0.005 mol·L-1附近,是ΔA在556 nm处出现明显吸收峰的分界点。从图2可以发现,当Cl-浓度为0.005 mol·L-1时,刚果红的光谱曲线刚好可以与纯水中的光谱曲线区分开来,表明0.005 mol·L-1的Cl-浓度很可能是引起刚果红分子聚集形成胶束的最低浓度,此时溶液中的刚果红胶束开始结合于β-葡聚糖上形成络合物,在差谱图的556 nm处产生一个吸收峰[图4(a)]。第二个临界浓度在0.200 mol·L-1附近,是ΔA在583 nm处出现明显吸收峰的分界点。此时ΔA在556 nm处的吸收峰消失,在583 nm处出现了新的吸收峰。以上变化表明,当NaCl浓度达到0.200 mol·L-1时,刚果红分子上的电荷被进一步屏蔽,致使刚果红/β-葡聚糖络合物之间借助刚果红的聚集而形成更大的超分子结构,导致吸收峰的红移,且在光谱的长波方向产生了明显的米氏散射效应[15][图4(a)]。
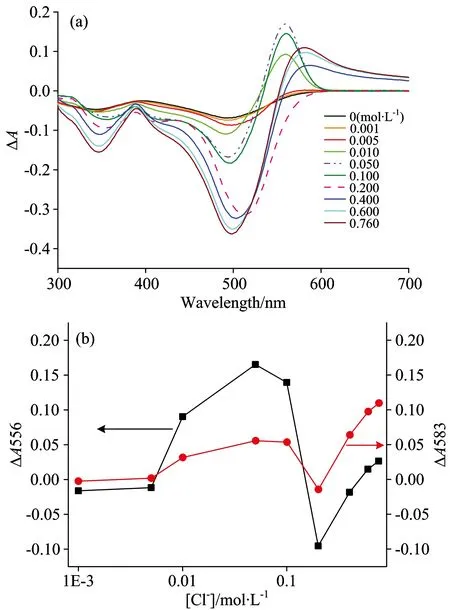
图4 Cl-浓度对刚果红/β-葡聚糖络合物的差谱(a), ΔA556和ΔA583(b)的影响
Fig.4 The effect of Cl-concentration on the difference spectra (a), ΔA556and ΔA583(b) of Congo red/β-glucan complex
3 结 论
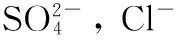
[1] Purkait M K,Maiti A,DasGupta S,et al. Journal of Hazardous Materials,2007,145(2): 287.
[2] Samiey B,Dargahi M R.Central European Journal of Chemistry,2010,8(4): 906.
[3] LIN Yu,CHEN Jun-pao,LIU Ling-juan,et al(林 煜,陈俊抛,刘凌娟,等). Chinese Journal of Neurology(中华神经科杂志),2000,33(4): 207.
[4] Barbara S,Barbara P,Leszek K,et al. Acta Biochimica Polonica,2003,4: 1213.
[5] Lendel C,Bertoncini C W,Cremades N,et al. Biochemistry,2009,48: 8322.
[6] MEN Rui-zhi,LIU Mei,CHENG Xin-min,et al(门瑞芝,刘 梅,程新民,等). Metallurgical Analysis(冶金分析),1988,18(3): 5.
[7] YANG Yi,GUO Guang-sheng,WANG Zhi-hua,et al(杨 屹,郭广生,王志华,等). Journal of Beijing University of Chemical Technology(北京化工大学学报),1999,26(3): 73.
[8] ZHANG Kai,SUN Qi-zhi,LIANG Hong-wei,et al(张 凯,孙其志,梁宏伟,等). Chinese Journal of Analysis Laboratory(分析试验室),1997,16(6): 40.
[9] LIU Shao-pu,HU Xiao-li,LIU Zhong-fang,et al(刘绍璞,胡小莉,刘忠芳,等). Science in China Series B: Chemistry(中国科学B辑化学),2006,36(4): 317.
[10] Maltsev A S,Grishaev A,Bax A.Biochemistry,2012,51: 631.
[11] Skowronek M,Stopa B,Konieczny L,et al.Biopolymers,1998,46: 267.
[12] Wood P J,Fulcher R G,Stone B A.Journal of Cereal Science,1983,1: 95.
[13] ZHANG Juan,DU Xian-feng,RAO Yan-qin(张 娟,杜先锋,饶砚琴). Journal of Anhui Agricultural University(安徽农业大学学报),2007,34(1): 23.
[14] Spano F C. Accounts of Chemical Research,2010,43(3): 429.
[15] Auweter H,Haberkorn H,Heckmann W,et al.Angewandte Chemie International Edition,1999,38(15): 2188.
(Received Oct. 9, 2015; accepted Feb. 25, 2016)
*Corresponding author
Characterization of the Effect of Anion on the Complex of Oat β-Glucan and Congo Red with UV-Vis Absorption Spectroscopy
WU Xiao-yan, ZHAO Lan, LI Lin-lin, LI Jian, WANG Han-yuan, WU Jia*
College of Biological Science and Engineering, Fuzhou University, Fuzhou 350116, China
The effects of concentration and type of anions on aggregation of Congo red in solution were studied with UV-Visible spectroscopy. And the influence of anions on the complex of Congo red and oat β-glucan was further studied. The results showed that the maximum absorption wavelength of Congo red in aqueous solution shifted toward the shorter wavelength, and the absorbency lowered considerably with increasing ionic concentration. There was a significant linear correlation between logarithm of anion concentration and the maximum absorption wavelength, with the peak absorbance, and the absorbance at 499 nm. The influence of anions on aggregation of Congo red was in accordance with Hofmeister series, indicating that hydrophobic interaction is an important driving force for Congo red molecules to assemble into micelles. As for the complexation of Congo red and oat β-glucan, when the concentration of anions exceeded the first critical concentration, the micelle of Congo red began to form and then combined to β-glucan. The absorption peak of the complex presented at 556 nm. When the concentration of anions exceeded the second critical concentration, the complex was developed into supramolecular structure through aggregation of Congo red micelles on Congo red/β-glucan complex, which resulted in the shift of absorption peak toward 583 nm. And the presence of Mie scattering effects at the longer wavelength indicated the formation of larger supramolecular structure. The effect of anions on the above supramolecular structures also followed the order of Hofmeister series, showing that the aggregation of Congo red/β-glucan complex into supramolecular structure was mainly driven through hydrophobic interactions between Congo red micelles on the complex. The research indicated that ions had an important effect on the aggregation of Congo red and the interaction between biopolymers and Congo red.
UV-Vis spectroscopy; Anion; Congo red; Oat β-glucan; Aggregation
2015-10-09,
2016-02-25
国家自然科学基金项目(31101224),福建省自然科学基金项目(2013J05049)资助
吴小燕,女,1991年生,福州大学生物科学与工程学院硕士研究生 e-mail: fzuerwxy@163.com *通讯联系人 e-mail: wujia@fzu.edu.cn
O657.3
A
10.3964/j.issn.1000-0593(2016)11-3597-05
