4种化疗方案治疗老年晚期胃癌的临床比较
2015-12-02朱海峰李小琴朱小霞陈文琪
朱海峰 李小琴 朱小霞 陈文琪
[摘 要] 目的:比较SOX、FOLFOX4、ECF和SP4个方案治疗老年晚期胃癌的疗效及不良反应。方法:选取本院2010年1月至2015年1月收治的老年晚期胃癌初治患者70例。随机数字表法分为4组,其中SOX组18例、FOLFOX4组17例、ECF组17例和SP组18例。对4组患者治疗周期、疗效、生命质量及不良反应进行对比。结果:70例患者共治疗327个周期。SOX组治疗90个周期,FOLFOX4组治疗86个周期,ECF组治疗74个周期,SP组治疗77个周期。SOX组有效率为61.1%,FOLFOX4组有效率为58.2%,ECF组有效率为52.9%,SP组有效率为55.6%。SOX组生命质量改善率为77.8%,FOLFOX4组改善率为76.5%,ECF组改善率为76.5%,SP组改善率为72.2%。4组近期疗效、生命质量总改善率比较差异无统计学意义(P>0.05)。SOX组与FOLFOX4组不良反应发生率低于ECF和SP。结论:SOX方案与FOLFOX4方案更适合治疗老年晚期胃癌。
[关键词] 晚期胃癌;替吉奥; 奥沙利铂;顺铂;化学治疗
中图分类号:R735.2 文献标识码:B 文章编号:2095-5200(2015)06-083-03
DOI:10.11876/mimt201506033
我国胃癌发病率和死亡率约为世界平均水平2倍[1]。由于早期胃癌缺乏特征性症状,当临床症状明显时,病变已属晚期,导致住院病例中超过90%胃癌病人往往在就诊时就已达到进展期或晚期[2-3]。晚期胃癌治疗以姑息性化疗为主综合治疗,根据情况给予放射治疗、姑息性手术、射频及介入治疗等局部治疗,同时给予止痛、对症营养支持。胃癌中常用化疗药物有多西他赛、紫杉醇、紫杉醇脂质体、表阿霉素、顺钿、奥沙利铂、5-氟尿啼淀、卡培他滨、替吉奥、伊立替康等。对于能够耐受化疗晚期胃癌患者首选两药或三药联合方案,而针对老年人这一特殊患病人群,寻找治疗有效且副作用小化疗方案尤为重要[4-5]。
本研究对SOX方案(替吉奥联合奥沙利铂)、FOLFOX4方案(奥沙利铂+氟尿嘧啶+亚叶酸钙)、ECF方案(表柔比星+顺铂+5-氟尿嘧啶)、SP方案(替吉奥联合顺铂)治疗老年晚期胃癌临床效果进行对比研究如下。
1 资料与方法
1.1 研究对象
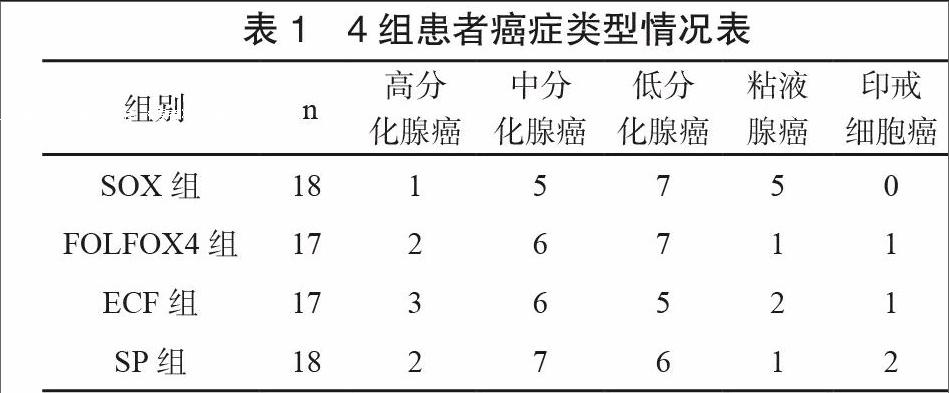
选取本院于2010年1月至2015年1月收治老年晚期胃癌初治患者70例,全部病例均经病理或细胞学检查确诊。其中男36例,女34例,年龄56~77岁,平均(63.9±3.24)岁。高分化腺癌8例;中分化腺癌24例;低分化腺癌25例;黏液腺癌9例;印戒细胞癌4例。TNM分期:Ⅲ期44例;Ⅳ期26例。转移部位:肺9例、肝脏14例、腹腔淋巴结15例、盆腔8例、锁骨上淋巴结 12 例、脑3例、两个以上部位转移9例。将70例患者随机数字表法分为4组,其中SOX组18例、FOLFOX4组17例、ECF组17例和SP组18例。4组患者年龄、性别等相关指标比较差异无统计学意义。
1.2 治疗方法
1.2.1 SOX方案化疗 在1个周期治疗第1天用奥沙利铂(连云港恒瑞药业,国药准字: H20040817)130mg/m2静滴2h;第1天到第14天连续口服替吉奥胶囊(山东新时代药业,国药准字: H20080802),计量根据体表面积计算:体表面积<1.25m2者40mg/次,体表面积1.25~1.5m2者50mg/次,体表面积>1.5m2者60mg/次,每天2次,21天为1周期。
1.2.2 FOLFOX 4方案化疗 在1个周期治疗第1天用奥沙利铂75mg/m2, 静脉滴注2h;另在治疗第1~2天加用:亚叶酸钙200mg/m2,静脉滴注2h;氟尿嘧啶(湖北一半天制药有限公司,国药准字H20143170)400 mg/m2,静脉推注;氟尿嘧啶600 mg/m2,持续静脉泵输注22h。每2周为1周期。
1.2.3 ECF方案化疗 在1个周期治疗第1天用表柔比星(浙江海正药业股份有限公司,国药准字H19990280)50mg/m2,静脉推注;另外在治疗第13天连续用顺铂(江苏豪森药业股份有限公司, 国药准字H20010743)20mg/m2,静脉滴注;治疗第15天用氟尿嘧啶500 mg/m2,静脉滴注。
1.2.4 SP方案化疗 在1个周期治疗第1~3天用顺铂(山东齐鲁制药,国药准字:H37021358)25mg/m2静滴,同时水化利尿;第1天到第14天连续口服替吉奥胶囊(山东新时代药业,国药准字: H20080802),计量根据体表面积计算:体表面积<1.25m2者40mg/次,体表面积1.25~1.5m2者50mg/次,体表面积>1.5m2者60mg/次,每天2次,21天为1周期。
1.3 评价标准
按WHO实体瘤疗效评价标准[6]评价疗效,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展 (PD),以CR+PR计算有效率(RR)。疾病进展时间(TTP)指从化疗开始至有客观证据表明疾病进展时间。不良反应按WHO标准分为0~4级进行评价。
以KPS评分标准[7]为指标评价生命质量,治疗结束后较治疗前评分增加20分以上者为改善,减少20分以上者为下降,增加或减少不足20分者为稳定。
1.4 数据统计学分析
采用 SPSS19.0统计分析软件包对所有数据进行分析。计数资料组间比较采用卡方检验,计量资料t检验,以P<0.05为差异有统计学意义。
2 结果
70例患者共治疗327个周期。SOX组治疗90个周期,平均5.0个周期;FOLFOX4组治疗86个周期,平均5.1个周期;ECF组治疗74个周期,平均4.4个周期;SP组治疗77个周期,平均4.3个周期。
2.1 患者近期疗效及生命质量评价比较
70例患者总有效率为57.1%。其中CR9例(12.8%),PR31例(12.8%),SD16例(12.8%),PD14例(12.8%)。SOX组有效率为61.1%,FOLFOX4组有效率为58.2%,ECF组有效率为52.9%,SP组有效率为55.6%。4组患者近期疗效比较差异无统计学意义(P>0.05)。
70例患者中患者生命质量明显改善40例,13例患者基本稳定,17例患者评分下降,总体生命质量改善率75.7%。SOX组生命质量改善率为77.8%,FOLFOX4组改善率为76.5%,ECF组改善率为76.5%,SP组改善率为72.2%。4组患者生命质量总改善率比较差异无统计学意义(P>0.05)。
2.2 4组患者不良反应比较
由表2可见,在0~2级不良反应方面,4组间未表现出明显差异。3~4级不良反应中, SOX组和FOLFOX4组白细胞减少、血小板减少、神经感觉异常等发生率稍低,与其他组别间具有统计学差异(P<0.05),提示SOX和FOLFOX4在晚期老年胃癌治疗方面安全性稍好。
3 讨论
全身化疗是胃癌综合治疗重要手段之一[8],与最佳支持治疗相比,全身化疗能显著延长生存期[9]。由于老年人各脏器储备功能较差,而且伴随着多种好发疾病,加上本身机体免疫力低,往往对化疗耐受性很差,所以寻找高效低毒化疗方案是目前治疗老年晚期胃癌最需要解决问题,其治疗方案选择是研究重
点[10]。目前全球尚无针对老年晚期胃癌患者标准化疗方案,尽管DCF、ECF方案已经被美国NCCN指南列为Ⅰ类推荐,但其过高不良反应严重限制了它们在老年晚期胃癌患者中临床应用[11]。
替吉奥[12]是新一代氟尿嘧啶类口服制剂,由替加氟吉美嘧啶和奥替拉西钾组成,口服给药后替加氟在体内缓慢转变为氟尿嘧啶,而氟尿嘧啶则通过抑制胸苷酸合成酶,阻止脱氧尿苷酸甲基化转变为脱氧胸苷酸,从而干扰DNA合成,发挥抗肿瘤作用。奥沙利铂[13-14]是继顺铂和卡铂之后第3代铂类药物,具有广谱体外细胞毒性和体内抗肿瘤作用,其与顺铂化学结构、抗癌谱及毒副反应均不完全相同,并与氟尿嘧啶形成互补抑制协同效应,有效杀伤肿瘤细胞,且对氟尿嘧啶耐药肿瘤仍有效,因而两药联合逐渐成为新研究方向[15-16]。
本研究发现,SOX方案用于老年晚期胃癌患者一线治疗时,其疗效与SP方案相似,但SOX方案毒副反应较低,因而该方案可能更适合老年晚期胃癌患者。SP方案与 FOLFOX4 方案近期疗效无统计学差异,但FOLFOX4方案毒副反应小、不适症状轻。FOLFOX4方案毒副反应较轻,主要为骨髓抑制、恶心、呕吐及外周感觉神经毒性,Ⅲ度以上毒副反应少见[17],适合于年老体弱者使用。而SP方案用药更方便,更容易被患者所接受,在患者依从性方面具有一定临床优势[18]。ECF方案主要不良反应为顺铂恶心呕吐和蒽环类药物心脏毒性[19],老年晚期胃癌患者本身即存在消化道症状,以心脑血管疾病为主基础疾病也决定了老年患者较年轻患者对顺铂和蒽环类药物耐受性差。
综上所述,老年晚期胃癌患者对常规化疗耐受性差是目前不能忽视问题,在循证医学研究成果基础上,制定个体化化疗方案意义重大。SOX治疗方案疗效肯定、毒性反应轻微,简单易执行,依从性较好缩短住院时间,经济负担较轻,患者容易接受,并能提高生命质量,比较适宜于老年晚期胃癌患者治疗。FOLFOX4方案化疗老年晚期胃癌患者生命质量大多有不同程度改善,但其远期疗效尚须进一步观察。
参 考 文 献
[1] Bang YJ, Van Cutsem E, Feyereislova A, et al. Trastu-zumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): aphase 3, open-label, randomised controlled trial[J]. Lancet, 2010, 376(42): 687-697.
[2] 刘培林.进展期胃癌的治疗进展[D].苏州:苏州大学,2014.
[3] Ali SM, Sanford EM, Klempner SJ, et al. Prospective comprehensive genomic profiling of advanced gastric carcinoma cases reveals frequent clinically relevant genomic alterations and new routes for targeted therapies[J]. Oncologist,2015,20(5):499-507.
[4] Kim HS, Kim HJ, Kim SY, et al. Second-line chemotherapy versus supportive cancer treatment in advanced gastric cancer: a meta-analysis[J]. Ann Oncol, 2013, 24(11):2850-2854.
[5] Huang Z, Xie DH, Guo L, et al. The utility of MRI for pre-operative T and N staging of gastric carcinoma: a systematic review and meta-analysis[J]. Br J Radiol, 2015,88(50):1120-1130.
[6] 张贺龙.实体瘤疗效评价标准及演变[J].现代肿瘤医学,2010,18(5):839-841.
[7] 乐薇.晚期胃癌患者预后与一线化疗过程中生活质量分数改善的关系[D].南昌:南昌大学,2013.
[8] Hu F, Wei F, Wang Y, et al. EGCG synergizes the therapeutic effect of cisplatin and oxaliplatin through autophagic pathway in human colorectal cancer cells[J].J Pharmacol Sci, 2015, 128(1):27-34.
[9] Zalba S, Contreras AM, Haeri A, Ten Hagen TL, Navarro I, Koning G, Garrido MJ. Cetuximab-oxaliplatin-liposomes for epidermal growth factor receptor targeted chemotherapy of colorectal cancer[J]. J Control Release, 2015,24(1):130-141.
[10] 赵林,应红艳,管梅,等.老年胃癌临床特点[J].中国医学科学院学报,2010,30(4):412-416.
[11] Klaver CE, Musters GD, Bemelman WA, et al. Adjuvant hyperthermic intraperitoneal chemotherapy (HIPEC) in patients with colon cancer at high risk of peritoneal carcinomatosis; the COLOPEC randomized multicentre trial[J]. BMC Cancer,2015,15(1):428.
[12] Shin HS, Oh SJ, Suh BJ. Two cases of advanced gastric carcinoma mimicking a malignant gastrointestinal stromal tumor[J]. J Gastric Cancer,2015,15(1):68-73.
[13] 肖明,契燕燕.FOLFOX方案加吡喃阿霉素治疗晚期胃癌30例[C].//第四届全国肿瘤学进展学术会议论文集.2007:128-130.
[14] Liu B,Ying J,Luo C, et al. S-1 combined with oxaliplatin as first linechemotherapy for Chinese advancedgastric cancer patients[J].Hepatogastroenterology,2012, 59( 114) : 649-653.
[15] Shitara K, Matsuo K, Muro K, et al. Correlation between overall survival and other endpoints in clinical trials of second- line chemotherapy for patients with advanced gastric cancer[J]. Gastric Cancer,2014,17(2):362-370.
[16] Barresi V, Branca G, Ieni A,et al. Phagocytosis (cannibalism) of apoptotic neutrophils by tumor cells in gastric micropapillary carcinomas[J].World J Gastroenterol,2015,21(18):5548-54.
[17] 王海英,郑瑞鹏,姚志华,等.SOX方案与FOLFOX4方案治疗老年晚期胃癌临床分析[J]. 中国老年学杂志,2015,35(6):1525-1527.
[18] Oh SY,Kwon HC, Jeong SH, et al. A phase Ⅱ study of S-1 and oxaliplatin(SOX) combination chemotherapy as a first-line therapy for patients with advanced gastric cancer[J]. Invest New Drugs,2012,30 (1) :350-356.
[19] 孙桂丽,王大鹏,任志红,等.替吉奥胶囊联合奥沙利铂治疗晚期胃癌临床观察[J].实用癌症杂志,2012,27(6):600-601.