TEA+MEA、TEA+DETA混合胺液脱除模拟天然气中H2S的性能
2015-07-02唐建峰史泽林徐明海花亦怀张新军
唐建峰, 史泽林, 陈 杰, 徐明海, 花亦怀, 姜 雪,李 晶, 张新军
(1.中国石油大学 储运与建筑工程学院,山东 青岛 266580;2.中海石油 气电集团技术研发中心,北京 100027)
TEA+MEA、TEA+DETA混合胺液脱除模拟天然气中H2S的性能
唐建峰1, 史泽林1, 陈 杰2, 徐明海1, 花亦怀2, 姜 雪1,李 晶1, 张新军1
(1.中国石油大学 储运与建筑工程学院,山东 青岛 266580;2.中海石油 气电集团技术研发中心,北京 100027)
以H2S体积分数为2%的H2S+CH4作为模拟天然气,在吸收温度50℃、吸收压力5 MPa、解吸温度105℃的操作条件下,实验研究了三乙醇胺(TEA)与乙醇胺(MEA)以及三乙醇胺(TEA)与二乙烯三胺(DETA)摩尔配比为2、4、14的TEA+MEA、TEA+DETA两种混合胺液的H2S吸收与解吸性能,以吸收负荷、吸收速率、解吸率为指标筛选相对较优的混合胺液配方。结果表明,在实验范围内, TEA+MEA混合胺液系列中,TEA/MEA摩尔比为2的TEA+MEA混合胺液具有最优的H2S吸收和解吸性能; TEA+DETA混合胺液系列中,TEA/DETA摩尔比为4的TEA+DETA混合胺液具有最优的H2S吸收和解吸性能。与TEA/MEA摩尔比为2的TEA+MEA相比,TEA/DETA摩尔比为4的TEA+DETA具有较高的H2S吸收速率与解吸率,综合脱硫效果较好。
醇胺法;天然气;H2S;吸收;解吸
煤、石油、天然气是我国的三大主要能源。近年来,随着石油需求的快速增长,国际油价节节攀升,而煤的燃烧又容易造成环境污染等诸多问题,因此,合理开发具有缓解煤炭能源紧缺、有效降低大气污染特点的天然气,成为确保能源供应,实现高效、快速经济可持续发展的有效途径[1-4]。天然气的主要成分是CH4,也含有少量的H2S、CO2、COS和其他非烃组分;这些组分由于呈现酸性而被称为酸性组分,其中H2S含量最高,危害也最严重[5-6]。天然气中含有的H2S除会造成诸多危害(如开采时易构成人身安全威胁,集输中会造成设备穿孔破损,燃烧产物SO2严重污染环境等[7-10])外,经回收后还可变成重要的硫磺资源。因此,除了安全与环境上的效益,脱除回收天然气中H2S也具有重要的经济效益[11-12]。
醇胺法自20世纪30年代问世以来,已被广泛应用于天然气、炼厂气及工业合成氨气体的净化[13-14]。工业中最常用的醇胺是一乙醇胺(MEA)、二乙醇胺(DEA)、三乙醇胺(TEA)、二乙烯三胺(DETA)、甲基二乙醇胺(MDEA)[15]。其中,MDEA、TEA为常用的主吸收剂[16]。目前,对MDEA脱硫研究得较多,TEA研究相对较少且多为保密配方,因此研究TEA脱硫的基本规律对工业生产具有极其重要的意义[17-19]。不同天然气中H2S含量不同,由石油天然气行业标准可得,当气藏中H2S体积分数大于2%时即为高含硫气藏。在本研究中,采用H2S体积分数为2%的H2S+CH4混合气模拟含硫量较高的天然气,实验研究以TEA为主吸收剂,分别以H2S吸收性能较优的MEA、DETA为添加剂的两种混合胺液对H2S的吸收与解吸性能,为天然气脱硫胺液的配方优选提供理论依据,并为天然气脱硫工业装置的设计提供基础数据。
1 实验部分
1.1 材料
原料气, H2S+CH4混合气,二者的体积分数分别为2%、98%,潍坊维氧气体厂提供;TEA,分析纯,西陇化工有限公司产品;MEA,分析纯,天津天泰精细化学品有限公司产品;DETA,分析纯,成都格雷西亚化学技术有限公司产品;N2,纯度99.9%,东营市双隆化工有限责任公司产品;盐酸,工业级,东营市新海化工有限公司产品;乙酸锌,分析纯,莱阳市康德化工有限公司产品;标准碘液、淀粉碘化钾指示剂,分析纯,济宁市鲁化生产力促进中心产品。
1.2 装置及流程
1.2.1 吸收实验装置及流程
吸收实验装置及流程如图1所示。其核心装置是带有磁耦合搅拌的高压釜。反应釜外壳为循环夹套,容积300 mL,釜顶盖采用哈氏合金且内部涂有防腐涂层。恒温水浴可提供一定温度的导热液体,用于吸收脱H2S过程中的温度控制,温控范围为室温以上5℃至100℃,温度波动度±0.1℃。反应釜最外层使用保温材料包裹,确保控温效果。真空泵采用水环泵,装置抽真空度根据泵上仪表进行监控。数据采集系统由数据变送器、数据采集卡和计算机构成,用于采集实验数据。实验用胺液体积100 mL,预先加至反应釜中,高压气瓶中的原料气经减压阀调压后通入高压反应釜,进行吸收H2S实验。
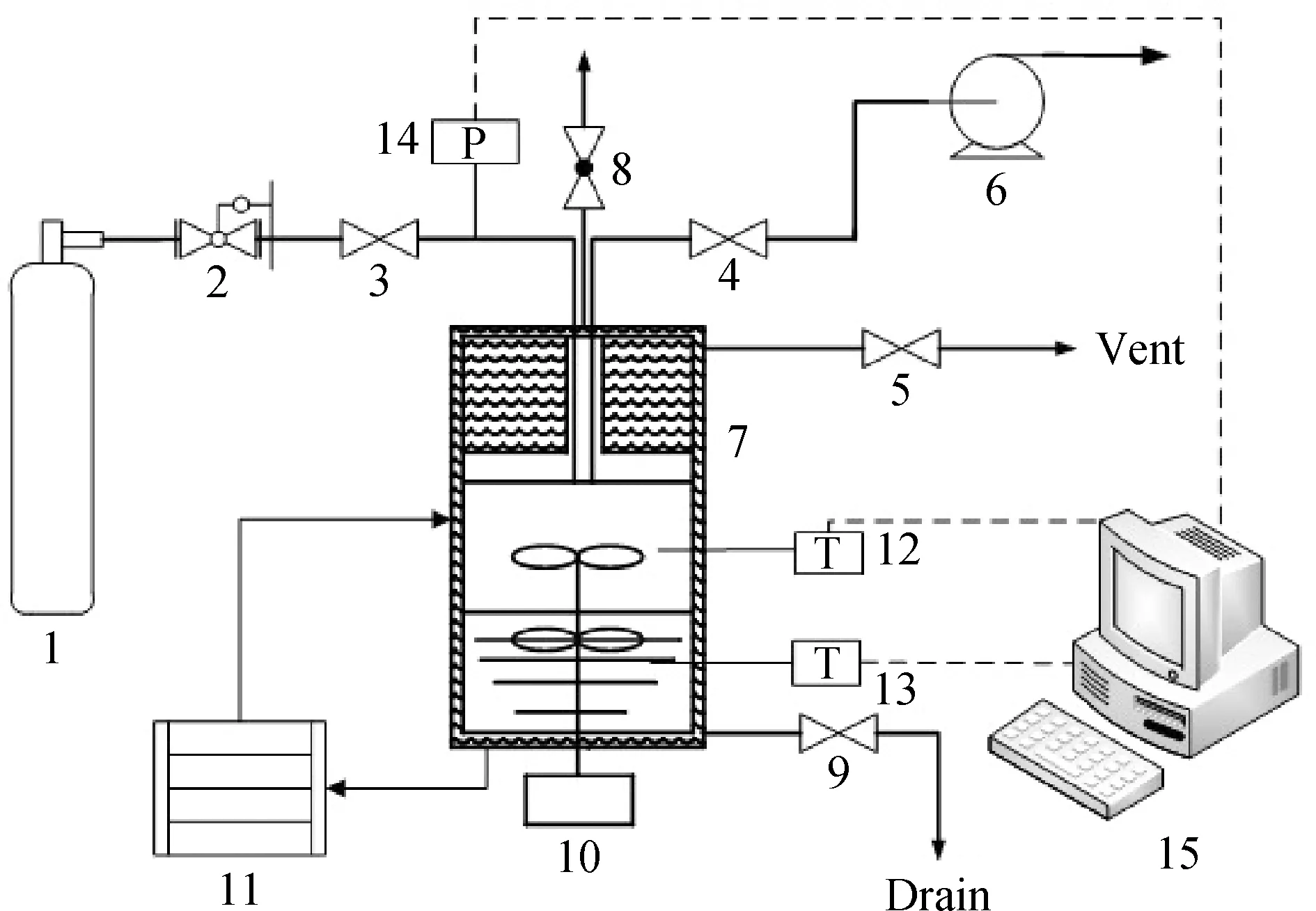
图1 吸收实验装置及流程
1.2.2 解吸实验装置及流程
性能优良的醇胺脱硫溶剂除了要具有较好的H2S吸收性能外,还应有良好的H2S解吸性能,以保证胺液的循环应用,降低脱硫成本。用于研究胺液H2S解吸性能的实验装置如图2所示。使用油浴恒温槽控制加热温度,吸收H2S后的胺液在三口烧瓶内进行解吸实验。解吸出的H2S气体中水蒸气含量较高,经冷凝管冷凝回流,剩余的酸气经干燥塔脱水干燥。脱水后的H2S气体通过皂膜流量计记录流量,最终被尾气吸收瓶中的NaOH溶液吸收。

图2 解吸实验装置及流程
1.2.3 碘液滴定测定胺液中H2S含量
将盐酸通过滴液漏斗滴加入胺液中,置换出吸收的H2S;将H2S通入乙酸锌溶液,生成硫化锌沉淀;以淀粉碘化钾为指示剂,0.1 mol/L标准碘液滴定硫化锌,根据滴定的碘液量计算胺液中H2S含量。利用该方法可分别获得吸收实验后和解吸实验后胺液中的H2S含量,用以评价胺液H2S解吸性能的好坏。
1.3 评价指标及数据处理
采用吸收负荷L、吸收速率N和解吸率λ3个指标评价混合胺液对H2S的吸收和解吸性能。3个指标分别可由式(1)~(3)计算得到。
(1)
(2)
(3)
式(1)~(3)中,n为混合胺液吸收H2S的物质的量,V1为混合胺液的体积,τ为吸收时间,V2为贫液滴定完全所需的碘液量,V3为富液滴定完全所需的碘液量。
吸收实验最终获得的数据为反应釜中的温度及压力变化值。由于实验中原料气充入釜内的初始压力为5 MPa,因此不能采用理想气体的方式处理,需进行数据转化。在本研究中,采用PR状态方程及其混合规则[20]处理实验数据,获得反应釜气相中H2S物质的量的变化,然后进一步求解胺液的吸收负荷及吸收速率。PR方程如式(4)、(5)所示。
(4)
(5)
式(4)、(5)中,Tc为气体的临界温度;Pc为气体的临界压力;ω为气体的偏心因子。H2S气体的Tc=373.2 K,pc=8.937 MPa,ω=0.1005;CH4气体的Tc=190.56 K,pc=4.599 MPa,ω=0.0114[21]。
PR方程的混合规则如式(6)所示。
(6)
式(6)中,xi,xj分别为气相或液相混合物中i和j组分的摩尔分数,kij为不同种类气体的交互作用系数,H2S与CH4气体间的交互作用系数为0.08[21]。
2 结果与讨论
2.1 TEA+MEA混合胺液配比的筛选
采用总浓度为3.0 mol/L,TEA/MEA摩尔比分别为2、4、14的混合胺液,在吸收温度50℃、吸收压力5 MPa条件下对H2S进行吸收实验,考察不同配比的TEA+MEA混合胺液的H2S吸收负荷随时间的变化及吸收速率随气相H2S浓度的变化,结果示于图3、4。TEA/MEA摩尔比分别为2、4、14的混合胺液分别记为TEA+MEA(2/1)、TEA+MEA(4/1)、TEA+MEA(14/1)。
由图3可见,不同配比混合胺液的H2S吸收负荷随时间的变化趋势大致相同,在0~30 min内随时间延长快速增加,呈线性关系,然后增加趋势逐渐变缓,最终于40 min左右达到平衡。在达到平衡前,从同一时刻H2S吸收负荷看,TEA+MEA(2/1)、TEA+MEA(14/1)、TEA+MEA(4/1)的吸收负荷依次降低,且TEA+MEA(2/1)的吸收负荷明显高于后二者。由图4可以看出,当气相中H2S浓度高于0.02 mol/L时,随气相H2S浓度的增加,各胺液对H2S的吸收速率近似呈线性增加;当H2S浓度低于0.02 mol/L时,受气相传质[22]的影响,H2S吸收速率基本一致。同一气相H2S浓度下,TEA+MEA(2/1)的H2S吸收速率明显高于TEA+MEA(4/1)和TEA+MEA(14/1),且后二者的H2S吸收速率基本一致。
综合分析图3、图4可得, TEA+MEA(2/1)的H2S吸收负荷及吸收速率均明显优于其余两种配比的胺液,具有较好的H2S吸收性能。
对吸收H2S后的胺液进行H2S解吸实验,测定贫、富液中的H2S含量,得到不同配比混合胺液的贫液残余负荷和解吸率,结果列于表1。

图3 不同配比的TEA+MEA混合胺液对H2S的吸收负荷(L)随吸收时间(τ)的变化

图4 不同配比的TEA+MEA混合胺液对H2S的吸收速率(N)随气相H2S浓度(c)的变化
表1 不同配比TEA+MEA胺液吸收H2S后的解吸实验数据
Table 1 Desorption experimental data of TEA+MEA with different molar ratios after H2S absorption

AminesolutionAbsorbingloadofrichliquid/(mol·L-1)Residualloadofpoorliquid/(mol·L-1)λ/%Desorptiontemperature/℃TEA+MEA(2/1)0 07770 02469 11105 6TEA+MEA(4/1)0 07860 02074 55105 4TEA+MEA(14/1)0 07880 02666 92105 2
由表1可看出,3种配比的TEA+MEA混合胺液的解吸温度基本相同,富液吸收负荷相差不大,但贫液残余负荷和解吸率不同。贫液残余负荷由大到小的TEA+MEA混合胺液依次为TEA+MEA(14/1)、TEA+MEA(2/1)、TEA+MEA(4/1),H2S解吸率由大到小的混合胺液依次为TEA+MEA(4/1)、TEA+MEA(2/1)、TEA+MEA(14/1)。
综合以上分析可得, TEA+MEA(2/1)混合胺液的H2S吸收负荷达到平衡的时间最短,且具有最大的吸收速率,H2S解吸率稍低于TEA+MEA(4/1),但相差不大。因此,TEA+MEA(2/1)混合胺液具有较好的H2S吸收与解吸性能。
2.2 TEA+DETA混合胺液配比的筛选
采用与TEA+MEA混合胺液配比筛选相同的条件,对TEA+DETA混合胺液配比进行筛选。采用的TEA/DETA摩尔比也分别为2、4、14,相应记为TEA+DETA(2/1)、TEA+DETA(4/1)、TEA+DETA(14/1)。不同配比的TEA+DETA混合胺液的H2S吸收负荷随时间的变化及吸收速率随气相H2S浓度的变化分别示于图5、6。H2S吸收实验后不同配比TEA+DETA混合胺液的贫液残余负荷和解吸率列于表2。

图5 不同配比的TEA+DETA混合胺液对H2S的吸收负荷(L)随吸收时间(τ)的变化

图6 不同配比的TEA+DETA混合胺液对H2S的吸收速率(N)随气相H2S浓度(c)的变化
由图5可以看出,不同配比的TEA+DETA混合胺液的H2S吸收负荷随时间变化的趋势大致相同,在初始时刻增长较快,随吸收时间的增加,增长趋势渐缓。同一时刻H2S吸收负荷由大到小的3种TEA+DETA依次为TEA+DETA(4/1)、TEA+DETA(2/1)、TEA+DETA(14/1)。由图6可得,当气相H2S浓度高于0.02mol/L时,随气相H2S浓度的增加,各混合胺液的H2S吸收速率近似呈线性增加;当H2S浓度低于0.02mol/L时,吸收过程受气相传质的影响,吸收速率基本一致。同一气相H2S浓度下,TEA+DETA(14/1)的吸收速率明显低于TEA+DETA(2/1)和TEA+DETA(4/1),而后二者的吸收速率基本一致。
综合分析图5、图6可得,TEA+DETA(2/1)和TEA+DETA(4/1)混合胺液均具有较高的H2S吸收负荷和吸收速率,H2S吸收性能较好。

表2 不同配比TEA+DETA混合胺液吸收H2S后的解吸实验数据
由表2可看出,3种配比混合胺液的富液吸收负荷和解吸温度基本相同,但贫液残余负荷和解吸率不同。贫液残余负荷由大到小的TEA+DETA混合胺液依次为TEA+DETA(2/1)、TEA+DETA(14/1)、TEA+DETA(4/1),解吸率由大到小TEA+DETA混合胺液依次为TEA+DETA(4/1)、TEA+DETA(14/1)、TEA+DETA(2/1)。
综合以上分析可得, TEA+DETA(4/1)和TEA+DETA(2/1)的H2S吸收负荷达到平衡的时间相似,同时二者具有相近的吸收速率,但前者的H2S解吸率高于后者。因此,TEA+DETA(4/1)具有较好的H2S吸收与解吸性能。
2.3 优选配方TEA+MEA(2/1)和 TEA+DETA(4/1)脱H2S性能比较
优选出的混合胺液TEA+MEA(2/1)和TEA+DETA(4/1)的H2S吸收负荷随时间变化和吸收速率随气相H2S浓度变化分别示于图7、8,二者的贫液残余负荷和解吸率列于表3。

图7 TEA+MEA(2/1)和 TEA+DETA(4/1)的H2S吸收负荷(L)随吸收时间(τ)的变化
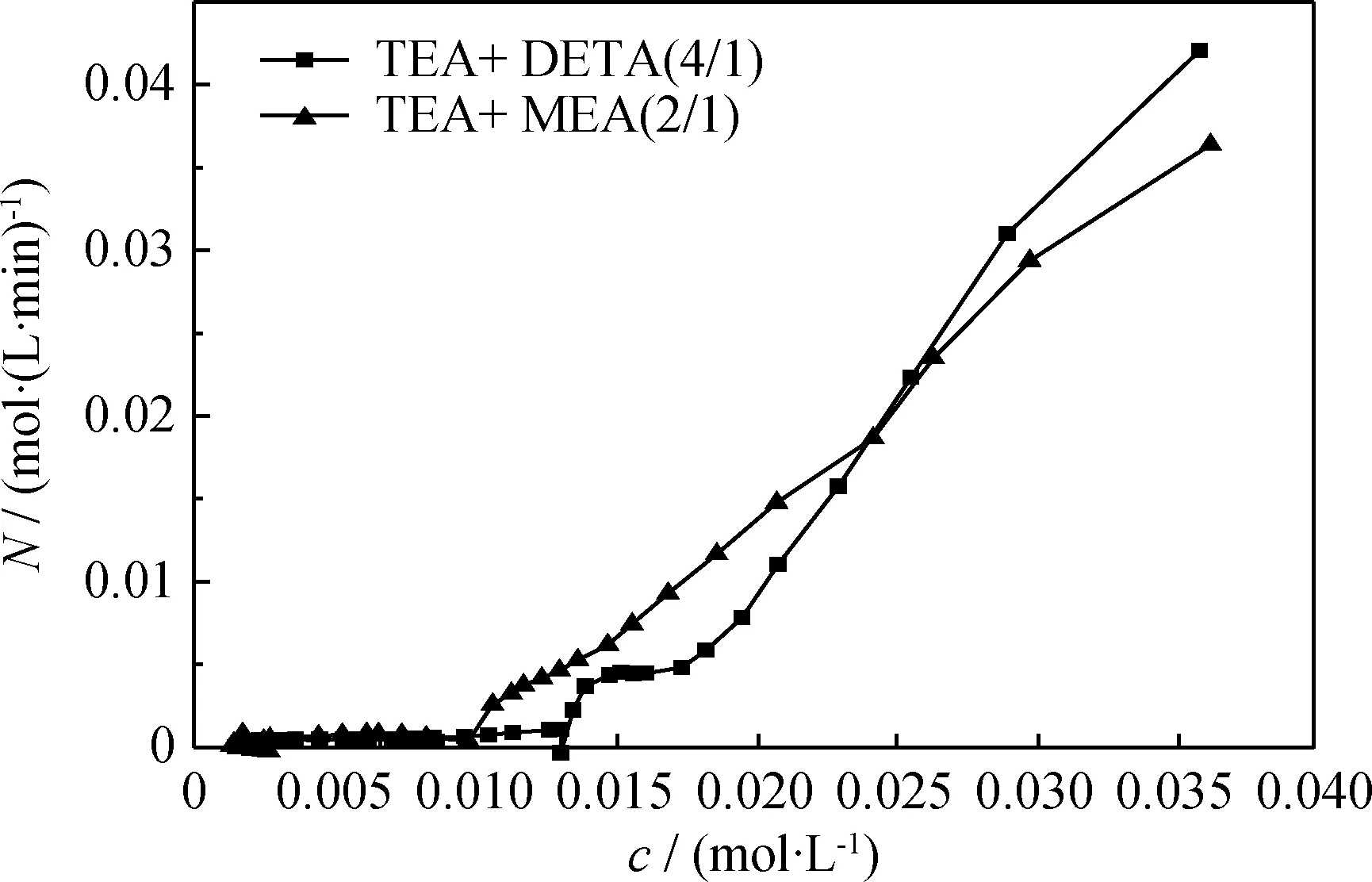
图8 TEA+MEA(2/1)和 TEA+DETA(4/1)的H2S吸收速率(N)随气相H2S浓度(c)的变化
由图7可以看出,TEA+MEA(2/1)较早达到较高的吸收负荷。由图8可以看出,在初始时刻,TEA+DETA(4/1)的吸收速率较高,与TEA+MEA(2/1)相比,随气相H2S浓度下降而降低的幅度较大。由表3可得,TEA+DETA(4/1)的H2S解吸率明显高于TEA+MEA(2/1)的。综合以上分析, TEA+DETA(4/1)混合胺液的H2S吸收、解吸性能最为优异,是本实验条件下的最佳混合胺液配方。

表3 TEA+MEA(2/1)和TEA+DETA(4/1)吸收H2S后的解吸实验数据
3 结 论
在H2S体积分数为2%的模拟天然气中,保持胺液总浓度一致,在吸收温度50℃、吸收压力5 MPa、解吸温度105℃的操作条件下,考察了主体吸收剂TEA溶液分别添加MEA、DETA溶液组成的混合胺液对H2S的吸收与解吸性能。
在TEA+MEA混合胺液系列中,TEA/MEA摩尔比为2的TEA+MEA(2/1)混合胺液具有最优的H2S吸收和解吸性能;在TEA+DETA混合胺液系列中,TEA/DETA摩尔比为4的TEA+DETA(4/1)混合胺液具有最优的H2S吸收和解吸性能。
与TEA+MEA(2/1)相比,TEA+DETA(4/1)具有较高的H2S吸收速率与解吸率,综合脱硫效果较好。
[1] LIU G, WILLIAMS R H, LARSON E D, et al. Design/economics of low-carbon power generation from natural gas and biomass with synthetic fuels co-production [J].Energy Procedia.2011, 9(4): 1989-1996.
[2] 王剑, 张晓萍, 李恩田, 等.天然气脱硫技术研究现状与发展趋势[J].常州大学学报 (自然科学版), 2013, 25(3) :88-92.(WANG Jian, ZHANG Xiaoping, LI Entian.Research on current status and development trends of natural gas desulfurization technology [J].Journal of Changzhou University(Natural Science Edition) 2013,25(3):88-92.)
[3] 王学谦, 宁平. 硫化氢废气治理研究进展[J].环境污染治理技术与设备, 2001, 2(4): 77-85.(WANG Xueqian, NING Ping.Progress of hydrogen sulfide waste gas treatment [J].Techniques and Equipment for Environmental Pollution Control, 2001, 2(4):77-85.)
[4] 唐炼. 世界能源供需现状与发展趋势[J].国际石油经济, 2005, 13(1): 30-33.(TANG Lian.Status of supply and demand and development trends of world energy[J].International Petroleum Economics, 2005, 13(1): 30-33.)
[5] 刘泽杰,杨琳. 石化装置中硫化氢的危害及治理[J].化学工程与装备,2010,(6):147-148.(LIU Zejie, YANG Lin.Hazard and control of hydrogen sulfide in petrochemical plant[J].Chemical Engineering & Equipment, 2010,(6):147-148)
[6] 刘露, 段振红, 贺高红.天然气脱除 CO2方法的比较与进展[J].化工进展, 2009, 28(1):290-292.(LIU Lu, DUAN Zhenhong, HE Gaohong.Compared and progress of natural gas decarbonization process[J].Chemical Industry and Engineering Progress, 2009, 28(1):290-292.)
[7] 朱光有,张水昌, 李剑,等.中国高含硫化氢天然气的形成及其分布[J].石油勘探与开发,2004,31(3): 18-21.(ZHU Guangyou, ZHANG Shuichang, LI Jian.Formation and distribution of hydrogen sulfide bearing gas in China [J].Petroleum Exploration and Development, 2004, 31(3): 18-21.)
[8] 王育明. 天然气处理工艺的优化[J].油气田地面工程, 2008, 27(2): 52-54.(WANG Yuming.Optimization of gas treatment process[J].Oil-Gasfield Surface Engineering, 2008, 27(2): 52-54.)
[9] 王澎. H2S对天然气处理设备的腐蚀及相应对策[J].天然气与石油, 2010, 28(2): 34-36.(WANG Peng.Corrosion of H2S on natural gas processing equipment and corresponding counter measures [J].Natural Gas and Oil, 2010, 28(2): 34-36.)
[10] 吕明晏, 张哲, 汪是洋.高含硫气田集输系统元素硫沉积防治措施[J].天然气与石油, 2011, 29(3): 17-20.(LÜ Mingyan, ZHANG Zhe, WANG Shiyang.Preventive measures for element sulfur deposition in gathering and transportation systems of high sour gas field [J].Natural Gas and Oil, 2011, 29(3): 17-20.)
[11] 王开岳. 天然气净化工艺的国内外现状及开发动向[J].石油规划设计, 1996, (3): :13-14.(WANG Kaiyue.The current status and development trends of natural gas purification process[J].Petroleum Planning & Engineering, 1996, (3):13-14.)
[12] 颜廷昭. 混合胺工艺在天然气净化中的应用[J].天然气与石油, 1998, 16(2): 9-15.(YAN Tingzhao.Application of mixed-amine technique in gas purification [J].Natural Gas and Oil, 1998, 16(2): 9-15.)
[13] 刘颖, 王治红. 天然气脱硫脱碳溶液研究进展与应用现状[J].广州化工, 2012, 40(7): 30-32.(LIU Ying, WANG Zhihong.The current status of the application and development of natural gas enrichment solvents [J].Guangzhou Chemical Industry, 2012, 40(7): 30-32.)
[14] MANDAL B P, BISWAS A K, BANDYOPADHYAY S S.Selective absorption of H2S from gas streams containing H2S and CO2into aqueous solutions ofN-methyldiethanolamine and 2-amino-2-methyl-1-propanol[J].Separation and Purification Technology, 2004, 35(3): 191-202.
[15] 韩鹏, 杨大静, 朱鹏, 等.天然气脱硫方法的选择及醇胺法的应用[J].内蒙古石油化工, 2007, (12): 177-178.(HAN Peng, YANG Dajing, ZHU Peng.Selection of gas desulfurization method and application of alcohol amine[J].Inner Mongolia Petrochemical Industry, 2007, (12): 177-178.)
[16] MANDAL B P, BANDYOPADHYAY S S.Simultaneous absorption of carbon dioxide and hydrogen sulfide into aqueous blends of 2-amino-2-methyl-1-propanol and diethanolamine[J].Chemical Engineering Science, 2005, 60(22): 6438-6451.
[17] 王遇冬, 王登海. MDEA 配方溶液在天然气脱硫脱碳中的选用[J].石油与天然气化工, 2003, 32(5): 291-294.(WANG Yudong, WANG Denghai.Selection and application of formulated MDEA solutions for H2S and CO2removal in natural gas treating [J].Chemical Engineering of Oil & Gas, 2003, 32(5): 291-294.)
[18] 杜建鹏. 醇胺法脱除天然气中硫化氢的研究[D].上海:华东理工大学,2012.
[19] 于淼,周理. 天然气中 H2S 的脱除方法[J].天津化工,2002,(5): 18-20.(YU Miao, ZHOU Li.Removal of hydrogen sulfide in natural gas[J].Tianjin Chemical, 2002, (5): 18-20.)
[20] 苏长荪. 高等工程热力学[M].北京:高等教育出版社,1987.
[21] 李玉星, 姚光镇. 输气管道设计与管理[M].东营:中国石油大学出版社,2008.
[22] GODINI H R, MOWLA D.Selectivity study of H2S and CO2absorption from gaseous mixtures by MEA in packer beds [J].Chemical Engineering Research and Design,2008,86(4):401-409.
Performance of TEA+MEA, TEA+DETA Mixed Amine in Removing H2S From Simulated Natural Gas
TANG Jianfeng1, SHI Zelin1, CHEN Jie2,XU Minghai1,HUA Yihuai2,JIANG Xue1, LI Jing1, ZHANG Xinjun1
(1.CollegeofPipelineandCivilEngineering,ChinaUniversityofPetroleum,Qingdao266580,China;2 .CNOOCGas&PowerGroupResearch&DevelopmentCenter,Beijing100027,China)
With the mixture of H2S+CH4as simulated natural gas, in which the volume fraction of H2S is 2%, under the operating conditions of absorption temperature 50℃, absorption pressure 5MPa, desorption temperature 105℃, the H2S absorption and desorption performance of triethanolamine(TEA)+monoethanolamine (MEA) and TEA+diethylenetriamine (DETA) mixed amine solutions with TEA/MEA or TEA/DETA molar ratio of 2, 4 and 14,respectively, were investigated. And the absorption load, absorption rate and desorption rate were used as the indices to get the optimum ratio of mixed amine solution. The results showed that in the experimental range the TEA+MEA solution with TEA/MEA molar ratio of 2 in the series of TEA+MEA mixed amine solutions and the TEA+DETA solution with TEA/DETA molar ratio of 4 in the series of TEA+DETA solutions both possessed optimal H2S absorption and desorption performance. Furthermore, the desulfurization performance of the TEA+DETA amine solution with TEA/DETA molar ratio of 4 was better than that of the TEA+MEA amine solution with TEA/MEA molar ratio of 2.
alcohol amine;natural gas;H2S;absorption;desorption
2014-06-23
国家重大基础研究“863”项目(2013AA09A216)和中央高校基本科研业务费专项资金(14CX05033A)资助
唐建峰,男,教授,博士,主要从事天然气预处理、LNG关键技术等研究工作;Tel:0532-86983173; E-mail:tangpaper@126.com
1001-8719(2015)05-1082-07
TE644
A
10.3969/j.issn.1001-8719.2015.05.008
