液相色谱检测水产品中喹诺酮类药物的方法改进研究
2015-04-27王丽娟张骊钱卓真汤水粉叶玫吴成业
王丽娟,张骊,钱卓真,汤水粉,叶玫,吴成业
(1.福建省水产研究所,福建厦门361013;2.中国兽医药品监察所,北京100081)
液相色谱检测水产品中喹诺酮类药物的方法改进研究
王丽娟1,张骊2,钱卓真1,汤水粉1,叶玫1,吴成业1
(1.福建省水产研究所,福建厦门361013;2.中国兽医药品监察所,北京100081)
采用正交试验法考察液相色谱法检测喹诺酮类药物保留时间漂移现象的主要影响因素。以诺氟沙星、环丙沙星和恩诺沙星保留时间的漂移率作为评价指标,考察流动相种类、前处理条件以及样品种类等因素对喹诺酮类药物保留时间的影响。结果表明,造成分析物色谱峰漂移的主要因素是流动相种类。在流动相中添加缓冲盐和优化前处理方法,可以明显改善目标分析物保留时间的漂移,改进后诺氟沙星、环丙沙星和恩诺沙星漂移率分别降低9.11%、7.74%和7.97%。通过实验获得最佳检测条件,以期为基层检测单位提供可选方法。
喹诺酮类药物;保留时间;漂移;液相色谱
喹诺酮类抗生素是近二三十年来发展迅速且应用广泛的广谱抗菌药物。此类药物对大多数鱼类易感染细菌的最低抑菌浓度(MIC)值较小,组织药物浓度高,且分布广泛,成为水产养殖中重要的抗感染药物之一,被广泛应用于预防和治疗鱼类全身性细菌感染[1-2]。但是,此类药物过量或者不正当使用造成的残留会对人体健康有危害,例如具有光毒性[3],肝和软骨毒性[4],可致中枢神经系统[5]和消化系统的不良反应,以及肌腱病症[6]和对血糖代谢的影响[7]。我国于2002年规定了环丙沙星、单诺沙星、恩诺沙星、沙拉沙星、二氟沙星、恶喹酸和氟甲喹等7种喹诺酮类药物在动物肌肉组织中的最高残留限量为10~500 μg/kg[8]。目前,水产品中喹诺酮类药物残留检测方法包括液相色谱-串联质谱法(LC-MS/MS)[9]和高效液相色谱法(HPLC)[10]。由于具有样品前处理简单、精密度好和仪器操作相对简便等特点,HPLC方法在基层检测机构中得到广泛应用。然而,在日常工作中发现,采用HPLC方法检测水产品中的氟喹诺酮类药物残留时,可能会出现明显的保留时间漂移,从而给阳性样品的确认带来困扰,干扰检测结果。在本研究中,采用正交实验方法考察各种HPLC方法中使用的流动相种类、前处理条件以及样品种类等因素对诺氟沙星、环丙沙星和恩诺沙星保留时间的影响,探究造成检测时间漂移的主要原因。在此基础上,对实验条件进行优化,从而解决保留时间漂移的问题,为基层检测单位改进水产中氟喹诺酮类药物残留的HPLC检测方法提供参考。
1 材料与方法
1.1 仪器与试剂 waters e2695液相色谱仪,配waters 2475荧光检测器(美国waters公司);AB204-E电子天平(梅特勒-托利多仪器有限公司);Milli-Q Academic去离子水发生器(上海百微生物科技有限公司);MS3 basic涡旋振荡器(德国IKA公司);DT5-5低速离心机(北京时代北利离心机有限公司);KQ-6000DE数控超声波清洗仪(昆山市超声仪器有限公司);固相萃取柱装置(美国奥泰科技有限公司);固相萃取柱(Oasis HLB,Waters公司);诺氟沙星、环丙沙星和恩诺沙星标准品(德国DR.Ehrenstorfer GmbH),纯度≥95.0%;甲醇、乙腈均为色谱纯(美国Tedia公司);四丁基溴化铵(国药集团化学试剂有限公司);其余试剂皆为分析纯。
酸化乙腈:乙腈+(1+1)盐酸=2500+20(V/V);0.01mol/L柠檬酸-三乙胺混合溶液:取2.1014 g的柠檬酸稀释定容至1000 mL,用三乙胺调节pH值至4.5[10];0.05 mol/L磷酸-三乙胺混合溶液:取3.4 mL的浓磷酸稀释定容至1000 mL,用三乙胺调节pH值至2.4[11];磷酸盐缓冲溶液:取磷酸二氢钾6.8001 g,加水使溶解并稀释至500 mL,用5 mol/L氢氧化钠调节pH至7.0。
1.2 仪器条件 色谱柱:Agilent色谱柱,Eclipse XDB-C18柱,5 μm,4.6 mm(id)×150 mm;流速1.0 mL/min,检测器:荧光检测器,激发波长280 nm,发射波长460 nm;柱温35℃;进样量10 μL;流动相:乙腈+柠檬酸-三乙胺溶液=14+86(V/V),乙腈+磷酸-三乙胺溶液=14+86(V/V),乙腈+四丁基溴化铵=6+94(V/V)。
1.3 方法
1.3.1 不同样品前处理方法 液液萃取法:准确称取5 g(精确到0.01 g)样品,依次加入10~15 g的无水硫酸钠和30 mL酸化乙腈,超声提取5 min,4000 r/min离心10 min,取上清液。往残渣中加入15 mL酸化乙腈,重复上述操作一次,合并上清液。将上清液置于分液漏斗中,加入25 mL正己烷,震荡,充分静置,取下层乙腈层转入烧瓶,40℃旋转蒸发至干。用1.0 mL流动相充分溶解残渣,加入1.0 mL正己烷涡旋洗涤后,移入5 mL离心管,8000 r/min离心后取下层,经滤膜过滤后,供液相色谱分析。
固相萃取法:如前所述,采用酸化乙腈提取两次,合并上清液转入烧瓶,40℃旋转蒸发至干。用5 mL磷酸二氢钾-甲醇溶液充分溶解残渣备用。固相萃取柱先依次用甲醇、水各3 mL预活化,取备用样品5 mL过柱,用5 mL水淋洗、挤干。用6 mL的6%的氨化甲醇洗脱挤干,收集洗脱液,于45℃氮气吹干,准确加入1.0 mL流动相溶液溶解残渣,经滤膜过滤后,供液相色谱分析。
液液萃取法与固相萃取法结合:如前所述,酸化乙腈超声提取两次合并置于分液漏斗中,加入正己烷静置分层后移出旋转蒸发至干。用5 mL流动相充分溶解残渣,过HLB固相萃取柱(同固相萃取法)。用1.0 mL流动相溶液溶解残渣,经滤膜过滤后,供液相色谱分析。
1.3.2 正交实验设计 为考察各因素影响的显著性,得出影响喹诺酮类药物保留时间漂移的最关键因素,本研究进行L9(34)正交实验设计。即以样品种类(A)、前处理方法(B)、流动相种类(C)为考察因素,设计3因素3水平的正交实验,每组实验重复三次。正交实验因素与水平设计见表1。

表1 因素水平表
1.3.3 漂移率的计算 样品中喹诺酮类药物色谱峰保留时间漂移率可由下式计算:×100%,式中,S为漂移率(%);T1为样品中喹诺酮类药物保留时间(min);T2为喹诺酮类标准品保留时间(min)。
1.3.4 方法改进 对6例实际样品进行检测,四丁基溴化铵/乙腈做为流动相时,在流动相中加入0.02 mol/L磷酸盐缓冲溶液(pH=3.0),观察改进前后3种喹诺酮类药物保留时间。
2 结果
2.1 正交实验结果 结果如表2、表3所示。

表2 L9(34)正交实验方案表
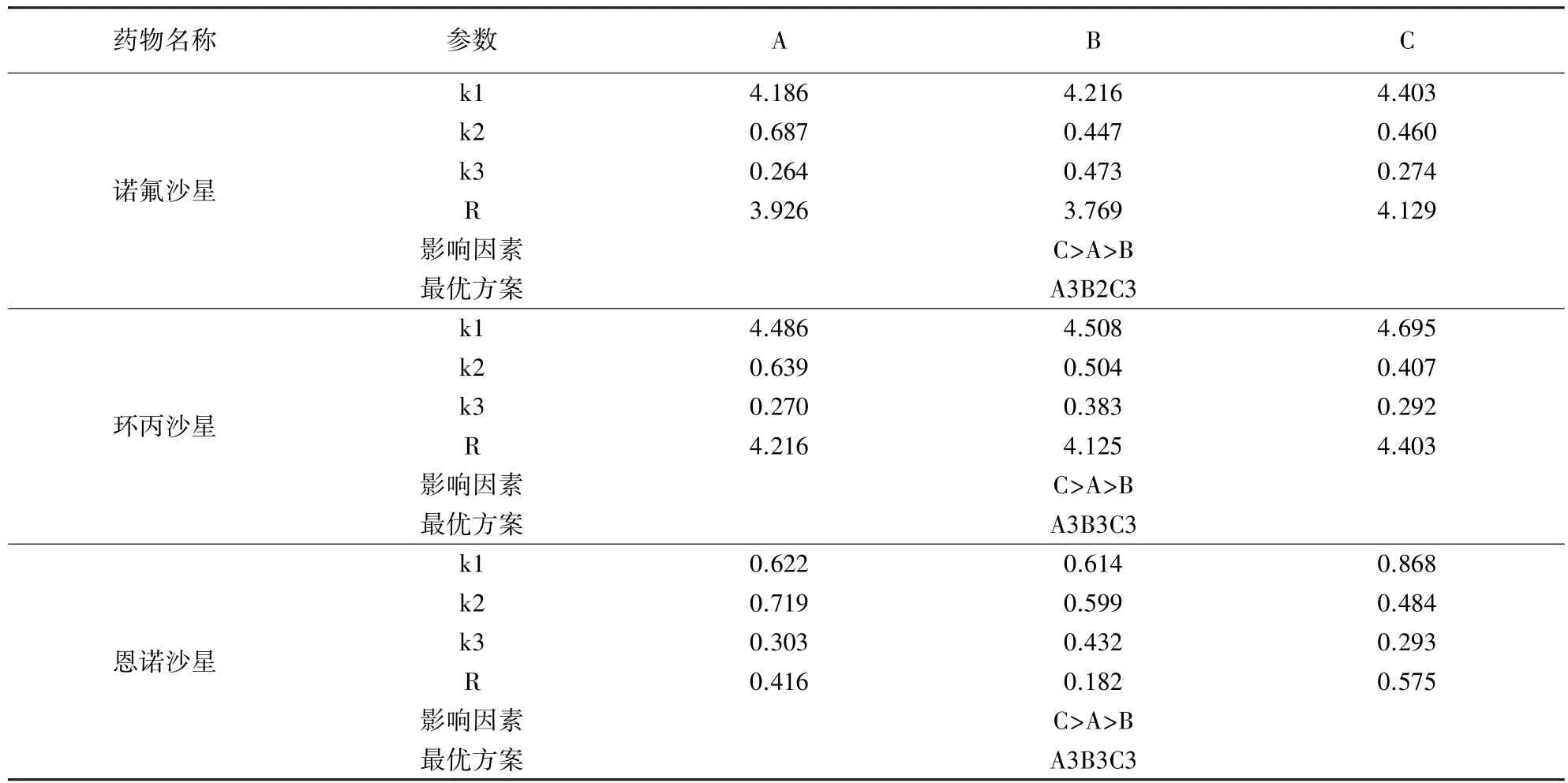
表3 正交实验数据直观分析表
由表2、表3分析结果可知,造成诺氟沙星、环丙沙星和恩诺沙星的保留时间漂移主次因素分别为C>A>B,即流动相种类>样品种类>前处理条件。当采用液液萃取法进行样品前处理,并使用四丁基溴化铵作为流动相时,南美白对虾样品中诺氟沙星和环丙沙星的保留时间较标准品出现了明显的漂移(图1)。
2.2 显著性分析 结果如表4所示。

图1 喹诺酮类药物液相色谱图(a标准品,100 ng/mL;b南美白对虾样品)

表4 方差分析表
通过表4方差分析进一步证明,流动相种类对其出峰时间漂移率影响最大。而对于不同的样品种类,基质的复杂性和酸碱度等可能有差别,因此,不同的前处理条件对喹诺酮类药物保留时间漂移的影响也不可忽视。
2.3 改进后结果 改进前、后不同样品中3种喹诺酮类药物保留时间漂移率结果,见表5。从SPSS软件处理后的结果(表6)可看出,诺氟沙星、环丙沙星和恩诺沙星(P<0.05)改进前后保留时间漂移率具有显著性差异。方法进行改进后,诺氟沙星、环丙沙星和恩诺沙星的保留时间漂移率分别降低了9.11%、7.74%和7.97%,且改进后的3种喹诺酮类药物保留时间的漂移率皆低于2%,从而满足检测要求。
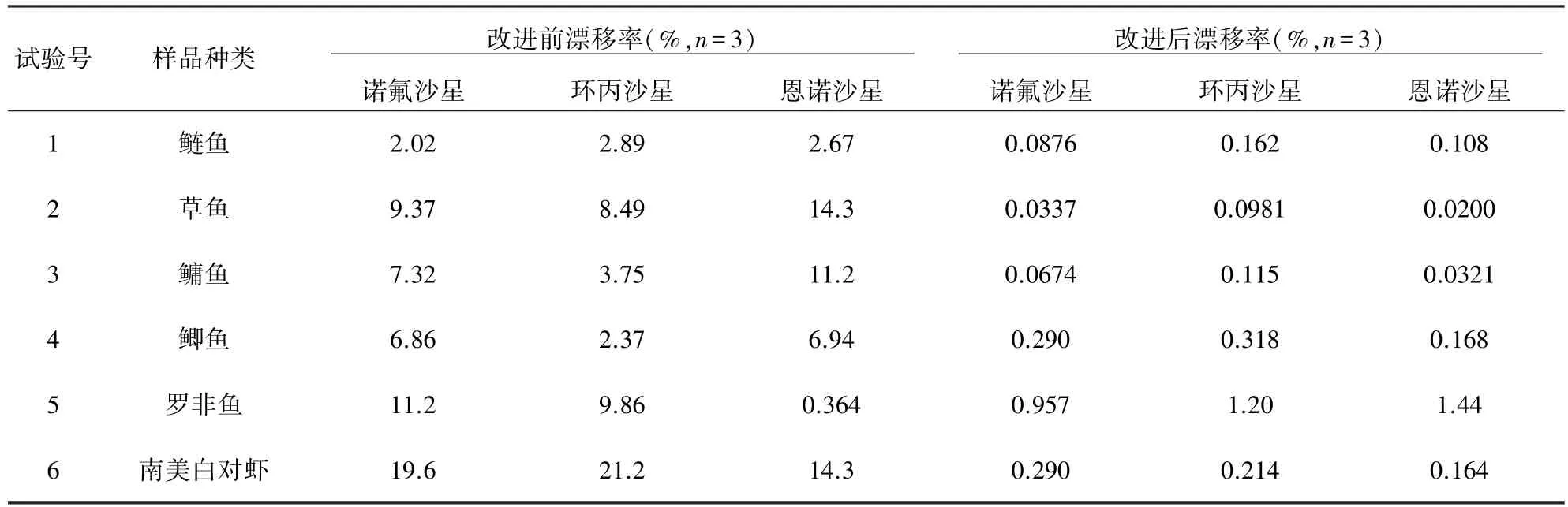
表5 改进流动相后样品检测结果%
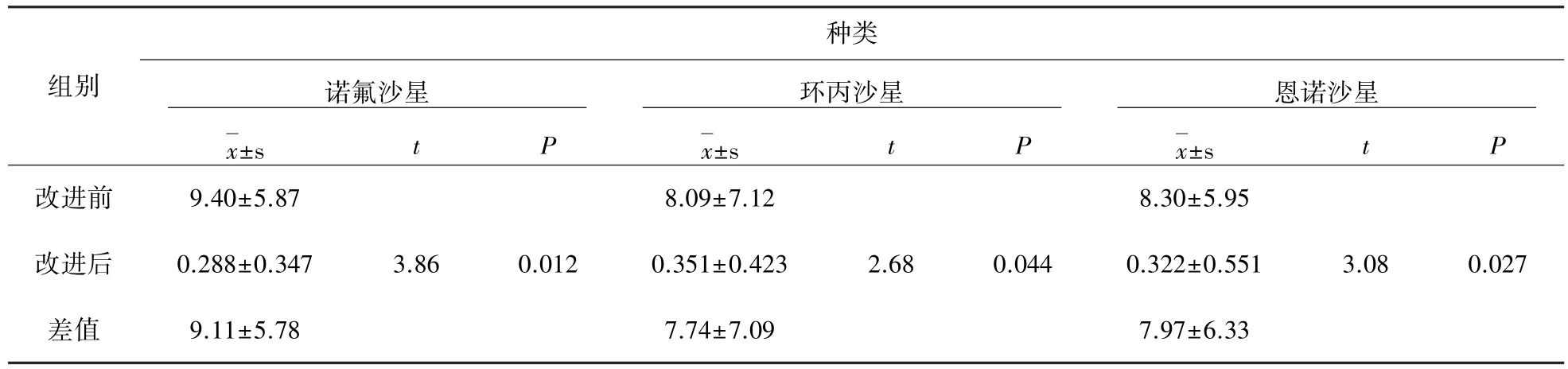
表6 改进前后诺氟沙星、环丙沙星和恩诺沙星SPSS软件处理结果%
3 讨论及小结
由于喹诺酮类药物的结构中同时包含有哌嗪基和羧基,属于两性分子,传统的色谱柱常常会因为残余硅醇基和金属不纯物的存在而导致色谱峰拖尾[11-12]。在某些检测方法中,通常在流动相中加入四丁基溴化铵试剂[10-14]作为离子对试剂降低其极性,从而改善峰形和提高分离度。但喹诺酮类样品在色谱柱保留时间对pH值很敏感,而离子对试剂本身无法起到有效的缓冲作用[15-16],可能造成不同样品分析物保留时间的漂移。因此本试验发现流动相种类是导致HPLC保留时间漂移的主要原因。当流动相为乙腈-四丁基溴化铵溶液时,诺氟沙星和环丙沙星的保留时间漂移加大。而流动相中加入缓冲溶液后,罗非鱼阳性样品中环丙沙星保留时间漂移率减小为1.20%,而未加前环丙沙星保留时间漂移率为9.86%,因此在实际样品的检测中,保留时间的漂移得到明显改善,从而消除了样品的pH值不同对喹诺酮类药物的HPLC保留时间的影响。另外,采用四丁基溴化铵试剂做为流动相时,色谱柱的平衡时间较长,也可能会影响保留时间的重复性。
通过直观分析发现除了流动相种类的影响其次为样品种类,而对于水产品来说,不同样品所含基质不同,且样品pH值也有差别。因此样品种类对检测时间漂移率的影响可归结为样品前处理影响和样品pH对流动相的影响(如上述可通过加入缓冲盐改善)。在HPLC分析前,如果样品前处理过程的净化效果不好,进样溶液中强保留基质组分可能会造成目标分析物在色谱柱上的保留时间不稳定,同时,本研究的结果表明,样品前处理也是影响喹诺酮类药物保留时间漂移的因素之一。在水产中喹诺酮类药物的多残留检测时,固相萃取在样品净化方面具有明显优势,并得到普遍应用[17-22]。因此,在本文研究中,在前处理过程中,采用固相萃取法对样品进行净化,也是防止保留时间漂移的手段之一。
在本文中,采用正交实验设计和显著性分析发现,在采用HPLC法检测水产品中的喹诺酮类药物残留时,造成分析物色谱峰漂移的主要因素是流动相种类。同时,样品前处理方法也是影响因素之一。根据以上结果,采用四丁基溴化铵作为流动相时通过在流动相中添加缓冲盐和优化前处理方法,可以明显改善目标分析物保留时间的漂移,从而避免实际检测中对可能阳性样品的错误判断。
[1] 张贞发,周伟澄.氟喳诺酮构效关系研究的新进展[J].中国医药工业杂志,1992,23(5):226.
[2] 沈建忠,谢联金.兽医药理学[M].北京:中国农业大学出版社,2000:162-167.
[3] 吴诗聪.左氧氟沙星注射液致不良反应24例分析[J].当代医学,2012,18(1):127-128.
[4] Carbon C.Comparison of side effects of levofloxacin versus other fluoroquinolones[J].Chemotherapy,2001,47(Suppl 3):9-44.
[5] Mccormack W M,Dalu Z A,Martin D H,et al.Double blind comparison of trovafloxacin and doxycycline in the treatment of uncomplicated Chlamydial urethritis and cervicitis[J].Sexually Transmitted Diseases,1999,26(9):531.
[6] 仲兆金.喹诺酮类药物的毒性[J].国外医药抗生素分册,2001,22(1):31-33.
[7] Umezawa N,Arakane K,Ryu A,et al.Participation of reactive oxygen species in phototoxycity induced by quinolone antibacterial agents[J].archives of biochemistry and biophysics,1997,342(2):275-281.
[8] 中华人民共和国农业部.中华人民共和国农业部第235号公告[S].
[9] 中华人民共和国农业部.中华人民共和国农业部第1077号公告-1-2008[S].
[10]中华人民共和国农业部.中华人民共和国农业部第783号公告-2-2006[S].
[11]钱卓真,苏秀华,魏博娟,等.高效液相色谱法同时测定水产品中6种喹诺酮药物的残留[J].食品科学,2010,31(6):185-189.
[12]陈丽,杨长志,刘永,等.高效液相色谱法同时测定水产品中多种氟喹诺酮类药物残留量[J].化学工程师,2009,168(9):25-27.
[13]张林田,黄少玉,陈小雪,等.高效液相色谱法测定水产品中四种氟喹诺酮类药物残留[J].理化分析-化学分册,2009,45(9):1086-1090.
[14]唐巍,卢艳芬,丑亚琴,等.高效液相色谱法同时测定鱼肉中四种喹诺酮类药物残留[J].中国兽药杂志,2012,46(12):26-29.
[15]李阳杰,龚志强,黄敏.HPLC测定呈味核苷酸二钠中IMP和GMP的含量[J].中国实验方剂学杂志,2012,18(7):116-118.
[16]郭根和,潘葳,苏德森,等.离子对高效液相色谱法同时测定鱼类中四种喹诺酮类药物的残留[J].色谱,2005,23(4):401-403.
[17]祝颖,张虹.UPLC-MS/MS法同时检测水产品中喹诺酮类药物残留[J].中国食品学报,2010,10(2):206-212.
[18]惠云华,沈晓盛,冯兵,等.固相萃取高效液相色谱法测定水产品中7种氟喹诺酮类药物残留[J].农药学学报,2009,11(4):462-466.
[19]丑亚琴,唐巍,卢艳芬,等.高效液相色谱法同时测定水产品中四种氟喹诺酮类药物残留前处理条件的优化[J].水产养殖,2013,34(1):21-27.
[20]尹燕敏,沈颖青,顾海东,等.固相萃取-液质联用法同时测定水中的喹诺酮类和磺胺类抗生素[J].化学分析计量,2013,22(3):29-32.
[21]张鑫,李丹妮,张文刚,等.畜禽肉蛋及水产中4种氟喹诺酮类药物残留的快速测定[J].分析试验室,2009,28(增刊):50-53.
[22]李盛安,冯敏玲,李拥军.超高效液相色谱法对罗非鱼中3种氟喹诺酮类兽药残留的测定[J].现代农业科学,2013,8:279-280.
(编辑:侯向辉)
Improvements of Retention Time of Quinolones in Liquid Chromatography
WANG Li-juan1,ZHANG Li2,QIAN Zhuo-zhen1,TANG Shui-fen1,YE Mei1,WU Cheng-ye1
(1.Fujian Fisheries Research Institute,Xiamen,Fujian 361013,China;2.China Institute of Veterinary Drugs Control,Beijing 100081,China)
Orthogonal test was employed to investigate the factors affecting retention time shift of quinolones in liquid chromatography.Retention time drift rate of norfloxacin,ciprofloxacin and enrofloxacin was used as evaluation criteria,and species of mobile phase,pretreatment conditions,sample types were investigated.It was shown that species of mobile phase was the main factor which affected retention time strongly.Retention time shift rate had obvious difference for norfloxacin,ciprofloxacin and enrofloxacin before and after adding the buffer salt mobile phase and optimizing the pretreatment conditions.The improved retention time drift rate reduced by 9.11%,7.74%and 7.97%respectively.Through this experiment,stable retention time of norfloxacin,ciprofloxacin and enrofloxacin by liquid chromatography was obtained,and the best detection method was attained.
quinolones;rentention time;shifts;liquid chromatography
2014-11-29
A
1002-1280(2015)05-0037-06
S859.84
福建省水产研究所青年科学研究创新基金项目(2014fjscq02)
王丽娟,博士,从事水产品质量安全和渔业环境监测研究。E-mail:wangguoqinli@163.com
张骊,硕士,从事兽药残留监测分析研究。E-mail:zhangli@ivdc.org.cn
