重组人干扰素α1b层析工艺中内毒素的去除
2015-01-16牛晓霞吴美英
牛晓霞 曹 艳 吴美英
北京三元基因工程有限公司,北京 102600
重组人干扰素α1b层析工艺中内毒素的去除
牛晓霞 曹 艳 吴美英▲
北京三元基因工程有限公司,北京 102600
目的通过检测评价重组人干扰素α1b各步层析工艺中内毒素的去除情况,为工艺验证提供参考。方法重组人干扰素α1b层析工艺采用DEAE Sepharose FF离子交换层析、单抗Sepharose-4B亲和层析和Sephacry-S100凝胶过滤层析。采用鲎试剂法检测层析各阶段产物中的内毒素含量,计算内毒素去除率。结果每步层析均有去除内毒素的作用,以亲和层析去除内毒素作用最强。最终所得蛋白的内毒素含量降至0.7EU/1mg以下,总去除率达到99.9999%。结论生产重组人干扰素α1b所用分离纯化层析技术在纯化蛋白的同时能有效去除产品中的内毒素,所得最终产品的内毒素含量远低于药典对注射剂的内毒素含量要求。
重组人干扰素α1b;柱层析;内毒素;去除
细菌内毒素(endotoxin)是革兰氏阴性细菌细胞壁外膜上的特有结构,其化学成分主要是脂多糖(LPS),只有当细胞死亡溶解或用人工方法破坏菌体细胞后才释放出来[1-2],所以叫做内毒素,又称之为热原。LPS具有极强的热原性,少量LPS(2ng/kg)经脉注射就可以引起发烧,大剂量的可以引起血液循环障碍和LPS休克症[3]。因此,非胃肠道给药制剂中内毒素的去除一直是一项重要的任务。
研究发现,LPS的一端是亲水的特异性多糖区,另一端是疏水的类脂A区,结构上类似表面活性剂。自然条件下,内毒素一般以聚合体形式存在,在亲水环境中还可以形成双层脂膜或脂囊。内毒素的磷酸集团和二价金属离子螯合,可进一步稳定内毒素分子间的聚合,形成更大的内毒素复合体,分子量可由几千到数千万不等[4]。正是由于这种性质的不均一性,生产者们难以找到一个简单的或者通用的内毒素去除方法。水溶液中去除内毒素的方法通常有超滤、活性炭吸附、化学降解和柱层析法等[5-6],各有优缺点,由于内毒素来源和工艺的多样性,在重组蛋白的内毒素去除时常采用多个工艺过程的结合。
重 组 人 干 扰 素α1b(recombination human interferon α1b,IFN-α1b)[7]基因工程蛋白采用大肠埃希菌作为表达系统进行发酵生产,在纯化前必须通过高压匀浆、超生破碎等方法将工程菌破壁,以释放蛋白。同时,细胞壁内的脂多糖也大量释放到缓冲液中,达到几万到几十万EU/mL的内毒素,这是IFN-α1b溶液中内毒素的主要来源。我们通过离子交换层析、亲和柱层析和凝胶过滤层析组合的分离纯化方法,使内毒素在IFN-α1b纯化过程中逐步被去除,最终使内毒素含量达到注射剂标准。
1 材料与方法
1.1 材料
细菌内毒素工作标准品购自中国食品药品检定研究院;鲎试剂及检查用水购自新北生化工业有限公司,鲎试剂采用实验室常规使用批次,已经灵敏度复核;DEAE Sepharose FF、Sepharose-4B和Sephacry-S100凝胶均购自GE公司;IFN-α1b发酵液及系列中间体由北京三元基因工程有限公司生产。
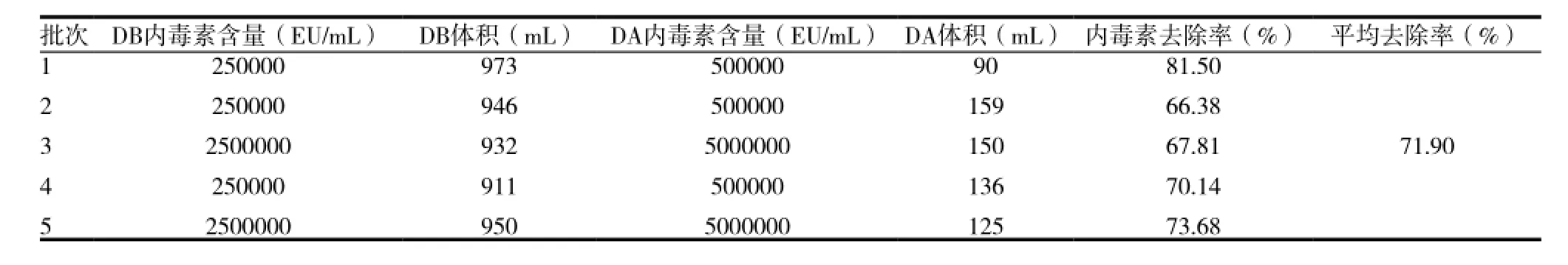
表1 DEAE Sepharose FF柱层析
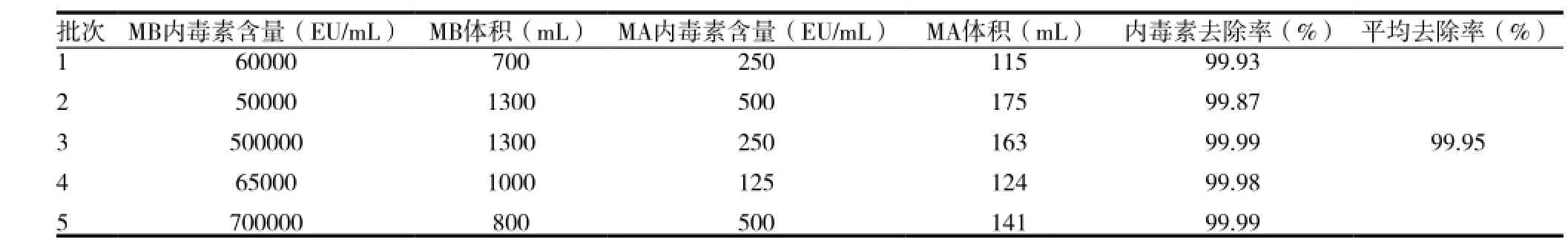
表2 单抗亲和层析
1.2 方法
1.2.1 DEAE Sepharose FF层析 取IFN-α1b粗提制品,以溶液Ⅰ(25mmmol/L Tris HCl,pH7.5)适当稀释(标记为DB),上样至用溶液Ⅰ平衡好的DEAE Sepharose FF层析柱,冲洗后以溶液Ⅱ(0.3mol/L NaCl 25mmmol/L Tris HCl,pH 7.5)洗脱得洗脱液(标记为DA)。记录上样体积和收样体积,分别取样。连续试验5批。
1.2.2 单抗亲和层析 将DA以溶液Ⅲ(20mmmol/L PBS,pH 7.0)适当稀释(标记为MB),上样至用溶液Ⅲ平衡好的Sepharose-4B单抗亲和柱,冲洗后用溶液Ⅳ(0.1mol/L甘氨酸pH2.5)洗脱,用NaOH调节pH至7.0,标记为MA,记录上样体积和收样体积,分别取样。连续试验5批。
1.2.3 Sephacry-S100凝胶过滤层析 将MA上样于用溶液Ⅴ(25mmmol/L PBS,pH7.0)平衡好的Sephacry-S100凝胶柱,以溶液Ⅴ作为洗脱液洗脱得到洗脱液SA。记录上样体积和收样体积,分别取样。连续试验5批。
1.2.4 干扰试验 选用TAL 0.25EU/mL,采用2010年版《中国药典》附录方法[8]对上述DB、DA、MB、MA及SA,进行干扰试验。
1.2.5 内毒素检测 选用TAL 0.25EU/mL,采用凝胶半定量试验法[5]。DB、DA稀释梯度为1万、10万、100万、1000万、5000万,在终点稀释度附近2倍系列稀释以确定准确的凝集终点;MB、MA稀释梯度为100、200、500、1000、2000、4000、8000、16000;SA稀释梯度为1、5、10、20、40、80、100;每一稀释度2个平行,以第一个出现阴性结果的稀释度作为反应终点。内毒素含量(EU/mL)=0.25×反应终点稀释倍数,内毒素总量(EU)=细菌内毒素含量×该溶液体积,内毒素去除率(%)=(1-上柱后内毒素总量/上柱前内毒素总量)×100%。
2 结果
2.1 干扰试验
干扰试验表明:SA无干扰作用,DB、DA、MB和MA在10倍以上稀释时无干扰作用,由于样品中含有较多内毒素,在实际检测中稀释倍数远远大于10倍,所以可用TAL 0.25EU/mL对样品进行内毒素检查。
2.2 DEAE Sepharose FF层析
取DEAE Sepharose FF层析前后的样品DB和DA,在规定条件下与TAL反应,结果显示:在连续5批的试验中,其内毒素去除率分别达到81.50%、66.38%、67.81%、70.14%和73.68%,平均去除率为71.90%(表1)。随着上样体积和洗脱液体积比的增大,其内毒素去除率增大。
2.3 单抗亲和层析
取单抗亲和层析前后的样品MB和MA,在规定条件下与TAL反应,结果显示:连续5批的试验中,其内毒素去除率分别达到99.93%、99.87%、99.99%、99.98%和99.99%,平均去除率99.95%(表2)。相对于DEAE Sepharose FF层析,其内毒素去除效果更高,更稳定。
2.4 Sephacry-S100凝胶过滤层析
取Sephacry-S100凝胶过滤层析后的样品,在规定条件下与TAL反应,计算其内毒素含量与MA相比对,结果显示:连续5批的试验中,其内毒素去除率分别达到99.73%、99.82%、99.72%、99.84%和99.92%,平均去除率为99.81%(表3)。SA中蛋白含量为以2mg/mL计算,其内毒素含量达到0.7EU/1mg以下。
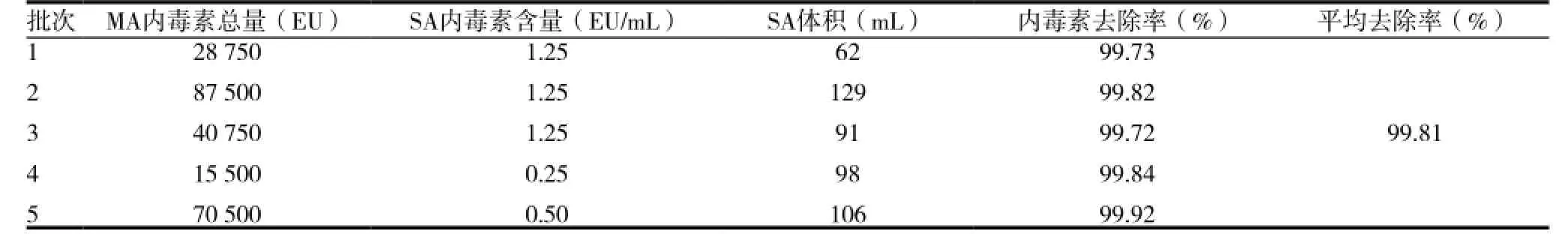
表3 Sephacry-S100凝胶过滤层析
DEAE Sepharose FF离子 交换层 析、单 抗Sepharose-4B亲和层析和Sephacry-S100凝胶过滤层析,以单抗亲和层析内毒素去除效果最好,经过上述三步纯化,总内毒素去除率达到99.9999%。
3 讨论
对于工艺中内毒素的去除,有的采用普通的纯化技术[9-10],也有的采用专门的内毒素去除工艺,如活性炭吸附。LIU等[11]发展了一种采用Triton X-114从重组蛋白中去除内毒素的方法。据报道,利用这种相分离的方法,对内毒素的去除率达到99%以上,蛋白质的回收率大于90%,且不影响有效成分的活性。本研究采用普通纯化技术组合法,随着工艺的推进,目的蛋白纯度升高,而内毒素逐渐清除减少。
离子交换层析速度快、载量高、浓缩效应好,在早期下游纯化中担当重要角色。一般而言,内毒素比蛋白质在DEAE介质上的结合强很多,分子量越小的内毒素结合得越强[12],但在目的蛋白洗脱条件下,仍然有大量内毒素被洗脱。即便如此,DEAE仍然有着重要的去除内毒素的作用,其内毒素去除的量是巨大的,虽然去除率不是最高的,可见在内毒素含量特别高的情况下,其内毒素去除率并不理想。DEAE去除内毒素的效果还跟其浓缩效应有关,一般来讲,洗脱前后浓缩倍数越大,其内毒素去除率越高。
单抗亲和层析在内毒素去除率上具有上佳表现,是由于单克隆抗体键合Sepharose-4B亲和介质与目标蛋白结合而不与内毒素结合,从而可以去除内毒素。但由于介质本身的非特异性吸附作用,使一部分内毒素因与介质结合而保留。由此看来,在洗脱前对亲和柱进行清洗,可以减少一些非特异性吸附,从而获得更高的内毒素清除率。
Sephacry-S100是一种凝胶过滤介质,其利用凝胶的网状结构根据分子大小进行分离的一种方法。常用于去除蛋白药物内的大分子寡聚物和小分子无机盐,也可以去除一部分内毒素。作为层析工艺的最后一步,它起着至关重要的作用。其内毒素去除作用机制大致有两个,一是因为IFN和内毒素分子量在其分离范围内,二是凝胶介质本身对内毒素有吸附作用。
通过上述几个层析步骤的组合,不仅获得了较纯的IFN-α1b蛋白,更是去除了其中的内毒素。了解这个过程中内毒素的变化规律,对于控制最终产品的质量是非常有意义的。
[1] Hase S,Hofstad T,Rietschel ET.Chemical structure of lipid A component of lipopolysaccharides from Fusobacterium nucleatum[J].J Bacteriol,1977,129(1):9-14.
[2] 苑庆华编译.细菌内毒素检查法-定量法[M].天津:天津药品检验所,1999:120-123.
[3] 邵英光,李京华,魏桂林,等.内毒素的去除策略[J].广州化学,2003,28(2):38-45.
[4] Harwood LJ,Russell NJ.Lipids and Plant membranes[S].1984:30-31.
[5] 陈昕.下游层析工艺中热原的去除[J].中国生物工程杂志,2002,22(4):100-103.
[6] 秦峰,刘学良,魏桂林,等.生物医药制剂中内毒素去除研究进展[J].药物生物技术,2003,10(1):53-56.
[7] 侯云德.干扰素及其临床应用[M].南京:江苏科学技术出版社,1981:50.
[8] 国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2010:附录95.
[9] 王素红,韩金祥,王世立,等.离子交换色谱法去除rhOP-1蛋白溶液中内毒素的方法[J].医学分子生物学杂志,2008,5(3):244-246.
[10] 徐向荣,马国昌,王昌梅,等.层析法去除重组人血清白蛋白干扰素α2b融合蛋白的内毒素[J].生物工程学报,2008,24(1):159-163.
[11] Liu SG,Rowel T,Shannon M,et al.Removal of endotoxin from recombinant protein preparations[J].Clinical Biochemistry,1997,30(6):455-463.
[12] Hou KC,Zaniewski R.Endotoxin removal by anionexchange polymeric matrix[J]. Biotechnology and Applied Biochemistry,1990,12(3):315-324.
Removal of endotoxin in the chromatography process of recombinant human interferon α1b
NIU Xiaoxia CAO Yan WU Meiying
Beijing Triprime Genetic Engineering Co.Ltd, Beijing 102600, China
ObjectiveEvaluated the removal of endotoxin in the chromatography process of recombinant human inerferen α1b(rHIFN-α1b),to provide a reference for the process validation.MethodsWe used chromatography to remove endotoxin during the purification of rHIFN-α1b. Ion exchange chromatography of DEAE Sepharose Fast Flow, affinity chromatography of monoclonal antibody bonding Sepharose-4B and gel filtration of Sephacry-S100 were applied consequently. The endotoxin levels were measured by Limulus Amebocyte Lysate gel-clot assay.ResultsEach step process can remove endotoxin, affinity chromatography has the strongest effect. In the final product, up to 99.9999% endotoxin of rHIFN-α1b was removed and to a concentration of 0.7EU/1mg.ConclusionThe process was effective to purify IFN-α1b and remove exdotoxin simultaneously. The endotoxin level of the final product is much lower than Chinese Pharmacopoeia requirements.
Recombinant human interferon α1b; Endotoxin; Chromatography; Removal
TQ464
B
2095-0616(2015)03-51-03
2014-12-02)
▲通讯作者
