苦碟子注射液联合光动力疗法与玻璃体内注射Ranibizumab治疗渗出型年龄相关性黄斑变性
2014-11-13陆秉文吴星伟
陆秉文 吴星伟
年龄相关性黄斑变性(age-related macular degeneration,AMD)又名老年性黄斑变性,是一种随年龄增长而发病率逐年上升并导致中心视力逐渐下降的疾病,是欧美国家老年人视力丧失的首要原因[1]。临床上将其分为萎缩型(干性)和渗出型(湿性)两种。前者以黄斑区地图状萎缩为特征,后者以脉络膜新生血管(choroidal neovascularization,CNV)形成为特征,常引起出血、纤维瘢痕化。临床近90%AMD患者的视力丧失是由CNV引起的,治疗也主要是针对CNV的抑制和消除。光动力疗法(photodynamic therapy,PDT)能有效稳定和减缓CNV引起的视力丧失,是目前国际公认的治疗黄斑部CNV安全有效的方法[2-5]。抗血管内皮生长因子(vascular endothelial growth factor,VEGF)药物是目前治疗渗出型AMD的研究热点,对于减少CNV渗漏、减轻黄斑水肿、保存或改善中心视力均有明显疗效[6-7]。我院吴星伟主任医师将我国传统中医药治疗理念与眼科现代新技术相结合,应用苦碟子注射液联合PDT与玻璃体内注射Ranibizumab治疗合并黄斑中心凹下或中心凹旁CNV的渗出型AMD患者,取得了较好的临床疗效。我们即应用该中西医结合治疗理念,对一组合并黄斑中心凹下或中心凹旁CNV的渗出型AMD患者进行了长期的临床随访观察,现将结果报告如下。
1 资料与方法
1.1 一般资料 回顾性分析2011年1月至2012年4月我院眼科门诊收治的41例(41眼)渗出型AMD患者的临床资料。所有患者均主述有视力下降、视物变形和中心暗影,经过视力、眼压、眼底检查、眼底荧光血管造影(fundus fluorescein angiography,FFA)和(或)吲哚菁绿血管造影(indocyanine green angiography,ICGA)及光学相干断层扫描(optical coherence tomography,OCT)检查确诊,最佳矫正视力为0.01~0.60。按治疗方法不同分为两组:联合组21例21眼,给予苦碟子注射液联合 PDT与玻璃体内注射Ranibizumab治疗;对照组20例20眼,仅行 PDT联合玻璃体内注射Ranibizumab治疗。治疗前两组患者年龄、视力、中央视网膜厚度(central retinal thickness,CRT)及CNV复合体厚度、CNV渗漏情况等差异均无统计学意义(均为P>0.05)。研究及治疗的潜在风险和益处均已清楚告知患者,均获得患者的知情同意并签字。两组患者临床资料见表1。

表1 两组患者的临床资料Table 1 Clinical data of patients in two groups
1.2 患者入选和排除标准 入选标准:(1)年龄50~80岁;(2)一眼或双眼符合渗出型AMD临床诊断且经FFA和(或)ICGA确诊为中心凹下CNV或中心凹旁CNV;(3)未经治疗者;(4)病程≤2 a者;(5)最佳矫正视力0.01~0.60;(6)屈光间质基本清晰,不妨碍眼底检查。排除标准:合并其他眼底疾病者、观察期间发生其他眼病者、观察期间使用其他药物影响疗效者以及不按时用药和复诊者。
1.3 治疗方法
1.3.1 PDT治疗方法 按照PDT治疗AMD(TAP)研究组[2]和维替泊芬 PDT 治疗(VIP)研究组[4]的方法进行。根据患者的体表面积,6 mg·m-2的维替泊芬(维速达尔,瑞士诺华制药有限公司)溶解于葡萄糖注射液中静脉滴注,注射15 min后,在表面麻醉下散大瞳孔,在半导体激光专用裂隙灯(ACTIVIS,法国光太公司)下,采用能量50 J·cm-2、强度600 mW·cm-2、曝光时间83 s的689 nm半导体激光行标准治疗。治疗后患者避光48 h。
1.3.2 玻璃体内注射 Ranibizumab方法 PDT治疗后1周内行玻璃体内注射Ranibizumab。玻璃体内注射操作均在手术室内进行,按照眼科手术的要求进行消毒和无菌操作,术眼术前用5 g·L-1左氧氟沙星滴眼液滴眼冲洗结膜囊,消毒铺巾,盐酸奥布卡因滴眼液滴眼行表面麻醉,于颞下方角巩膜缘后3.5 mm 处进针,注射 0.5 mg Ranibizumab(Lucentis,Genentech Inc.),术毕涂抗生素眼膏,包扎。随访期内,如果病变有持续渗漏或复发性视网膜水肿,间隔4~6周重复玻璃体内注射一次。
1.3.3 苦碟子注射液干预 联合组患者随访观察期间,同时予苦碟子注射液干预治疗。苦碟子注射液(沈阳双鼎有限公司)20 mL加入250 mL生理盐水内静脉滴注,每天1次,每个疗程连续注射10 d;1个月为1个疗程。对照组不做处理。
1.4 随访 联合治疗后1个月、3个月、6个月、12个月各随访1次。所有病例由指定医师全程进行治疗前后的临床观察,用与治疗前相同的方法和设备对患者进行眼部检查:采用标准视力表行最佳矫正视力检查;采用日本TOPCON公司的非接触式眼压计CT-80行眼压检查;采用日本Nikon公司的免散瞳眼底相机进行眼底彩色照相;采用德国海德堡血管造影仪行FFA及ICGA检查,明确CNV渗漏部位及面积;采用德国海德堡OCT仪对黄斑部进行检查。
1.5 疗效评价 以末次随访时的最佳矫正视力、FFA和(或)ICGA、OCT检查结果作为疗效评价指标。
1.5.1 最佳矫正视力 视力提高2行或以上为提高,视力波动在1行以内为稳定,视力下降2行或以上为下降。
1.5.2 CNV渗漏情况 根据 FFA和(或)ICGA检查结果评定CNV的渗漏情况,将CNV闭合情况分为4级[8]:(1)CNV完全闭合:病灶中CNV完全没有荧光素渗漏,仅表现为CNV组织染色;(2)CNV大部分闭合:渗漏不足治疗前CNV渗漏范围的50%;(3)CNV小部分闭合:渗漏占治疗前 CNV渗漏范围的50%或以上;(4)CNV复发:出现新的CNV或CNV渗漏范围超过原来病灶的边界。
1.5.3 OCT 检查结果 参照 García-Layana 等[9]和Karacorlu等[10]的研究,制定 CRT及 CNV复合体厚度的测量标准:CRT为视网膜内层反光带最高点到CNV反光团块下界延长线之间的距离;CNV复合体厚度为视网膜色素上皮-脉络膜毛细血管层向神经上皮层内隆起的团块反光表面最高点到CNV反光团块下界延长线之间的距离。
1.6 统计学处理 计量资料以均数±标准差表示,用t检验;计数资料组间总体比较及治疗前后比较用卡方检验;数据处理用SPSS 17.0软件包。P<0.05为差异有统计学意义。
2 结果
2.1 视力 末次随访时,对照组 20眼中 11眼(55.0%)视力提高,7眼(35.0%)视力稳定,2眼(10.0%)视力下降,11眼(55.0%)视物变形减轻,5眼(25.0%)中心暗点减小;联合组 21眼中 13眼(61.9%)视力提高,7眼(33.3%)视力稳定,1眼(4.8%)视力下降,16眼(76.2%)视物变形减轻,7眼(33.3%)中心暗点减小。
末次随访时,对照组与联合组最佳矫正视力较治疗前均明显提高,差异均具有显著统计学意义(t=6.086、5.605,均为 P<0.01);治疗后 1 个月、3个月、6个月、12个月,联合组最佳矫正视力改善情况均优于对照组(表2)。
2.2 FFA和(或)ICGA检查 所有治疗眼渗出病灶缩小,出血及神经上皮水肿完全吸收或消失。联合组21眼CNV完全闭合16眼(占76.2%),大部分闭合5眼(占23.8%);对照组20眼 CNV完全闭合15眼(占 75.0%),大部分闭合 5眼(占 25.0%)。随访期内CNV均未见复发。
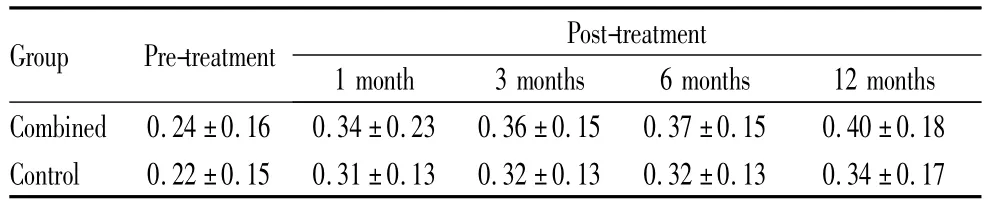
表2 两组治疗前后不同时间最佳矫正视力情况Table 2 Preoperative and postoperative best corrected visual acuity at different time points in two groups
2.3 OCT检查 所有患眼CNV周围视网膜水肿吸收或好转,神经上皮脱离复位或好转;CNV强反射区域明显缩小,CNV复合体厚度降低。
末次随访时,对照组与联合组CRT较治疗前均明显减少,差异均具有显著统计学意义(t=11.192、10.149,均为P<0.01);对照组与联合组CNV复合体厚度较治疗前亦均明显减少,差异均具有显著统计学意义(t=8.986、10.299,均为 P <0.01)。治疗后 1 个月、3个月、6个月、12个月,联合组CRT与CNV复合体厚度减少情况均优于对照组(表3-表4)。
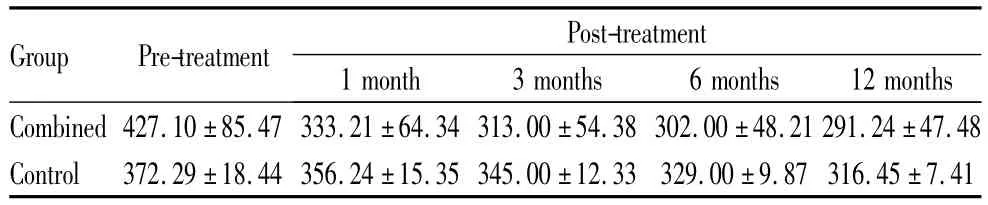
表3 两组患者治疗前后不同时间CRT情况Table 3 Preoperative and postoperative CRT at different time points in two groups (l/μm)
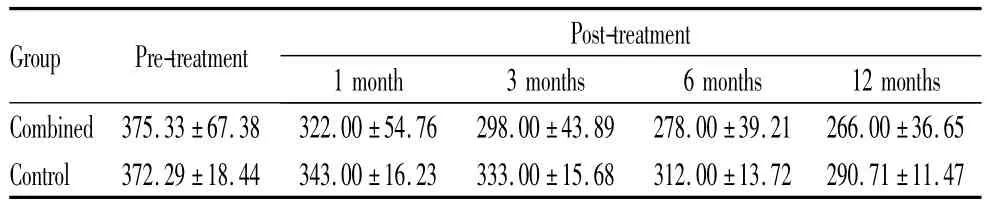
表4 两组患者治疗前后不同时间CNV复合体厚度情况Table 4 Preoperative and postoperative CNV complex thickness at different time points in two groups(l/μm)
2.4 治疗次数 所有治疗眼均接受1次PDT治疗。联合组中13眼行1次玻璃体内注射治疗,8眼行2次玻璃体内注射治疗;联合组Ranibizumab玻璃体内注射治疗次数为(1.38±0.50)次。对照组中4眼行1次玻璃体内注射治疗,13眼行2次玻璃体内注射治疗,2眼行3次玻璃体内注射治疗,1眼行4次玻璃体内注射治疗;对照组Ranibizumab玻璃体内注射治疗次数为(1.96±0.83)次。
2.5 并发症情况 所有患者治疗过程中均未发现光敏剂渗漏,治疗后未出现皮肤光毒性反应。随访期间未见眼内感染、白内障、青光眼及与玻璃体内注药相关的并发症发生。
3 讨论
AMD是目前老年人的主要致盲因素,临床近90%AMD患者的严重视力丧失是由CNV引起的[1]。因此,有效、持久地控制CNV的发生发展是治疗渗出型AMD的关键。
PDT是目前公认的治疗黄斑中心凹下和中心凹旁CNV的较好方法[2-5],因其可以有效地靶向性破坏CNV,且不会损伤临近的视网膜和脉络膜组织及感觉神经系统。但是,PDT是针对CNV的破坏性治疗,只对已形成的病理性新生血管有效,并不能防止CNV的再发生和发展,因此往往需要重复治疗,2 a内重复治疗平均高达 5.6次[3-4],价格昂贵;且 PDT治疗后阻塞侧支脉络膜毛细血管将会导致缺血,引起促血管生成因子和炎症因子的表达增加,不利于患者中心视力的提高[11-12]。抗VEGF药物是目前治疗渗出型AMD的研究热点。Ranibizumab是重组人源化抗VEGF单克隆抗体片段,可与VEGF所有异构体结合并使其失活,抑制新生血管形成并增加血管通透性,于2006年6月被美国FDA批准用于治疗渗出型AMD[13]。已有大范围的随机临床实验表明,玻璃体内注射Ranibizumab对于CNV引起的AMD有较好的效果[6-7],可明显减少CNV渗漏、减轻黄斑水肿、促进脱离的RPE复位、保存或改善现有视力。但是,抗VEGF药物并不能靶向针对病灶或从根本上阻止VEGF的不断产生,且单独应用时需长期、多次重复注射,价格昂贵,亦增加了眼内炎等严重并发症发生的风险[14]。PDT与抗VEGF药物联合治疗能够取长补短,既能有效闭塞已经形成的病理性新生血管,又能通过下调VEGF表达水平阻止其复发或再生,改善或稳定患者视力,减少PDT与玻璃体内注射的次数,并减少单一治疗的副作用。已有大量国内外文献报道,联合治疗组的平均治疗次数明显少于单一治疗组[15]。有研究表明,PDT治疗后1周内VEGF明显上调[11],因此,我们在封闭 CNV后 1周内联合玻璃体内注射Ranibizumab。
苦碟子为菊科植物苦荬菜的提取物,又名满天星,具有清热解毒、活血化瘀、排脓及止痛等功效,苦碟子注射液连续静脉滴注可起到较好的利水渗湿、化痰消瘀的作用。在临床实践中,我们将该中医药疗法应用于渗出型AMD患者,取得了较好的疗效。因此,我们进一步的设想是:将传统的中医药治疗理念与眼科现代新技术相结合,能否事半功倍,使疗效更显著、稳定,且使需要重复治疗的次数进一步减少,从而降低治疗费用,让更多人获益。
本研究选用PDT联合玻璃体内注射二联治疗的患者作为对照组,观察联合中医药治疗理念后的三联治疗能否在临床取得更佳的疗效。在对病例的随访观察中我们发现,患者的视力预后均较好,末次随访时的最佳矫正视力与治疗前相比明显提高;且大部分患者的视力在治疗后第1个月改善明显,之后保持稳定;部分患者随访时出现视力再次下降,CNV复发或新发,给予再次玻璃体内注射治疗,患者视力仍会提高。患者的黄斑区视网膜水肿均较治疗前明显消退,且在随访观察期间保持稳定。视力提高与病灶区视网膜厚度没有必然联系,但我们发现对于病程短、治疗前视力较好的患者,局部视网膜水肿的消退、脱离的神经上皮的复位有助于视网膜功能的恢复或接近正常。患者的CNV复合体厚度亦较治疗前明显减小,且在随访观察期间保持稳定。这与FFA和(或)ICGA检查结果显示的所有治疗眼渗出病灶缩小,出血及神经上皮水肿完全吸收或消失相吻合,说明联合(二联/三联)治疗对于CNV病灶的封闭及对新生血管的阻断有较好疗效。
本研究中,联合组患者的视力改善、黄斑区视网膜厚度以及CNV复合体厚度的减少都比对照组显著,这可能与苦碟子注射液利水消肿的作用有关,可减少视网膜层间积液,减少瘢痕形成。联合组治疗次数也明显低于对照组,根据欧洲和北美的多中心研究,第1年内每眼重复 PDT治疗的次数平均为2.4次[16],且重复治疗的比例在90%以上。而根据PDT联合抗VEGF治疗的研究,玻璃体内注射的次数平均为1.65次[15]。我们的研究结果发现二联治疗的重复治疗次数为1.96次,大致与国内外研究结果相符,而三联治疗的平均治疗次数仅为1.38次,更具有经济学效益,可被更多人接受。
本研究结果表明,中西医结合新方法(三联治疗)对渗出型AMD的治疗可达到较好的标本兼治,减少患者所需重复治疗的次数,取得更好的社会效益。但本研究样本量不大、随访时间有限,故仍需大样本、多中心、前瞻性的随机对照研究来深入探讨,以期寻求治疗渗出型AMD患者的最佳方案,达到最佳的临床疗效并取得最大的社会效益。
1 Bunce C,Wormald R.Leading cause of certification for blindness and partial sight in England & Wales[J].BMC Public Health,2006,6(1):58-65.
2 Treatment of age-related macular degeneration with photodynamic therapy(TAP)study group.Photodynamic therapy of subfoveal choroidal neovascularization in age-related macular degeneration with verteporfin:one-year results of 2 randomised clinical trials-TAP report[J].Arch Ophthalmol,1999,117(10):1329-1345.
3 Bressler NM,Treatment of age-related macular degeneration with photodynamic therapy(TAP)study group.Photodynamic therapy of subfoveal choroidal neovascularization in age-related macular degeneration with verteporfin:two-year results of 2 randomized clinical trials-TAP report 2[J].Arch Ophthalmol,2001,119(2):198-207.
4 Verteporfin in photodynamic therapy study group.Verteporfin therapy of subfoveal choroidal neovascularization in age-related macular degeneration:two-year results of a randomized clinical trial including lesions with occult with no classic choroidal neovascularizatlon-vertepofin in photodynamic therapy report 2[J].Am J Ophthalmol,2001,131(5):541-560.
5 Blumenkranz MS,Bressler NM,Bressler SB,Donati G,Fish GE,Haynes LA,et al.Verteporfin therapy for subfoveal choroidal neovascularization in age-related macular degeneration:three-year results of an open-label extension of 2 randomized clinical trials--TAP Report no.5[J].Arch Ophthalmol,2002,120(10):1307-1314.
6 Rosenfeld PJ,Brown DM,Heier JS,Boyer DS,Kaiser PK,Chung CY,et al.Ranibizumab for neovascular age-related macular degeneration[J].N Engl J Med,2006,355(14):1419-1431.
7 Dhoot DS,Kaiser PK.Ranibizumab for age-related macular degeneration[J].Expert Opin Biol Ther,2012,12(3):371-381.
8 张美霞,陆方,严密,张军军,孟 丹,杜彩凤,等.光动力疗法治疗渗出型老年性黄斑变性四年临床观察总结[J].中华眼底病杂志,2004,20(5):275-279.
9 García-Layana A,Salinas-Alamán A,Maldonado MJ,Sainz-Gómez C,Fernández-Hortelano A.Optical coherence tomography to monitor photodynamic therapy in pathological myopia[J].Br J Ophthalmol,2006,90(5):555-558.
10 Karacorlu SA,Ozdemir H,Senturk F,Karacorlu M.Optical coherence tomography after photodynamic therapy for patients with pathologic myopia[J].Retina,2006,26(7):752-756.
11 Bottoni F,Romano M,Massacesi A,Berqamini F.Remodeling of the vascular channels in retinal angiomatous proliferations treated with intravitreal triamcinolone acetonide and photodynamic therapy[J].Graefes Arch Clin Exp Ophthalmol,2006,244(11):1528-1533.
12 Augustin AJ,Schmidt-Erfurth U.Verteporfin therapy combined with intravitreal triamcinolone in all types of choroidal neovascularization due to age-related macular degeneration[J].Ophthalmology,2006,113(1):14-22.
13 Heier JS,Antoszyk AN,Pavan PR,Leff SR,Rosenfeld PJ,Ciulla TA,et al.Ranibizumab for treatment of neovascular age-related macular degeneration:a phase I/II multicenter,controlled,multidose study[J].Ophthalmology,2006,113(4):633-637.
14 Scott AW,Bressler SB.Long-term follow-up of vascular endothelial growth factor inhibitor therapy for neovascular age-related macular degeneration[J].Curr Opin Ophthalmol,2013,24(3):190-196.
15 Krebs I,Vécsei Marlovits V,Bodenstorfer J,Glittenberg C,Ansari Shahrezaei S,Ristl R,et al.Comparison of Ranibizumab monotherapy versus combination of Ranibizumab with photodynamic therapy with neovascular age-related macular degeneration[J].Acta Ophthalmol,2013,91(3):e178-183.
16 Gomi F,Ohji M,Sayanagi K,Sawa M,Sakaguchi H,Oshima Y,et al.One-year outcomes of photodynamic therapy in age-related macular degeneration and polypoidal choroidal vasculopathy in Japanese patients[J].Ophthalmology,2008,115(1):141-146.
