羧基化多壁碳纳米管固相萃取-液相色谱-串联质谱法测定环境水体中四溴双酚A和双酚A
2014-08-03寇立娟梁荣宁
寇立娟, 梁荣宁
(1.中国科学院海岸带环境过程与生态修复重点实验室,山东省海岸带环境过程重点实验室,中国科学院烟台海岸带研究所,山东烟台264003;2.中国科学院大学,北京100049)
四溴双酚A(tetrabromobisphenol A,TBBPA)是全球使用最广泛的溴化阻燃剂,全球每年产量大约为1.2×105t,主要应用于电子线路板及电子产品中的塑料高聚物中[1];双酚A(bisphenol A,BPA)作为重要的有机化工原料,主要用于生产聚碳酸酯、环氧树脂及聚砜树脂等多种高分子材料[2]。二者化学性质非常相似,被认为是一类潜在的环境激素,有研究表明它们可扰乱动物体正常的内分泌系统,并具有致畸、致癌和致突变的作用,目前这类化合物已成为环境/健康领域研究的热点[3,4]。在应用过程中它们均以共价键键合形式存在,但酸、碱、热条件可破坏共价酯键使其缓慢释放到环境中,并且TBBPA在环境条件下可以降解为BPA[5](二者结构式见图1)。现已有研究显示 TBBPA和BPA在全球多种环境介质中被广泛检出[6-9]。因此建立快速、准确、灵敏高效的TBBPA和BPA分析方法尤为重要。

图1 TBBPA和BPA的结构式Fig.1 Structures of tetrabromobisphenol A(TBBPA)and bisphenol A(BPA)
目前,TBBPA和BPA类环境污染物质残留检测方法主要有高效液相色谱法(HPLC)、气相色谱-质谱法(GC-MS)和液相色谱-串联质谱法(LC-MS/MS)[5,9,10]。其中 GC-MS 需要对样品进行复杂的衍生化处理[5];而 LC-MS/MS可直接对环境样品中TBBPA和BPA进行定性和定量检测,且具有高灵敏度、高准确度、分析快速等优点,是目前应用较多的酚类环境激素检测方法。然而,由于酚类环境激素化合物在环境水体中的残留浓度低,且水体中干扰物较多,因此需要对样品进行富集和浓缩。固相萃取(solid-phase extraction,SPE)技术具有富集效率高、使用溶剂少、操作简单、快速以及可有效消除样品的基体效应等优点,已被广泛用于TBBPA和 BPA 检测的样品前处理中[7,11]。
固相萃取吸附剂是影响固相萃取效果的关键因素,常见的吸附剂填料为硅胶、C8以及C18等。利用这类材料的强疏水性,已发展了众多固相萃取方法用于水体中 TBBPA 和 BPA 的富集与分离[8,11],但这种方法对水相中的大多数有机物有保留作用。分子印迹聚合物(MIPs)是人工合成的一种聚合物微球,其对特定分子具有特异选择性,已被广泛用作固相萃取吸附剂[12,13]。然而,MIPs的合成主要是基于模板分子和功能单体之间的氢键作用,因此主要应用在有机溶剂提取液中待测物质的富集,在水相环境中直接应用受到很大限制。新型纳米材料由于具有比表面积大和吸附能力强等特点,其作为固相萃取吸附剂引起了越来越多的关注。磁性纳米粒子依靠静电作用力可吸附BPA,已被用作固相萃取剂富集牛奶中的BPA[14],但pH可干扰两者之间的静电作用力从而影响固相萃取效果。多壁碳纳米管(MWCNT)是一种以碳为基础的纳米材料,具有多孔的疏水表面和离域大π电子系,可以非共价吸附芳香类化合物,且不受氢键和pH干扰,是一种理想的固相萃取吸附剂,已成功应用于水体中多环芳烃、有机农药和磺胺类药物等污染物质的富集与分离[15-17]。然而,关于 MWCNT和足球烯 C60对有机酚酸类小分子的富集效率的比较还未见报道。本研究比较了MWCNT、羧基功能化多壁碳纳米管(COOH-MWCNT)和C60作为固相萃取剂对TBBPA和BPA的富集效率,并采用COOH-MWCNT作为固相萃取剂,结合HPLC-MS/MS技术,建立了环境水体中TBBPA和BPA的分离分析方法,并将其应用于实际样品的测定。
1 实验部分
1.1 仪器、试剂与材料
TSQ Quantum Access MAX三重四极杆LCMS仪(美国ThermoFisher公司);固相萃取仪(美国Supelco公司);Pall超纯水仪(美国Pall公司);氮吹仪(天津奥特赛恩斯仪器有限公司)。
TBBPA(纯度99%)和BPA(纯度99%)购自美国Sigma Aldrich公司。甲醇(色谱纯)和乙腈(色谱纯)购自德国CNW有限公司。其他所用试剂均为分析纯,购自上海国药集团化学试剂公司。MWCNT(纯度﹥95%,直径﹤8 nm;长度0.5~2 μm)、COOH-MWCNT(纯度﹥95%,直径﹤8 nm;长度0.5~2 μm;羧基化率3.86%)和 C60(纯度98%)购自南京吉仓纳米科技有限公司。0.45 μm玻璃纤维滤膜、有机相针式过滤器和固相萃取小柱(Polypro,3 mL)购自上海安谱科学仪器有限公司。
1.2 溶液的配制
用乙腈配制100 mg/L的TBBPA和BPA混合标准储备液,固相萃取条件考察时用纯水逐级稀释至所需浓度,LC-MS/MS定量分析时用乙腈逐级稀释至所用浓度。
1.3 样品前处理
分别准确称取 60.0 mg MWCNT、C60或COOH-MWCNT,装填在两端有筛板的聚丙烯固相萃取小柱中。SPE小柱依次经过3 mL甲醇和3 mL纯水活化平衡,10 mL水样或加标样品以1 mL/min的速度通过SPE柱富集,然后采用3 mL超纯水淋洗残留在SPE柱上的离子及强极性的干扰物质,最后用6 mL乙酸乙酯洗脱目标物质;洗脱液经氮气吹至干,再用乙腈定容至0.2 mL,过0.45 μm 滤膜,待LC-MS/MS分析。
1.4 LC-MS/MS 条件
LC条件:色谱柱为Thermo Scientific Hypersil C18(150 mm ×4.6 mm,3 μm);柱温为40 ℃;流动相为乙腈/水(8∶2,v/v);流速为1.0 mL/min;进样量为 10 μL。
MS/MS条件:离子源为加热电喷雾电离源(HESI),负离子模式;蒸发温度为120℃;喷雾电压为3.0 kV;离子传输管温度为275℃;碰撞气为氩气。其他质谱参数见表1。
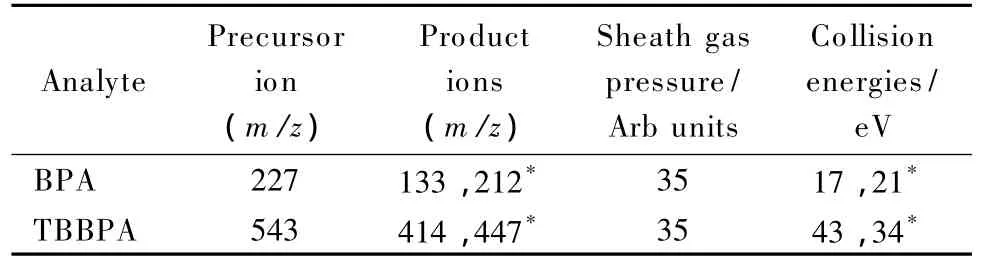
表1 TBBPA和BPA的质谱采集参数Table 1 MS/MS parameters of TBBPA and BPA
2 结果与讨论
2.1 LC-MS/MS条件的优化
考察了1.0 mg/L的TBBPA和BPA混合标准溶液在不同乙腈-水体系下的分离效果。结果表明,采用乙腈-水作为流动相时,TBBPA和BPA的分离效果与以乙腈-水(含0.1%(v/v)甲酸)为流动相基本一致;并且随乙腈含量升高,分离效果变差。综合两种化合物质谱响应的离子强度和峰形,最终确定以乙腈-水(8∶2,v/v)作为LC的流动相。TBBPA和BPA的总离子流图显示:TBBPA和BPA的保留时间分别为1.98 min和3.08 min(见图2)。此外,还分别考察了TBBPA和BPA在正、负离子模式下的响应,发现在负离子模式下响应较好;同时优化了碰撞电压、锥孔电压等质谱条件,采用多反应监测(MRM)模式,选择丰度最高的子离子作为定量离子,其次的子离子作为定性离子(见表1)。

图2 TBBPA和BPA的总离子流图和MRM图Fig.2 Total ion chromatogram and MRM chromatograms of a mixed solution of TBBPA and BPA standards
2.2 固相萃取条件的优化
首先考察了MWCNT、C60和COOH-MWCNT 3种固相萃取柱对TBBPA和BPA的吸附效率,当样品中添加水平为1 mg/L、上样量为10 mL水溶液时,MWCNT和 COOH-MWCNT几乎全部保留了TBBPA和BPA,而C60吸附了约95%的TBBPA,但仅保留了约50%的BPA(见图3),这主要是因为碳纳米管材料具有由众多碳原子六元环组成的大共轭平面结构,与TBBPA和BPA的π-π作用力较强;而C60每面仅有一个碳原子六元环或五元环,和BPA形成的π-π作用力较弱,故对其保留性差,有报道指出C60对苯酚类化合物的吸附效率不超过55%[18];C60对TBBPA的吸附效率高于BPA,可能是由于TBBPA苯环上含有4个溴原子,它又具有未共用的p电子,与苯环形成了p-π共轭,使其和C60之间的非共价作用加强而达到较好的保留效果。

图3 不同碳材料对TBBPA和BPA的固相萃取吸附效率Fig.3 Adsorption efficiencies of TBBPA and BPA on three different carbon materials
选择MWCNT和COOH-MWCNT作为固相萃取剂,考察了不同洗脱溶剂对TBBPA和BPA的洗脱效果。结果显示:乙酸乙酯的洗脱效果优于乙腈和甲醇;当COOH-MWCNT作为SPE吸附剂时,用6 mL乙酸乙酯洗脱可获得满意的回收率;而相同情况下MWCNT固相萃取对TBBPA和BPA的回收率分别为50%和80%左右(见图4),这可能因为碳纳米管表面羧基化后,目标物和纳米管表面的π-π作用减弱,虽然目标物和碳纳米管表面的羧基基团还存在氢键作用,但整体作用力要小于未修饰的碳纳米管,因此以COOH-MWCNT作固相萃取剂时目标化合物较容易被洗脱。此外,TBBPA较BPA需用更多的洗脱溶剂才能获得满意的回收率,这主要是由于TBBPA和碳纳米管之间强π-π作用所致。综合以上考虑,采用COOH-MWCNT作为SPE吸附剂,用6 mL乙酸乙酯作为洗脱剂。
2.3 分析方法的评价
分别用乙腈配制质量浓度为0.02、0.05、0.1、0.5和1.0 mg/L系列浓度的TBBPA和BPA混合标准溶液并进行LC-MS/MS测定。以定量离子的峰面积作为纵坐标,目标物的质量浓度作为横坐标绘制标准工作曲线,并计算相关系数。结果表明,TBBPA和BPA在0.02~1.0 mg/L范围内线性关系良好(r2≥0.99),空白样品中S/N=3时,本方法可最低检出环境水样中TBBPA和BPA的质量浓度分别为0.04 μg/L 和 0.2 μg/L。

图4 洗脱剂种类及用量对TBBPA和BPA回收率的影响Fig.4 Effects of types and amounts of elution solvent on the recoveries of TBBPA and BPA
为了进一步验证方法的准确度和可靠性,用湖水和海水样品进行添加回收率和精密度试验。样品中TBBPA和BPA的添加浓度分别为5.0和20.0 μg/L,每个浓度平行进行3次试验,结果显示,TBBPA和BPA的加标回收率分别为82%~89%和90%~99%,精密度(RSD)小于5.0%(见表2),说明该方法准确、可靠。
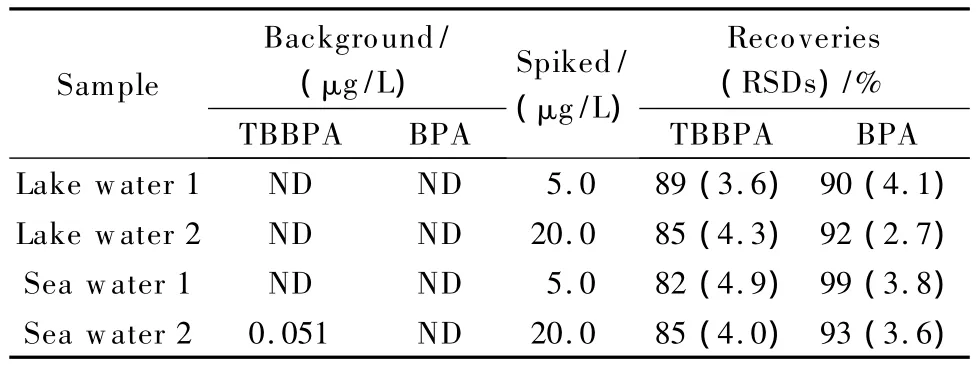
表2 环境水体样品中TBBPA和BPA的添加回收率Table 2 Recoveries of TBBPA and BPA spiked in environmental water samples
2.4 方法的应用
环境水样品采自当地某水库和近海,经0.45 μm玻璃纤维滤膜过滤后放在棕色样品瓶备用。由于环境水体如湖水和海水中盐含量较高,因此,在实际样品前处理过程中,上样后采用纯水淋洗除去高浓度盐及强极性物质,降低了质谱检测的基质效应。将建立的方法应用于当地湖水和近海海水中TBBPA和BPA的检测,分别测试了不同地点的4个样品,其中在1个海水样品中检出TBBPA,其浓度为0.051 μg/L,其余样品均未检出目标污染物。
3 结论
本研究考察了不同的碳材料作固相萃取剂对TBBPA和BPA的吸附效率,建立了羧基化多壁碳纳米管固相萃取-液相色谱-串联质谱检测环境水体中TBBPA和BPA的分析方法。实际应用时可用纯水淋洗除去环境水体中高浓度盐及强极性干扰物质。该方法线性范围良好,检测灵敏度低,回收率和精密度高,可以满足环境样品分析的要求。
[1] De Wit C A.Chemosphere,2002,46(5):583
[2] Qiu X Z,Guo H S,Chen B Q.Chinese Journal of Chromatography(丘秀珍,郭会时,陈步青.色谱),2013,31(8):809
[3] Vom Saal F S,Hughes C.Environ Health Persp,2005,113(8):926
[4] Vandenberg L N,Hauser R,Marcus M,et al.Reprod Toxicol,2007,24(2):139
[5] Sanchez-Brunete C,Miguel E,Tadeo J L.J Chromatogr A,2009,1216(29):5497
[6] Dorival-Garcia N,Zafra-Gomez A,Navalon A,et al.J Chromatogr A,2012,1253:1
[7] Vega-Morales T,Sosa-Ferrera Z,Santana-Rodriguez J J.J Hazard Mater,2010,183(1/2/3):701
[8] Labadie P,Tlili K,Alliot F,et al.Anal Bioanal Chem,2010,396(2):865
[9] Zhang X L,Luo X J,Chen S J,et al.Chinese Journal of Analytical Chemistry(张秀蓝,罗孝俊,陈社军,等.分析化学),2009,39(11):1577
[10] Wang X M,Liu J Y,Liu A F,et al.Anal Chim Acta,2012,753:1
[11] Gallart-Ayala H,Moyano E,Galceran M T.J Chromatogr A,2011,1218(12):1603
[12] Li J H,Wen Y Y,Chen L X.Chinese Journal of Chromatography(李金花,温莹莹,陈令新.色谱),2013,31(3):181
[13] Zhang K G,Hu Y L,Hu Y F,et al.Chinese Journal of Chromatography(张凯歌,胡玉玲,胡玉斐,等.色谱),2012,30(12):1220
[14] Wu X H,Ding L,Xiao J Y,et al.Chinese Journal of Chromatography(吴新华,丁利,肖家勇,等.色谱),2011,29(5):399
[15] Asensio-Ramos M,D'Orazio G,Hernandez-Borges J,et al.Anal Bioanal Chem,2011,400(4):1113
[16] Guo L,Lee H K.J Chromatogr A,2011,1218(52):9321
[17] Zhao H X,Liu H P,Yan Z Y.Chinese Journal of Chromatography(赵海香,刘海萍,闫早婴.色谱),2014,32(3):297
[18] Ballesteros E,Gallego M,Valcarcel M.J Chromatogr A,2000,869(1/2):101