比色法测定不同产地黑豆皮中总黄酮的含量
2013-09-06张丽娟刘占云刘岱琳
张 翠,张丽娟,刘占云,刘岱琳,*
(1.天津中医药大学,天津300193;2.中国人民武装警察部队后勤学院生药教研室,天津300162)
黑豆是我国一种传统种植的农作物,其具有悠久的食用和药用历史,自古以来民间就有用黑大豆补血、活血、乌发养颜的记载。黑豆皮,为豆科植物黑大豆Glycine max(L.)Merr.的干燥成熟种皮,又称料豆衣、乌衣、橹豆衣等,有解毒利尿、明目益精、养血疏风之功效,可治疗阴虚烦热、盗汗、眩晕、头痛、风痹等症[1]。此外黑豆皮提取物还具有很强的抗氧化活性[2]、抑制诱变[3-4]、抗炎[5]、预防癌症[6]等功效。文献报道黑豆皮中含有大量的花青素、黄酮醇等多种黄酮类成分[7]。有人曾用紫外分光光度法测定蓝莓果渣[8]、小飞蓬[9]等样品中的总黄酮含量,但关于不同产地的黑豆皮中总黄酮的含量测定方面的研究报道较少。本文在文献调研基础上,采用芦丁为对照品,硝酸铝显色,利用比色法建立了黑豆皮总黄酮的含量测定方法;同时为准确测定黑豆皮中总黄酮的真实含量,利用正交实验法确定了提取黑豆皮总黄酮的最佳前处理方法。本文的研究结果考察了测定不同产地黑豆皮中的总黄酮含量,为黑豆皮的综合开发和利用提供依据。
1 材料与方法
1.1 材料与仪器
八种不同产地的黑豆皮 黄仁黑豆皮(产自湖北)、青仁黑豆皮(产自东北)、KL0901青圆黑豆皮(产自山东滨州市)、KL0902青扁黑豆皮(产自安徽)、有机黄仁黑豆皮(产自东北)、6号黑豆皮(产自镇川)、7号黑豆皮(产自横山)、8号黑豆皮(产自山西塑州),所有黑豆皮样品均由天津市尖峰天然产物有限公司提供;芦丁对照品 天津市科曼思特医药科技发展有限公司提供,纯度达95%,供含量测定用;乙醇、亚硝酸钠、硝酸铝、氢氧化钠 均为分析纯。
UV-1601型紫外分光光度计 日本岛津公司;FA1204B电子天平 上海精科;HH-2数字显示恒温水浴锅 常州市国华仪器有限公司出产。
1.2 实验方法
1.2.1 对照品溶液的制备 精密称取芦丁对照品0.0286g,置于100mL棕色容量瓶中,加50%乙醇溶解并定容,摇匀即得。
1.2.2 显色方法[10]取待测溶液1mL,置于25mL容量瓶中,依次加入5%亚硝酸钠溶液1mL,混匀,放置6min,10%硝酸铝溶液1mL,混匀,放置 6min,4%氢氧化钠溶液10mL。最后用50%乙醇定容,混匀,放置15min。用1mL 50%乙醇代替对照品溶液按上述方法配制空白溶液。
1.2.3 测定波长的选择 取对照品溶液1mL,按1.2.2项下方法显色后,紫外分光光度计在200~800nm进行全波长扫描,结果如图1所示。反应液在320~510nm期间有明显的特征峰。为了避开黑豆皮中其他含有苯环的酚酸类成分的干扰,因此选取可见区域510nm的特征吸收峰位作为检测波长。
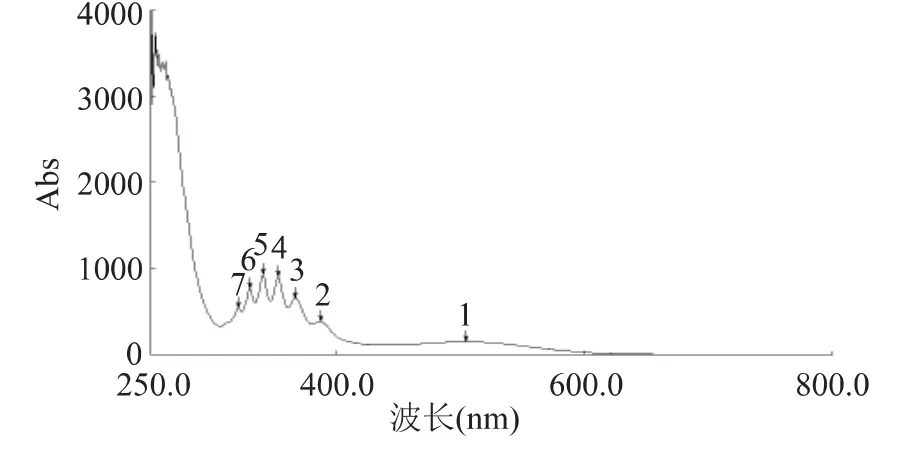
图1 对照品的紫外吸收图Fig.1 UV absorption spectrum of reference material
1.2.4 总黄酮含量标准曲线绘制 精密移取芦丁标准品0.25、0.5、1.0、2.0、2.5、4.0、5.0mL 分别置于 25mL棕色容量瓶中,按1.2.2项下操作,在510nm下测定吸光度。每个浓度平行测定三次,取平均值。以芦丁浓度C为横坐标,吸光度A为纵坐标绘制标准曲线,计算线性回归方程。
1.2.5 样品前处理的最佳提取方法考察 分别称取9份青圆黑豆皮,每份2.0g,按表L9(34)采用乙醇回流提取的方法进行正交实验,因素水平见表1。提取液过滤得到滤液并转移到100mL容量瓶中,用相应的溶剂定容,即得黑豆皮总黄酮样品溶液。准确移取样品溶液1mL置于25mL容量瓶中,按照1.2.2项下操作,在510nm下测定吸光度,根据标准曲线计算样品中总黄酮浓度。每组样品平行测定三次,取平均值。
1.2.6 供试品溶液的制备 分别称取黄仁、青仁、KL0901青圆、KL0902青扁、有机黄仁黑豆皮和6、7、8号黑豆皮样品,每个样品称取3份,每份2.0g,水浴加热到80℃,按照1.2.5项下确定的最佳前处理提取方法进行提取,过滤,合并滤液,转移到100mL容量瓶中,并用相应的溶剂定容,即得供试品溶液。
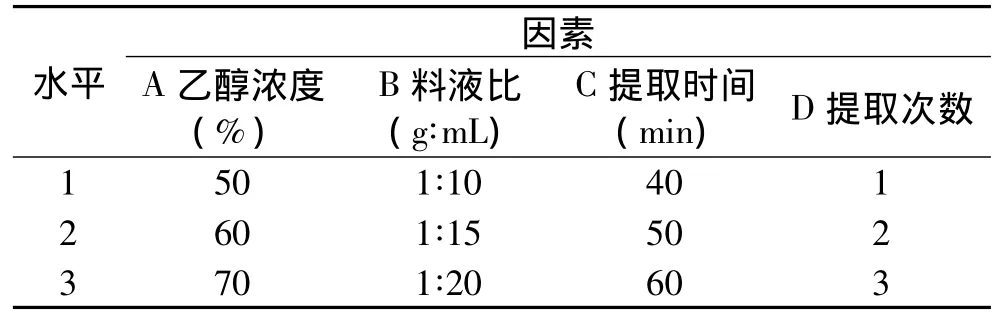
表1 因素水平表Table 1 Factor and level of orthogonal experiment
1.2.7 精密度考察 精密量取对照品溶液1mL,置于25mL容量瓶中,按1.2.2项下操作,在510nm处平行测定吸光度值5次,计算RSD值。
1.2.8 稳定性考察 取同一供试品溶液,按1.2.2项下操作,分别于0、2、4、6、8、10、12h 测定其吸光度,计算RSD值。
1.2.9 重复性考察 取同一种样品5份,按1.2.6项下方法制备供试品溶液,按照1.2.2项下操作,在510nm处测定其吸光度,计算RSD值。
1.2.10 加样回收率实验 精密吸取同一份供试品溶液5份,每份0.2mL,置于25mL容量瓶中,分别加入0.5、1.0、1.5、2.0、2.5mL 芦丁标准品,按照 1.2.2 项下操作,在510nm处测定其吸光度,计算加样回收率。
1.2.11 样品总黄酮含量的测定 分别准确移取各供试品溶液0.5mL,按照1.2.2项下操作,在510nm处测定其吸光度A,平行测定三次,代入标准曲线方程得到样品中总黄酮的浓度C(mg/mL),根据公式计算样品中总黄酮含量。
总黄酮含量(%)=(C×25/0.5)×100/M×100
式中,M为样品的质量(mg)。
2 结果与分析
2.1 总黄酮含量标准曲线
以芦丁浓度C为横坐标,吸光度A为纵坐标绘制标准曲线,得到回归方程式:Y=12X-0.0009,相关系数R2=0.9999,表明芦丁在0.003~0.057mg/mL范围内与吸光度有良好的线性关系。
2.2 黑豆皮总黄酮样品前处理的正交实验结果
运用统计软件SPSS11.1对数据进行分析,通过对比各因素的极差值(R)可以看出,影响总黄酮含量的因素顺序为A>D>B>C。由实验结果确定的提取方法为A1B3C2D3,即乙醇的浓度为50%,料液比为1∶20,提取时间为50min,提取次数为3次。
在最佳样品提取前处理方法下,进行提取两次和提取三次的实验,利用建立的总黄酮测定方法测定,提取三次(8.637%)比提取两次(6.873%)总黄酮的含量仅增加2%。因此为节约溶剂,故最终选择提取两次。因此,确定最佳提取方法为:乙醇的浓度为50%,料液比为1∶20,提取时间为50min,提取次数为2次,此时的总黄酮含量为6.873%,比正交实验中最高组的6.57%高出约0.3%。
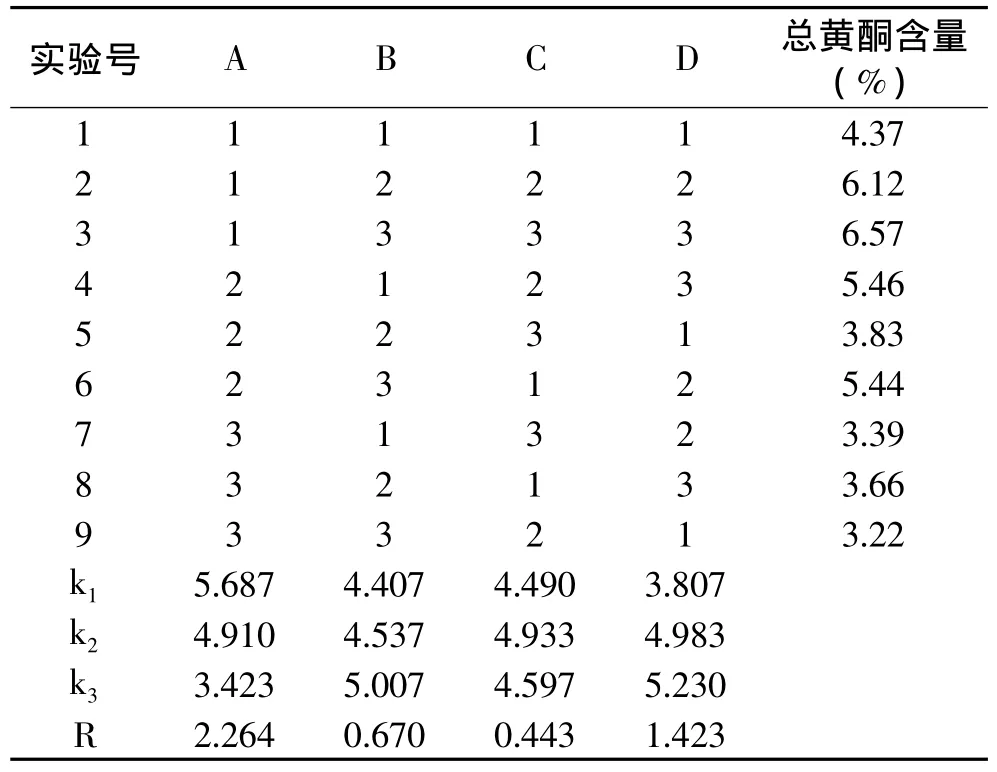
表2 正交实验设计结果Table 2 The result of orthogonal experimental design
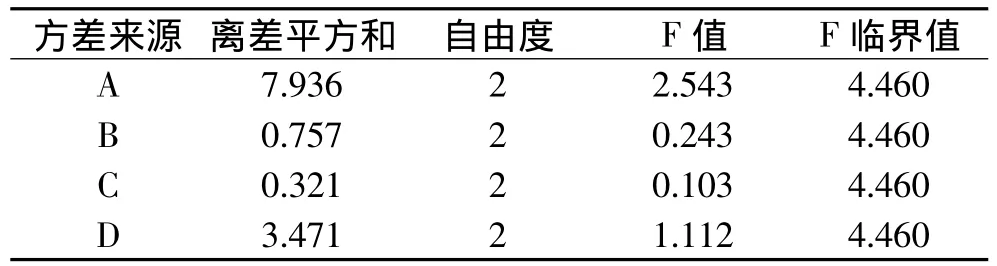
表3 正交实验方差分析结果Table 3 The result of orthogonal experimental analysis of variance

表4 稳定性考察结果Table 4 The result of stability tests
2.3 稳定性考察
稳定性考察结果见表4,实验结果RSD值为1.42%,表明所制备的供试品溶液在12h内进行测定稳定性良好。
2.4 精密度考察
精密度考察结果见表5。实验结果RSD值为0.39%,表示精密度良好。
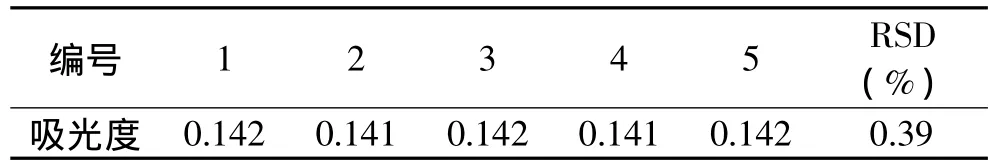
表5 精密度考察结果Table 5 The result of precision tests
2.5 重复性考察
重复性考察结果见表6。实验结果的RSD值为1.87%,表示其重复性良好。
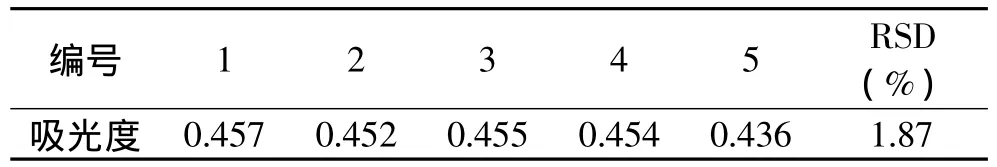
表6 重复性考察结果Table 6 The result of repeatability tests
2.6 加样回收率实验
结果如表7所示,平均回收率为104.6%,RSD值为2.41%,表明本法具有良好的回收率。
2.7 不同产地黑豆皮中总黄酮含量的测定
结果如表8所示,不同产地黑豆皮中总黄酮含量在6.873%~17.017%之间。
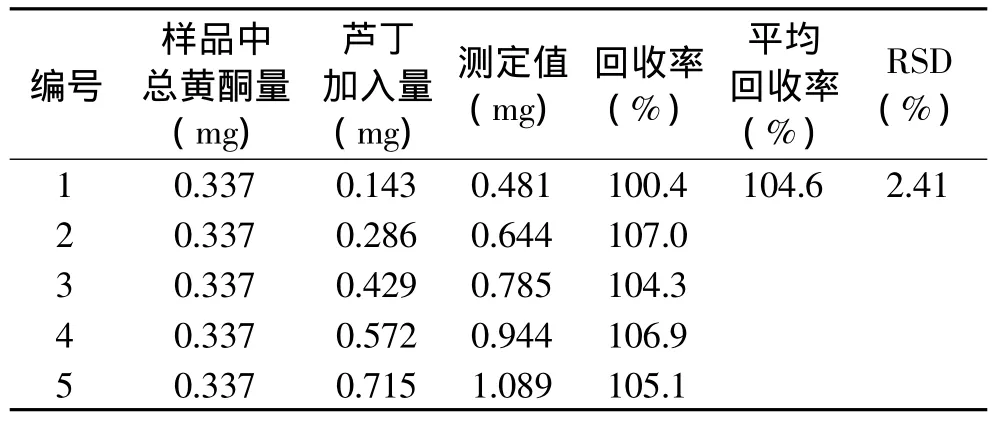
表7 加样回收率实验结果Table 7 The result of recovery tests
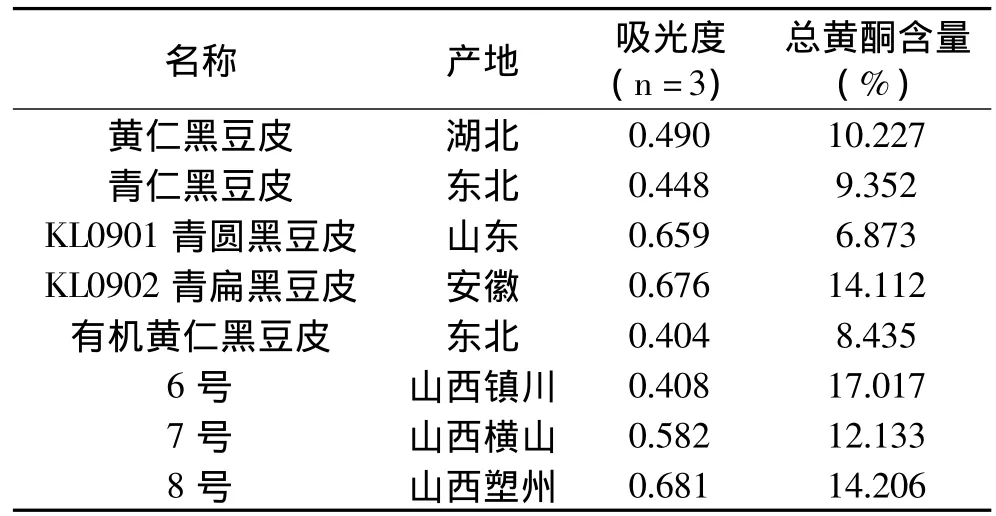
表8 不同产地黑豆皮中总黄酮含量Table 8 The contents of total flavonoids in black soybean seed coat from different regions
3 结论与讨论
本文首次利用紫外分光光度法测定国内不同产地黑豆皮中总黄酮的含量,结果表明总黄酮含量在6.873%~17.017%之间,其中山西省几个地区的黑豆皮含量均较高,此外安徽产地黑豆皮中总黄酮含量也较高。由此可知,不同产地的黑豆皮中总黄酮含量相差较大,可能由于生长环境如温度、光照、土壤、水质、采收时间、贮藏加工等因素对黑豆皮中总黄酮的形成产生了影响。因此本文的实验结果为农产品深加工中选取黑豆皮原料深入开发提供了可以借鉴的参考和实验依据,并保证产品质量的优良。
本实验所采用的总黄酮测定方法中,其反应液选取的测定波长为510nm,但黑豆皮自身含有的花青素在510nm可见区域处也有吸收。为了考察实验中反应液的干扰情况,测定本实验项下的黑豆皮提取液自身在510nm下的吸光度极低仅为0.003,干扰很小。此外测定时是加入反应液实施反应后再进行测定,则干扰更低。反应液在进行波长扫描时也发现在200~400nm处也有特征吸收,而本课题组前期研究发现,黑豆皮中含有的许多其他酚酸类成分[11]在此区也有吸收,但其在可见区域无吸收,为了排除这些成分对实验的测定结果的影响,最终采用了510nm为测定波长,保证了测定结果的准确性。
黑豆皮总黄酮的含量测定方法中样品的前处理也是至关重要的,其提取结果如何,直接影响样品的测定结果。因此本文在建立含量测定方法同时利用正交实验考察了黑豆皮总黄酮的前处理方法:水浴加热到80℃,用20倍量的50%乙醇加热回流提取两次,每次50min,采用此方法黑豆皮总黄酮的提取率为6.873%,此方法保证了黑豆皮中总黄酮的测定结果能够真实反映原料的真实含量,为农作物黑豆皮的进一步开发利用奠定坚实的实验基础。
[1]黄昉,李汴生,徐志宏,等.黑豆种皮色素的测定和提取[J].食品工业科技,2004,25(4):112-114.
[2]Ignasius Radix Astadi,Mary Astuti,Umar Santoso,et al.In vitro antioxidant activity of anthocyanins of black soybean seed coat in human low density lipoprotein(LDL)[J].Food Chemistry,2009,112(3):659-663.
[3]Yen-Ju Wang,Lee-Yan Sheen,Cheng-Chun Chou,et al.Storage effects on the content of anthocyanin,mutagenicity and antimutagenicity of black soybean koji[J].LWT-Food Science and Technology,2010,43(4):702-707.
[4]Yu-Hsiang Hung,Hui-Yu Huang,Cheng-Chun Chou,et al.Mutagenic and antimutagenic effects of methanol extracts of unfermented and fermented black soybeans[J].International Journal of Food Microbiology,2007,118(1):62-68.
[5]Irina Tsoy Nizamutdinova,Young Min Kim,Jong Il Chung,et al.Anthocyanins from black soybean seed coats stimulate wound healing in fibroblasts and keratinocytes and prevent inflammation in endothelial cells[J].Food and Chemical Toxicology,2009,47(4):2806-2812.
[6]刘岱琳,陆艳玲,刘丹,等.黑豆皮中花青素的研究进展[J].中草药,2007,38(增):324-325.
[7]林纪伟.黑豆皮化学成分研究[D].天津:天津科技大学,2010.
[8]刘玮,钱慧碧,辛秀兰,等.蓝莓果渣中总黄酮的提取纯化及抗氧化性能的研究[J].食品科技,2011,36(2):216-219.
[9]赵爽,严铭铭,赵大庆,等.小飞蓬总黄酮提取工艺优选及体外抗氧化活性研究[J].中成药,2011,33(2):348-350.
[10]王小平,刘峰,韩翠,等.正交实验法优化丹参总黄酮提取工艺[J].辽宁中医药大学学报,2010,12(6):133-134.
[11]刘占云.黑豆皮的化学成分和质量控制方法研究[D].沈阳:沈阳药科大学,2012.
