合成3-(2-吡啶氨基)丙酸乙酯的工艺改进
2012-11-21张伟光蔡志强刘洪强徐为人汤立达
张伟光, 蔡志强, 刘洪强, 徐为人, 汤立达
(1. 天津药物研究院 天津市新药设计与发现重点实验室 释药技术与药代动力学国家重点实验室,天津 300193;2. 天津中医药大学,天津 300193; 3. 辽宁科技学院 生物医药与化学工程学院,辽宁 本溪 117004)
达比加群酯(Dabigatran)是德国勃林格殷格翰公司开发的具有多种特点的新型抗凝血药物,于2008年4月首先在德国和英国上市,商品名为Pradaxa,用于防治急性静脉血栓。这是继华法林之后50年来首个上市的抗凝血口服新药,是抗凝血治疗领域和潜在致死性血栓预防领域的又一个里程碑。美国食品和药品监督管理局于2010年10月19日批准Pradaxa胶囊用于有心律异常(心房颤动)患者的预防中风和凝血。达比加群酯口服经胃肠吸收后,在体内转化为具有直接抗凝血活性的达比加群;药物结合于凝血酶的纤维蛋白特异结合位点,阻止纤维蛋白原裂解为纤维蛋白,从而阻断了凝血瀑布网络的最后步骤及血栓形成[1]。
3-(2-吡啶氨基)丙酸乙酯(1)是合成达比加群酯必需的重要中间体。文献[2]以2-氯吡啶为起始原料,经双氧水氧化、缩合、Pt/C催化加氢还原得到1,总收率56.0%。该方法在合成过程中需要在氮气下回流72 h,耗时长,且需要柱层析纯化,不利于工业化生产,收率相对较低。
本文在文献[3~8]方法的基础上对其进行改进,以2-氨基吡啶(2)和丙烯酸乙酯(3)为原料,经一步缩合反应成功地合成了1(Scheme 1),其结构经1H NMR和ESI-MS确证。并对缩合反应条件进行优化,得出较佳的反应条件为:2120 mmol,n(2) ∶n(3)=1.00 ∶1.08,于100 ℃回流反应24 h,收率79.6%。
改进方法具有原料廉价易得、操作简单、收率较高、对环境污染小、且不需要柱层析分离等优点,适合工业化生产。
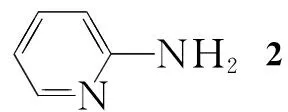
Scheme1
1 实验部分
1.1 仪器与试剂
X-4型显微数字熔点仪(温度未校正);Bruker ARX-400NMR型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Agient1100型四级杆液质联用仪。所用试剂均为分析纯。
1.2 1的合成
氮气保护,在反应瓶中依次加入211.2 g(120 mmol)和313.8 g(140 mmol),搅拌下回流(100 ℃)反应24 h。过滤,滤液浓缩至干,残余物用乙酸乙酯重结晶得白色固体1 21.0 g,收率79.6%, m.p. 52 ℃~53 ℃;1H NMRδ: 1.14~1.18(t,J=7.2 Hz, 3H, CH3), 2.52~2.56(t,J=6.8 Hz, 2H, CH2), 3.44~3.49(dd,J=6.8 Hz, 12.8 Hz, 2H, CH2), 4.02~4.07(dd,J=7.2 Hz, 14.4 Hz, 2H, CH2), 6.43~6.46(m, 2H, ArH), 6.51~6.54(m, 1H, NH), 7.31~7.35(m, 1H, ArH), 7.94~7.96(m, 1H, ArH); ESI-MSm/z: 195.1{[M+H]+}。
2 结果与讨论
2.1 反应条件优化
为提高1的收率,对缩合反应条件进行优化。
(1) 反应温度
2120 mmol,其余反应条件同1.2,考察温度对反应的影响,结果见表1。由表1可以看出,温度对反应影响较大,在低温条件下几乎不反应,可能是在低温条件下很难达到反应的能量壁垒,使反应无法进行。最佳反应温度为100 ℃(回流)。
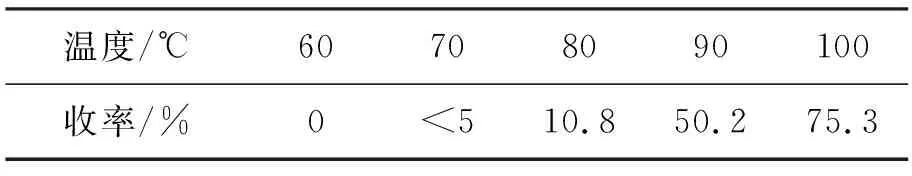
表1 温度对缩合反应的影响*Table 1 Effect of temperature on condensation reaction
*2120 mmol,其余反应条件同1.2
(2) 反应时间
反应温度100 ℃,其余反应条件同2.1,考察反应时间对反应的影响,结果见表2。从表2可知,收率随着反应时间的延长而增加;当时间为24 h时,收率近80%;再延长反应时间收率降低,可能在此条件下产物会继续生成其他副产物。反应时间以24 h为宜。

表2 时间对缩合反应的影响*Table 2 Effect of time on condensation reaction
*反应温度100 ℃,其余同表1
(3) 重结晶溶剂
反应温度100 ℃,反应时间24 h,其余反应条件同2.1,考察重结晶溶剂对收率的影响,结果见表3。从表3可知,选用乙酸乙酯为重结晶溶剂时收率最高。

表3 重结晶溶剂对1收率的影响*Table 3 Effect of recrystallization solvent on yield of 1
*反应温度100 ℃,反应时间24 h,其余反应条件同2.1
综上所述,合成1的最佳反应条件为:2120 mmol,n(2) ∶n(3)=1.00 ∶1.08,回流(100 ℃)反应24 h,收率79.6%。
[1] Blech S, Ebner T, Ludwing-Schwellinger E,etal. The metabolism and disposition of the oral direct thrornbin inhibitor,dabigatran,in hunman[J].Drug Metab Dispos,2008,36(2):386-399.
[2] 邢松松,王晓蕾,周付刚,等. 达比加群酯的合成[J].中国医药工业杂志,2010,41(5):321-325.
[3] Norbert H H, Herbert N, Henning P,etal. Structure-based design of novel potent nonpeptide thrombin inhibitors[J].J Med Chem,2002,45(9):1757-1766.
[4] Wiley M R, Fisher M J. Review: Small-molecular direct thrombin inhibitors[J].Expert Opin Ther Pat,1997,7:1265-1282.
[5] Obst U, Banner D W, Weber L,etal. Molecular recognition an the thrombin active site:Structure-based design and synthesis of potent and selective thrombin inhibitors and the X-ray crystal structures of two thrmbin-inhibitor complexes[J].Chem Biol,1997,4(4):287-295.
[6] Das J, Kimball S D. Thrombin active site inhibitors[J].Bioorg Med Chem,1995,3:999-1007.
[7] Marchais S, Nowicki B, Wikström H V,etal. Short and efficient syntheses of analogues of WAY-100635:New and potent 5-HT1A receptor antagonists[J].Bioorg Med Chem,2001,9(3):695-702.
[8] 林国强,马景毅,徐亮等. 一种合成非手性,非肽类的抗凝血酶抑制剂的方法[P].CN 186 159 6A,2006.
