苄达赖氨酸眼用凝胶的制备及质量控制
2011-11-11孔飞飞谭兴起郭良君
王 萍,孔飞飞,谭兴起,郭良君,郑 巍
解放军第九八医院,浙江湖州 313000
苄达赖氨酸眼用凝胶的制备及质量控制
王 萍,孔飞飞,谭兴起*,郭良君,郑 巍
解放军第九八医院,浙江湖州 313000
目的:探讨苄达赖氨酸眼用凝胶的制备及其质量控制。方法:以透明质酸钠(HA)或羟丙基甲基纤维素(HPMC)或两者合用为凝胶基质,以氯化钠调节渗透压,硼酸-硼砂调节pH,柳硫汞作抑菌剂,用高效液相色谱法测定其含量,考察制剂的稳定性。结果:苄达赖氨酸在0.06~0.43mg/ml范围内线性关系良好,r=0.999 8,加样回收率为99.5%,RSD为1.2%(n=9)。结论:本法制备眼用凝胶,工艺简单易行,制剂质量稳定。
苄达赖氨酸;眼用凝胶;高效液相色谱
苄达赖氨酸(bendazac lysine,BDZL)首先由Angelini制药集团于1983年在意大利上市,随后在20多个国家开展进一步研究。经研究发现该药作为醛糖还原酶 (aldehyde reductase,AR)抑制剂,无论口服还是局部滴眼均能进入眼组织和房水,并在晶状体内浓集,不仅对糖性白内障有效,还对多种类型的早期老年性白内障有预防和治疗作用。国内首先由华西医科大学和江苏省药物研究所开展研究,后由浙江平湖制药厂(现更名为浙江莎普爱思制药有限公司)于1997年取得新药证书和生产批文[1]。目前,苄达赖氨酸在国内外上市的剂型有滴眼液及片剂,尚无眼用凝胶剂。
与传统滴眼液相比,眼用凝胶能较长时间与眼部紧密结合,不仅克服了传统滴眼液会很快被泪液冲刷而无法达到有效药物浓度的缺点,还减少了使用频率,提高了生物利用度,增加了患者的顺应性[2];同时由于凝胶体系的三维网状结构高度亲水,可将药物束缚于其中或其间隙中,从而使得药物的释放度得以控制。因此,在本制剂中笔者采用高分子亲水性聚合物为基质作为药物载体,制备成眼用凝胶制剂。
苄达赖氨酸眼用凝胶制剂,它含有有效剂量的苄达赖氨酸、适量的凝胶基质和其他药物可接受的载体。本实验对凝胶基质、离子缓冲对、抑菌剂及渗透压调节剂等在制剂处方中的相互影响进行研究,经处方筛选和工艺研究制备出性状良好、性质稳定的凝胶剂;同时,本实验对筛选出的凝胶剂进行含量测定及方法学考察。
1 仪器和试药
1.1 实验仪器
岛津LC-10AT高效液相色谱仪-泵 (日本岛津);岛津SPD-6AV检测器(日本岛津);N-2000色谱工作站(浙江大学);VSC502超声波清洗器 (上海波龙电子设备有限公司);HH-BⅡ电热恒温培养箱(天津实验仪器厂);BS124S型电子分析天平(北京赛多利斯仪器系统有限公司);WD-1药物稳定性试验箱(天津药典标准仪器厂);DF-Ⅱ集热式磁力加热搅拌器(江苏省金坛市医疗器械厂);GNP-9160隔水式恒温培养箱(上海精宏实验设备厂)。
1.2 试剂与药品
苄达赖氨酸对照品(100561-200401,中国药品生物制品检定所);苄达赖氨酸原料(批号:4017205,宁夏康亚制药有限公司);卡波姆-940(批号:20070603,安徽山河药用辅料有限公司);卡波姆-934(批号:070307,安徽山河药用辅料有限公司);卡波姆-941(批号:070514,安徽山河药用辅料有限公司);HPMC(批号:070401,安徽山河药用辅料有限公司);HA(批号:0508111,山东正大福瑞达制药有限公司);泊洛沙姆-188(批号:070515,安徽山河药用辅料有限公司);硼酸-硼砂(广州市汉普医药有限公司);庚烷磺酸钠(批号:070111,上海凌峰化学试剂有限公司);甲醇(色谱纯)(天津市四友精细化学品有限公司);冰醋酸等试剂为分析纯;纯化水等。
2 方法与结果
2.1 处方筛选
2.1.1 研究中常用的几种基质 羟丙基甲基纤维素(HMPC)、卡波姆(carbomer)、泊洛沙姆(ploxamer)、聚乙烯吡咯烷酮(PVP)、透明质酸钠(HA)是研究中较常用的基质。HPMC为非离子化合物,和一些氧化剂有配伍禁忌[4],具有增稠能力、排盐性、pH稳定性、保水性、尺寸稳定性、优良的成膜性以及广泛的耐酶性、分散性和粘结性等特点。卡波姆(Carbomer)具有内在特有的交联结构,其良好的黏滞性和亲水凝胶性使其具有较好的控缓释作用。卡波姆与碱性药物可形成内盐,也有延缓释药的作用[3]。卡波姆遇二苯酚变色,且和苯酚、阳离子聚合物、强酸、强碱等均有配伍禁忌[4]。流洛沙姆具有很强的吸湿性,与苯酚和羟苯酯类有配伍禁忌[4]。单独使用泊洛沙姆-188用量太大且性能不一定好,而单纯的泊洛沙姆-407溶液胶凝温度较低[2]。PVP具有很强的膨胀性能及与多类物质的络合能力,可与磺胺噻唑、水杨酸钠、苯巴比妥等化合物在溶液中形成分子加合物,而且PVP与抑菌剂硫柳汞会形成复合物,从而使硫柳汞的抑菌能力减弱。HA在眼科领域,可作为眼用制剂媒介加在眼溶液里,从而构成一层膜覆盖于角膜内皮表面,这样有利于眼组织对药物持久而有效的吸收,使其生物利用度明显增加[5],它还可作为眼科黏弹性保护剂应用于临床,开创了眼科手术“软壳技术”的新时代。
可见,HPMC、卡波姆、HA均可单独作为凝胶基质,泊洛沙姆用量太大,可以考虑和其他基质联合使用,而PVP不太适宜作为凝胶基质,但可作为增溶剂等。
2.1.2 基质的筛选 本实验通过考察基质与主药及其他辅料配伍后的外观性状等指标对上述5种比较常用的眼用凝胶基质进行了筛选。取苄达赖氨酸0.05 g,精密称定7份,分别置于7个烧杯中,加10 ml纯化水,搅拌,使其充分溶解,再分别向其中加入以下7种基质,搅拌,使其充分溶解,观察并记录实验结果。见表1。

表1 基质与苄达赖氨酸的配伍情况
通过表1可以得出以下结论:①PVP由于在用量增加的情况下稠度与黏度仍不能符合凝胶的要求,因此不考虑单独使用PVP为凝胶基质,但是可以考虑把PVP作为增溶剂与其他凝胶基质配合使用;②泊洛沙姆-188虽然符合凝胶的要求,但是用量太大,操作起来也不方便,且在实际过程中会造成大量的损失,因此也不考虑单独使用泊洛沙姆-188为凝胶基质;③HPMC和HA这两种基质均具有良好的黏度与稠度,且与主药有很好的兼容性,没有配伍禁忌,所以可以以这两种基质来制备良好的凝胶;④卡波姆-934、卡波姆-940、卡波姆-941与主药配伍后均产生絮状沉淀,不考虑单独使用卡波姆作为苄达赖氨酸的凝胶基质。有文献报道可以通过加入其他凝胶基质来消除卡波姆与苄达赖氨酸之间的配伍禁忌,得到性状良好的凝胶基质,因此可以考虑卡波姆与其他一种或几种凝胶基质联合使用。
参考《辅料手册》[4]中卡波姆不同型号的性能介绍,用泊洛沙姆-188和PVP来试着消除卡波姆与苄达赖氨酸的配伍禁忌。实验情况见表2。
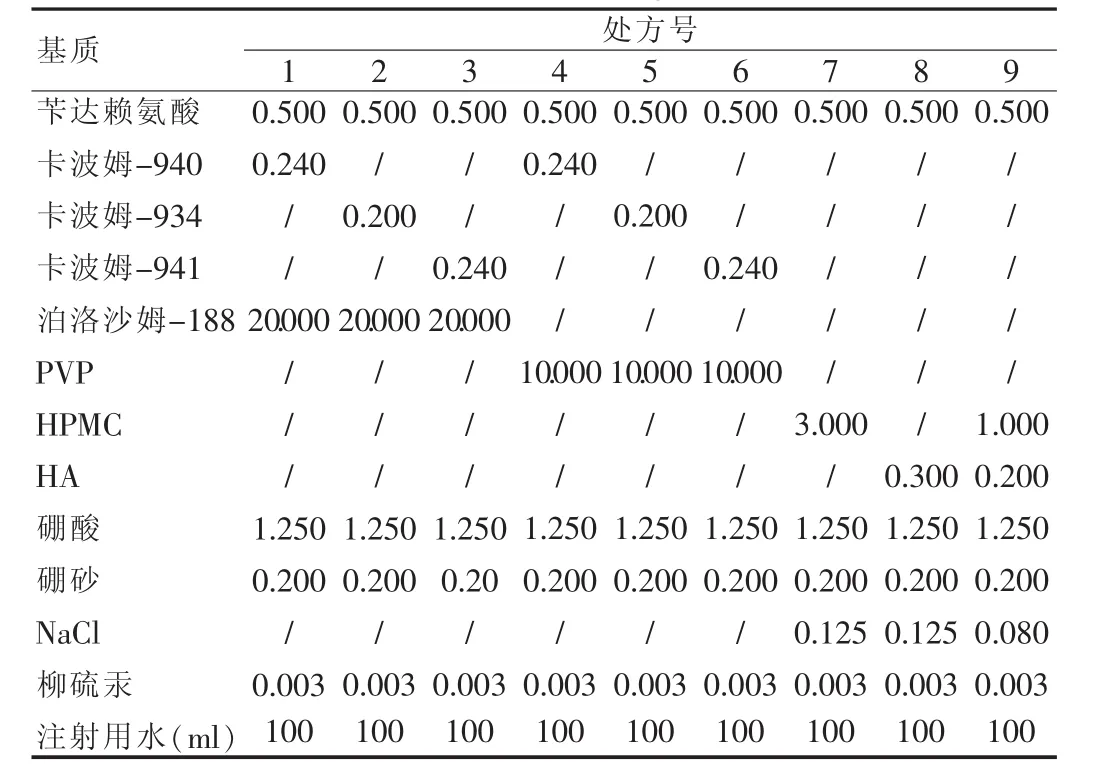
表2 基质筛选(g)
通过表2了解到,处方1、2、3均具有良好的外观性状,但是毫渗压摩尔比均不符合规定,又通过实验了解到泊洛沙姆-188单独溶于水能产生一定的渗透压,而当降低泊洛沙姆-188的加入量时,各处方毫渗压摩尔比降低的同时,均有白色沉淀析出,证明不能通过降低泊洛沙姆-188的加入量来调整毫渗压摩尔比;处方4、5、6外观性状均为白色浑浊,即PVP与卡波姆联合使用不能消除主药与卡波姆的配伍禁忌。处方7、8、9均具有良好的外观性状,且各条件均符合要求。
因此,以苄达赖氨酸为主药制备眼用凝胶时不宜采用卡波姆作为凝胶基质。最终决定以HPMC或HA或HPMC与HA联合使用为凝胶基质。
2.1.3 pH值的选择 pH值的不当易对眼睛造成刺激,增加泪液的分泌,导致药物迅速流失,甚至角膜损伤;同时,pH的调节还应兼顾药物的溶解度和稳定性的要求。正常眼可耐受的pH值为5.0~9.0,参考《中国药典》二部(2005年版)苄达赖氨酸滴眼液标准[6]及莎普爱思滴眼液质量标准[7]中规定的pH值 (pH值应为6.8~7.8),最终确定该凝胶剂的pH值范围仍为6.8~7.8。本研究针对pH值的筛选,结果见表3。
2.1.4 缓冲对的筛选及处方评价 滴眼剂中常用的缓冲盐一般为磷酸盐与硼酸盐。磷酸盐较适合用于酸性溶液,硼酸盐较适合用于碱性溶液。见表4。
从表4可知:根据苄达赖氨酸的pH值范围(5.5~7.5)及苄达赖氨酸滴眼液的pH值范围(6.8~7.8),选择硼酸盐缓冲对作为该滴眼液的缓冲离子对。通过实验证明该缓冲对适合苄达赖氨酸及其相关辅料(表5),故选择该缓冲对作为苄达赖氨酸眼用凝胶的缓冲对。
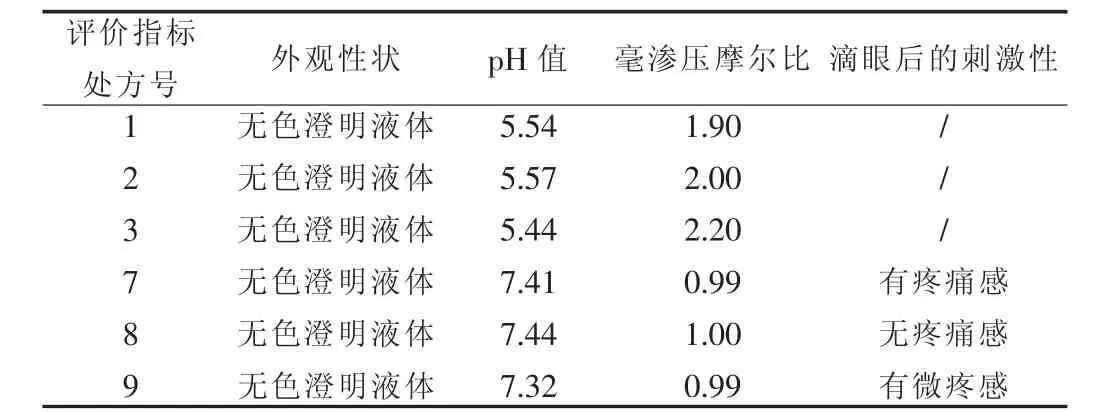
表3 处方评价结果

表4 缓冲对的筛选(g)

表5 处方评价
2.1.5 抑菌剂的筛选及处方评价 抑菌剂的选择研究实验结果,见表6。处方评价见表7。

表6 抑菌剂的选择研究实验(g)

表7 处方评价
从表7可知,以HPMC为基质、硼酸-硼砂为缓冲对的处方中,除以苯扎溴氨和苯扎氯铵为抑菌剂的处方产生白色沉淀、外观性状不符合规定外,其他处方性状均良好。虽然以尼泊金酯类为抑菌剂的处方外观性状良好,但通过紫外扫描发现尼泊金酯类抑菌剂干扰苄达赖氨酸的最小吸收,因此,尼泊金类不能作为苄达赖氨酸眼用凝胶的抑菌剂。而以三氯叔丁醇为抑菌剂制备的样品pH值不稳定,制得处方当日测得的 pH值为 7.40,在室温下放置 5、10、15 d,pH分别为7.32、7.26、7.11,pH值呈下降趋势。因此,三氯叔丁醇也不宜作为苄达赖氨酸眼用凝胶的抑菌剂。
综合考虑,选择硫柳汞作为苄达赖氨酸眼用凝胶的抑菌剂。
2.1.6 渗透压调节剂的筛选 根据规定渗透压调节剂为NaCl或葡萄糖,参考《中国药典》二部(2005年版)苄达赖氨酸滴眼液标准[6]与莎普爱思说明书[7]中所选用的渗透压调节剂为NaCl,因此,本研究也采用NaCl作为苄达赖氨酸眼用凝胶的渗透压调节剂。
2.2 制备工艺
2.2.1 称取处方量的基质,在快速搅拌下缓缓将基质加入到适量注射用水中使其分散均匀。得溶液A,备用。
2.2.2 称取处方量的缓冲盐、渗透压调节剂、抑菌剂,加适量注射用水搅拌使其溶解(必要时可加热溶解),称取处方量的主药,加入到上述溶液中搅拌溶解。得溶液B,备用。
2.2.3 将溶液A、B混合均匀,补充注射用水至全量,除菌过滤,灌装,即得。
2.2.4 影响因素试验及处方的确定过程如下:从上述众多的处方中,选择外观性状(无色澄明液体)、pH(6.8~7.8)和毫渗压摩尔比(0.90~1.10)均符合要求的处方进行影响因素试验。可见,符合要求的共有三个处方,分别是处方7、8和处方9。见表8。其中影响因素的试验过程,见表9~14。
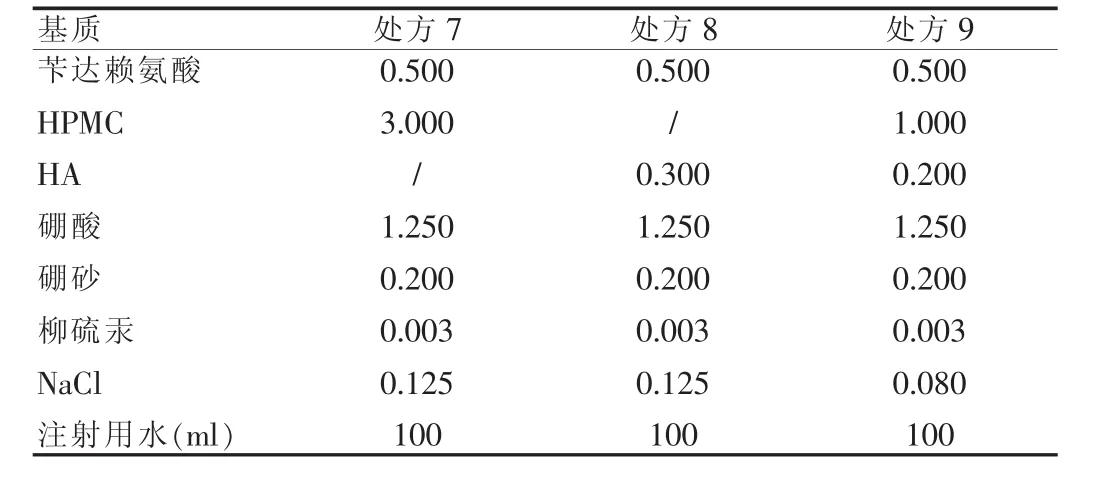
表8 良好处方

表9 处方7影响因素第5天
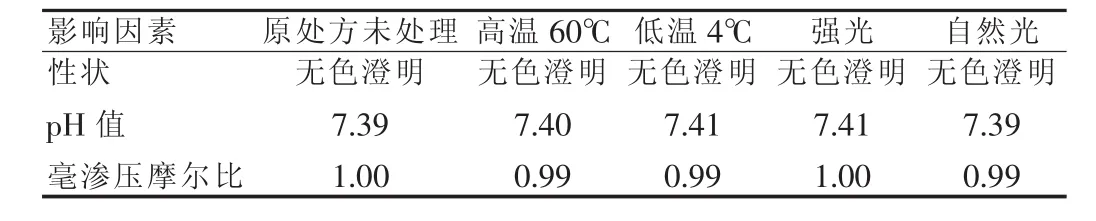
表10 处方7影响因素第10天

表11 处方8影响因素第5天

表12 处方8影响因素第10天

表13 处方9影响因素第5天

表14 处方9影响因素第10天
从上述三个处方的影响因素试验可以得出一个结论,处方7、8、9制得的凝胶剂都相当稳定,从经济角度出发,以HA为基质的凝胶剂成本远远高于以HPMC为基质的凝胶剂,但是从另一方面,HA有作为眼用制剂媒介加在眼溶液里,可以构成一层膜覆盖于角膜内皮表面,有利于眼组织对药物持久而有效的吸收,使其生物利用度明显增加的特性,所以本凝胶基质采用HPMC和HA联合使用,最终决定采用处方9进行后续的质量研究。
2.3 苄达赖氨酸眼用凝胶的质量控制
采用处方9制备三批样品(批号分别为080501、080502、080503)进行质量研究。
2.3.1 pH值检查 pH值应在6.8~7.8范围内。实验中制备的处方9的三批样品的pH分别为7.33、7.32、7.33,符合要求。
2.3.2 渗透压 眼球能适应的毫渗压摩尔比的范围为0.90~1.10。实验中制备的处方9的三批样品的毫渗压摩尔比分别为 0.99、1.00、0.99,符合要求。
2.3.3 性状 实验中制备的处方9的三批样品的外观性状均为无色澄明液体。
2.4 苄达赖氨酸眼用凝胶的含量测定与方法学考察
2.4.1 色谱条件 依利特 C18(5μm,4.6 mm×150 mm)色谱柱;流动相为甲醇∶水∶冰醋酸(64∶36∶0.5)内含 0.05 mmol/L 的庚烷磺酸钠;流速:1.0ml/min;检测波长:λ=307 nm;柱温:室温[8]。
2.4.2 对照品及样品溶液的制备 ①对照品溶液的制备:取苄达赖氨酸对照品(100561-200401,中国药品生物制品检定所)适量,精密称定,加水制成每1 m l含5 mg苄达赖氨酸对照品的溶液,摇匀,过0.45μm微孔滤膜,供HPLC分析用。②样品溶液的制备:取处方9的三批样品适量,分别加水稀释制成0.2mg/m l的溶液,摇匀,过0.45μm微孔滤膜,供HPLC分析用。③检测波长的选择:取苄达赖氨酸对照品适量,加水制成5mg/ml的溶液,在200~400 nm波长范围内进行紫外扫描,在307 nm处有最大吸收。参照《中国药典》二部(2005年版)依然选择307 nm作为检测波长。
2.4.3 流速考察 分别以0.8、1.0、1.2 ml/min的流速对样品进行流速考察,均符合规定。因此仍选用1.0 ml/min作为该样品含量测定的流速。
2.4.4 色谱柱考察 迪马 C18(150 mm×4.6 mm,5μm)色谱柱和依利特 C18(5 μm,4.6 mm×150 mm)色谱柱,分别进样,峰形均对称,柱效高,但迪马色谱柱的出峰时间为11min,依利特色谱柱的出峰时间为5.9min,因此选用依利特色谱柱。
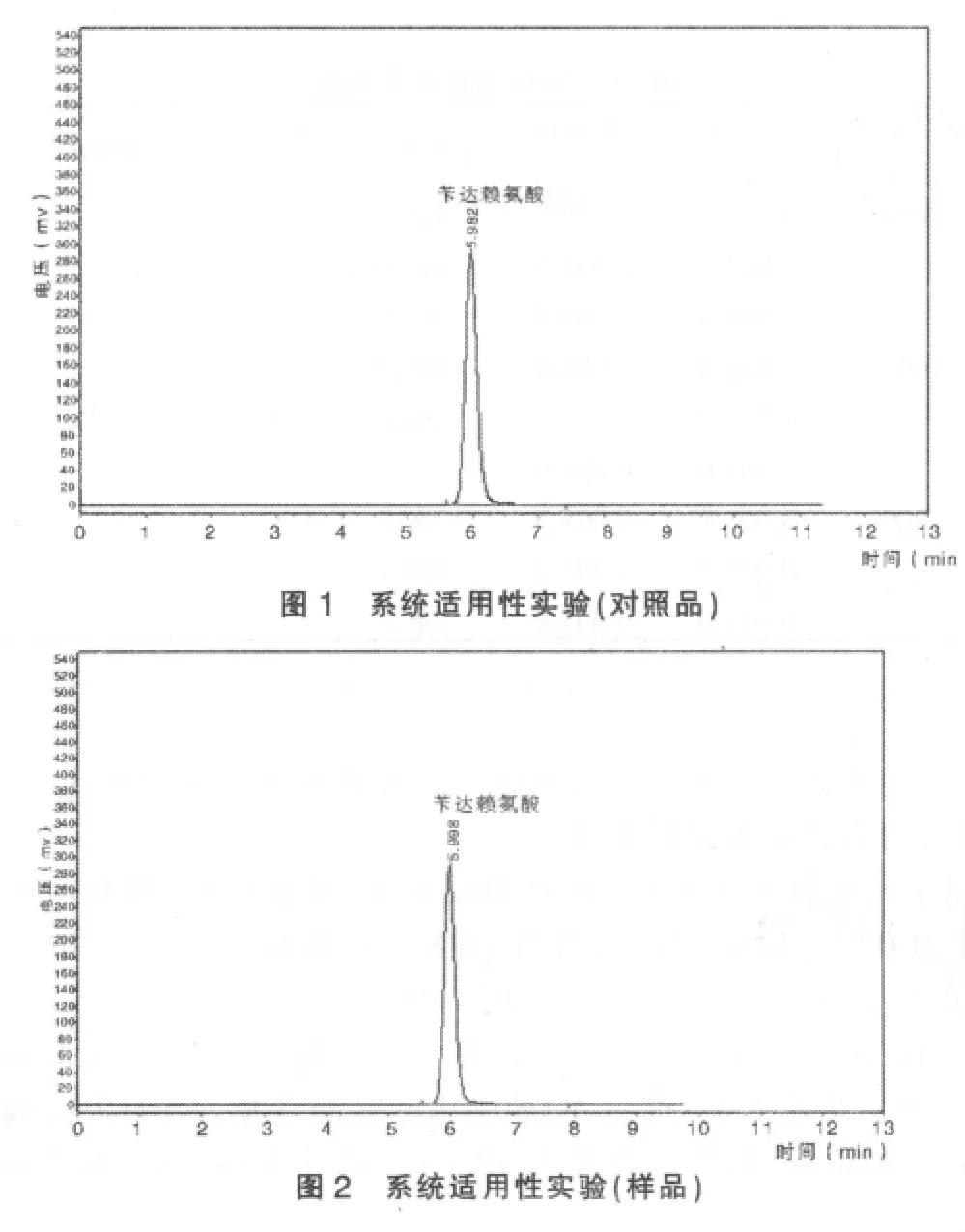
2.4.5 系统适用性试验 分别制备含苄达赖氨酸0.1mg/ml的对照品溶液及样品溶液,进样20μl,色谱图见图1、2。可见两组溶液峰形均对称,柱效高,保留时间分别为5.982、5.998min,理论塔板数以苄达赖氨酸峰计算分别为5 303、5 333。
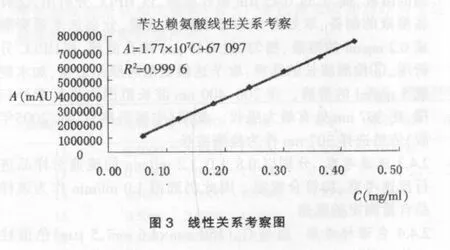
2.4.6线性关系考察 精密称定苄达赖氨酸对照品适量,加水制成3mg/m l的溶液,摇匀,作为储备液。分别量取储备液1、2、3、4、5、6、7m l置 50ml容量瓶中,加水稀释至刻度,摇匀,过0.45μm微孔滤膜,供HPLC分析用。分别进样20μl,记录色谱图。以苄达赖氨酸的峰面积(A)对浓度(C)作线性回归,计算回归方程。结果表明,采用本法测定含量,苄达赖氨酸在0.06~0.43mg/ml的浓度范围内,主峰的峰面积与浓度呈良好的线性关系,线性方程为 A=1.77×107C+67 097,r=0.999 8,n=7。见图3。
2.4.7 精密度试验 精密量取样品溶液(0.2mg/ml),进样20μl,重复6次,测得苄达赖氨酸的峰面积RSD为0.32%。仪器精密度良好。
2.4.8 回收率试验 取苄达赖氨酸原料约4、5、6mg,各3份,分别精密称定,置25 ml容量瓶,加不含苄达赖氨酸的空白辅料,稀释至刻度,摇匀。在307 nm的波长处分别测定峰面积,计算回收率。见表15。
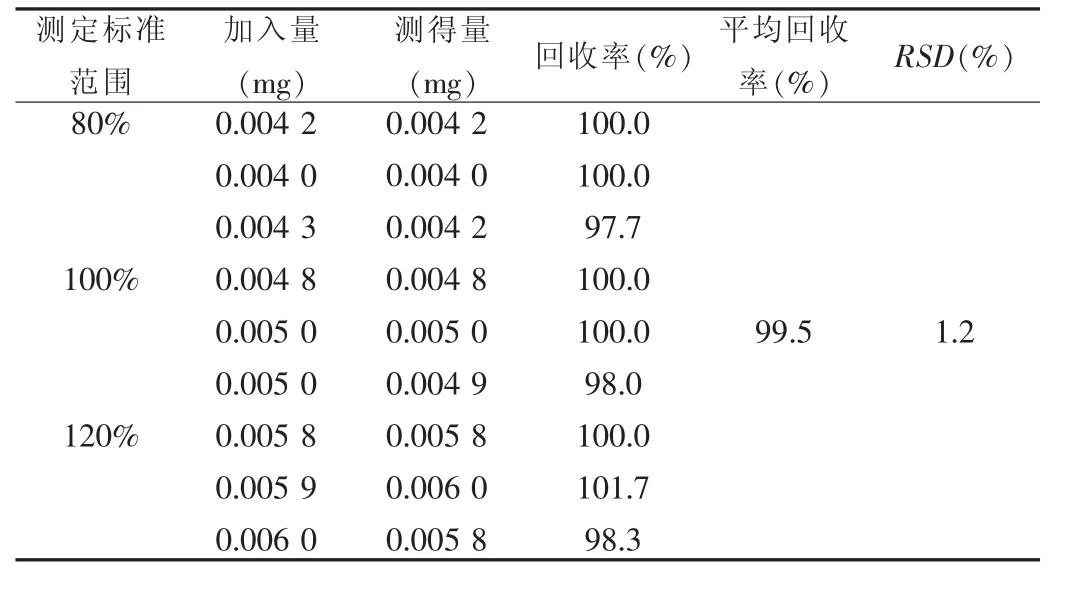
表15 加样回收率考察表
结果表明,采用本法测定苄达赖氨酸的含量准确度高,能够符合含量测定的要求。
2.4.9 最低检测限考察 取对照品溶液,反复稀释,稀释至浓度为 0.015μg/m l时,信噪比(S/N)=3,即最低检出浓度为0.015 μg/ml,最小检测量为 3.024×10-7g。 见图 4。
2.4.10 样品含量的测定 对处方9的三批样品进行含量测定,测定结果如下:批号为080501的样品含量为104.7%,批号为0080502的样品含量为98.3%,批号为080503的样品含量为96.5%,含量测定均符合要求,平均含量为99.8%。

通过对多种基质、缓冲对、抑菌剂等的筛选及制备工艺的确定,最终制备出了性状良好,性质稳定的凝胶剂。最终通过实验得到最佳测定参数为:以依利特C18(5μm,4.6mm×150mm)色谱柱为固定相,以甲醇-水-冰醋酸(64∶36∶0.5),内含0.5mmol/L庚烷磺酸钠为流动相,紫外检测波长307 nm,流速为1.0m l/min,柱温为室温,外标法定量测定。方法学验证表明苄达赖氨酸在0.06~0.43 mg/ml范围内线性关系良好,r=0.999 8,加样回收率为99.5%,RSD为1.2%(n=9)。 精密度、回收率高,最低检出限度、重现性、线性关系良好。试验结果表明该法适用于苄达赖氨酸的含量测定。
3 讨论
结果显示,处方1、2、3的pH虽然可以通过NaOH来调整至适宜范围内(6.8~7.8),但毫渗压摩尔比在未加渗透压调节剂的情况下就已经远远超出了范围(0.90~1.10)。且泊洛沙姆-188单独溶于水后就能够产生渗透压,因此无法通过减少泊洛沙姆-188的量来降低毫渗压摩尔比值。在今后的研究中,可以再通过研究其他基质来消除卡波姆与苄达赖氨酸的配伍禁忌。
凝胶的制备工艺大致相同,在制备凝胶基质时要注意使基质充分溶解后,再与主药及其他辅料混合均匀。由于基质的性能易受温度、pH等因素的影响,制备时更应考虑到这些影响产品质量的重要因素。而该类凝胶用于人眼,必须考虑到其安全、有效、可行的特点。应用与主药相适合的凝胶基质将原来的滴眼液制备成眼用凝胶后,大大地提高了药物的顺应性和生物利用度,并起到降低刺激性的作用[9],使患者在使用过程中感到更加舒适。但在基质的选择与筛选过程中,仍需要通过大量的试验来取舍。
本研究通过多次的试验,筛选出了比较合理的处方及工艺,制备得到的眼用凝胶剂性状良好,性质稳定,pH及渗透压均能符合要求,达到了预期的结果;且苄达赖氨酸有极好的抗白内障作用,将其设计成凝胶剂能够很好地提高药物有效利用率,延长药物作用时间,使得其在晶状体内浓集,发挥良好的抗白内障作用,这在临床用于治疗白内障现有的药物中极为少见的,且有些药物甚至不能到达晶状体,因此制备出苄达赖氨酸眼用凝胶意义深远。
[1]严汉英.抗白内障新药苄达赖氨酸的研究进展[J].中国新药与临床杂志,1999,18(4):240-243.
[2]王艳,王柏.原位凝胶在滴眼剂中的应用[J].中国药业,2008,17(1):19-20.
[3]陆伟,蒋新国.卡波姆和聚卡波菲在药剂学中应用的新进展[J].中国医院药学杂志,2002,22(8):491-492.
[4]舍斯基,韦勒.药用辅料手册[M].北京:化学工业出版社,2005.
[5]凌沛学,员象敏,张天民.玻璃酸钠在眼用溶液中的作用[J].中南药学,2004,2(4):229-231.
[6]国家药典委员会.中华人民共和国药典[S].2部.北京:化学工业出版社,2005.
[7]苄达赖氨酸滴眼液(商品名:莎普爱思)说明书.浙江莎普爱思制药有限公司.国药准字H19890101.
[8]徐宏祥,胡正国.离子对-反相高校液相色谱法测定苄达赖氨酸及其滴眼液的含量[J].药物分析杂志,2002,20(4):243-244.
[9]魏刚,徐晖,郑俊民.原位凝胶的形成机制及在药物控制释放领域的应用[J].中国药学杂志,2003,38(8):564-568.
Preparation and quality study of bendazac lysine eye gel
WANG Ping,KONG Feifei,TAN Xingqi*,GUO Liangjun,ZHENGWeiThe 98th Hospital of PLA,Zhejiang Province,Huzhou 313000,China
Objective:To study the preparation method and quality control of bendazac lysine eye gel.MethodsHA or HPMC or both combined were used as gelmatrix,sodium chloride iorder was added to regulate the osmotic pressure,the boric acid-borax was used to adjust pH,and sodium mercurothiolate was used as bacterial inhibitor,HPLC was adopted to determine the content ofmain drugs and study the stability of the formulation.ResultsThe content of bendazac lysine showed good linear relationship over the range of 0.06-0.43mg/m l(r=0.999 8).The average recovery was 99.5%with RSD of 1.2%(n=9).ConclusionThe processof preparation is simple and reliable,and the quality of the ophthalmic gel is stable.
Bendazac lysine;Eye gel;HPLC
R988.1
A
1673-7210(2011)08(c)-060-06
王萍,药师,主要从事药品管理工作。
谭兴起,副主任药师,主要从事天然药物化学工作。
2011-00-00)
