Toll样受体信号传导与炎症相关肿瘤的关系
2011-05-28曾治民何静刘安文
曾治民 何静 刘安文
南昌大学第二附属医院肿瘤科,江西 南昌 330006
Toll样受体信号传导与炎症相关肿瘤的关系
曾治民 何静 刘安文
南昌大学第二附属医院肿瘤科,江西 南昌 330006
Toll样受体(toll-like receptors,TLRs)属先天性免疫的病原相关分子模式(pathogenassociated molecular patterns,PAMPs)识别受体,主要表达于天然免疫细胞,在机体抵抗外来病原微生物入侵中起关键作用。TLRs在多种恶性肿瘤细胞及组织中均有表达,大量研究认为TLRs对肿瘤的发生、发展有重要影响,特别是与炎症相关肿瘤,如肝癌、结肠癌、胃癌和宫颈癌等。TLRs可能通过促进肿瘤细胞增殖、抑制肿瘤细胞凋亡及免疫逃逸等机制参与炎症相关性肿瘤的发生、发展。
Toll样受体; 信号传导; 炎症; 肿瘤
Toll样受体(toll-like receptors,TLRs)属于病原相关分子模式识别受体,在天然免疫及其继发的获得性免疫中起重要作用。TLRs通过激活核转录因子(nuclear factor-kappa B, NF-κB)进而调控多种重要的细胞因子、黏附分子和趋化因子的表达,在机体的免疫应答、炎症反应及组织修复等方面发挥重要的作用,其活化也参与细胞增殖和凋亡的过程。近来大量研究表明,TLRs与肿瘤密切相关,特别是与炎症相关肿瘤。本文就TLRs及其诱导的信号途径与炎症相关肿瘤的关系作一综述。
1 TLRs概述
人类天然性免疫系统具有高度特异性,能正确地区分自我与异己。这种能力是通过发达的高度保守的识别受体家族来实现,其中TLRs在宿主防卫病原微生物入侵中起到极为重要的作用,并且其激活也参与了机体获得性免疫反应。目前在哺乳动物中共发现11种:TLR1~TLR11[1]。TLRs与白介素-1受体(interleukin-1 receptors,IL-1Rs)同属一个超家族成员,主要的区别是细胞外区域:TLRs胞外富含亮氨酸重复序列,辅助识别病原微生物及其产物。而IL-1Rs含有3个免疫球蛋白样功能区域。TLRs是Ⅰ型跨膜糖蛋白,胞质区与IL-1Rs胞质区结构相似,称TIR结构域。TLRs胞内结构域含3个高度保守区,在TLRs和信号转导衔接蛋白的启动中发挥作用。TLRs胞外富含亮氨酸区域是受体接受区域,不同的受体识别不同的配体。TLR2与TLR1、TLR6的二聚体识别细菌脂肽/蛋白或脂膜酸,不同的是TLR1/TLR2二聚体识别三酰基脂肽,而TLR2~TLR6识别二酰基脂肽;TLR4与MD2及共刺激分子CD14结合识别革兰氏阴性菌特有的内毒素成分脂多糖(LPS);TLR3识别病毒双链RNA(dsRNA);TLR5识别细菌的鞭毛蛋白;TLR7、TLR8识别单链RNA(sRNA);TLR9识别细菌和病毒的未甲基化的CpG基序(CpGDNA motif)。TLRs主要表达于天然性免疫系统细胞,如间质中单核细胞、巨噬细胞、树突状细胞,外周血中各种单核细胞、自然杀伤细胞、T及B淋巴细胞[2-3],参与天然性免疫并与树突状细胞成熟有关。一些非免疫细胞如上皮细胞、内皮细胞等也表达TLRs。TLRs在人细胞中定位不同,TLRl、2、5、6、10主要定位于质膜,而TLR3、4、7、8、9主要定位于胞质内。TLRs被相关配体识别后,引发下游信号级联反应,经过复杂的分子间作用引起机体对外来物质的反应。
2 TLRs的信号传导途径
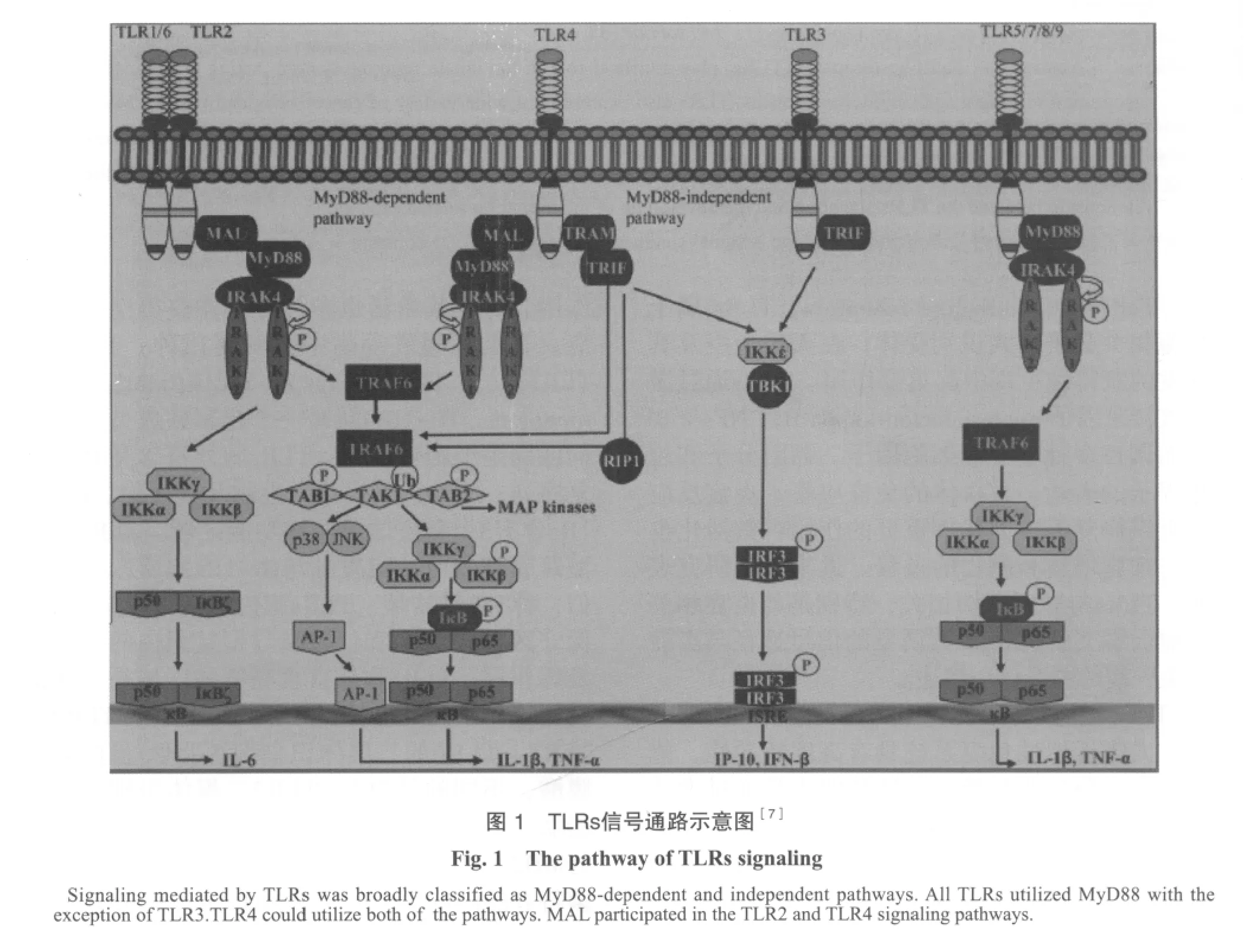
TLRs在相应配体刺激下导致下游相关适配蛋白被募集并促进其与IL-1相关激酶(IL-1R-associated kinase,IRAK)的相互关系。现有4种适配蛋白分别是:MyD88(myeloid differentiation primary response gene 88)、TIRAP/MAL(TIR domain-containing adaptor protein/MyD88-adaptor-like)、TRIF(TIR domain containing adaptor inducing IFN-β)、TRAM(TRIF related adaptor molecule)[4]。根据信号传导是否依赖MyD88,TLRs信号可分为两条信号转导通路[1,5](图1):一条为MyD88依赖性信号转导通路。IRAK-4募集、活化并激活IRAK-1和IRAK-2。IRAK-4、IRAK-1依次磷酸化导致 TNF相关因子6(TRAF-6)和泛素化酶E3等形成复合体,激活转化生长因子B活化酶Ⅰ(transforming growth factor-B-activated kinase 1,TAKⅠ)、TAB2和 TAB3。TAKⅠ活化下游的IKK(inhibitor of kappa-B kinase,IKK)和丝裂原活化蛋白酶(mitogen-activated protein kinase,MAPK)通路IKK-α、IKK-β和磷酸化IKB(B细胞K轻链增强子的抑制子)蛋白形成复合体,磷酸化作用降解IKB蛋白,引起转录因子NF-κB、IRF家族等相关基因易位、下游MAPK通路的激活诱导另一个转录因子AP-1的生成诱导前炎性细胞因子表达如IL-6、IL-12、IL-1、TNF-α、NO和协同共刺激分子CD40、CD80和 CD86等生成。TAK1激活JNK和p38导致炎症因子的产生。另一条是经TRIF介导的非MyD88依赖性信号转导通路。TRIF间接激活IFN调节因子3(interferon receptor factor 3,IRF-3)、NF-κB和AP-1,最终导致Ⅰ型干扰素及各种炎症因子产生等分泌。有研究认为同时和依次激活依赖MyD88及非MyD88依赖途径将分别导致协同和启动作用;然而同时用同一TLR的不同激动剂将导致耐受[6]。除各种免疫细胞表达TLRs外,许多上皮细胞及肿瘤细胞表达TLRs。
3 与TLRs相关的几种肿瘤
局部炎症与肿瘤有关[8]:⑴炎症性疾病增加发展成恶性肿瘤的风险;⑵NSAIDs类药能减少肿瘤发生并降低死亡率;⑶炎症信号通路影响癌基因的下游信号;⑷炎症因子、细胞及趋化因子等大量存在于肿瘤微环境中;⑸以炎症信号NF-κB、STAT等为靶点的药物降低癌症的发生与进展;⑹炎症因子的过度表达促进肿瘤生长。
3.1 TLRs与肝癌
肝癌的主要病因有乙肝病毒、丙肝病毒、黄曲霉素和乙醇及血色素沉着等。根据病因的不同,与肝癌有关的TLRs也不同。
国内肝癌患者大多由病毒性肝炎后肝硬化发展而来,肝硬化患者体内常有较多内毒素等。肝炎患者及肝癌细胞系HepG2与HepG2.2.15细胞质内表达TLR4;内毒素诱导HepG2.2.15肝癌细胞分泌TNF,且TLR4 mRNA水平比HepG2细胞明显更高,TLR4表达上调与慢性肝炎相关[9]。另外,Machida等[10]用LPS分别刺激野生型鼠(WT型)、TLR4-/-鼠、HCV非结构蛋白5A转基因鼠(NS5A Tg mice )和TLR4-/-NS5A Tg鼠4种鼠模型,发现NS5A Tg鼠产生较严重炎症反应是因肝细胞上TLR4所致,而非库弗细胞上TLR4所致。NS5A能协同乙醇诱导TLR4在乙醇饲养12个月的NS5A鼠中肝肿瘤形成;并证明干细胞标志基因Nanog作为一种新的TLR4下游基因对NS5A及乙醇诱导的内毒素血症协同致肝癌作用。因此,TLR4上调间接或直接与肝癌形成相关。
肝癌的又一个病因是乙肝病毒。TLR9可识别非甲基化CpGDNA,而乙肝病毒富含此片段。TLR9参与乙肝病毒致肝癌。非甲基化CpG DNA能使正常肝细胞(L-02细胞)及HepG2、HuH7和Hep3B等肝癌细胞经TLR9途径激活NF-κB;并且非甲基CpGDNA刺激L-02细胞后,因BCL-2及DNA甲基转移酶Ⅰ(DNMT-1)表达增加,而对TNF-α所诱导的凋亡更不敏感。肝癌细胞膜内外均表达TLR9。细胞表面TLR9信号能促进其增殖,并能上调Bcl-xL, XIAP和 cFLIP等抑凋亡因子而减少多柔比星的细胞毒性[11]。最新研究表明,TLR9信号不经NF-κB信号及Ⅰ型IFN分泌途径,而是上调多种肿瘤相关基因及转录因子而致肿瘤发生并进展[12]。
肝癌的另一病因丙肝病毒。TLR3表达于肝癌细胞及组织中,识别ds-RNA。Yoneda等[13]认为内源性的TLR3能诱导细胞凋亡,细胞表面的则主要经NF-κB途径产生炎症介质。转染聚肌苷酸-聚胞苷酸(Poly I∶C)入细胞内可下调抗凋亡蛋白及协同放大肿瘤坏死因子相关诱导凋亡配体(TRAIL)两种方式诱导凋亡。Poly I∶C刺激肝细胞内外TLR3都只分泌少量IFN-β。Khvalevsky等[14]也认为TLR3信号途径在HepG2、Huh7等肝癌细胞系中倾向于诱导凋亡,而不是诱导产生促炎因子。
因此,TLRs与肝癌的关系,因病因的不同而不同。TLR4、TLR9主要协同相关病因促进肝癌形成并发展,而TLR3在肝癌细胞中倾向于凋亡。
3.2 TLRs与结直肠癌
大约1%~2%的结直肠癌由炎症性肠炎引起的。肠道中存在多种革兰氏阴性肠道菌群,结肠内皮细胞及结肠癌细胞表达TLR4。大量研究表明,TLR4在炎症及肿瘤的发生、发展中产生重要影响[15-18]。在溃疡性肠炎向恶性肿瘤转化过程中有多种分子机制参与,其中2个关键基因是COX-2及NF-κB。
TLR4的激活进一步诱导COX-2表达和EGFR信号,而EGFR及COX-2高表达与肿瘤形成有关。COX-2的下游产物pGE2能控制炎症及修复黏膜作用;肠道损伤鼠模型在恢复期额外给予大剂量的pGE2,TLR4-/-鼠致癌率与野生型对照组鼠相同。Hernandez等[19]认为这是因为恢复期额外给予的pGE2打破了内源性pG的平衡。TLR4-COX-2-pGE2构成信号轴对机体致癌。
在转化过程中另外一个与TLR有关的重要分子是NF-κB。NF-κB作为TLR的下游信号,能促进炎症介质的产生及有利于肿瘤的形成。Tang等[16]认为TLR4激活ERK1/2、p38及NF-κB信号引发大量炎症因子如IL-6、基质酶及尿激酶纤溶酶促进肠癌进展[20]`。然而,Doan等[21]却认为TLR4是增加Akt磷酸化(PI3K)/Akt信号。免疫抑制剂雷帕霉素作用于TLR4而抗肿瘤机制:⑴破坏TLR4激活Akt介导的Bcl-xL上调,而减弱肿瘤抗凋亡[22];⑵通过下调TLR4的表达并抑制NF-κB信号,抑制TLR4触发的IL-6及PGE2的产生,从而产生抗癌作用[23]。因此,TLR4信号过度将促进肿瘤发生,TLR4信号阻断将减缓肿瘤生长。
3.3 TLRs与胃癌
胃上皮细胞表达多种T L R s,胃癌细胞表达TLR2、TLR4、TLR5和TLR9等TLRs,并对胃癌发生、发展产生重要影响[24-26]。目前以TLR4和TLR2在胃癌中的作用研究较为深入,但尚存争议。
幽门螺杆菌(HP)与慢性萎缩性胃炎、消化性溃疡、胃黏膜相关淋巴瘤和胃癌等消化性疾病有密切关系。Maeda等[27]研究了HP与胃癌细胞系MKN45及单核细胞THP-1上TLRs的作用。HP诱导NF-κB激活在胃癌细胞及单核细胞间是两种不同的机制。单核细胞激活NF-κB是经TLR4途径并依赖共刺激分子CD4及IRAK,胃癌细胞则不经TLR4,也不依赖CD4及IRAK,而依赖cag致病岛。然而Huang等[26]在小鼠模型发现,李氏特菌通过TLR2信号激活NF-κB及MAKP途径对肿瘤促增殖并抑制凋亡的作用,而非TLR4途径促进肿瘤生长,并且只对较大实体肿瘤有促进作用。Chochi等[28]认为LPS是经TLR4途径而非TLR2途径影响肿瘤细胞。但是只有HP及其LPS能减弱单核细胞对胃癌细胞的细胞毒作用和减少CD57NK细胞穿孔素的产生,而大肠埃希菌的LPS无此功能。正因如此使得宿主对胃癌更易感。胃癌细胞系MKN28及MKN45微弱表达TLR4。Yokota等[29]认为HPLPS是通过LPS-TLR2-MEK1/2-ERK1/2MAPK-NF-Y途径上调TLR4表达,促胃癌细胞增殖。然后TLR4的表达反过来产生更多的炎性反应进一步促进肿瘤生长及转移,TLR2及TLR4共同参与了胃癌的发展。
即使是同一种TLR也可能因为单核苷酸多态性(single nucleotide polymorphism,SNP)的原因而产生不同的结果。某基因正因存在多态性而对于整个群体是有利的;然而对于独立的个体,这一基因的携带或突变可能改变对某疾病的易感性,从而致病[30]。有报道认为白种人中CD14-159C/T和TLR9-1237T/C启动子多态性与HP引起的胃炎有关,并且与白种人中胃癌癌前病变有关。两独立大样本的病例对照统计分析表明:CD14-159C/T和TLR9-1237T/C启动子多态性与胃癌无明显相关性[31]。TLR4最常见的SNPAsp299Gly及Thr399Ileu,在白种人及印度人群中与胃癌及其癌前病变有关,在日本等亚洲人群中不存在;而亚洲人群癌前病变与TLR4+3725 G/C多态性有关[32]。另外,Hold等[33]认为TLR4+896A>G多态性是非贲门胃癌的危险因子。正是由于TLRs的多态性使得其编码的蛋白或传导的信号与正常有所不同,而使特定人群出现对胃癌等易感。目前对于TLRs SNP的研究大部分都是临床数据统计分析,具体机制有待进一步研究。
3.4 TLRs与宫颈癌
宫颈癌的一个重要病因是HPV的持续感染,尤其是高风险性HPV16及HPV18基因型。Hasan等[34]研究认为感染高风险性HPV16阳性细胞系及宫颈癌细胞能显著下调TLR9的表达及信号传导,而HPV18相对弱一些。HPV早期基因E6及E7能干扰TLR9转录顺式作用元件的-3227至-2923和-1451至-1017区域,从而下调了TLR9的启动子活性,在基因水平上直接抑制TLR9 mRNA的形成,从而减少了机体先天性免疫机制清除病毒的可能,这可能是宫颈癌细胞的免疫逃逸及HPV持续感染的一个原因。Lee等[35]研究认为TLR9在宫颈低级别上皮非典型增生到侵袭性宫颈癌组织中的表达逐渐升高。但该研究并未进一步阐明TLR9升高与癌症发生的内在关系。由于宫颈经常接触多种细菌,Yu等[36]认为宫颈癌进展与TLR4的作用有关,其观察到在宫颈癌患者中TLR4表达下降,并且与HPV P(16INK4A)基因整合进宿主细胞有关。因宫颈癌与HPV有密切关系,故TLR9与HPV在宫颈癌中可能起重要作用。
4 结语
TLRs作为识别病原微生物的重要分子之一,在免疫细胞中被激活对宿主防疫微生物起重要作用。肿瘤细胞表面或细胞质内表达的TLRs对炎症相关肿瘤产生重要影响。这种影响因肿瘤各异;即使是同一种肿瘤,也视TLRs分型的不同而不同。TLRs激活后引起下游信号传导并导致肿瘤发生、进展;然而对于哪种TLRs在某肿瘤中起主导作用抑或是共同作用目前尚有待进一步研究。
[1]AKIRA S, TAKEDA K. Toll-like receptor signaling[J]. Nat Rev Immunol, 2004, 4(7): 499-511.
[2]SIEDNIENKO J, MIGGIN S M. Expression analysis of the Toll-like receptors in human peripheral blood mononuclear cells[J]. Methods Mol Biol, 2009, 517: 3-14.
[3]HEMMI H, AKIRA S. TLR signalling and the function of dendritic cells[J]. Chem Immunol Allergy, 2005, 86: 120-135.
[4]O’NEILL L A. The role of MyD88-like adapters in Toll-like receptor signal transduction[J]. Biochem Soc Trans, 2003,31(Pt 3): 643-647.
[5]KRISHNAN J, LEE G, CHOI S. Drugs targeting Toll-like receptors[J]. Arch Pharm Res, 2009, 32(11): 1485-1502.
[6]BAGCHI A, HERRUP E A, WARREN H S, et al. MyD88-dependent and MyD88-independent pathways in synergy,priming, and tolerance between TLR agonists[J]. J Immunol, 2007, 178(2): 1164-1171.
[7]KRISHNAN J, SELVARAJOO K, TSUCHIYA M, et al. Tolllike receptor signal transduction[J]. Exp Mol Med, 2007,39(4): 421-438.
[8]MANTOVANI A, ALLAVENA P, SICA A, et al. Cancerrelated inflammation[J]. Nature, 2008, 454(7203): 436-444.
[9]WEI X Q, GUO Y W, LIU J J, et al. The significance of Tolllike receptor 4(TLR4) expression in patients with chronic hepatitis B[J]. Clin Invest Med, 2008, 31(3): E123-E130.
[10]MACHIDA K, TSUKAMOTO H, MKRTCHYAN H, et al.Toll-like receptor 4 mediates synergism between alcohol and HCV in hepatic oncogenesis involving stem cell marker Nanog[J]. Proc Natl Acad Sci U S A, 2009, 106(5):1548-1553.
[11]LIU X, XU Q, CHEN W, et al. Hepatitis B virus DNA-induced carcinogenesis of human normal liver cells by virtue of nonmethylated CpG DNA[J]. Oncol Rep, 2009, 21(4):941-947.
[12]TANAKA J, SUGIMOTO K, SHIRAKI K, et al. Functional cell surface expression of toll-like receptor 9 promotes cell proliferation and survival in human hepatocellular carcinomas[J]. Int J Oncol, 2010, 37(4): 805-814.
[13]YONEDA K, SUGIMOTO K, SHIRAKI K, et al. Dual topology of functional Toll-like receptor 3 expression in human hepatocellular carcinoma: differential signaling mechanisms of TLR3-induced NF-kappaB activation and apoptosis[J].Int J Oncol, 2008, 33(5): 929-936.
[14]KHVALEVSKY E, RIVKIN L, RACHMILEWITZ J, et al.TLR3 signaling in a hepatoma cell line is skewed towards apoptosis[J]. J Cell Biochem, 2007, 100(5): 1301-1312.
[15]FUKATA M, ABREU M T. TLR4 signalling in the intestine in health and disease[J]. Biochem Soc Trans, 2007, 35(Pt 6):1473-1438.
[16]TANG X Y, ZHU Y Q, WEI B, et al. Expression and functional research of TLR4 in human colon carcinoma[J]. Am J Med Sci, 2010, 339(4): 319-326.
[17]FUKATA M, CHEN A, VAMADEVAN A S, et al. Toll-like receptor-4 promotes the development of colitis-associated colorectal tumors[J]. Gastroenterology, 2007, 133(6):1869-1881.
[18]FUKATA M, HERNANDEZ Y. Innate immune signaling by Toll-like receptor-4 (TLR4) shapes the inflammatory microenvironment in colitis-associated tumors[J]. Inflamm Bowel Dis, 2009, 15(7): 997-1006.
[19]HERNANDEZ Y, SOTOLONGO J, BREGLIO K, et al. The role of prostaglandin E2 (PGE 2) in toll-like receptor 4(TLR4)-mediated colitis-associated neoplasia[J]. BMC Gastroenterol, 2010, 10: 82.
[20]KILLEEN S D, WANG J H, ANDREWS E J, et al. Bacterial endotoxin enhances colorectal cancer cell adhesion and invasion through TLR-4 and NF-kappaB-dependent activation of the urokinase plasminogen activator system[J].Br J Cancer, 2009, 100(10): 1589-1602.
[21]DOAN H Q, BOWEN K A, JACKSON L A, et al. Toll-like receptor 4 activation increases Akt phosphorylation in colon cancer cells[J]. Anticancer Res, 2009, 29(7): 2473-2478.
[22]SUN Q, ZHENG Y, LIU Q, et al. Rapamycin reverses TLR4 signaling-triggered tumor apoptosis resistance by disrupting Akt-mediated Bcl-xL upregulation[J]. Int Immunopharmacol, 2008, 8(13-14): 1854-1858.
[23]SUN Q, LIU Q, ZHENG Y, et al. Rapamycin suppresses TLR4-triggered IL-6 and PGE(2) production of colon cancer cells by inhibiting TLR4 expression and NF-kappaB activation[J]. Mol Immunol, 2008, 45(10):2929-2936.
[24]张隆, 魏涛, 倪振华, 等. 髓样分化因子88与胃癌细胞BGC823紫杉醇耐药性关系研究[J]. 中国癌症杂志,2010, 20(7): 515-519.
[25]SCHMAUSSER B, ANDRULIS M, ENDRICH S, et al. Tolllike receptors TLR4, TLR5 and TLR9 on gastric carcinoma cells: an implication for interaction with Helicobacter pylori[J]. Int J Med Microbiol, 2005, 295(3): 179-185.
[26]HUANG B, ZHAO J, SHEN S, et al. Listeria monocytogenes promotes tumor growth via tumor cell toll-like receptor 2 signaling[J]. Cancer Res, 2007, 67(9): 4346-4352.
[27]MAEDA S, AKANUMA M, MITSUNO Y, et al. Distinct mechanism of Helicobacter pylori-mediated NF-kappa B activation between gastric cancer cells and monocytic cells[J]. J Biol Chem, 2001, 276(48): 44856-44864.
[28]CHOCHI K, ICHIKURA T, KINOSHITA M, et al.Helicobacter pylori augments growth of gastric cancers via the lipopolysaccharide-toll-like receptor 4 pathway whereas its lipopolysaccharide attenuates antitumor activities of human mononuclear cells[J]. Clin Cancer Res, 2008, 14(10):2909-2917.
[29]YOKOTA S, OKABAYASHI T, REHLI M, et al. Helicobacter pylori lipopolysaccharides upregulate toll-like receptor 4 expression and proliferation of gastric epithelial cells via the MEK1/2-ERK1/2 mitogen-activated protein kinase pathway[J]. Infect Immun, 2010, 78(1): 468-476.
[30]EL-OMAR E M, NG M T, HOLD G L. Polymorphisms in Toll-like receptor genes and risk of cancer[J]. Oncogene,2008, 27(2): 244-252.
[31]HOLD G L, RABKIN C S, GAMMON M D, et al. CD14-159C/T and TLR9-1237T/C polymorphisms are not associated with gastric cancer risk in Caucasian populations[J]. Eur J Cancer Prev, 2009, 18(2): 117-119.
[32]HISHIDA A, MATSUO K, GOTO Y, et al. Toll-like receptor 4+3725 G/C polymorphism, Helicobacter pylori seropositivity,and the risk of gastric atrophy and gastric cancer in Japanese[J]. Helicobacter, 2009, 14(1):47-53.
[33]HOLD G L, RABKIN C S, CHOW W H, et al. A functional polymorphism of toll-like receptor 4 gene increases risk of gastric carcinoma and its precursors[J]. Gastroenterology,2007, 132(3): 905-912.
[34]HASAN U A, BATES E, TAKESHITA F, et al. TLR9 expression and function is abolished by the cervical cancerassociated human papillomavirus type 16[J]. J Immunol,2007, 178(5): 3186-3197.
[35]LEE J W, CHOI J J, SEO E S, et al. Increased toll-like receptor 9 expression in cervical neoplasia[J]. Mol Carcinog, 2007, 46(11): 941-947.
[36]YU L, WANG L, LI M, et al. Expression of toll-like receptor 4 is down-regulated during progression of cervical neoplasia[J]. Cancer Immunol Immunother, 2010, 59(7):1021-1028.
The relationship between TLRs signaling and inflammation-related-cancers
ZENG Zhi-min, HE Jing, LIU An-wen(The Oncology Department, the Second Affiliated Hospital, Nanchang University, Nanchang Jiangxi 330006, China)
LIU An-wen E-mail:awliu666@163.com
Toll-like receptors (TLRs) play a critical role in the innate immune system, acting as pathogenrecognition receptors against microorganisms. TLRs also express on a wide variety of cancer cells and tissues. Many evidences showed that TLRs have an effect on the tumorigenesis and progress, especially inf l ammation related cancers such as liver cancer, colorectal cancer, gastric cancer and cervical cancer and so on. This review focused on the relationship between the TLRs signaling and the developing of inf l ammation related cancers.
Toll-like receptors; Signal conduct; Inf l ammation; Neoplasm
10.3969/j.issn.1007-3969.2011.06.014
R730.231
A
1007-3639(2011)06-0489-06
刘安文 E-mail:awliu666@163.com
2011-03-28
2011-05-25)
