氟维司群治疗绝经后转移性乳腺癌患者的疗效及安全性
2011-05-28王佳玉袁芃马飞樊英张频李青徐兵河
王佳玉 袁芃 马飞 樊英 张频 李青 徐兵河
中国医学科学院北京协和医学院肿瘤医院内科,北京 100021
氟维司群治疗绝经后转移性乳腺癌患者的疗效及安全性
王佳玉 袁芃 马飞 樊英 张频 李青 徐兵河
中国医学科学院北京协和医学院肿瘤医院内科,北京 100021
背景与目的:氟维司群是一种雌激素受体(estrogen receptor,ER)拮抗剂,该药对既往经内分泌治疗后进展的转移性乳腺癌(MBC)仍有较好疗效。本研究观察氟维司群对他莫昔芬(TAM)治疗后进展的绝经后MBC患者的疗效及安全性。方法:氟维司群250 mg,肌肉注射,每月1次,直至肿瘤进展。主要研究终点为至疾病进展时间(TTP),次要终点为客观有效率(ORR),缓解期(DoR)及临床获益率(CBR)。结果:本组21例患者中位TTP为4个月,ORR为19.0%,CBR为33.3%,其中部分缓解(PR)4例,疾病稳定(SD)超过24周3例,有效患者的中位DoR为8个月,1年生存率为42.8%,2年生存率为23.8%,中位总生存时间(OS)为11个月。氟维司群的疗效与患者ER状态、术后无病生存期(DFS)及是否为初始治疗等因素相关:ER高表达者较ER低表达者更易从氟维司群治疗中获益(CBR分别为100%和17.6%,P=0.002),DFS超过2年者的CBR明显较DFS小于2年者高(分别为46.7%和0,P=0.040),氟维司群为MBC初始治疗者的CBR较非初始治疗者明显增高(分别为80.0%和18.8%,P=0.01)。有肺转移者氟维司群的疗效较无转移者好(CBR分别为55.6%和16.7%,P=0.061)。全组不良反应较轻微,主要表现为乏力、潮热、关节疼痛、皮疹及食欲减退等。在接受氟维司群长时间(8~16个月)治疗的MBC患者中有4例(28.5%)出现上肢麻木等外周神经症状,且进行性加重。结论:氟维司群250 mg是治疗TAM失败后的绝经后MBC患者的有效内分泌治疗药物,且耐受性较好。
绝经后妇女; 转移性乳腺癌; 雌激素受体; 氟维司群
乳腺癌的发生、发展与患者血中雌激素水平密切相关,以减少雌激素水平或拮抗雌激素受体为目的的内分泌治疗受到越来越多的关注。他莫昔芬(TAM)能竞争性的与肿瘤细胞雌激素受体(estrogen receptor,ER)结合,阻断雌激素与ER的结合,从而抑制肿瘤细胞增殖[1]。该药是经典的内分泌治疗药物,它对雌激素敏感乳腺癌有较好的疗效,但仍有部分患者最终出现TAM耐药[1]。大量临床研究证实,选择性芳香化酶抑制剂(包括阿那曲唑、来曲唑及依西美坦)对TAM耐药的绝经后MBC有较好 疗效[2-3]。但临床仍需要更多安全有效的药物,用作二线甚至三线内分泌治疗。
氟维司群是一种ER拮抗剂。该药与TAM和芳香化酶抑制剂的作用机制不同,它与ER有极强的亲和力,并能有效地降解ER受体蛋白,下调ER受体水平[4-5]。Ⅲ期临床研究(0020号和0021号研究)表明:氟维司群对TAM治疗后进展的MBC的疗效与阿那曲唑相当[6-8]。基于该结果,氟维司群于2002年获FDA批准在美国上市,2004年在欧洲上市。
FAST是由中国医学科学院肿瘤医院牵头的一项氟维司群注册临床试验[9]。本研究对我院参加该试验经氟维司群治疗的21例患者进行总结,以评价氟维司群用于经TAM治疗后进展的绝经后MBC患者的疗效特点及安全性。
1 资料和方法
1.1 一般资料
2006年6月1日—2008年1月30日我院收治的经TAM治疗失败的MBC 21例。全组均为绝经后、ER阳性女性患者,中位年龄55岁(37~68岁),自然绝经者18例,行卵巢去势术者3例。ECOG评分中位数为1(0分14例,1分5例,2分2例)分。全组患者均接受过乳腺癌改良根治术或根治术,原发肿瘤均经病理确诊为乳腺癌,转移灶经X线、CT、MR或骨ECT等证实。有17例患者曾接受术后辅助化疗。曾行TAM辅助内分泌治疗者17例,复发转移后行TAM治疗者4例、化疗者16例。本组患者均未经芳香化酶抑制剂治疗,且患者复发转移后接受过不超过2个化疗方案的治疗。肝、肺等内脏转移者14例,非内脏转移者7例。全组患者术后中位无病生存期(DFS)36个月。本组病例氟维司群为复发转移后的初始治疗者5例,非初始治疗者16例。
1.2 治疗方法
氟维司群 250 mg,肌肉注射,每28天为1个周期,至少用2个周期。本组患者每周期记录不良事件,每2个周期评价疗效,有效者继续氟维司群治疗,直至肿瘤进展或出现不可耐受的毒性,无效患者出组采用其他方法治疗。
1.3 疗效及毒性评价标准
疗效评价按照RESIST1.0疗效评价方法。主要研究终点为TTP(氟维司群治疗开始到肿瘤进展的时间)。次要终点包括有效率(response rate,RR),临床获益率(clinical benefit response rate,CBR):CR+PR+SD(稳定)≥24周,缓解期(DoR,首次达PR或CR疗效开始到肿瘤进展的时间)及总生存期(OS,从接受氟维司群治疗开始至患者死亡或末次随诊的时间)。
临床不良事件强度分级按照美国国立癌症研究所扩大通用毒性标准(NCIC CTC3.0)。
1.4 统计学处理
本研究采用SPSS 13.0统计软件中χ2检验对患者基线临床病理因素进行单因素分析,寻找可能影响疗效的因素。
2 结 果
2.1 疗效
21例患者总计接受108个周期氟维司群治疗,中位治疗4个周期(2~17个周期)。氟维司群的剂量强度为原定剂量的100%。患者中位TTP为4个月(2~48个月),ORR为19.0%(4/21),CBR为33.3%(7/21),其中CR 0例,PR 4例(19.0%),SD超过24周的3例(14.3%),PD 14例(66.7%)。有效患者的中位DoR为8个月(4~17个月),1年生存率为 42.8%(9/21),2年生存率为23.8%(5/21),中位OS为11个月。随访截止至2010年9月30日,尚有3例患者存活。
2.2 疗效的影响因素
经χ2检验分析结果显示:CBR与ER状态、术后DFS及该药是否为转移后初始治疗等因素相关,并且肺转移患者的CBR更高(表1)。本组患者ER高表达(IHC+++)及ER中、低水平表达(IHC+/++)的CBR分别为100%和23.1%,差异有统计学意义(P=0.006);其次,疗效与术后DFS的长短密切相关:7例临床获益的患者术后DFS均超过2年,而另6例DFS不足2年者无一例有效,两组CBR分别为46.7%和0(P=0.040);另外,CBR与氟维司群是否为初始治疗相关:氟维司群初始治疗的5例患者中80%获肿瘤缓解或长时间稳定(SD≥24周),而非初始治疗的16例患者仅18.8%的CBR,两组差异有统计学意义(P=0.011)。氟维司群的疗效与患者内脏转移与否无关,但对肺转移疗效更好,有肺转移的9例患者中5例临床获益,CBR为55.6%,无肺转移的12例患者CBR仅为16.7%(P=0.061),两者差异接近有统计学意义。其他,如PR状态、Her-2状态及患者一般状况等因素与疗效无相关性。
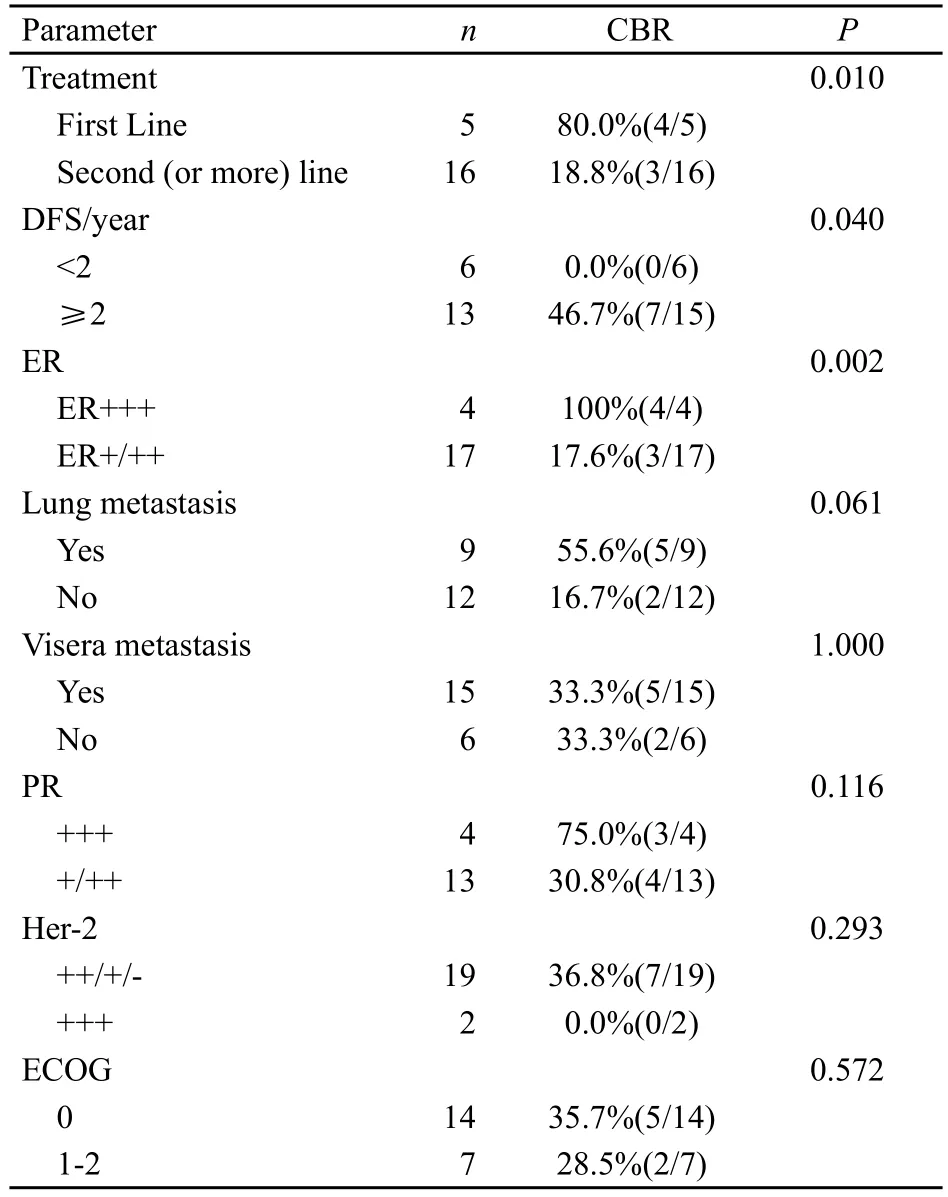
表 1 氟维司群近期疗效影响因素Tab. 1 Inf l uencing factors to the response of Fulvestrant
2.3 不良反应
本组患者氟维司群单药治疗的主要不良反应为乏力42.8%(9例)、潮热28.6%(6例)和注射部位疼痛及瘙痒28.5%(6例)。全组未出现Ⅲ度以上不良反应,亦没有因不良反应停药或延迟治疗者。多数患者表现为轻微不适,不影响日常生活(Ⅰ度反应)。少数患者出现Ⅱ度不良反应,包括:乏力14.3%(3例)、上肢麻木9.5%(2例)、肌力减退9.5%(2例)、关节疼痛9.5%(2例)、肝功能损伤(转氨酶增高)4.8%(1例)。其他较轻微的不良反应还包括:皮疹9.5%(2例)、恶心或食欲减退14.3%(3例)、胸闷头晕4.8%(1例)、外阴瘙痒4.8%(1例)及上肢麻木9.5%(2例)等。全组未出现与治疗相关的严重不良事件。
3 讨 论
本研究入组患者均为TAM治疗后进展的MBC,且大部分患者在复发转移后还接受过多程化疗,在接受氟维司群治疗后仍能获得接近20%的RR、33.3%的CBR以及8个月的中位DoR。其结果充分印证了该药临床前研究的发现:氟维司群是有别于TAM的ER拮抗剂,它能降解ER蛋白,有效下调ER水平,对TAM耐药的乳腺癌有较高的抗肿瘤活性[4]。本研究结果与文献报道的氟维司群二线治疗MBC疗效相似[7],且与目前临床常用于治疗绝经后MBC的内分泌药物,如来曲唑、依西美坦及阿那曲唑的疗效相似[11,13]。
χ2检验结果显示,原发肿瘤ER、患者的术后DFS、氟维司群是否为初始治疗等是影响氟维司群疗效的重要因素。结果符合MBC的内分泌治疗的重要适应症:ER或PR高表达、DFS相对较长(>2年)。徐兵河等[9]报告的氟维司群对比阿那曲唑治疗MBC的临床研究中曾指出,MBC经多线治疗后再接受氟维司群治疗可能会影响其疗效。Mello等[14]的研究也证实,氟维司群一线治疗的TTP较二线治疗更长(TTP分别为12个月和6个月)。这一观点与本研究结果不谋而合:氟维司群初始治疗的疗效明显高于非初始治疗者(CBR分别为80.0%和18.8%,P=0.01)。本研究结果提示,激素受体敏感型绝经后MBC患者尽早使用氟维司群会获得较好疗效。
本研究发现氟维司群的疗效与患者肺转移相关,肺转移者与无肺转移者CBR分别为55.6%和16.7%(P=0.061),两者差异接近有统计学意义,且4例经氟维司群治疗获PR的患者均有肺转移。结果提示氟维司群对肺转移患者可能有较好疗效。Robertson等[15]曾报道,氟维司群并不像传统的内分泌治疗药物对内脏转移的疗效欠佳,该药在Her-2阳性及有内脏转移的乳腺癌中仍能取得较好的疗效(CBR为44%)。但此结论尚需更充分的数据及研究论证。
本组病例在接受氟维司群治疗期间不良反应较轻微,主要表现为乏力、潮热、关节疼痛、皮疹和食欲减退等,发生率与既往文献报道类似[9,16-18]。氟维司群的不良反应与临床上常用的内分泌治疗药物类似。另外,由于该药独特的给药方式(肌注)以及药物溶剂的影响,相当一部分患者表现为注射部位瘙痒或疼痛(28.5%)。因此,在给患者实施治疗时,要求护士缓慢肌注(约3~5 min)十分重要。上肢麻木的症状出现在开始治疗的第4~6个月,其中2例患者随着疗程的延长麻木感进行性加重并伴有同侧上肢的肌力减退。氟维司群导致麻木的原因尚不清楚,此前也鲜有文献报道,可能由于长期氟维司群治疗后,其药物溶剂(蓖麻油)所致的神经毒性有关。但此观点尚需更细致的研究论证。
总之,氟维司群250 mg每月肌注是治疗绝经后MBC患者的有效内分泌治疗药物,且耐受性较好。ER高表达、术后DFS较长(大于2年)及初始治疗的MBC对氟维司群的反应性较好,该药对乳腺癌肺转移的患者可能有较好的疗效。
[1]徐兵河. 乳腺癌[M]. 北京: 北京大学医学出版社, 2005,187-189.
[2]GEISLER J, KING N, DOWSETT M, et al. Influence of anastrozole(Arimidex), a selective, non-steroidal aromatase inhibitor, on in vivo aromatisation and plasma oestrogen levels in postmenopausal women with breast cancer[J]. Br J Cancer, 1996, 74: 1286-1291.
[3]Letrozole, a new oral aromatase inhibitor: randomised trial comparing 2. 5 mg daily, 0. 5 mg daily and aminoglutethimide in postmenopausal women with advanced breast cancer.Letrozole International Trial Group (AR/BC3)[J]. Ann Oncol, 1998, 9: 639-645.
[4]OSBORNE C K, JARMAN M, MCAGUE R, et al. The importance of tamoxifen metabolism in tamoxifen-stimulated breast tumor growth[J]. Cancer Chemother Pharmacol,1994, 34(2): 89-95.
[5]WAKELING A E, BOWLER J. ICI 182, 780, a new antioestrogen with clinical potential[J]. J Steroid Biochem Mol Biol, 1992, 43: 173-177.
[6]VERGOTE I, ROBERTSON J F, KLEEBERG U, et al.Postmenopausal women who progress on Fulvestrant (Faslodex)remain sensitive to further endocine therapy[J]. Breast Cancer Res and Treat, 2003, 79(2): 207-211.
[7]HOWELL A, ROBERTSON J F R, QUARESMA ALBANO J, et al. Fulvestrant, formerly ICI 182, 780, is as effective as anastrozole in postmenopausal women with advanced breast cancer progressing after prior endocrine treatment[J]. J Clin Oncol, 2002, 20(16): 3396-3403.
[8]OSBORNE C K, PIPPEN J, JONES S E, et al. Double-blind,randomized trial comparing the efficacy and tolerability of Fulvestrant versus anastrozole in postmenopausal with advanced breast cancer progressing on prior endocrine therapy: results of a North American trial[J]. J Clin Oncol 2002; 20: 3386-3395.
[9]XU B, JIANG Z, SHAO Z, et al. Fulvestrant 250 mg versus anastrozole for Chinese patients with advanced breast cancer:results of a multicentre, double-blind, randomised phase III trial[J]. Cancer Chemother Pharmacol, 2011, 67(1): 223-230.
[10]ROBERTSON J F, OSBOME C K, HOWELL A, et al.Fulvestrant versus Anastrozole for the Treatment of Advanced Breast Carcinoma in Postmenopausal Women A Prospective Combined Analysis of Two Multicenter Trials[J]. Cancer,2003, 98 (2): 229-238.
[11]DOMBERNOWSKY P, SMITH I, FALKSON G, et al.Letrozole, a new oral aromatase inhibitor for advanced breast cancer: double-blind randomized trial showing a dose effect and improved efficacy and tolerability compared with megestrol acetate[J]. J Clin Oncol, 1998, 16(2): 453-461.
[12]KAUFMANN M, BAJETTA E, DIRIX L Y, et al. Exemestane is superior to megestrol acetate after tamoxifen failure in postmenopausal women with advanced breast cancer: results of a phase Ⅲ randomized double-blind trial. The Exemestane Study Group[J]. J Clin Oncol, 2000, 18(7): 1399-1411.
[13]BUZDAR A U, HORTOBAGYI G. Update on endocrine therapy for breast cancer[J]. Clin Cancer Res, 1998, 4:527-534.
[14]MELLO C A, CHINEN L T, DA SILVA S C, et al. Prolonged time to progression with Fulvestrant for metastatic breast cancer[J]. Med Oncol. 2010 Mar 20. [Epub ahead of print].
[15]ROBERTSON J F, STEGER G G, NEVEN P, et al. Activity of Fulvestrant in HER2-overexpressing advanced breast cancer[J]. Ann Oncol, 2010, 21(6): 1246-1253.
[16]HOWELL A, ROBERTSON J F, QUARESMA ALBANO J,et al. Fulvestrant, formerly ICI 182, 780, is as effective as anastrozole in postmenopausal women with advanced breast cancer progressing after prior endocrine treatment[J]. J Clin Oncol, 2002, 20(16): 3396-3403.
[17]HOWELL A, ROBERTSON J. Response to a specific antioestrogen (ICI 182780) in tamoxifen-resistant breast cancer[J]. Lancet, 1995, 345(8955): 989-990.
[18]HOWELL A, DEFRIEND D, ROBERTSON J F, et al.Pharmacokinetics, Pharmacological, and anti-tumor effects of the specific anti-oestrogen ICI 182780 in women with advanced breast cancer[J]. Br J Cancer, 1996, 74(2): 300-308.
Fulvestrant in treating postmenopausal patients with metastatic breast cancer
WANG Jia-yu, YUAN Peng,MA Fei,FAN Ying, ZHANG Pin, LI Qing,XU Bing-he(Department of Medical Oncology,Cancer Institute and Hospital, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100021, China)
XU Bing-he E-mail:bhxu@hotmail.com
Background and purpose:Fulvestrant, an estrogen receptor (ER) antagonist with no known agonist effects, has shown activity in patients with recurrent ER-positive advanced breast cancer or those patients who have disease progression after endocrine therapy of TAM. This prospective study was designed to evaluate the efficacy and safety of fulvestrant in advanced breast cancer of Chinese women who failed to previous TAM treatment.Methods:Twenty-one patients were enrolled and treated with 250 mg/month of fulvestrant every four weeks via an intramuscular injection. The primary endpoint was to fi nd the time to progression (TTP), secondary endpoints included objective response rate (ORR), duration of response (DoR) and clinical benefit rate (CBR).Results:The median TTP was 4 months with an overall response rate of 19%. One-year survival rate was 42.8%. Two-year survival rate was 32.8%. Median DoR from response to disease progression was 8 months. CBR was 33.3%, including 4 patients who showed a partial response(PR) and 3 patients who achieved stable disease(SD)≥24 weeks. Patients with high ER expression had higher CBR than patients with ER lower expression(100%vs17.6%,P=0.002). Patients with longer postoperative DFS had higher CBR than patients with shorter DFS (46.7%vs0,P=0.040). Patients treated with fulvestrant as fi rst line got more benefit than those as second line(CBR: 80.0%vs18.8%,P=0.01). Patients with lung metastasis had higher CBR than those without lung metastasis (CBR: 55.6%vs16.7%,P
fulvestrant for more than 8 months, had adverse events (AE) in peripheral neuropathy.Conclusion:This data demonstrates that 250 mg of fulvestrant is effective and tolerable in the treatment of postmenopausal women with advanced breast cancer whose disease has progressed or recurred after prior endocrine treatment.
Postmenopausal women; Matastasis breast cancer; Estrogen receptor; Fulvestrant
10.3969/j.issn.1007-3969.2011.06.008
R737.9;R730.7
A
1007-3639(2011)06-0461-04
徐兵河 E-mail:bhxu@hotmail.com
2011-02-18
2011-04-15)
