窈窕茶的质量标准研究
2011-05-26宋粉云钟兆健李健奇
周 欣, 宋粉云, 钟兆健, 李健奇
(广东药学院,广东 广州 510006)
窈窕茶为香港北京制药厂提供,是由决明子、枳实、厚朴、陈皮等药材经粉碎后制成的茶包,具有通便散热结、利水消肿、理气健脾的功效,临床主要用于治疗肠胃积热、水湿内停导致的肢体沉重浮肿,大便秘结、腹胀、腹痛,口干口燥,小便不利等症状。该产品尚未见相关质量标准报道,为评价窈窕茶的质量,确保临床疗效,本实验研究建立了决明子、枳实、厚朴的薄层色谱鉴别方法,该方法简便、可行,重复性好;其中厚朴具有燥湿消痰、下气除满的作用,常用于食积气滞、腹胀便秘等症状的治疗[1],是窈窕茶的重要组成部分,厚朴的主成分为厚朴酚及和厚朴酚,因此通过采用反相高效液相色谱法对其进行定量测定来对该药进行质量控制[2-4],该法具有分离效果好、灵敏、准确等优点。
1 仪器和试药
安捷伦公司生产Agilent 1100高效液相色谱仪,Agilent 1100系列双元泵,Agilent 1100 nm可变波长检测器,Agilent 1100/化学工作站;昆山市超声仪器有限公司生产超声波清洗器 KQ5200[频率:(35±5)%KHz;功率:250 W]。
大黄酚对照品(中国药品生物制品检定所,0796-200105),大黄素对照品(中国药品生物制品检定所,0795-200205),辛弗林对照品(中国药品生物制品检定所,0727-200105),厚朴酚对照品(中国药品生物制品检定所,110729-200310),和厚朴酚对照品(中国药品生物制品检定所,110730-200609);窈窕茶(香港北京制药厂,批号:I0509Y、H1201Y、I0620Y),规格为2 g/包;水为双蒸水,甲醇为色谱纯,其他化学试剂均为分析纯。
2 定性鉴别
2.1 决明子的鉴别 取窈窕茶内容物10 g于100 mL具塞锥形瓶中,加入20%盐酸溶液(37%浓盐酸溶液约27 mL配成50 mL溶液),超声30 min,滤过,用三氯甲烷萃取2次,每次20 mL;合并三氯甲烷层后浓缩至3~5 mL,作为供试品溶液;按此法制得3份不同批号供试品溶液。取大黄酚、大黄素对照品适量,加甲醇配成每1 mL各含1 mg的混合溶液,作为对照品溶液。按处方从中除去决明子,依法制成阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录VIB)试验,吸取3个批号供试液和阴性溶液各10 μL,对照品溶液5 μL;分别点于同一硅胶G薄层板上,以石油醚(30~60℃)-正己烷-乙酸乙酯-甲酸(4∶14∶5 ∶0.1)为展开剂,展开,取出后晾干。置365 nm紫外光灯下检视。供试品色谱中在与对照品相应的位置上显相同黄色荧光斑点,阴性对照无干扰。结果见图1。

图1 决明子薄层色谱图1.阴性对照 2.大黄酚和大黄素对照品3-5.样品(I0509Y,I0620Y,H1201Y)Fig.1 TLC of Cassiae Semen1.negative sample without Cassiae Semen 2.reference substances of emodin and chrysophanol 3-5.samples(I0509Y,I0620Y,H1201Y)
2.2 枳实的鉴别 取窈窕茶内容物4 g于100 mL具塞锥形瓶中,加入甲醇40 mL,超声处理20 min,滤过,滤液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液;按此法制得3份不同批号的供试品溶液。取辛弗林对照品适量,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。按处方从中除去枳实,依法制成阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录VIB)试验,吸取上述溶液各5 μL,分别点于同一硅胶G薄层板上,以甲醇-丙酮-三氯甲烷-浓氨水(3∶4 ∶13 ∶0.5)为展开剂,展开,取出后晾干,喷以0.5%茚三酮乙醇显色,在105℃加热约10 min至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同的红色斑点,阴性对照无干扰。结果见图2。
2.3 厚朴的鉴别 取窈窕茶10 g于100 mL具塞锥形瓶中,加甲醇100 mL,密塞,静置过夜,超声30 min,滤过,取一半滤液水浴蒸干,残渣用1~2 mL甲醇溶解作为供试品溶液;按此法制得3份不同批号的供试品溶液。取厚朴酚及和厚朴酚对照品,加甲醇制成每1 mL各含1 mg的混合溶液,作为对照品溶液。按处方从中除去厚朴,依法制成阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录VIB)试验,吸取上述溶液各5 μL,分别点于同一硅胶G薄层板,以石油醚(60~90℃)-乙酸乙酯-甲酸(17∶3∶0.4)为展开剂,展开,取出后晾干,喷以1%香草醛硫酸溶液,105℃加热至斑点清晰。供试品色谱中在与对照品相应的位置显相同颜色的斑点,阴性对照无干扰。结果见图3。
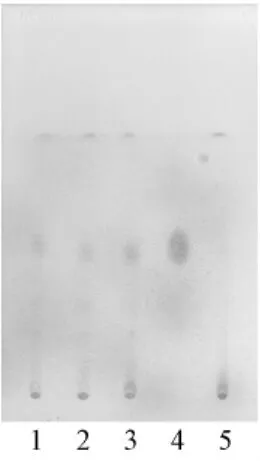
图2 枳实的薄层色谱图1-3.样品(I0509Y,I0620Y,H1201Y)4.辛弗林对照品 5.阴性对照Fig.2 TLC of Aurantii Fructus immaturus1-3.sample(I0509Y,I0620Y,H1201Y)4.reference substance of synephrine 5.negative sample without Aurantii Fructus immaturus
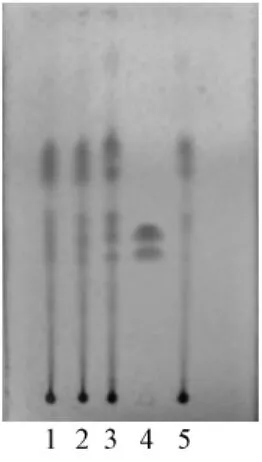
图3 窈窕茶中厚朴的薄层色谱图1-3.样品(I0509Y,I0620Y,H1201Y)4.厚朴酚及和厚朴酚对照品 5.阴性对照Fig.3 TLC of Magnoliae officinalis Cortex1-3.samples(I0509Y,I0620Y,H1201Y)4.reference substance of magnolol and honokio 5.negative sample without Magnoliae officinalis Cortex
3 样品测定
3.1 样品制备
3.1.1 对照品溶液的制备 精密称取厚朴酚对照品11.1 mg置于50 mL量瓶中,和厚朴酚对照品10.0 mg置于100 mL量瓶中,分别加甲醇溶解并稀释至刻度,摇匀,作为对照品贮备液,含厚朴酚为222 μg/mL,和厚朴酚为 100 μg/mL。

图4 厚朴酚及和厚朴酚高效液相色谱图A.混合对照品溶液 B.供试品溶液 C.阴性对照溶液 1.和厚朴酚 2.厚朴酚Fig.4 HPLC chromatogramsA.mixed reference substances B.sample C.negative sample 1.honokio 2.magnolol
3.1.2 供试品溶液的制备 取本品装量差异项下的内容物混匀,取约10 g,精密称定,置100 mL具塞锥形瓶中,精密加入甲醇100 mL,密塞,称定质量,静置过夜,超声处理20 min,放冷,用甲醇补足失重,摇匀,滤过,即得供试品溶液。
3.1.3 阴性对照液的制备 按处方从中除去厚朴,照3.1.2项下的制备方法处理得阴性对照溶液。
3.2 色谱条件及系统适应性试验 色谱柱为 DiamonsidTM-C18柱(迪马公司,250 mm ×4.6 mm,5 μm),流动相甲醇-0.3%磷酸(68∶32);体积流量1.0 mL/min;检测波长294 nm;柱温30℃。分别取混合对照品溶液(含厚朴酚为77.7 μg/mL、和厚朴酚为30.0 μg/mL)、供试品溶液和阴性样品溶液各10 μL注入液相色谱仪,理论塔板数以厚朴酚峰计算应不低于15 000,厚朴酚、和厚朴酚的拖尾因子为0.98、1.00;厚朴酚、和厚朴酚与其它组分的分离度都大于1.5;阴性对照不干扰样品测定。结果见图4。
3.3 方法学考察
3.3.1 标准曲线制备 分别吸取一定量的厚朴酚、和厚朴酚对照品贮备液,混合,加甲醇稀释成厚朴酚质量浓度为 44.4、55.5、66.6、77.7、88.8、99.9、111.0 μg/mL,和厚朴酚质量浓度为 15.0、20.0、25.0、30.0、35.0、40.0、45.0 μg/mL 的溶液。依次进样10 μL,每个浓度测定3次以上。以峰面积(A)及对照品溶液系列浓度(C)进行回归,得厚朴酚回归方程A=12.18C-26.55,相关系数r=0.999 3;和厚朴酚回归方程为A=13.98C-4.63,相关系数r=0.999 1。表明厚朴酚质量浓度在 44.4 ~ 111.0 μg/mL 之间、和厚朴酚质量浓度在 15.0 ~45.0 μg/mL之间与峰面积线性关系良好。
3.3.2 精密度试验 取厚朴酚质量浓度为77.7 μg/mL、和厚朴酚为30.0 μg/mL的混合对照品溶液10 μL连续进样,测定5次,RSD分别为1.28%和1.52%,表明仪器精密度良好。
3.3.3 稳定性试验 取供试品溶液(批号I0509Y)在0、2、4、6、8、12 h 分别进样 10 μL,RSD 分别为0.95%和1.24%,表明供试品溶液在12 h内稳定。3.3.4 重复性试验 取同一批号(批号I0509Y)样品6份,按3.1.2项下的制备方法处理、分别测定3次,结果厚朴酚平均质量分数为0.88 mg/g,RSD为1.83%;和厚朴酚平均质量分数为 0.33 mg/g,RSD为2.30%,表明分析方法重复性良好。
3.3.5 加样回收试验 精密称取窈窕茶样品(批号I0509Y)共6份,加入相应量的厚朴酚、和厚朴酚对照品,按3.1.2项下的制备方法处理并测定,计算回收率。厚朴酚平均回收率为 99.2%,RSD为1.53%;和厚朴酚平均回收率为 96.2%,RSD为1.49%,表明本方法准确可靠,见表1、2。
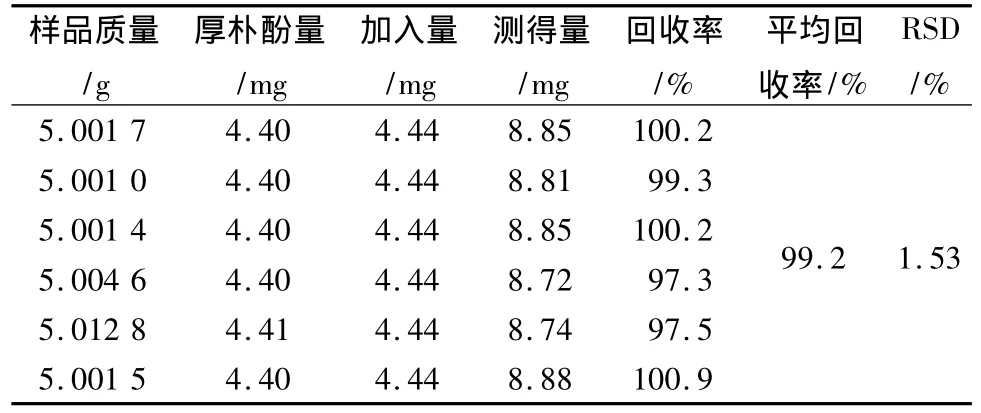
表1 厚朴酚回收率试验结果 (n=6)Tab.1 Recovery test results of magnolol(n=6)
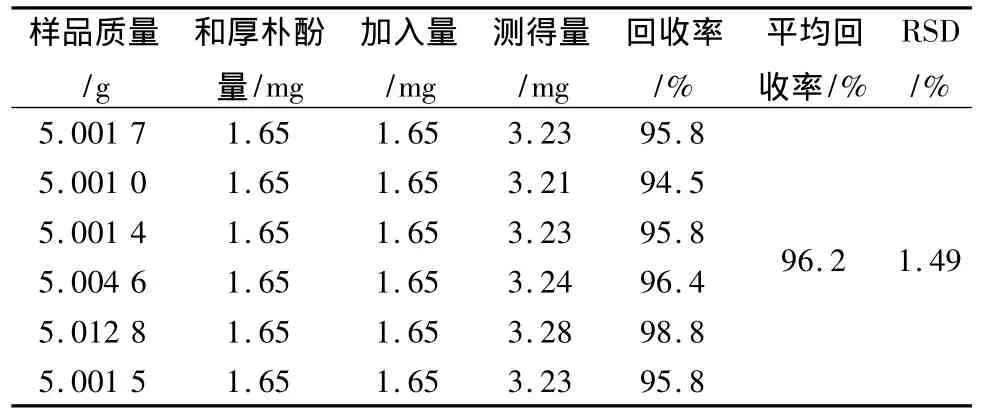
表2 和厚朴酚回收率试验结果 (n=6)Tab.2 Recovery test results of honokio (n=6)
3.4 样品测定 取窈窕茶3个不同批号样品(平均装量 I0509Y 为2.29 g/袋、H1201Y 为2.24 g/袋、I06620Y 为2.24 g/袋),按 3.1.2 项下的制备方法处理后测定,得厚朴酚及和厚朴酚的量,结果见表3。
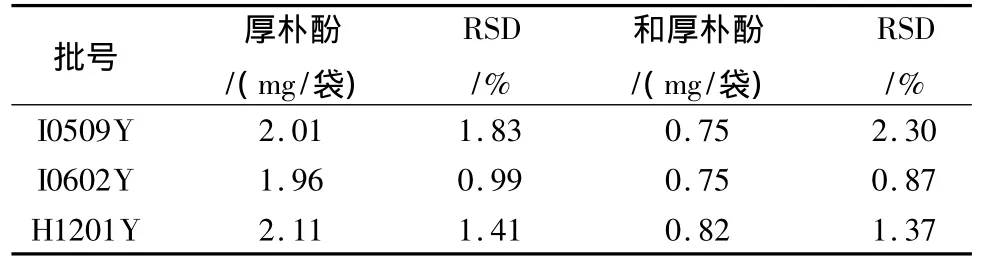
表3 样品测定结果 (n=3)Tab.3 Determination results of samples (n=6)
4 讨论
4.1 决明子的薄层鉴别中,提取过程将提取和水解[1]两步结合在一起,改用超声30 min的方法;并且萃取后对三氯甲烷层进行浓缩而不是蒸干,确保了溶液成分的完整和稳定。薄层展开中以石油醚(30~60℃)-正己烷-乙酸乙酯-甲酸(4∶14∶5∶0.1)为展开剂[5],使用硅胶 G 板和 H 板展开,均能看到斑点,但用G板展开速度明显快于H板,且薄层斑点效果更清晰。
4.2 枳实的薄层鉴别中,以甲醇-丙酮-三氯甲烷-浓氨水(3∶4∶13 ∶0.5)为展开剂[6-7],直接点于硅胶G薄层板,喷以0.5%茚三酮乙醇显色,相较于中国药典中采用1%氢氧化钠碱性硅胶G板[1],薄层结果更清晰易见。
4.3 厚朴的薄层鉴别中,以石油醚(60~90℃)-乙酸乙酯-甲酸(17 ∶3 ∶0.4)为展开剂[8],取代中国药典中以苯-甲醇(27∶1)为展开剂[1],避免了溶剂苯的使用,提高了实验的安全性。
4.4 关于HPLC流动相的选择,流动相曾直接采用甲醇-水[9],谱图中色谱峰的对称性都较差,后尝试采用加入 0.1% ~0.3%的磷酸[10-11],结果显示加入0.3%的磷酸时,色谱峰对称性最好;考察流动相甲醇-0.3%磷酸的不同配比,结果显示,选用甲醇-0.3%磷酸(68∶32)为流动相时,色谱峰分离效果最好,分离度都大于1.5,理论塔板数不低于15 000。
4.5 关于阴性色谱图中12 min和19 min出现的比样品中大的谱峰是因为在阴性对照的制备中使用的药材与窈窕茶样品使用药材并非同一批号,由于不同规格、产地、生长环境、采收时间都可能影响药材中有效成分的量,所以造成在此处某一药材的成分量偏高,峰面积较样品突出的原因。从整个谱图看,此两峰并未对本实验研究的厚朴酚及和厚朴酚的定量测定造成影响。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:135,230,235.
[2]干国平,熊 丽,陆海涛,等.高效液相色谱法测定香砂养胃丸中厚朴酚与和厚朴酚含量[J].中国医院药学杂志,2002,22(12):734-735.
[3]蒋 平,王文清,王 晨,等.RP-HPLC测定开胸顺气滴丸中厚朴酚与和厚朴酚含量[J].华西药学杂志,2006,21(6):577-579.
[4]张方杰,李 轲.中华肝灵胶囊中厚朴酚与和厚朴酚含量测定的研究[J].当代医学,2008,149:43-44.
[5]高保拴,聂丽萍.近视灵口服液中决明子的TLC鉴别[J].河北省科学报,1996,1(1):38-40.
[6]李琦智,曾 安,朱 敏,等.枳实消食胶囊质量标准研究[J].职业卫生与病伤,2004,19(1):29-30.
[7]张志红,刘爱芹,于胜海,等.咳喘宁冲剂的薄层色谱鉴别[J].齐鲁药事,2005,24(5):288-289.
[8]张 俊.清肝利胆胶囊的薄层色谱鉴别法[J].江苏药学与临床研究,2004,12(2):20-21.
[9]邱蔚芬,邹玉繁.HPLC测定保婴丹中厚朴酚及和厚朴酚含量[J].食品与药品,2007,9(1):24-25.
[10]钟小群,蔡庆顺,李玉云,等.HPLC测定藿香正气胶丸厚朴酚及和厚朴酚含量[J].中成药,2006,28(2):288-290.
[11]谢友良,曾惠芳,林 吉,等.HPLC测定黄芩正气胶囊中橙皮苷、黄芩苷、和厚朴酚、厚朴酚的含量[J].中成药,2006,28(1):34-35.
