药物性肝损伤诊断评分系统的比较及应用体会
2011-03-11高旭东樊艳华
高旭东,樊艳华
(中日友好医院 消化内科,北京 100029)
药物性肝损伤 (drug-induced liver injury,DILI)又称药物性肝病,是常见的肝病之一,其发病率仅次于病毒性肝炎、脂肪性肝病(酒精和非酒精性),因未引起广泛的重视,常被误诊或漏诊[1]。长期以来,对于DILI的诊断一直存在困惑。一方面,DILI患者发病时间存在很大差异,临床表现与用药的关系常较隐蔽,易被临床医师忽视。另一方面,对于DILI至今仍没有一个很好的确诊方法和非常规范可靠的诊断标准。本文总结了33例DILI患者,分析DILI因果关系评价表(Roussel Uclaf causality assessment method,RUCAM)[2]与临床诊断量表(clinical diagnostic scale,CDS)[3]的一致性及优缺点,并提出对评分系统的改进建议及应用评价。
1 材料与方法
1.1 研究对象
收集2003年1月~2009年1月在中日友好医院住院诊断为“DILI”的病例,剔除资料不全的病例,共有33例入选。
1.2 研究方法
采用回顾性研究方法,记录患者性别、年龄、用药史、临床表现、实验室及辅助检查,并记录治疗后肝功能变化情况。分别按RUCAM及CDS评分系统进行量化评分。
1.3 临床诊断与标准
33例病例经肝穿病理确诊和/或符合2007年消化病分会肝胆疾病协作组提出的急性DILI临床诊断标准[4];①有与DILI发病规律相象的潜伏期,初次用药后出现肝损伤的潜伏期一般在5d~90d;②有停药后异常肝脏指标迅速恢复的临床过程;③必须排除其他病因或疾病所致的肝损伤;④再次用药反应阳性。其中重症DILI 4例,非重症29例。
1.4 诊断评分系统的改良
比较RUCAM及CDS评分系统的差别,结合临床资料的分析结果,提出对2种评分系统的改进建议,并进行应用评价。
1.5 统计学方法
统计学处理应用SAS7.0统计软件,组间比较采用配对χ2检验。
2 结果
2.1 患者一般情况
33例DILI患者中男19例(57.58%)、女14例(42.42%),男女之比为1.36:1。年龄18~76岁,平均49.91±15.45岁。33例中伴有发热、皮疹、白细胞降低、嗜酸细胞增加等肝外过敏反应表现分别为36.36%、9.09%、18.18%、12.12%。33例中12例(36.36%)在停药后发病,其中停药时间<7d者占8例,7d~15d者2例,>15d者2例。
2.2 导致DILI的药物
西药21例(63.64%),中药(包括中草药和中成药)11例(33.33%),保健品(含西洋参皂苷)1例(3.03%)。
2.3 2种评分系统比较
对33例DILI患者按RUCAM及CDS评分系统进行量化评分,结果以确定(或高度可能)、可能性大、可能、可能性小(或不大可能)表示,具体见表1。33例中2种评分系统评分结果完全符合有13例(39.39%),相差1级有16例(48.48%),相差2级有4例(12.12%)。
按CDS评分系统判定为确定和可能性大者16例(48.48%),RUCAM评分系统判定为高度可能和可能性大者25例(75.76%),具体见表2。经配对χ2检验,两者存在统计学差异 (P<0.05),RUCAM评分系统较CDS评分系统更接近临床诊断。
2.4 改良RUCAM评分系统的应用及比较
我们建议的改良RUCAM评分系统见表3。将33例DILI患者按改良的RUCAM评分系统与原始的RUCAM评分系统进行评价比较,结果见表4。33例中2种评分系统评分结果完全符合有27例(81.82%),相差1级有6例(18.18%),无相差2级者。
33例中,按RUCAM评分系统判定为高度可能和可能性大者占25例(75.76%),按改良的RUCAM评分系统判定为确定和可能性大者29例(87.88%),具体见表5。经配对χ2检验,两者存在显著性差异(P<0.01),改良的RUCAM评分系统较原始的RUCAM评分系统更符合临床诊断。
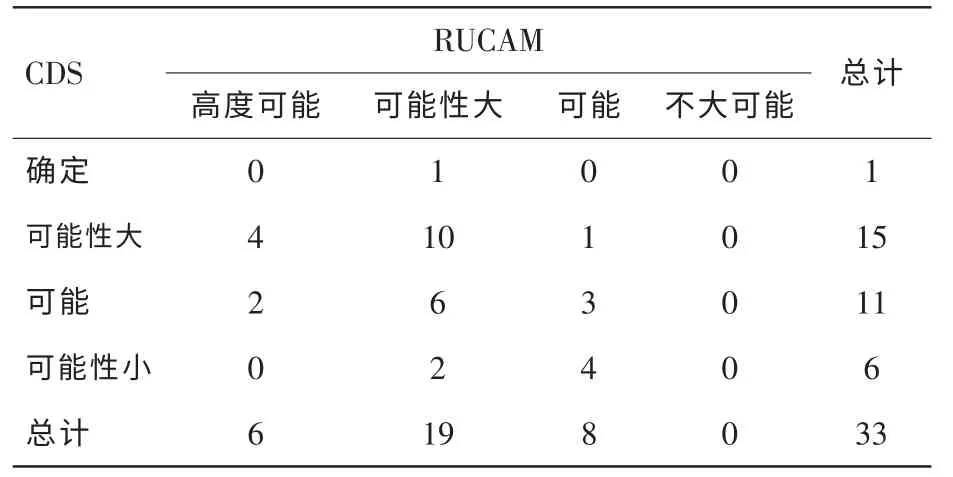
表1 RUCAM及CDS评分系统的应用评价结果(n)

表2 RUCAM及CDS评分系统评分结果比较(n)
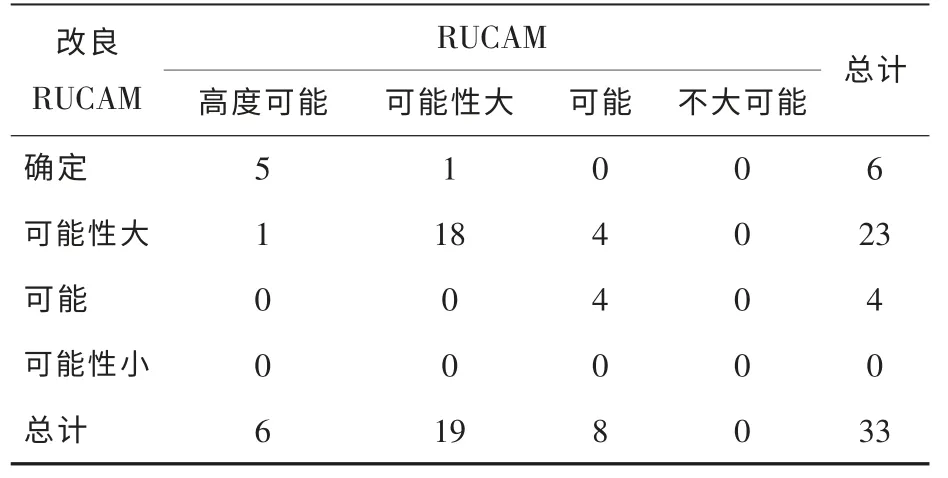
表4 改良RUCAM及原始RUCAM评分系统的应用评价结果(n)

表5 改良RUCAM及原始RUCAM评分系统评分结果比较(n)

表3 改良的RUCAM评分系统
3 讨论
3.1 DILI诊断标准
对DILI的诊断至今没有一个很好的诊断方法和非常规范的诊断标准。1978年日本“肝和药物”研究会首先提出DILI的诊断方案[5],该方案仅针对过敏或特异质性较明显者。1981年提出的Naranjo不良反应量表法应用于DILI的诊断,简便可行,但为非特异性诊断方法,灵敏性较低[6,7]。随着认识加深,1989年~1990年,在法国巴黎举行的一系列国际专家共识性会议上,国际医学组织理事会(CIOMS)组织相关专家制订了DILI标准定义及因果关系评估标准[8],即Danan方案,但该方案较烦琐,实际操作困难。1993年,国际共识会通过了改良Danan方案[2],即RUCAM评分系统,又称ICM标准,进一步提高了诊断可操作性和准确率,该方案沿用至今。1997年,Maria等[3]提出了较简捷改良方案,即CDS评分系统,又称Maria标准,进一步提高了DILI诊断的可操作性,但没有考虑到肝损伤的分型特点。2004年DDW-日本会议上,日本肝病学会提出了新方案,在RUCAM量表的基础上增加了药物淋巴细胞刺激试验(DLST)[9]。该试验方法是分离外周血单个核细胞(PBMC),将其暴露于某种药物后,应用3HTdR检测淋巴细胞增殖情况。日本一直推荐这一检测,但其尚未在美国获FDA批准,可能因该检测缺乏标准化和可重复性不够[10]。我国很少开展淋巴细胞刺激试验,而且某些中药成分可引起假阳性,故此标准并不适用于我国[11]。目前,临床上应用最广的DILI诊断方案仍是RUCAM评分系统和CDS评分系统[12]。
3.2 DILI诊断评分系统的比较
本组研究将临床诊断为DILI的33例分别按RUCAM以及CDS评分系统进行量化评分,经配对χ2检验,提示RUCAM评分系统较CDS评分系统的临床一致性高。这可能与CDS评分系统更注重药物过敏反应,且在用药时间与起病关系上限制较严有关。本组33例中伴有发热、皮疹、白细胞降低、嗜酸细胞增加等肝外过敏反应表现分别为36.36%、9.09%、18.18%、12.12%,按CDS评分系统,大多数无此类症状患者要获得高分(>14分)较为困难。在用药时间与起病关系上,CDS评分系统要求在服药4d~8周内才能获得高分,RUCAM评分系统则定在5~90d内;CDS评分系统要求在停药7d内起病才能得分,7~15d不能得分,≥15d扣分,而在RUCAM评分系统中,肝细胞损伤型≤15d,胆汁淤积型或混合型≤30d起病均可得分。本组33例中36.36%(12/33)患者在停药后发病,其中停药时间<7d者占66.67%(8/12),7d~15d者 占16.67%(2/12),>15d者 占16.67%(2/12),这12例在RUCAM评分系统中均可得分。Lucena等[13]研究结果亦提示,RUCAM评分系统更具实效性,评价结果更接近临床判断。
CDS评分系统简单易行,但对于无肝外过敏反应、潜伏期稍长的药物反应、胆汁淤积型或混合型肝损伤的评价与临床一致性不高。Camargo等[14]比较RUCAM和CDS评分系统,结果也显示CDS评分系统对长潜伏期、停药后演变为慢性肝损伤者的诊断准确性较差。而RUCAM评分系统缺乏对肝外过敏表现和部分无临床表现患者的评价。许建明等[15]应用RUCAM评分系统,未能确定的DILI占54.5%,大多数DILI在关联性评价中仍处于可能或不太可能的疑似水平,提示RUCAM评分系统为临床诊断DILI提供了一个框架,但是还应不断改进。
3.3 DILI评分系统的改良
综合以上各点,我们尝试在RUCAM评分系统基础上进行如下修改:(1)考虑到部分患者可无临床表现,加入用药与化验检查异常的时间关系。(2)参考巴黎会议共识意见,将碱性磷酸酶(ALP)与总胆红素(TBIL)并列为胆汁淤积型/混合型肝损伤的评分标准。(3)考虑到有相关过敏史和肝脏、肾脏基础病可增加机体对药物毒性的敏感性,加入用药前是否存在肝肾功能损伤,是否存在DILI史或家族中有此类药物所致肝损伤这2个危险因素。(4)考虑到潜在其他疾病范围过大,更改为自身免疫系统疾病如系统性红斑狼疮、类风湿性关节炎、干燥综合征等。(5)考虑到胆汁淤积型和混合型肝损伤,再用药反应中加入ALP指标,并根据新近的分型标准[16],将ALT升高≥2倍正常值改为≥3倍正常值。(6)参考CDS评分系统加入肝外过敏反应表现,包括发热、皮疹、关节痛、白细胞减少、嗜酸细胞增多(>5%)。(7)调整评分范围:最高为20分,最低为-8分,判断标准为:≥10分确定,6~9分可能性大,3~5分可能,1~2分不大可能,≤0分可除外。
本文采用改良的RUCAM评分系统(见表3)对33例DILI患者进行判断,结果显示改良的RUCAM评分系统较原始RUCAM评分系统更符合临床诊断。但此评分系统还不能对DIIL进行早期诊断,且本组样本量不够大,此改良建议还需要进一步评估和验证。
[1] Nathwani RA,Kaplowitz N.Drug hepatotoxicity[J].Clin Liver Dis,2006,10:207-217.
[2] Danan G,Benichou C.Causality assessment of adverse reactions to drug-Ⅰ.A novel method based on the conclusions of international consensus meetings:application to drug-induced liver injuries[J].J Clin Epidemiol,1993,46:1323-1330.
[3] Maria VA,Victorino RM.Deve1opment and va1idation of a c1inical scale for the diagnosis of drug-induced hepatitis[J].Hepatology,1997,26:664-669.
[4] 中华医学会消化病学分会肝胆疾病协作组.急性药物性肝损伤诊治建议(草案)[J].中华消化杂志,2007,27(11):765-767.
[5] 舛本後,恩地森一.薬物性肝障害の诊断[J].肝胆胰,2000,40:887-897.
[6] Naranjo CA,Busto U,Sellers EM,et a1.A method for estimating the probability of adverse drug reactions[J].Clin Pharmacol Ther,1981,30:239-245.
[7] García-Cortés M,Lucena MI,Pachkoria K,et a1.Evaluation of naranjo adverse drug reactions probability scale in causality assessment of drug-induced liver injury[J].Aliment Pharmacol Ther,2008,27(9):780-789.
[8] Benchiou C.Criteria of drug-induced liver disorders report of an international consensus meeting[J].J Hepatol,1990,11(2):272-276.
[9] 滝川一,恩地森一,高森賴雪,他.DDW-J2004ヮ—クショップ药物性肝障害诊断基准の提案[J].肝臓,2005,46(2):85-90.
[10] 陈成伟.药物性肝损害诊断标准的评价[J].诊断学理论与实践,2009,8(2):121-124.
[11] 马博,刘思纯.急性药物性肝病常见诊断标准的比较及存在的问题[J].新医学,2010,41(1):61-63.
[12] 唐岸柳,沈守荣,贺达仁.药物性肝损伤的诊断思维[J].医学与哲学,2009,30(11):63-65.
[13] Lucena MI,Camargo R,Andrade RJ,et al.Comparison of two clinical scales for the causality assessment[J].Hepatology,2001,33:123-130.
[14] Camargo R,Andrade R.J,Lucena MI,et al.Comparison of two algorithms for the diagnosis of drug-induced hepatotoxicity:CIOMS and Maria and Victorino(M&V)[J].J Hepatol,2000,32(l2):124-124.
[15] 许建明,徐张巍,胡祥鹏.112例药物性肝损伤的临床关联性评价[J].中华消化杂志,2005,25(8):451-453.
[16] Navarro V.Hepatic adverse event nomenclature document[R/OL].Available from:http://www.fda.gov/cder/livertox/presentations2005/Vic_Navarro.ppt(Accessed,2006,Nov 17).
